Биохимия. Предмет биохимии
 Скачать 0.58 Mb. Скачать 0.58 Mb.
|
|
ФЕРМЕНТЫ. Еще в 1878 году Куне с целью унификации терминологии предложил называть каталитически активные соединения энзимами. В последние пятьдесят лет этот термин стал общепризнанным в литературе на всех языках. В переводе с греческого этот термин означает: «из дрожжей». В литературе на русском принят термин «ферменты» (fermentatio (с латинского) - сбраживание), хотя изучение ферментов и процессов с их участием традиционно называют «энзимология» . По завершении девятилетних исследований в 1926 году Самнер сообщил о выделении из бобов фермента уреаза, и предположил, что она имеет белковую природу, что сочли поначалу нелепым. Последующие исследования Самнера и независимо Нортропа и Стэнли привели к выделению еще нескольких ферментов (например, в 1930 – 31 году Нортроп получил в чистом виде пепсин и трипсин). Катализаторы – это вещества, ускоряющие химические реакции. Ферменты являются белковыми катализаторами биохимических реакций. В отличие от небелковых катализаторов, каждый фермент способен катализировать лишь очень небольшое число реакций, часто только одну. Таким образом ферменты являются специфическими катализаторами. Практически все биохимические реакции катализируются ферментами. В 1814 году Киркгофф выделил амилазу из семян проросшего ячменя, которая сбраживала крахмал. В то время господствовало виталистичесое деление ферментов на «организованные» и «неорганизованные». В конце 19 века М. М. Манасеина, А. И. Лебедев (Россия) и братья Бюхнер (Германия) показали, что так делить ферменты нельзя. В начале двадцатого века И. П. Павлов предположил белковую природу ферментов. И, наконец, в 1935 году белковая природа ферментов стала общепризнанной, Это имело большое значение (достаточно сказать, что за эти открытия в 1946 году Самнеру, Нортропу и Стенли была присуждена Нобелевская премия). За последние пятьдесят лет было выделено из всех типов организмов около 2500 ферментов, часть из них получена в кристаллическом виде, для более пятидесяти ферментов открыта третичная структура. В клетках кишечной палочки содержится около тысячи различных ферментов, а у человека еще больше. Функции ферментов сводится к ускорению химических реакций, причем ферменты отличаются тремя уникальными свойствами: 1 )Это самые эффективные из всех известных катализаторов, так что даже очень малые (микромолярные) концентрации ферментов способны в очень большой степени ускорять реакции (в миллион и более раз, чем если бы реакция протекла бы без фермента). В самом деле в отсутствие ферментов скорость большинства реакций в биологических системах практически неощутима. Такая простая реакция, как гидратирование углекислого газа. В отсутствие фермента перенос углекислого газа из тканей кровь и затем в воздух легочных альвеол был бы не полон. Карбангидраза, катализирующая этот процесс является одним из самых активных ферментов. Каждая ее молекула способна гидратировать десять в пятой степени молекул углекислого газа в секунду. При этом скорость реакции в присутствии фермента в десять в седьмой степени раз выше, чем в его отсутствие. 2) Большинство ферментов отличаются специфичностью действия (практически каждая реакция катализируется специальным ферментом). Специфичность проявляется как в отношении катализируемой реакции, так в и отношении субстратов. Каждый фермент катализирует какую-либо одну химическую реакцию или несколько очень сходных реакций. Степень специфичности к субстрату очень высока, а иногда практически абсолютна. Рассмотрим в качестве примера протеолитическте ферменты. Они катализируют реакцию гидролиза пептидной связи; многие протеолитические ферменты катализируют еще и иную, но сходную реакцию гидролиза эфирной связи. Протеолитические ферменты сильно различаются по степени субстратной специфичности. Например, субтилизин (он синтезируется определенным видом бактерий) расщепляет практически любые пептидные связи в независимости от того, какими аминокислотами они образованы. Трипсин расщепляет пептидные связи, образованные только карбонильными группами лизина и аргинина. Тромбин (участвующий в свертывание крови) разрывает только те петидные связи, котрые образованы карбонильной группой аргинина и аминогруппой глицина. 3) Действия большинства ферментов регулируется (то-есть они способны переходить из состояния с низкой активностью к состоянию с высокой активностью и обратно). В совокупности эти механизмы регуляции представляют сложную систему, посредством которой организм контролирует все свои функции. Некоторые ферменты синтезируются в форме неактивного предшественника и переходят в активное состояние в физиологически соответствующем месте и времени. Примером регуляции такого типа могут служить пищеварительные ферменты. Так, например, пепсиноген синтезируется в поджелудочной железе, а активируется в тонком кишечнике, где в результате расщепления пептидной связи образуется активная форма – трипсин. Такой же тип регуляции многократно используется в последовательности ферментативных реакций, ведущих к свертыванию крови. Каталитически неактивные предшественники протеолитических ферментов называются проферментами или зимогенами. С помощью ферментов осуществляется трансформация различных видов энергии. Во многих биохимических реакциях энергия реагирующих веществ переходит из одной формы в другую с высокой степенью эффективности. Например, при фотосинтезе энергия света переходит в энергию химических связей. В митохондриях свободная энергия, содержащаяся в низкомолекулярных веществах поступающих с пищей переходит в энергию АТФ, которая затем может использоваться во многих процессах – при мышечном сокращении, при трансмембранном транспорте и так далее. Ферменты не сдвигают равновесие химических реакций, они лишь ускоряют наступление этого равновесия. Отсутствие даже одного фермента или его дефект могут иметь очень серьезные отрицательные последствия для организма. Впервые фермент синтезировал в 1966 году (рибонуклеазу) Меррифилд. Поскольку ферменты – белки, они могут быть мономерными (одна полипептидная цепь) – это пепсин, трипсин, уреаза и так далее; или олигомерными (например, ЛДГ). Олигомеры в определенных условиях могут дисссоциировать на мономеры. Биологическая активность олигомерных ферментов проявляется либо в диссоциированном, либо в не диссоцированном состоянии. Все ферменты относятся к глобулярным белкам. Соответствнно ферменты могут быть простые (рибонуклеаза) и сложные (каталазы). Максимальная активность сложных белков (ферментов) зависит от участия небелковых соединений, называемых ко-факторами. Молекулярный комплекс белка и ко-фактора называется холоферментом и обладает максимальной каталитической активностью. Белковый компонент, лишенный ко-фактора называется апоферментом, он обладает очень низкой активностью, а часто вообще не активен. Некоторые ферменты требуют два или три различных ко-фактора и обычно один из них неорганический ион. Связь между белковым компонентом (апоферментом) и ко-фактором может быть ковалентной или нековалентной. Внекоторых случаях ко-фактор и фермент существуют отдельно и связываются друг с другом только на время протекания реакции. В других случаях ко-фактор и фермент связаны постоянно, иногда очень прочно, ковалентными связями. Вообще говоря, роль ко-фактора сводится: 1) к изменению трехмерной структуры белка и (или) связанного субстрата для улучшения условий взаимодействия фермента с субстратом; 2) к непосредственному участию в реакции в качестве еще одного субстрата. Различают неорганические ко-факторы (например, ионы цинка, магния, марганца, железа, меди, калия и натрия) и органические (их обычно называют ко-ферменты – это около десятка соединений различной структуры). Как правило, связь между ко-фактором неорганической природы и апоферментом прочная и, если ее разорвать, то ни ко-фактор, ни белковая часть фермента не проявляют активности. Большая часть ко-ферментов либо образуется из витаминов, либо представляют собой витамины, либо витамины являются частью ко-фермента. Поэтому, неорганические ионы, перечисленные выше, и витамины должны обязательно входить в рацион для любого организма. В качестве примера витаминов, входящих в неизменном виде в состав фермента, можно привести биотин, липоевую кислоту и так далее. Так, биотин связывает углекислоый газ, а липоевая кислота переносит ацильную групу. Такие же витамины, как рибофлавин (витамин В2) превращаются в ФАД или ФМН, то-есть в качестве ко-фермента выступают их производные, которые участвуют в окислительно-востановительных реакциях. Органические ко-ферменты обычно выступают в качестве дополнительных субстратов. Участие ко-ферментов в процессе обычно сводится к донорным или акцепторным функциям (по отношению к другим субстратам или субстрату) определенной химической группировки. Может происходить, например, перенос метильной группы – СН3, аминогруппы – NH2, электролитов. В соответстви с этим ко-фермент называют «переносчиком групп». Например, в присутствии передоксальфосфатзависимого фермента перенос аминогруппы осуществляется за одну реакцию, а для другого случая – электрон вместе с протоном – в результате двух реакций, катализируемых разными ферментами, но с участием одного ко-фермента (НАД):   НАД + НАДН НАД+ ко-фермент участвует в обеих реакциях, причем в одной НАД – это продукт, а в другой – реагент. Такие реакции называются сопряженными. Мы уже упоминали, что ферменты могут быть мономерные и олигомерные. В свою очередь, олигомерные могут иметь в своем составе одинаковые субъединицы (например, каталаза имеет 6 субъединиц и все одинаковые) или разные, что предопределяет возникновение изомерных форм ферментов (например, ЛДГ – тетрамер, но имеет два типа субъединиц). Чем больше разных субъединиц входит в состав фермента, тем больше появляется его изомерных форм. Таким образом, мы можем сказать, что изоферменты – это ферменты, катализирующие одну и ту же реакцию, но отличающиеся по каталитической активности., физико-химическим свойством и составу. Например, ЛДГ имеет два вида субъединиц: Н (hart) и М (muscle). Соответственно образуется пять различных изоферментов (тетрамеров). Варианты: НННН, НННМ, ННММ, НМММ, ММММ, или их называют, соответствнно ЛДГ1, ЛДГ2, ЛДГ3, ЛДГ4, ЛДГ5. Соотношение изоферментных фракций в разных органах различно (например, в сердце преобладает ЛДГ1, в мышцах и в печени ЛДГ5). Изучая изоферментный спектр, можно судить о локализации патологическго процесса и о степени тяжести. Биологическое значение изоферментов заключается в том, что они обеспечивают протекание химических реакций в различных тканях, в зависимости от условий обмена в данной ткани. Например ЛДГ1 и ЛДГ2 наиболее активны в тканях с высокой скоростью окисления и высоким содержанием кислорода. Эти изоферменты обладают высоким сродством к кислороду и наиболее активны в эритроцитах и миокарде. ЛДГ5 наиболее активна в тканях с меньшим содержанием кислорода, например в печени и скелетных мышцах – где высокая концентрация молочной кислоты. С возрастом происходит изменение активности изоферментов в тканях (у детей). Изоферментные формы характерны для тех ферментов которые в тканях выполняют особо важные функции то-есть стоят на перекрестке особо важных каталитических процессов (например ЛДГ – на границе аэробного и анаэробного процессов). НОМЕНКЛАТУРА ФЕРМЕНТОВ. 1)Тривиальная, исторически сложившаяся (пепсин – от pepsis – пищеварение; трипсин – от tripsis - расжижение). Цитохромы (cytos – клетка, chromos - цвет) – окрашивающие клетку. 2) Рабочая: а) название субстрата плюс окончание «аза». Например , сахараза, мальтаза, липаза. Иногда берется греческое или латинское название, например amylos (крахмал) – фермент называется амилаза. б) По названию типа катализируемой реакции (гидролаза, синтетаза, дегидрогеназа, и так далее). в) По типу расщепляемой связи (пептидаза, эстераза, гликозидаза и так далее). 3) Систематическая (международная): необходимо дать точное название субстрата (химическое название), указать характар процесса и прибавить окончание «-аза». Например, попросту уреаза, а по международной номенклатуре: карбамидамидогидролаза (то-есть карбамид-мочевина и разрыв-гидролиз амидной связи). Если в реакции участвует ко-фермент, то это тоже должно быть отражено в названии. Например, попросту ЛДГ, а по международной номенклатуре – альфа-лактат-НАД-оксидоредуктаза. КЛАССИФИКАЦИЯ ФЕРМЕНТОВ. Принята международным союзом биохимиков в 1961 году в Москве. По этой системе ферменты делятся на шесть основных классов, согласно общему типу реакций, которые они катализируют. Классы делятся на подклассы и подподклассы, чтобы можно было описать специфичность каждого индивидуального фермента. Каждому ферменту приписывают код или шифр, например: 2.1.3.4., где первая цифра – номер класса, вторая цифра – номер подкласса, третья цифра – номер подподкласса, четвертая – порядковый номер в подподклассе. Например: 1,1,1,1 – алкоголь-НАД-оксидоредуктаза (алкогольдегидрогеназа); 3,5,1,5 – карбамидамидогидролаза (уреаза). Различают следующие классы: 1) Оксидоредуктаза (катализирует окислительно-восстановительные реакции всех типов). Деление на подклассы: дегидрогеназы, оксигеназы и так далее (то-есть по типу окисления или восстановления): а) аэробные дегидрогеназы (оксидазы); б) анаэробные дегидрогеназы (RН2 + Х = ХН2 + R); в) цитохромы (переносят электроны); г) пероксидазы (окисляют с помощью перекисей); д) каталаза (2 Н2О2 = 2 Н2О + О2); е) гидроксилазы и оксигеназы (катализируют окисление субстрата путем внедрения в субстрат одного или двух атомов кислорода) 2) Трансферазы (катализируют перенос отдельных групп атомов от донорной молекулы к акцепторной). Деление на подклассы происходит в зависимости от характера переносимых групп: аинотрансферазы (NН2), метилтрансферазы (СН3) формилтрансфераза, ацилтрансфераза и так далее. 3) Гидролазы (катализируют разрыв химических связей с присоединением молекул воды по месту разрыва, то-есть реакции гидролиза). Деление на подклассы зависит от характера разрываемой связи: пептидазы (пепсин, трипсин), эстеразы (сульфоэстеразы, фосфоэстеразы), гликозидазы (амилаза, сахараза, лактаза), фосфотазы , амидазы и так далее. 4) Лиазы (катализируют разрыв химической связи без присоединения воды по месту разрыва, при этом в субстратах образуются двойные связи). На подклассы делят от характера разрываемой связи: - C – C - ; - C – N -; - C – O - и т. д. Например альдолаза разрывает – С – С - связь в сахарах. Декарбоксилоза отщепляет карбоксильную группу, дегидротазы (отщипляют воду). 5) Изомеразы (катализируют взаимопревращение различных изомеров). Деление на подклассы зависит от формы: L – D , цис-, транс-, альфа – бета, лактим-лактам (эпимеразы, таутомеразы, рацимазы) и т.д. 6) Лигазы (синтетазы) – катализируют образование нового вещества из двух других веществ. При этом используется молекула АТФ или другого макроэрга для обеспечения энергией. Деление на подкласы осуществляется в зависмости от того какие вещества вступают в реакцию конденсации (например, глутаминсинтетаза). ПРИРОДА КАТАЛИЗА. Известно, что результатом любой химической реакции является образование продуктов реакции. Согласно теории «переходного состояния» продукты реакции образуются лишь после того, как реагирующие частицы: 1) – встречаются в определенной пространственной ориентации, и 2) - обладают достаточной энергией, чтобы достичь «переходного состояния» для которого возможны одновременное образование новых и разрыв старых химических связей. Очевидно, что чем легче достигается «переходное состояние», тем выше скорость реакции. Разность между общей энергией исходных реагирующих частиц и энергии возбужденного переходного состояния называется энергией активации, которая характеризует данную химическую реакцию и определяет условия, при которых она происходит.      С Переходное состояние (1) - субстрат В (2) - продукт О (3) – общая энергия Б (4) – энергия активации  О Д Н (4) А Я Э   Н ____(1)_______________________ Е Р (3) Г _________________________________ (2)  И Я Время протекания реакции Согласно теории переходного состояния катализатор увеличивает скорость химической реакции, изменяя ее путь так, что новый путь характеризуется более низкой энергией активации. Таким образом вероятность достижения переходного состояния повышается и скорость реакции увеличивается. Хотя энергия активации при действии фермента ниже, энергия общая не меняется.    Переходное состояние без катализатора                    С В О Б (1) О Д Н Переходное состояние в присутствии катализатора  А Я (1) – Энергия активации (2) (2) – Энергия активации 2 Э (3) – Общая энергия - колличество Н выделяемой энергии Е Р Субстрат (3) Г И Я Продукт  Время протекания реакции Будучи катализатором, ферменты действительно уменьшают энергию активации. Однако, ферментативный катализ характеризуется еще одной особенностью – способностью фермента связывать и ориентировать реагирующие молекулы по отношению друг к другу, так, чтобы образование продуктов реакции происходило максимально эффективно (это одно из положений переходного состояния о котором мы уже говорили). С выполнением этих функций ферментов связан определенный участок на его поверхности, который называют активным центром. Но о нем речь позднее. Хотя детальный механизм действия каждого фермента уникален, все ферменты «работают» сходным образом. Первый подход к изучению действия ферментов разработал Генри (1903г.) и позднее Михаэлис и Ментен (1913г.). Генри, а также Михаэлис и Ментен предложили практически одну и ту же модель, однако Михаэлис и Ментен обосновали свой подход данными тщательно проведенных эксппериментов. Внастоящее время модель Генри-Михаэлиса-Ментена лежит в основе ферментативной кинетики. МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ. На скорость химической реакции влияют различные факторы – концентрация веществ, температура, химическая природа реагирующих веществ. Скорость зависит от наличия активных молекул, поскольку только они могут участвовать в реакциях. 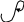 Nакт = Nобщее х е –Е/RT х № общее – концентрация вещества l – постоянная величина основания логорифма общего типа представляют собой мощные катализаторы многих органических реакций, протекающих в водных средах. Е – энергия активации системы. Этот параметр характеризует природу реагирующих веществ. Чем выше Е, тем меньше скорость реакции, так как становится меньше число активных молекул. R – универсальная газовая постоянная Т – температура системы (в градусах Кельвина). Чем выше температура, тем больше скорость реакции, так как увеличивается количество активных молекул.  -стерический коэффициент, его величина от 0 до 1, то-есть это число удачных столкновений. Он вводится в формулу для органических соединений.  Ферменты уменьшают энергию активации. Например, для реакции 2 Н2О2 2 Н2О + О2 энергия активации составляет 18000 кал / моль. При применении в качестве катализатора платины энергия уменьшается до 11000 кал/моль. Если не работает фермент каталаза, энергия снижается до 1700 кал / моль. Ферменты повышают стерический коэффициент. То-есть фермент одновременно влияет и на энергию активации и на стерический коэффициент, особенно это справедливо для бимолекулярных реакцийю Энергия активации сснижается в следствие образования фермент-субстратных комплексов. Эти комплексы не стойкие и распадаются с образованием продукта реакции и фермента в неизменном виде и количестве:    F + S FS FS* P + F 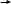 В образовании фермент-субстратного комплекса участвуют разные связи (водородная, гидрофобная, электростатического взаимолействия и так далее). Фермент-субстратный комплекс представляет собой реально существующие химические соединения. Некоторые из таких соединений действительно удалось выделить. Фермент-субстратный комплекс образуется в результате связывания фермента с субстратом, то-есть подтверждается основополагающая идея, что при выполнении любой динамической функции белка первым этапом неизменно является связывание. Без связывания белок не может функционировать. И, действительно, связывание, как правило, единственный фактор, определяющий специфичность действия ферментов. Следующим событием в процессе превращения FS F + P является химическая реакция разрыва и образование связи с образованием продукта. В ходе образования фермент-субстратного комплекса происходит перераспределение внутримолекулярной энергии за счет смещения электронов, происходит поляризация связей, ослабляющая их (это те связи, которые в процессе катализируемой реакции должны разрушаться ). Тем самым снижается энергия активации. Это может быть электрофильная NH3+ ; Mg++. Или нуклеофильная -ОН, N-- атака, смещения кислотно-щелочного    равновесия (ОН-,Н+), NH устранения стабилизирующей роли воды и так далее. Распад фермент-субстратного комплекса происходит с высокой скоростью. Размер молекулы субстрата субстрата намного меньше, чем молекула фермента (например, молекулярная масса каталазы равна 250000), поэтому взаимодействие субстрата происходит не со всей молекулой фермента, а с определенным ее участком называемом активным центром. Активный центр может быть один, а может их быть несколько, чаще до четырех. Если фермент – олигомер то активный центр может быть расположен и на одной и на нескольких субъединицах. Участки, удаленные от активного центра представляют собой аллостерические зоны.  | | R161 |  R162 R160  | | S R170 R163 R1 R2 | | R3 |     По химической структуре активный центр это часть молекулы фермента имеющая сложную пространственную конфигурацию и образованная радикалами входящих в состав фермента аминокислот. Наиболее часто в активный центр входит карбоксильные группы аспарагиновой и глутаминовой кислот, амино-группы аспаргина и лизина, тио-группы цистина и цистеина, гидроксо-группы серина, N-- -группы гистидина. Входят ионы NH Металлов (цинк, медь, кобальт, калий, натрий, кальций, магний и так далее), входят простетические группы. Все эти радикалы, металлы и простетические группы определенным образом ориентированы в пространстве. Некоторые из них принимают участие в связывание субстрата, другие - в химических превращениях субстрата в продукт. Некоторые группы способны участвовать в обоих процессах. Большинство этих групп занимает удаленное положение в составе полипептидной цепи и пространственно сближены только благодаря многочисленным изгибам, поворотам и скручиванию полипептидной цепи. Очевидно, что аминокислотные остатки, ответственные за связывание и каталитический процесс весьма существенны для активности фермента . Однако не меньшее значение имеют структурные радикалы, благодаря упорядоченному взаимодействию которых образуется и стабилизируется структура молекулы в целом и которые, таким образом, участвуют в формирование активного центра. Свой вклад вносит и ко-фактор. Оптимальная конформация и, следовательно, максимальная активность зависит от выполнения физиологических условий в которых белок сохраняется в интактном состоянии (температура приблизительно 35 – 37градусов по Цельсию, оптимум рН (в среднем 6,5 – 7,5) и так далее). Исключения составляют лишь некоторые ферменты, действующие в экстремальных условиях, например, пепсин, находящийся в кислом желудочном соке. Активный центр состоит из зоны связывания и каталитической зоны. При этом субстрат по конфигурации должен соответствовать зоне связывания (см. рис.). При этом молекула субстрата может взаимодействовать с разными функциональными группами фермента (R1……R163). Зона связывания узнает “свой” субстрат, что определяется пространственным соответствием. Изменения в субстрате, которые позволяют ему подходить к ферменту «как ключ - замок», определяются каталитической зоной. В ней есть высоко активные группы (тиогруппа – тиоловые ферменты, соответственно те вещества, которые связывают эти группы называются - тиоловые яды; гидроксогруппы из серина – сериновые яды; карбоксильные, аминогруппы и так далее) Все эти группы соответсвуют изменению конфигурации субстрата. В момент сближения фермента и субстрата происходит изменение конфигурации каталитической зоны фермента под влиянием истинного субстрата. Теорию образования фермент-субстратного комплекса предложил Э. Фишер, который утверждал, что фермент и субстрат изначально подходят друг к другу как «ключ и замок». Более сответствует действительности теория Кошланда, согласно которой субстрат как бы «подстраивает » каталитическую зону под себя. Если субстрат не вызывает изменение каталитической зоны, то нет и продукта реакции, то-есть не образуется фермент-субстратный комплекс при вхождении в активный центр, субстрат жестко ориентирован, что и вызывает увеличение стерического коэффициента. Ферменты повышают скорости катализируемых ими реакций в 108 – 1012 раз. Например, уреаза ускоряет гидролиз мочевины в десять в четырнадцатой степени раз при pH =8 и 20 градусах по Цельсию. Существует четыре основных фактора определяющих способность ферментов ускорять химические реакции: 1) сближение и ориентация субстрата по отношению к каталитической группе. То-есть фермент способен связывать молекулу субстрата таким образом, что атакуемая ферментом связь оказывается не только расположенной в непосредственнрй близости от каталитической группы, но и правильно ориентируемой по отношению к ней. В результате этого вероятность того, что фермент-субстратный комплекс достигнет переходного состояния значительно увеличивается. 2) Напряжение и деформация с чувствительной к действию фермента связи, возникающие в следствие индуцированного соответствия между молекулами субстрата и фермента. То-есть присоединение субстрата может вызвать конформационные изменения в молекуле фермента, которые приводят к напряжению структуры активного центра, а также несколько деформируют связанный субстрат, облегчая тем самым достижение фермент-субстратным комплексом «переходного состояния». При этом возникает так называемая «индуцированное соответствие» фермента субстрату. Таким образом, небольшие изменения третичной или четвертичной структуры относительно крупной молекулы фермента могут приводить к деформации молекулы субстрата. 3) Общий кислотно-основной катализ. В активном центре фермента могут находиться группы специфических аминокислотных остатков, которые являются хорошими донорами (карбоксильная, NH3+, тиогруппа и др.) или акцепторами протонов (- СОО-, аминогруппа, -S-, и так далее). Такие кислотные или основные группы реакции, причем значительно быстрее, чем в случае не катализируемых реакций. 4) Ковалентный катализ. Ферменты реагируют со своим субстратами, образуя очень нестабильные, ковалентно связанный фермент-субстратные комплексы, из которых в ходе последующих реакций образуются продукты СВОЙСТВА ФЕРМЕНТОВ. Ферменты харктеризуются очень высокой активностью, гораздо большей, чем обычные катализаторы. Наример одна молекула каталазы способна за одну минуту расщепить 5000000 молекул перекиси водорода . Одна молекула карбангидразы за одну минуту катализирует взаимодействие 36000000 молей углекислого газа в реакции: СО2 + Н2О = Н2СО3. Молярная активность большинства ферментов оценивается превращением 1000 – 10000 молей. Но даже такие значения говорят о существенном ускорении реакции, если принять во внимание, что для большинства органических реакций в отсутствии катализатора даже при нагревании требуются минуты и часы. В отличие от неорганических катализаторв, ферменты обладают специфичностью. Это определяется соответствием конфигурации активного центра фермента и субстрата. Различают следующие виды специфичности: 1) Абсолютная – фермент действует только на одно определенное вещество. Например, L-аргиназа расщепляет только L-аргинин. Так действуют большинство дегидрогеназ (ЛДГ, и т. д.). 2) Абсолютная групповая – фермент вызывает один и тот же каталитический эффект у группы соединений (как правило, у соединений одного гомологического ряда). Например, алкогольдегидрогеназа – окисляет этиловый, пропиловый, бутиловый и т. д. спирты. 3) Относительная групповая – идет катализ разных классов органических веществ. Например, трипсин прояввляет пептидазную активность в белках и эстеразную в сложных эфирах. 4) Стереохимическая – расщипляется только определенная форма изомеров (D-L, альфа–бета, цис – транс и т. д.). Активность ферментов в значительной мере зависит от рН. При этом для работы каждого фермента характерен свой оптимум рН. Например,пепсин наиболее активен при рН = 1 – 2, амилаза – при рН = 7; аминокислотоксидаза – при рН = 10 – 11. Чувствительность к изменеию рН объясняется следующим образом: при изменении реакции среды изменяется тип ионизации функциональных групп ферментов, в результате этого образуются новые ионные связи, или разрушаются старые, и , как следствие, изменяется конформация молекулы белка-фермента. Это в свою очередь приводит к изменению физико-химических свойств и биологической активности. В клинике при такой ситуации вводятся буферные растворы, которые способствуют нормализации рН, соответственно восстанавливается и активность фермента. Например, при уменьшении кислотности желудочного сока вводится раствор соляной кислоты, что приводит к восстановлению активности пепсина. Ферменты термолабильнны. При увеличении температуры на каждые 10 градусов скорость реакции увеличивается в 2 – 4 раза. Оптимальная температура для работы фермента 37 – 40 градусов по Цельсию. При дальнейшем повышении температуры ферменты, являясь белками, подвергаются денатурации, теряя ферментативную активность. В этом случае денатурация будет необратима. При снижении температуры ферменты тоже теряют свою активность, но это явление обратимое. Это свойство используется в криохирургии, чтобы в тканях замедлить все процессы, чтобы запасов кислорода и энергии в тканях хватило на более длительное время; для хранения ферментов. Ферменты фотолабильны. Они очень чувствительны к ультрафиолетовым лучам, так как ферменты – это белки и они при действии ультрафиолета денатурируют (это лежит в основе ультрафиолетового облучения в медицине). ОСНОВЫ ФЕРМЕНТАТИВНОЙ КИНЕТИКИ. Кинетика – это раздел физической химии, изучающий скорости протекания реакций. Кинетические исследования лежат в основе понимания механизма реакции: во сколько стадий протекает химическая реакция, какова природа превращений на каждой стадии, какая стадия самая медленная, то-есть определяющая скорость суммарной реакции. Описание реакций в таких понятиях и называется механизмом реакции. Хотя скорости реакций определяются экспериментально, соотношение между скоростью и концентрациями реагентов можно выразить в виде простого уравнения. При записи таких уравнений используется константа скорости К. При постоянной температуре К – это постоянная, характеризующая быстроту протекания реакции. Большое значение для объяснния ферментативной кинетики имели работы Михаэлиса и Ментена. Они работали с дрожжевым экстрактом, содержащим инвертазу: сахароза = глюкоза + фруктоза (реакция идет под действием инвертазы). В одной серии опытов [S] = const, а количество фермента изменялось (отмечалась линейная зависимость), во второй – [F] = const, а [S] – изменялась (увеличивалась), при этом отмечалась нелинейная гиперболическая зависимость скорости от [S]. Для обьяснения полученных результатов предполагалось образование фермент- субстратного комплекса.  K1 K3  F + S FS P + F  K2 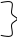 V1 = K1 [F] [S] V2 = K2 [FS] На основании закона действующих масс. V3 = K3 [FS] Наиболее важна V3, так как дает продукт реакции. Но [FS] определить практически невозможно. Используют суммарное уравнение Михаэлиса – Ментена: K3 [F0] [S] K2 + K3   \/ = Km = Km + [S] , где K1 V3 – скорость приводящая к образованию продукта. К3 – константа этой скорости. [F0] – сумма фермента в свободном состоянии и в составе фермент-субстратного комплекса ([F] + [FS] ). [S] – концентрация субстрата. Кm – константа Михаэлиса. Модель фермент-субстратного комплекса, построенная на основе лабораторных методов определения V3 при изменении [S] и при [F] = константа и приводящая к кинетическому уравнению Михаэлиса – Ментена и составляет основу ферментативной кинетики. Константа Михаэлиса и максимальная скорость – кинетические параметры, отражающие механизм действия фермента, так что они являются основой для понимания того, как действует фермент. Еще большую информацию дают изменения константы Михаэлиса и (или) максимальной скорости, полученной вследствии изменений условий реакций, наличие другого субстрата или благодаря обработки фермента, приводящей к изменению его структуры. Значение константы Михаэлиса и максимальной скорости находят путем анализа кинетических данных. Проанализируем уравнение Михаэлиса – Ментона: 1)Концентрация субстрата постоянна и намного больше концентрации фермента. В таком случае скорость реакции будет зависеть только от концентрации фермента и, если концентрация фермента будет приближаться к концентрации субстрата, то скорость реакции замедлится.   V3  [F0] 2) Допустим, что концентрация фермента постоянна и достаточно высока. Проанализируем в этих условиях уравнение Михаэлиса – Ментона: а) Концентрация фермента намного больше константы Михаэлиса. Тогда в знаменателе [S] мы можем пренебречь; К3, константа Михаэлиса и [F0] – величины постоянные и выходит что скорость реакции зависит прямо пропорционально только от концентрации субстрата в числителе. Но это справедливо только для малых концентраций субстрата, что мы обговорим в предварительных условиях.  V3 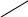  [S]  б) Концентрация субстрата намного больше константы Михаэлиса. Тогда в знаменателе мы можем пренебречь константой Михаэлиса, концентрации субстрата в числителе и в знаменателе сокращаются и получается, что при значительных концентрациях субстрата скорость реакции от концентрации субстрата не зависит. Такую скорость называют максимальной (Vmax). Vmax * [S] 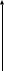  V3 Следовательно: V3 = Km + [S] Так как полное насыщение фермента субстратом, то Vmax = K3 * [FS] = K3 * [E0], то-есть [E0] = [FS], Vmax так как [E] = 0       [S] При достижении максимльной скорости происходит полное насыщение фермента субстратом. Максимальная скорость характеризует каталитическую силу фермента, а также активирующий эффект активатора и силу ингибитора. То-есть, по сути, максимальная скорость выражает эффективность действия фермента. Для сравнения каталитической активности различных ферментов максимальную скорость выражают через количество (в молях) каждого фермента. Такое преобразование приводит к величине, которую называют молярной активностью. Она выражается числом молей субстрата, реагирующего с одним молем фермента за единицу времени (за одну минуту или секунду). Например, карбангидраз, каталаза и так далее. Активнрсть фермента так же можно выражать в единицах ферментативной активности. Одна энергия катализирует превращение субстрата со скоростью 1мкмоль в минуту. Удельная активность – это ферментативная активность, отнесенная на 1 мг белка. Мы уже упоминали, что Км = (К2 + К3) / К1. Но, К1,2,3 нельзя определить практически, так как не известно сколько существует [FS]. Константу Михаэлиса можно рассчитать графически. Допустим , что \/3 = ½ \/мах, то-есть при 50% насыщения фермента субстратом, тогда \/мах/2=(\/мах х [S]) /(Km + [S]), то-есть 2[S]=Км+[S] Получается, что константа Михаэлиса численно равна концентрации субстрата, при которой скорость ферментативной реакции равна ½ максимальной скорости. При этом связывается половина имеющегося фермента. Константу Михаэлиса выражают в единицах концентрции (моль). Для одномолекулярных реакций константа Михаэлиса равна десять в минус второй – десять в минус пятой степени моль. Ферменты могут иметь одинаковые каталитические силы, но разные константы Михаэлиса. Константа Михаэлиса характеризует специфичность фермента к субстрату. Чем меньше константа Михаэлиса, тем выше специфичность, тем быстрее образуется фермент-субстратный комплекс, или фермент-субстратный комплекс быстрее распадается на продукт и фермент, или и то и другое. Активаторы и ингибиторы влияют на константу Михаэлиса и максимальную скорость. Пример, гексакиназа (фермент, катализирующий превращение простых сахаров в фосфоэфиры). Для ее насыщения субстратом на 50% глюкозы требуется в 1000 раз меньше, чем аллозы. О = С – Н О = С – Н | | Н – С – ОН Н – С - ОН | | HO – C – H H – C – OH | | H – C - OH H – C – OH | | H – C – OH H – C – OH | | CH2OH CH2OH      Глюкоза аллоза  \/3  \/мах -| - - - - - - - - |- - - - | _ _ _ |_ _ _ _ _ _ | | | | | | | | | [S] Км Км2 Из этих дух графиков видно, что из этих двух ферментов более специфичен тот, который имеет меньшую величину константы Михаэлиса, так как в этих условиях быстрее достигается максимальная скорость реакции. Определить константу Михаэлиса можно и используя уравнение обратных величин (рассчитанное Лайнуивером - Бэрком), на основании которого строится одноименный график: 1 / \/3 Этот метод называеися методом двойных обратных величин и основан на алгебраическом преобразовании исходного уравнения гиперболы по Михаэлису-Ментону к уравнению прямой.     1 / \/мах  - 1 / Км 1[S] ИНГИБИТОРЫ ФЕРМЕНТОВ. Активность ферментов зависит от действия активаторов и ингибторов ферментов. Соответственно, ингибиторы – это вещества, действие которых снижает активность ферментов, а активаторы – вещества, при действии которых активность ферментов повышается. Различают по специфичности: специфические (антитрипсин) и неспецифические; по месту действия: на активный центр, аллостерические. Антибиотики, ативирусные агенты, противоопухолевые средства, инсектециды и гербициды – о существовании этих средств теперь знают все. Действие многих из них основаго на способности ингибировать (то-есть затормаживать) работу клеточных ферментов, обычно какого-то определенного фермента. Ингибирование ферментов происходит и в природе, представляя собой одну из систем биорегуляции. Ферменты никогда не работают монотонно. Их активность постоянно меняется и в значительной мере зависит от постоянно меняющихся условий внешней и внутренней среды.   Различают обратимое ингибирование: ингибитор + фермент (ингибитор – фермент) и необратимое ингибирование: ингибитор + фермент (ингибитор-фермент). В свою очередь обратимые ингибирование делят на конкурентное и неконкурентное. Конкурентное ингибирование основано на близости структур молекул ингибитора и субстрата, то-есть возникает конкуренция за фермент, за его активный центр. Например, субстратом для действия фермента сукцинатдегидрогеназы является янтарная кислота: СООН СООН | | СН2 - H2 СН F – сукцинатдегидрогеназа.  | || СН2 F СН | | СООН СООН Янтарная Фумаровая кислота кислота Сильнейшим ингибитором этого фермента является малоновая кислота (СООН – СН2 - СООН ): образуется комплекс (фермент-ингибитор), который не дает продукта реакции, так как не может идти дегидрирование. При этом уменьшается число молекул свободного фермета, способного взаимодействовать с субстратом и скорость понижается. Но этот вид ингибирования обратим, его можно пресечь постепенным насыщением среды субстратом, то-есть увеличением его концентрации, то-есть мы можем сделать вывод, что при конкурентном ингибировании существует прямая зависимость от концентраций субстрата и ингибитора. При конкурентном ингибировании максимальная скорость постоянна, но константа Михаэлиса увеличивается (то-есть снижается специфичность) и для достижения максимальной скорости нужно повышать концентрацию субстрата.   1 / \/3 не конкурентное ингибирование  -- конкурентное ингибирование  без ингибирования   1 / Км 1 / [S] Зная принципы конкурентного ингибирования, можно искусственно находить (например, синтезировать) ингибиторы ферментов, что и используется на практике. Например, парааминобензойная кислота используется для синтеза фолиевой кислоты, необходимой для жизнедеятельности микроорганизмов. Ингибитором фермента, катализирующего эту реакцию является сульфаниловая кислота, которая входит в состав сульфаниламидных препаратов (сульфадиметоксин, сульфадимезин и т. д.). Введение этих препаратов ингибирует синтез фолиевой кислоты, не давая возможности жить и развиваться микроорганизмам. COOH SO3H O   | | || N   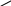 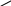  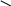 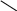 HN __R  1 2 3  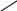  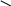 H2N 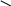  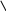   | | NH2 NH2 1 – парааминобензойная кислота; 2 – сульфониловая кислота; 3 – фоливая кислота. Тетрогидрофоливая кислота – это очень важный ко-фермент нескольких ферментов, участвующих в синтезе ДНК и РНК. При введении сульфаниламидных препаратов, немедленно наблюдается ингибирование фермента, катализирующего утилизацию парааминобензойной кислоты (ПАБК) при синтезе фолиевой кислоты. Пониженный уровень фолиевой кислоты приводит к уменьшению синтеза нуклеиновых кислот. Окончательным результатом этих событий является гибель микроорганизмов. Или, на основе урацила получен препарат 5 – фторурацил, который используется для лечения опухолей, так как блокирует синтез нуклеиновых кислот. О | |     HN -- F 5 – фторурацил. O NH Аллопуринол (применяется при лечении конкурентного ингибирования). В некоторых случаях конкурентным ингибированием можно объяснить ингибирующие действие конечного продукта на фермент,участвующий в синтезе этого продукта. Такой тип биорегуляции часто встречается, его называют – ингибирование конечным продуктом. Неконкурентные ингибиторы взаимодействуют не со всем активным центром, а с отделными функциональными группами в каталитической зоне. Такие ингибиторы имееют химическое сродство к какой-либо функциональной группе. Например, ионы серебра, ртути являются тиоловыми ядами, то-есть блокируют тиогруппы. Цианиды – соли синильной кислоты, являются дыхательными ядами, они связывают двух- и трехвалентное железо в составе простетической группы сложных белков-ферментов. Могут связываться и другие группы (карбоксильная, гидроксо- и т.д.). Притаком виде ингибировании повышение концентрации субстрата (чтобы прекратить ингибирование) не эффективно. Этот вид ингибирования можно убрать, вытесняя ингибитор из фермента. Например, в случае действия тиоловых ядов, добавляют вещества, имеющие тиогруппу (тиолы), например, цистеин. При этом виде ингибирования константа Михаэлиса является постоянной, то-есть специфичность не меняется, но уменьшается максимальная скорость, то-есть снижается каталитическая сила. К такого рода ингибиторам относятся: иприт, люизит. Снижение каталитической силы фермента (то-есть уменьшение максимальной скорости) при неизменной константе Михаэлиса возможно в случае, когда субстрат имеет одинаковое сродство к ферменту и фермент-ингибиторному комплексу, а ингибитор – к ферменту и к фермент-субстратному комплексу. Если сродство субстрата и ингибитора к ферменту и соответствующему комплексу различно (а чаще бывает, что так и есть), то меняются и максимальная скорость и константа Михаэлиса. Это во многих случаях характерно для ингибирования конечными продуктами. |
