Цитология методичка 1-15 сабак. Саба 1 Апаратты дидактикалы топтама
 Скачать 1.99 Mb. Скачать 1.99 Mb.
|
|
SOS-репарациясы. Егер жоғарыда айтылған репарациялық жүйелер арқылы ДНҚ молекуласындағы өзгерістерді жөндлмей қалып қойса, ал жасуша репликациялану сәтіне жетсе не болады? Репликация үрдісі бірінші түзетілмеген зақымдалған жерге келгенде тоқтап, ондай зақымдаулар өте көп болса, жасуша жойылуы қажет. Мұндай жағдайда жасушада, 1974 жылы югославиялық ғалым Мирослав Радманмен ашылған, қауіпті репарация механизмі іске асады. Мұндай жағдайда арнайы ақуыздар синтезі іске қосылып, ДНК полимеразамен кешен түзіп, оның жұмысын «дөрекілендіретін» осындай «бұзылған» кешен ДНҚ молекуласының жаңа тізбегін матрицалық тізбектегі қателіктерге қарама-қарсы синтездейді, бірақ, жаңа синтезделген ДНҚ тізбегінде көптеген қателіктер, мутациялар пайда болатындығын анықтады. SOS-репарациялар нәтижесінде жасуша бұл кезеңдегі жойылудан аман қалады: оның ДНҚ молекуласы қателіктермен болса да екі еселеніп, жасушаның бөлінуі жүре алады, бірақ, бәрібір де өмірлік маңызды қызметтерге зақым келген болса, мұндай жасушалар кейінірек дұрыс қызымет атқара алмау нәтижесінде жойылады. Егер де, пайда болған мутациялар летальды әсер етпесе, жасуша жақсылы-жаманды болса да тіршілігін сақтайды және оның келесі ұрпақтарының бәрі бір уақытта болған осы мутациялық апаттың зардабын ұрпақтарына беріп отырады. Репарациялық жүйедегі ақаулықтар және тұқымқуалайтын аурулар. Арнайы бақылаулар арқылы сүтқоректелердің және адамдардың ұрық жасушалары линияларының геномында жылына 6 нуклеотидтік алмасулар болатындығы анықталған. Сомалық жасушаларда да осындай мутациялар болуы мүмкін. Олардың жылдар бойы жинақталуы, жас ұлғайған сайын рак жасушаларының пайда болу қаупін жоғарлатады. Жалпы алғанда, барлық рак ауруларының 80 - 90% ДНҚ репарациясының іске аспауымен байланысты. Қазіргі уақытта жасушаның өзгерістерді жөндей алу қабілетімен тек мутациялар ғана емес, сонымен қатар, тұқым қуалайтын аурулардың және ісіктердің пайда болуы, қартаю сияқты түбегейлі үрдістер толығымен байланысты екендігі анық. Көптеген тұқымқуалайтын аурулар да репарация жүйесінің қызметінің дұрыс болмайына байланысты. Оларға жатады: 1) пигменттік ксеродерма (тері пигментациясының өзгеруі, тері жамылғысының мүйіздену, эпидермистегі атрофикалық өзгерістер, дәнекер ұлпаларының дистрофиясы, қатерлі ісіктер; 2) триходистрофия (шаш жасушаларында күкірттің жеткіліксіздігі нәтижесінде олардың сыңғыш болуы, тері мен тістердің аномалиялары, жыныстық жетілудегі бұзылыстар; 3) Коккейн синдромы (бойдың қысқалығы, кереңдік, көру нервісінің атрофиясы т.б.); 4) Фанкони анемиясы (қанның барлық элементтерінің санының азаюы, қаңқадағы өзгерістер, микроцефалия, кереңдік) және т.б. аурулар. Гендік (нүктелік) мутациялардың молекулалық-генетикалық механизмдері Гендік мутациялар (нүктелік мутациялар немесе трансгенациялар) дегеніміз бұл – ДНҚ молекуласында бір геннің нуклеотиттер қатарын қамтитын құрылысындағы өзгерістер. Гендік мутацияның себептері бұл – физикалық, химиялық және биологиялық мутагендік факторлар. Көбінде, химиялық мутагендік факторлар ДНҚ молекуласындағы өзгерістерге алып келеді. Гендік муатациялар екі классқа бөлінеді: 1) репликация қателіктері – жұп негіздердің алмасуы. Азоттық негіздердің алмасуы. Аталған мутациялардың себептері: а) репликация қателіктері; б) арнайы химииялық агенттердің әсері. Химиялық агенттер әсерінен қосылған нуклеотидтің азоттық негіздерінің құрылысы өзгеруі мүмкін. Синтезделіп жатқан ДНҚ молекуласына негізі өзгерген нуклеотидтің қате жалғануы себеп болуы мүмкін. Егер бұл өзгеріс репарация ферменттері арқылы анықталмайтын болса, өзгерген негіз репликация үдерісіне қатысып, жұп негіздердің басқа негізге алмасуына алып келеді. Бір пуриндік негіздің (аденин) басқа пуриндік негізге (гуанин), бір пиримидиндік негіздің (цитозин) басқа пиримидиндік негізге (тимин) алмасуы транзиция деп аталады. Бір пуриндік негіздің (адениннің немесе гуаниннің) пиримидиндік негізге (цитозинге немесе тиминге) алмасуы трансверсия деп аталады. Азоттық негіздің алмасуынан болатын мутация алғашында ДНҚ молекуласының бір тізбегінде болады. Егер ол өзгерістер репарация механизмдері арқылы түзетілмесе, келесі репликация кезінде өзгерістер ДНҚ молекуласының екі тізбегінде де сақталып қалады. 2) оқылу ретінің жылжуы (фреймшифт) – нуклеотидтердің түсіп қалуы немесе қосылуы нәтижесінде болады. Мұндай мутациялар жиірек кездеседі және жасуша үшін қауіпті. Аталған өзгеріс ДНҚ молекуласына кейбір химиялық элементтер әсер еткенде, сонымен қатар, радиоактивті сәулелену нәтижесінде орын алады. Осындай өзгерістер салдарынан полипептидтік тізбектің аминқышқылдық құрамының, ақуыздың құрылысы мен қызыментінің бұзылуы, фенотиптің өзгеруі болады. Инверсия – мутацияның бұл типі ДНҚ молекуласының белгілі бір бөлігінің 180° бұрылуынан болады. Бұл өзгерістер химиялық агенттердің және кейбір физикалық факторлардың репликация және рекомбинация үрдістерінің молекулалық-генетикалық механизмін бүзуы нәтижесінде орын алады. Экзондардағы өзгерістердің бірнеше типін ажыратуға болады: Миссенс-мутациялар –триплетті кодтайтын нуклеотидтің өзгеруі нәтижесінде оның басқа кодтаушы триплетке алмасуы, яғни триплеттің мағынасының өзгеруі. Миссенс мутациялар кодондағы ақпараттың өзгеруіне және ақуыздың аминқышқылдық құрамының өзгеруіне алып келеді. Бұл гендік мутациялардың негізгі классы болып табылады. Нонсенс-мутациялар – триплеттегі нуклеотидтің өзгеруі нәтижесінде оның нонсенс триплетке немесе мағынасыз триплетке алмасуы. 64 кодонның үшеуі терминалды, яғни ақуыз синтезін тоқтататын (УАА, УАГ, УГА) кодондар болып табылады. Нонсенс-мутациялар нәтижесінде трансляция үрдісі терминалды кодон кездескен жерде тоқтайды. Нәтижесінде ген тек полипептидттік тізбектің үзіндісін ғана синтездей алу кабілетіне ие болады. Сеймсенс – мутациялар генетикалық кодтың артықтылық қасиеті нәтижесінде триплеттің кодтау мүмкіндігі өзгермейді, яғни ақуыздың аминқышқылдық құрамы алмаспайды. Сплайсинг –мутациялар экзон мен интронның түйіскен жерінде пайда болып, сплайсингтің донорлық немесе акцепторлық сайттарын өзгерту арқылы ақпараттың іске асуын бұзады. Гендік мутациялардың жеке бір категориясына геннің промоторлық немесе кодтаушы бөлігіндегі триплеттердің қайталанулар санының артуынан болатын «динамикалық» мутацияларды жатқызуға болады. Мутацияның мұндай типтері тек адамдарда ғана анықталған. Динамикалық мутациядан болатын, экспансия ауруларының ондаған нозологиялық формалары тіркелген және бұл тізім үнемі толықтырылуда. Бұл аурулардың этиологиясы триплеттер қайталанулар (CGG)n, (CTG)n, (CAG)n экспансиясымен байланысты. «Экспансия ауруларының» барлығына бас миының құрылымының өзгеруі тән болып келеді. Аурудың ауырлығы, оның басталуы қайталанулар санына қарай ауытқып отырады. Сонымен қатар, мутациялар геннің реттеуші бөлімінде (промоторда, энхансерде, сайлансерде және атеннюаторда) болуы мүмкін. Мұндай гендік мутаациялар регуляторлық мутациялар деп аталады. Олар ақуыздың немесе ферменттің синтезінің азаюына, артуына немесе тоқтап қалуына алып келеді. Нейтралды мутация — рецессивті мутациялар гетерозиготалы генотипте фенотипте жарыққа шықпайды, яғни бейтарап болады. Гендік мутация нәтижесінде молекулалық деңгейде келесі өзгерістер болуы мүмкін: аномальды ақуыздың синтезделуі; ген өнімінің синтезінің артуы; алғашқы өнім синтезінің болмауы; қалыпты алғашқы ген өнімінің синтезінің төмендеуі. Гендік мутациялардың механизмдерін зерттеудің және түсінудің болашақ дәрігерлер үшін үлкен теориялық және тәжірибелік мәні бар. Өйткені, адамның көптеген тұқымқуалайтын ауруларының себебі гендік мутациялар болып табылады. Гендік мутациялардың пайда болу механизмдерін білу адамның гендік ауруларының патологиялық үдерістерінің мәнін түсінуге, диагностикалау әдістерін ойластыруға, емдеуге және алдын-алу жұмыстарын жүргізуге мүмкіндік береді. Сабақ 14. Қатерлі ісік дамуының молекулалық механизмдері Рак – кең таралған және қауіпті инфекциялық емес аурулардың бірі. «Рак» (cancer) термині әлем бойынша барлық қатерлі жаңа түзілістерді атауға қолданады. Ісік немесе жаңа түзілістер – бұл жасушалардың өсуіне әсер ететін фактордың болмауына қарамастан, олардың бақыланусыз бөлінуінен ұлпа көлемінің шамадан тыс (қалыпты емес) өсуі. Қалыпты жағдайда (дені сау ағзада) жасушалардың бөліну үрдісі бірін-бірі теңестіріп отыратын, бөлінуді симулдайтын және тежейтін, екі факторлармен бақыланып отырады. Мутация нәтижесінде жасушаның бөлінуінің реттелуі бұзылған жағдайда, олар көбейіп, ісік деп аталатын масса түзеді. Қалыпты жасушаның трансформацияланған (ісік) жасушаға айналу үрдісі онкогенез немес канцерогенез деп аталады. Бұл өте күрделі, көп сатылы, жылдар бойы кейде ондаған жылдарды қамтитын ұзақ үрдіс. Рак полиэтиологиялық немесе көп факторлы ауруға жатады. Жасушаның ісіктік трансформациясына алып келетін факторларды - канцерогендік факторлар деп атайды. Олар жіктеледі: 1. Физикалық канцерогендер: иондаушы сәулелер (лейкоздар, сүйектің, қалқанша безінің рагі), ультракүлгін сәулелері (тері рагі) және т.б.. Иондаушы сәулелердің канцерогендік фактор ретінде маңызы жылдан-жылға артуда. Адамдар иондаушы сәулені медицинада қолданудан бастап, атом электр станцияларындағы апаттар нәтижесінде алуы мүмкін. 2. Химиялық канцерогендер: полицикды ароматты көмірсулар; гетероциклды ароматты көмірсулар; ароматты аминдер; аминдік қосылыстар; нитро қосылыстар; афлатоксиндер; (уретан, винилхлорид, металлдар, пластмасса және т.б.). Кейбір химиялық заттар тікелей канцерогендер болып табылса, кейбірі ағзадағы метаболиттік үдерістерден кейін канцерогендік әсерге ие болады. 3. Биологиялық канцерогендер: вирустар (ДНҚ-лы немес РНҚ-лы). Кейбір вирустардың геномында онкогендік белсенділігі бар гендер болады. Қатерлі жаңа түзілістер генетикалық өзгерген бір ғана жасушадан дамиды. Алайда, кейдір қатерлі жаңа түзілістер тұқым қуалап беріледі. Оларға алып келетін мутациялар, негізінен ДНҚ репликация кезіндегі қателіктерден немесе канцерогендік факторлар әсерінен сомалық жасушаларда болады. Әдетте, жасушаның тек генетикалық материалының зақымдалуы ісікке (ісіктік трансформация) айналуға жеткіліксіз. Белгілі ұзақ уақыт аралығында бірнеше ген өнімін бұзатын 5-10 мутациялардың жинақталуы қатерлі жаңа түзілістердің пайда болуына алып келеді. Мұндай жағдайда қалыпты жасушаларда мутация әсерінен протоонкогендер онкогенге айналуы мүмкін. Сонымен қатар, ісікке қарсы супрессорлық гендердің және репарация жүйесінің гендерінің мутациясы да ісіктік трансформацияға алып келеді. 1-сурет.      Мутагендік факторлар (радиация, химиялық канцерогендер, вирустар, бос радикалдар, өсу факторлары)                 Протоонкогендер p53 супрессорлық геннің мутациясы Жасуша репарация жүйесінің зақымдалуы Онкогендер p53 геніндегі ақаулық супрессорлық белсенділіктің тоқтауы Апоптоз супрессорлары гендерінің белсенді болуы апоптоза Гендердің амплификациясы. Хромосомалық қайта құрылулар. Жасушаның тоқтаусыз көбеюі. Атиптік клондардың түзілуі атипичных (опухолевых) клеток 1-сурет. Мутациялық канцерогенездің сызбасы Жасушаның ісікке айналуына алып келетін арнайы гендер топтары (класс) бар. Бұл гендер онкогендер деп аталады. Қазіргі уақытта әдебиеттерде 100-ден астам вирустық онкогендер және соған сайкес протоонкогендер сипатталған. Протоонкогендер жасушалардың бөлінуін, жіктелуін, жасуша рецепторларының қызмет атқаруын, ДНҚ репарациясын және сырттан келетін сингалдарға жауап реакцияларын қамтамасыз ететін маңызды гендер тұқымдастары болып табылады. Бұл гендердің өнімдері өсу факторлары деп аталатын ақуыздар болып табылады. Протоонкогендер жасушалық онкогенге екі жолмен айналуы мүмкін. Олардың бірі онкоген өнімінің шамадан тыс көбеюі, екіншісі протоонкогеннің кодтаушы бөлігіндегі қатарлардағы мутациялар арқылы іске асады. Онкоген өнімдерінің артуы, инсерцтік мутация және геннің амплификациясы арқылы да болады. Ретровирустар онкогендері қожайын геномындағы онкогендер жанына немесе тікелей генге ену арқылы геннің промоторы ретінде әсер етіп, оның қарқынды экспрессиясына алып келеді. Бұл құбылыс «ендірме» канцерогенез деген атауға ие. Сонымен қатар, жасуша үшін күйзеліс жағдайында протоонкогендердің амплификациялануы жүреді. Бұл құбылыс - протоонкогеннің амплификациясы (көшірмелерінің көбеюі) олардың белсенділігін артырып, протоонкоеннің онкогенге айналуына алып келеді. Хромосоманың транслокациясы арқылы протоонкогенге жаңа транскрипциялық промотордың жалғануы нәтижесінде протоонкоген тоқтаусыз жұмыс істеп, ақуыздар үнемі бақылаусыз синтезделіп, онкогенге айналады. Кейбір гендік (нүктелік) мутациялар протоонкогенмен синтезделетін ақуыз құрылымын өзгертеді, мысалы оның қызметін бақылайтын ингибиторлармен байланысу орталығының өзгеруіне алып келеді. Ақуыз үнемі белсенді болуы үрдістің бақылаусыз жүруіне жағдай жасайды. Осылайша, протоонкогеннің онкогенге айналуының ең басты және жалпы механизімің негізінде, протоонкогеннің белсенділігі мен бақылауының қалыпты үрдісінің бұзылуы жатыр. 2-сурет. 2-сурет. Протоонкогеннің онкогенге айналуы                     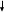   ПРОТООНКОГЕН нүктелік мутация амплификация инсерцтік мутация хромосома транслокациясы Протоонкогеннің жасушалық онкогенге айналуы Онкоақуыздың қарқынды синтезделуі Жасушаның қарқынды бөлінуі және жіктелуінің бұзылуы Ісіктік трансформация, инвазивті өсу, метастаз беру Жасушаның ісіктік трансформациясында онкогендерден басқа да гендер қатысады. Геномда ағзаны және оның жасушаларын канцерогендік факторлар әсерінен, сонымен қатар олардың ісіктік трансформациясынан қорғайтын гендер де бар. Оларды ісіктің супрессорлық гендері немесе антионкогендер деп атайды. Ісіктің супрессорлық гендері қалыпты жағдайда, онтогенездің белгілі кезеңдерінде жасушаның пролиферациясын бастырмалайды, яғни протоонкогендердің экспрессиясын реттейді (тежейді). Супрессор гендердің мутациялары құрылымы мен қызметі бұзылған ақуыздардың синтезделуіне және түрлі мүшелер мен жүйелердегі ісіктік трансформацияның басталуына әкеледі. Қазіргі уақытта 20-ға жуық ісіктің супрессорлық гендері анықталған. Олардың мутациялары ісіктің дамуына алып келеді. Супрессорлық гендерде жиі кездесетін мутациядардың түрлері - геннің кодтаушы бөлігінде жүретін миссенс мутациялар және нүктелік делециялар. p53 және Rb антионкогендері жақсы зерттелген. Ретинобластомада (жиілігі — 20 мың баланың ішінде біреуінде) Rb генінің қызметінің тоқтауы байқалады. 60% жағдайда ретинобластома спорадикалды түрде дамиды, ал 40% жағдайда аутосомды-доминантты түрде тұқым қуалап беріледі. Rb генінің тұқым қуалайтын ақаулығы жағдайында, екінші аллелі қалыпты, сондықтан ісіктің дамуы тек екінші (қалыпты) аллелде қосымша мутация болған жағдайда жүруі мүмкін. Спонтанды түрде дамитын ретинобластомада Rb геннінің қызметінің тоқтауы екі алеллді де бірдей қамтиды (3-сурет). 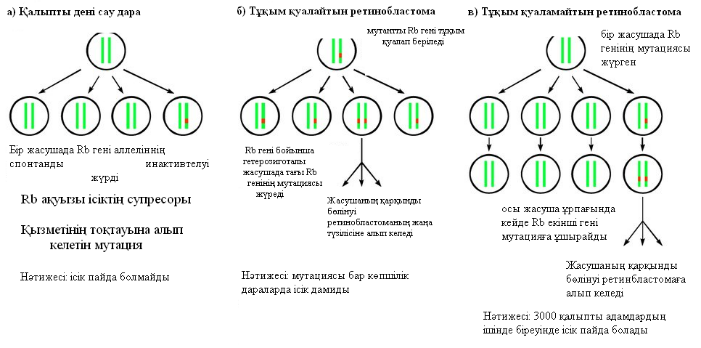 |
