кроветворная система. Селезенка
 Скачать 1.32 Mb. Скачать 1.32 Mb.
|
|
Селезенка - Селезенка, lien (греч. splen), представляет собой богато васкуляризованный лимфоидный орган. 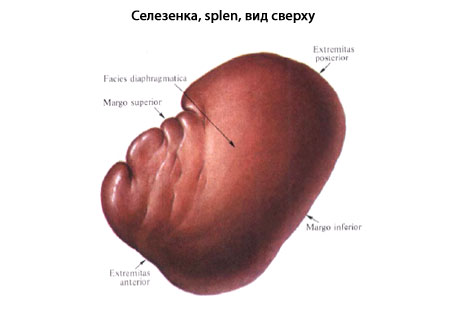 В селезенке кровеносная система входит в тесное соотношение с лимфоидной тканью, благодаря чему кровь здесь обогащается свежим запасом развивающихся в селезенке лейкоцитов. Кроме того, проходящая через селезенку кровь освобождается благодаря фагоцитарной деятельности макрофагов селезенки от отживших красных кровяных телец («кладбище» эритроцитов) и от попавших в кровяное русло болезнетворных микробов, взвешенных инородных частиц и т. п. В селезенке кровеносная система входит в тесное соотношение с лимфоидной тканью, благодаря чему кровь здесь обогащается свежим запасом развивающихся в селезенке лейкоцитов. Кроме того, проходящая через селезенку кровь освобождается благодаря фагоцитарной деятельности макрофагов селезенки от отживших красных кровяных телец («кладбище» эритроцитов) и от попавших в кровяное русло болезнетворных микробов, взвешенных инородных частиц и т. п. 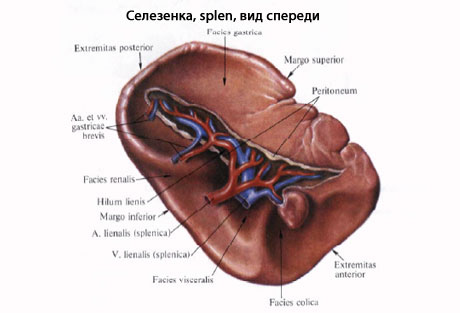 Величина селезенки благодаря богатству сосудами может довольно значительно изменяться у одного и того же человека в зависимости от большего или меньшего наполнения сосудов кровью. В среднем длина селезенки равняется 12 см, ширина 8 см, толщина 3-4 см, масса около 170 г (100-200 г). Во время пищеварения наблюдается увеличение селезенки. Величина селезенки благодаря богатству сосудами может довольно значительно изменяться у одного и того же человека в зависимости от большего или меньшего наполнения сосудов кровью. В среднем длина селезенки равняется 12 см, ширина 8 см, толщина 3-4 см, масса около 170 г (100-200 г). Во время пищеварения наблюдается увеличение селезенки.Цвет селезенки на поверхности темно-красный с фиолетовым оттенком. По форме селезенку сравнивают с кофейным зерном. В селезенке различают две поверхности (facies diaphragmatica и facies visceralis), два края (верхний и нижний) и два конца (передний и задний). Наиболее обширная и обращенная в латеральную сторону facies diaphragmatica выпукла, она прилежит к диафрагме. На висцеральной вогнутой поверхности, на участке прилежащем к желудку (facies gastrica), имеется продольная борозда, hilus lienis - ворота, через которые в селезенку входят сосуды и нервы. Кзади от facies gastrica находится продольно расположенный плоский участок, это - facies renalis, так как здесь селезенка соприкасается с левыми надпочечником и почкой. Близ заднего конца селезенки заметно место соприкосновения селезенки с colon и lig. phrenicocolicum; это - facies colica. Топография селезенки. Селезенка расположена в левом подреберье на уровне от IX до XI ребра, длинник ее направлен сверху вниз и кнаружи и несколько вперед почти параллельно нижним ребрам в их задних отделах. Различают высокое положение селезенки, когда передний полюс ее достигает VIII ребра (наблюдается при брахиморфном телосложении), и низкое, когда передний полюс лежит ниже IX ребра (наблюдается при долихоморфном типе телосложения). Брюшина, срастаясь с капсулой селезенки, покрывает ее со всех сторон, за исключением ворот, где она загибается на сосуды и переходит на желудок, образуя lig. gastrolienale. От ворот селезенки к диафрагме близ места входа пищевода тянется складка брюшины (иногда отсутствует) - lig. phrenicolienale. Кроме того, lig. phrenicocolicum, растянутая между colon tranusversum и боковой стенкой живота, в области левого XI ребра образует род кармана для селезенки, которая своим нижним концом упирается в эту связку. Строение. Кроме серозного покрова, селезенка обладает собственной соединительнотканной капсулой, tunica fibrosa, с примесью эластических и неисчерченных мышечных волокон. 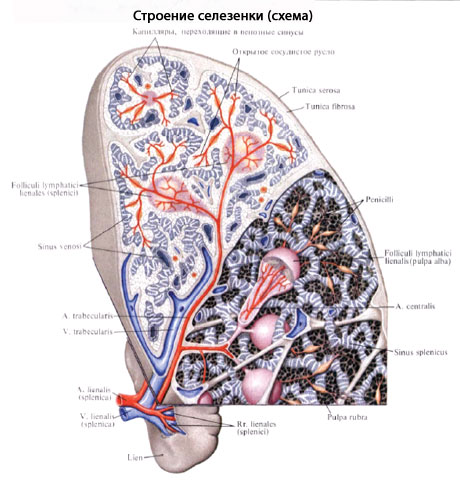 Капсула продолжается в толщу органа в виде перекладин, образуя остов селезенки, разделяющей ее на отдельные участки. Здесь между трабекулами находится пульпа селезенки, pulpa lienis. Пульпа имеет темно-красный цвет. На свежесделанном разрезе в пульпе видны более светло окрашенные узелки - folliculi lymphatici lienales. Они представляют собой лимфоидные образования круглой или овальной формы, около 0,36 мм в диаметре, сидящие на стенках артериальных веточек. Пульпа состоит из ретикулярной ткани, петли которой наполнены различными клеточными элементами, лимфоцитами и лейкоцитами, красными кровяными тельцами, в большинстве уже распадающимися, с зернышками пигмента. Капсула продолжается в толщу органа в виде перекладин, образуя остов селезенки, разделяющей ее на отдельные участки. Здесь между трабекулами находится пульпа селезенки, pulpa lienis. Пульпа имеет темно-красный цвет. На свежесделанном разрезе в пульпе видны более светло окрашенные узелки - folliculi lymphatici lienales. Они представляют собой лимфоидные образования круглой или овальной формы, около 0,36 мм в диаметре, сидящие на стенках артериальных веточек. Пульпа состоит из ретикулярной ткани, петли которой наполнены различными клеточными элементами, лимфоцитами и лейкоцитами, красными кровяными тельцами, в большинстве уже распадающимися, с зернышками пигмента.Функция. В лимфоидной ткани селезенки содержатся лимфоциты, участвующие в иммунологических реакциях. В пульпе осуществляется гибель части форменных элементов крови, срок деятельности которых истек. Железо гемоглобина из разрушенных эритроцитов направляется по венам в печень, где служит материалом для синтеза желчных пигментов. Сосуды и нервы. Сравнительно с величиной органа селезеночная артерия отличается крупным диаметром. Близ ворот она распадается на 6-8 ветвей, входящих каждая отдельно в толщу органа, где они дают мелкие веточки, группирующиеся в виде кисточек, penicilli. Артериальные капилляры переходят в венозные синусы, стенки которых образованы эндотелиальным синцитием с многочисленными щелями, через которые кровяные элементы и попадают в венозные синусы. Начинающиеся отсюда венозные стволики в отличие от артериальных образуют между собой многочисленные анастомозы. Корни селезеночной вены (вены 1-го порядка) выносят кровь из относительно изолированных участков паренхимы органа, называемых зонами селезенки. Под зоной подразумевается часть внутриорганного венозного русла селезенки, которая соответствует распределению вены 1-го порядка. Зона занимает целый поперечник органа. Кроме зон, выделяют еще сегменты. Сегмент представляет собой бассейн распределения вены 2-го порядка; он составляет часть зоны и располагается, как правило, по одну сторону от ворот селезенки. Количество сегментов варьирует в больших пределах - от 5 до 17. Наиболее часто венозное русло состоит из 8 сегментов. В зависимости от положения в органе они могут быть обозначены как передний полюсной сегмент, передний верхний, передний нижний, средний верхний, средний нижний, задний верхний, задний нижний и задний полюсной сегмент. Селезеночная вена впадает в v. portae. Пульпа не содержит лимфатических сосудов. Нервы от plexus coeliacus проникают вместе с селезеночной артерией. Селезенка - непарный паренхиматозный орган, расположенный глубоко в заднем отделе левого подреберья. Брюшина покрывает ее со всех сторон, кроме ворот органа. Наружная поверхность селезенки прилежит к реберной части диафрагмы. Зона проекции ее соответствует левому реберно-диафрагмальному синусу и может быть определена при перкуссии. В норме селезенка проецируется между IX и XI ребром по средней подмышечной линии, не выходя вперед за переднюю подмышечную линию. Задний конец селезенки отстоит от позвоночника на 4-6 см и соответствует уровню Х-ХI грудных позвонков. Селезенка имеет продолговатую или овальную форму. Крайние формы селезенки - короткая и широкая (у детей), длинная и узкая (у взрослых ). В ней различают два конца или полюса, задний - закругленный, обращенный к позвоночнику, и передний - заостренный, направленный к реберной дуге, а также две поверхности - наружную (диафрагмальную) и внутреннюю (висцеральную). Размеры селезенки непостоянны. Длина ее чаще 12-14 см, ширина - 8-10 см и толщина - 3-4 см.На внутренней поверхности, в центральной части по продольной оси находятся ворота селезенки. Аномалии развития - врожденное отсутствии селезенки, недоразвитие ее, наличие добавочных селезенок и др. Селезенка обладает подвижностью, т.к. связана с подвижными органами (желудок, диафрагма). Связочный аппарат, кровоснабжение Связки селезенки образованы листками брюшины, идущими от соседних органов и стенок брюшной полости в основном к воротам органа. Различают желудочно-селезеночную, диафрагмально-селезеночную, поджелудочно-селезеночную связки. В фиксации селезенки диафрагмально-селезеночная связка выполняет основную функцию, в ней содержатся сосудисто-нервные образования селезенки. В связке выделяют два листка брюшины, идущие от поясничной части диафрагмы. Задний листок подходит к заднему краю ворот селезенки, покрывает ее почечную поверхность, а передний листок с ножек диафрагмы - к воротам селезенки, где и соединяется с задним листком. Нижний участок переднего листка, натянутый от хвоста поджелудочной железы к воротам селезенки - поджелудочно-селезеночная связка. Диафрагмально-ободочная связка - дупликатура брюшины, тянется от нижней поверхности диафрагмы к левому изгибу поперечной ободочной кишки и замыкает снизу слепой карман, куда спускается передний конец селезенки. Различают наружную фиброзную оболочку, которая тесно сращена с висцеральной брюшиной, трабекулы и пульпу. Фиброзная капсула прочна, эластична и растяжима, способствует предотвращению разрыва паренхимы при травме. Основным источником кровоснабжения органа является селезеночная артерия, отходящая от чревного ствола. Артерия отдает ряд ветвей к телу и хвосту поджелудочной железы, к желудку и большому сальнику. В воротах она делится на 2 ветви - верхнюю и нижнюю. Верхняя - к верхней (задней) половине, нижняя - к нижней (передней). Вены селезенки собираются в селезеночную вену. В селезеночную вену впадают короткие вены желудка, левая желудочно-сальниковая вена, вены хвоста и тела поджелудочной железы, а также нижняя брыжеечная вена. Селезенка Селезенка, lien(splen), орган кровеносной и лимфатической системы, расположенный в области левого подреберья, между диафрагмой и желудком. Селезенка имеет форму кофейного боба с одной выпуклой, другой вогнутой поверхностью. Длина селезенки 12 см, ширина 7-8 см, толщина 3-4 см, масса 150-200 г. Однако размеры и масса селезенки индивидуальны и физиологически очень изменчивы. Цвет селезенки буровато-красный, консистенция мягкая, на разрезе она состоит из белого и красного вещества - мякоти селезенки. Своей длинной осью она расположена почти параллельно нижним ребрам; сверху, сзади вниз и вперед. В селезенке различают поверхности: выпуклую наружную, обращенную к диафрагме - диафрагмальную поверхность, facies diaphragmatica, и несколько вогнутую внутреннюю, обращенную к желудку и другим органам, - висцеральную поверхность, facies visceralis. Обе поверхности селезенки отделены одна от другой верхним и нижним краями: тупой нижний край. margo inferior, обращен назад и вниз, острый верхний край, margo superior, спереди и кверху; он несет на себе две или три вырезки. Оба края сходятся у концов селезенки. Различают задний конец. cxtremitas posterior, обращенный кверху и назад к позвоночнику, и передний конец, extremitas anterior, обращенный вниз и вперед к левой реберной дуге. Широким размером селезенка проецируется на грудную клетку между IX и XI левым ребром по средней подмышечной линии: задний конец ее на 4-5 см не достигает позвоночного столба, передний конец проецируется на группой клетке по передней подмышечной линии. Диафрагмальная, выпуклая, поверхность селезенки гладкая. Висцеральная поверхность слегка вогнута; она несет на себе отпечатки нескольких прилегающих к ней органов. По середине внутренностной поверхности, занимая 2/, длины, расположено несколько углублений, составляющих борозду ворот селезенки, liilus lienis, - место вхождения в паренхиму нервов и сосудов. Ворота селезенки оставляют свободным небольшой участок у заднего конца и больший - у переднего и делят висцеральную поверхность селезенки - facies visceralis -на боковую и медиальную половины. Половина селезенки, расположенная латерально (кверху) от ворот, представляет собой участок прилегания желудка и называется желудочной поверхностью, facies gastrica; на желудке она соответствует задней поверхности его тела, примыкающей около дна к большой кривизне. Медиальная половина висцеральной поверхности селезенки соответствует месту прилегания левого надпочечника и левой почки - почечная поверхность, facies renalis. К переднему концу медиальной половины селезенки, у самых ее ворот, примыкает конец хвоста поджелудочной железы. Ниже, занимая участок у extremitas anterior, прилежит левый, селезеночный, изгиб ободочной кишки - ободочная поверхность, facies colica. Селезенка одета со всех сторон висцеральной брюшиной; лишена брюшины только висцеральная поверхность на протяжении ворот, где входят селезеночные сосуды, a. et v. lienales, нервы. От ворот селезенки идут две брюшинные связки - желудочно-селезеночная и диафрагмально-селезеночная, lig. gastro-lienale et lig. phrenicolienale, представляющие продолжение одна другой; они являются левой частью дорсальной брыжейки желудка, в которую как бы вставлена сбоку селезенка (см. "Брюшина"). В составе желудочно-селезеночной связки к воротам селезенки подходит хвост поджелудочной железы. Передний конец селезенки, направленный вниз и вперед, покоится на левой диафрагмально-ободочной связке, соединяющей левый изгиб ободочной кишки с париетальной брюшиной диафрагмы, lig. phrenicocolicum sinistrum, и ограничивает селезеночное углубление, recessus lienalis. сальниковой сумки. Нередко в желудочно-селезеночной связке могут находиться небольшие добавочные селезенки, lien accessorius. Строение селезенки. Селезенка покрыта серозной оболочкой, tunica serosa, и соединительнотканной волокнистой оболочкой, tunica fibrosa. От фиброзной оболочки в глубь органа проходят перегородки - перекладины селезенки, trabeculae lienis, которые могут соединяться друг с другом либо свободно заканчиваться. В составе волокнистой оболочки и перекладин имеются гладкие мышечные волокна. Перекладины составляют соединительнотканный остов селезенки. Пространство между перекладинами заполнено мякотью селезенки, pulpa lienis. состоящей из нежной ретикулярной ткани, ячейки которой наполнены различными видами кровяных клеток, и из густого сплетения кровеносных сосудов. По ходу артерии в селезенке образуются селезеночные лимфатические фолликулы, folliculi lymphatic! lienales. Артерии селезенки переходят в расширенные вены, из которых красные кровяные тельца попадают в синусы селезенки, sinus lienis. Лимфатические фолликулы составляют белую мякоть селезенки: пространства ретикулярной ткани, заполненные красными кровяными тельцами, составляют ее красную мякоть. Иннервация: plexus lienalis (периартериальное сплетение по ходу селезеночной артерии). Кровоснабжение: a. lienalis. http://www.eurolab.ua/anatomy/system/hematogenic/Кроветворная система - Костный мозг — важнейший орган кроветворной системы, осуществляющий гемопоэз, или кроветворение — процесс создания новых клеток крови взамен погибающих и отмирающих. Он также является одним из органов иммунопоэза. Для иммунной системы человека костный мозг вместе с периферическими лимфоидными органами является функциональным аналогом так называемой фабрициевой сумки, имеющейся у птиц. Костный мозг — единственная ткань взрослого организма, в норме содержащая большое количество незрелых, недифференцированных и низкодифференцированных клеток, так называемых стволовых клеток, близких по строению к эмбриональным клеткам. Все другие незрелые клетки, например незрелые клетки кожи, всё же имеют большую степень дифференцировки и зрелости, чем клетки костного мозга, и имеют уже заданную специализацию.Содержание [убрать] 1 Красный костный мозг 2 Чувствительность к цитостатикам и излучению [править] Красный костный мозг Gray's Anatomy Клетки красного костного мозга. Красный, или кроветворный, костный мозг у человека находится, в основном, внутри тазовых костей и, в меньшей степени, внутри эпифизов длинных трубчатых костей и, в ещё меньшей степени, внутри тел позвонков. Он состоит из фиброзной ткани стромы и собственно кроветворной ткани. В кроветворной ткани костного мозга выделяют три ростка, или три клеточных линии (англ. cell lines), три популяции клеток, являющиеся родоначальниками соответствующих клеток крови — лейкоцитарный, эритроцитарный и тромбоцитарный ростки. Все эти клеточные ростки имеют общих предков — так называемые плюрипотентные стволовые клетки-предшественники, которые при созревании и дифференцировке идут по одному из трёх путей развития. Костный мозг в норме защищён барьером иммунологической толерантности от уничтожения незрелых и созревающих клеток собственными лимфоцитами организма. При нарушении иммунологической толерантности лимфоцитов к клеткам костного мозга развиваются аутоиммунные цитопении, в частности аутоиммунные тромбоцитопении, аутоиммунные лейкопении, и даже апластическая анемия. Количество полипотентных стволовых клеток, то есть клеток, которые являются самыми первыми предшественниками в ряду кроветворных клеток, в костном мозге ограничено, и они не могут размножаться, сохраняя плюрипотентность, и тем самым восстанавливать численность. Ибо при первом же делении плюрипотентная клетка выбирает путь развития, и её дочерние клетки становятся либо мультипотентными клетками, у которых выбор более ограничен (только в эритроцитарный или лейкоцитарный ростки), либо мегакариобластами и затем мегакариоцитами — клетками, от которых отшнуровываются тромбоциты. Мазок красного костного мозга у больного лейкемией (препарат окрашен красителем Романовского — Райта). [править] Чувствительность к цитостатикам и излучению Клетки нормального костного мозга, подобно другим незрелым клеткам — клеткам злокачественных опухолей, а также стволовым клеткам кожи и слизистых, — обладают повышенной по сравнению с другими, более зрелыми, клетками организма чувствительностью к ионизирующим излучениям и цитостатическим противоопухолевым химиопрепаратам. Но чувствительность клеток костного мозга всё же ниже чувствительности клеток злокачественных опухолей, что и позволяет применять химиотерапию и облучение, уничтожая злокачественные опухоли или тормозя их размножение и метастазирование при сравнительно меньшем (хотя во многих случаях и весьма значительном) повреждении костного мозга. Особенно высокой, более высокой, чем у клеток нормального костного мозга, чувствительностью к химиотерапии обладают лейкозные клетки. Те цитотоксические химиопрепараты, которые уничтожают или повреждают полипотентные клетки, обладают кумулятивным, то есть накапливающимся, повреждающим воздействием на костномозговое кроветворение. Ибо они приводят к исчерпанию невозобновимого костномозгового резерва первичных клеток-предшественников. Подобный кумулятивный угнетающий эффект на костномозговое кроветворение характерен, в частности, для бусульфана и производных нитрозомочевины. Передозировка любого из цитостатических агентов, обладающих кумулятивным действием на клетки-предшественники, вызывает необратимую аплазию костного мозга — апластическую анемию. Проведение пункции. И напротив, химиопрепараты, в основном повреждающие или уничтожающие более поздние промежуточные стадии развития кроветворных клеток, например мультипотентные клетки, почти не обладают кумулятивным угнетающим действием на костномозговое кроветворение — после прекращения химиотерапевтического воздействия численность костномозговых клеточных популяций полностью или почти полностью восстанавливается за счёт костномозгового резерва первичных клеток-предшественников. Таким свойством — относительно мало уничтожать невозобновимую популяцию первичных полипотентных клеток — обладает большинство противоопухолевых препаратов, например, циклофосфамид, цитозин-арабинозид. Именно это позволяет применять эти лекарства при опухолях и лейкозах. Костный мозг Костный мозг (medulla ossium) — центральный орган кроветворения, расположенный в губчатом веществе костей и костно-мозговых полостях. Выполняет также функции биологической защиты организма и костеобразования. У человека костный мозг впервые появляется на 2-м месяце эмбриогенеза в закладке ключицы, на 3-м месяце — в лопатках, ребрах, грудине, позвонках и др. На 5-м месяце эмбриогенеза К. м. функционирует как основной кроветворный орган, обеспечивая дифференцированное костномозговое кроветворение с элементами гранулоцитарного, эритроцитарного и мегакарциоцитарного рядов. В организме взрослого человека различают красный костный мозг, представленный деятельной кроветворной тканью, и желтый, состоящий из жировых клеток. Красный костный мозг заполняет промежутки между костными перекладинами губчатого вещества плоских костей и эпифизов трубчатых костей. Он имеет темно-красный цвет и полужидкую консистенцию, состоит из стромы и клеток кроветворной ткани. Строма образована ретикулярной тканью, она представлена фибробластами и эндотелиальными клетками; содержит большое количество кровеносных сосудов, в основном широких тонкостенных синусоидных капилляров. Строма принимает участие в развитии и жизнедеятельности кости. В промежутках между структурами стромы находятся клетки, участвующие в процессах кроветворения стволовые клетки, клетки-предшественники, эритробласты, миелобласты, монобласты, мегакариобласты, промиелоциты, миелоциты, метамиелоциты, мегакариоциты, макрофаги и зрелые форменные элементы крови. Формирующиеся клетки крови в красном костный мозг располагаются в виде островков. При этом эритробласты окружают макрофаг, содержащий железо, необходимое для построения геминовой части гемоглобина. В процессе созревания зернистые лейкоциты (гранулоциты) депонируются в красном костным мозге, поэтому их содержание в 3 раза больше, чем эритрокариоцитов. Мегакариоциты тесно связаны с синусоидными капиллярами; часть их цитоплазмы проникает в просвет кровеносного сосуда. Отделяющиеся фрагменты цитоплазмы в виде тромбоцитов переходят в кровяное русло. Формирующиеся лимфоциты плотно окружают кровеносные сосуды. В красном костном мозге развиваются предшественники лимфоцитов и В-лимфоциты. В норме через стенку кровеносных сосудов красного костный мозг проникают только созревшие форменные элементы крови, поэтому появление в кровяном русле незрелых форм свидетельствует об изменении функции или повреждении костномозгового барьера. Костный мозг занимает одно из первых мест в организме по своим репродуктивным свойствам. В среднем у человека в день образуется 20×109 лимфоцитов, 200×109 эритроцитов, 120×109 гранулоцитов и 150×109 тромбоцитов. В детском возрасте (после 4 лет) красный костный мозг постепенно замещается жировыми клетками. К 25 годам диафизы трубчатых костей целиком заполняются желтым мозгом, в плоских костях он занимает около 50% объема костного мозга. Желтый костный мозг в норме не выполняет кроветворной функции, но при больших кровопотерях в нем появляются очаги кроветворения. С возрастом объем и масса костного мозга изменяются. Если у новорожденных на его долю приходится примерно 1,4% массы тела, то у взрослого человека — 4,6%. Костный мозг участвует также в разрушении эритроцитов, реутилизации железа, синтезе гемоглобина, служит местом накопления резервных липидов. Поскольку в нем содержатся лимфоциты и мононуклеарные фагоциты, он принимает участие в реакции иммунного ответа. Деятельность костного мозга как саморегулирующейся системы контролируется по принципу обратной связи (число зрелых клеток крови влияет на интенсивность их образования). Эта регуляция обеспечивается сложным комплексом межклеточных и гуморальных (поэтины, лимфокины и монокины) воздействий. Предполагается, что основным фактором, регулирующим клеточный гомеостаз, является количество клеток крови. В норме по мере старения клеток они удаляются и на их место приходят другие. При экстремальных состояниях (например, кровотечении, гемолизе) изменяется концентрация клеток, срабатывает обратная связь; в дальнейшем процесс зависит от динамической устойчивости системы и силы воздействия вредных факторов. Состояние костного мозга оценивают по результатам исследования его пунктатов, которые получают из различных участков костей с помощью специальных игл. Наиболее широко используется стернальная пункция, а также трепанобиопсия подвздошной кости. Результаты исследования фиксируются в миелограмме, отражающей качественный и количественный состав клеток костного мозга. Для определения процентного соотношения различных видов клеток подсчитывают 500—1000 клеток. Для оценки кроветворения пользуются лейкоэритробластическим индексом — отношением клеточных элементов лейко- и эритробластического рядов, который у здоровых лиц равен 4(3):1, индексом созревания нейтрофилов — отношением молодых гранулоцитов (промиелоцитов, миелоцитов, метамиелоцитов) к зрелым формам клеток (палочко-ядерным и сегментоядерным нейтрофильным лейкоцитам), в норме он равен 0,6—0,8, и другими индексами. При исследовании костного мозга, характер патологического процесса определяют по соотношению кроветворной и жировой ткани, клеточному составу, состоянию стромы и строению костной ткани. Под воздействием эндогенных и экзогенных факторов происходит нарушение кроветворной функции костного мозга. Нередко патологические изменения, происходящие в костном мозге, особенно в начале какого-либо заболевания, не сказываются на показателях, характеризующих состояние крови. Возможны уменьшение числа клеточных элементов костного мозга (гипоплазия) или их увеличение (гиперплазия). При гипоплазии костный мозг уменьшается количество миелокариоцитов, отмечается цитопения, нередко жировая ткань преобладает над миелоидной. Гипоплазия кроветворения может быть самостоятельным заболеванием (например, апластическая анемия). В редких случаях она сопровождает такие заболевания, как хронический гепатит, злокачественные новообразования, встречается при некоторых формах миелофиброза, мраморной болезни, аутоиммунных заболеваниях. При некоторых заболеваниях уменьшается количество клеток одного ряда, например красного (парциальная красноклеточная аплазия), или клеток гранулоцитарного ряда (агранулоцитоз). При ряде патологических состояний, кроме гипоплазии кроветворения, возможен неэффективный гемопоэз, для которого характерны нарушение созревания и выхода клеток гемопоэза в кровь и их интрамедуллярная гибель. Гиперплазия костного мозга имеет место при различных лейкозах. Так, при остром лейкозе появляются незрелые (бластные) клетки; при хроническом лейкозе возрастает число морфологически зрелых клеток, например лимфоцитов при лимфолейкозе, эритроцитов при эритремии, гранулоцитов при хроническом миелолейкозе. Гиперплазия клеток эритроцитарного ряда характерна также для гемолитических анемий, В12-дефицитной анемии. Красный костный мозг - Костный мозг - важнейший орган кроветворной системы, осуществляющий гемопоэз, или кроветворение - процесс создания новых клеток крови взамен погибающих и отмирающих. Он также является одним из органов иммунопоэза. Для иммунной системы человека костный мозг вместе с периферическими лимфоидными органами является функциональным аналогом так называемой фабрициевой сумки, имеющейся у птиц. Различают красный костный мозг (medulla ossium rubra) с преобладанием кроветворной миелоидной ткани и жёлтый с преобладанием жировой ткани. Красный костный мозг сохраняется в течение всей жизни в плоских костях (ребрах, грудине, костях черепа, таза), а также в позвонках и эпифазах трубчатых костей. У человека он составляет около 1,5% массы тела. С возрастом кроветворная ткань в полостях трубчатых костей замещается жировой и костный мозг в них становится жёлтым. Развитие костного мозга Костный мозг у человека появляется впервые на 2-м месяце внутриутробного периода в ключице эмбриона, затем на 3-4 -м месяце он образуется в развивающихся плоских костях, а также в трубчатых костях конечностей - лопатках, тазовых костях, затылочной кости, ребрах, грудине, костях основания черепа и позвонках, а в начале 4-го месяца развивается также в трубчатых костях конечностей. До 11-й недели это остеобластический костный мозг, который выполняет остеогенную функцию. В данный период костный мозг накапливает стволовые клетки, а клетки стромы с остеогенными потенциями создают микросреду, необходимую для дифференцировки стволовых кроветворных клеток. У 12-14-недельного эмбриона человека происходят развитие и дифференцировка вокруг кровеносных сосудов гемопоэтических клеток. У 20-28-недельного плода человека в связи с интенсивным разрастанием костного мозга отмечается усиленная резорбция костных перекладин остеокластами, в результате чего образуется костномозговой канал, а красный костный мозг получает возможность расти в направлении эпифизов. К этому времени костный мозг начинает функционировать как основной кроветворный орган, причем большая часть образующихся в нем клеток относится к эритроидному ряду гемопоэза. У зародыша 36 нед. развития в костном мозге диафиза трубчатых костей обнаруживаются жировые клетки. Одновременно появляются очаги кроветворения в эпифизах. Строение красного костного мозга Костный мозг - единственная ткань взрослого организма, в норме состоящая из незрелых, недифференцированных и низкодифференцированных клеток, так называемые стволовые клетки, близких по строению к эмбриональным клеткам. Все другие незрелые клетки, например незрелые клетки кожи, все же имеют большую степень дифференцировки и зрелости, чем клетки костного мозга, и имеют уже заданную специализацию. Красный, или кроветворный, костный мозг у человека находится в основном внутри тазовых костей и, в меньшей степени, внутри эпифизов длинных трубчатых костей и в ещё меньшей степени внутри тел позвонков. Он состоит из фиброзной ткани стромы и собственно кроветворной ткани. В кроветворной ткани костного мозга выделяют три ростка, или три клеточных линии (англ. cell lines), три популяции клеток, являющиеся родоначальниками соответствующих клеток крови - лейкоцитарный, эритроцитарный и тромбоцитарный ростки. Все эти клеточные ростки имеют общих предков - так называемые плюрипотентные стволовые клетки-предшественники, которые при созревании и дифференцировке идут по одному из трех путей развития. Костный мозг в норме защищен барьером иммунологической толерантности от уничтожения незрелых и созревающих клеток собственными лимфоцитами организма. При нарушении иммунологической толерантности лимфоцитов к клеткам костного мозга развиваются аутоиммунные цитопении, в частности аутоиммунные тромбоцитопении, аутоиммунные лейкопении, и даже апластическая анемия. Количество полипотентных стволовых клеток, то есть клеток, которые являются самыми первыми предшественниками в ряду кроветворных клеток, в костном мозге ограничено, и они не могут размножаться, сохраняя плюрипотентность, и тем самым восстанавливать численность. Ибо при первом же делении плюрипотентная клетка выбирает путь развития, и ее дочерние клетки становятся либо мультипотентными клетками, у которых выбор более ограничен (только в эритроцитарный или лейкоцитарный ростки), либо мегакариобластами и затем мегакариоцитами - клетками, от которых отшнуровываются тромбоциты. Масса костного мозга 1,6-3,7 кг, что составляет 3-6% от массы тела. Красный костный мозг имеет темно-красный цвет. Консистенция его полужидкая. Это позволяет делать из него тонкие мазки, изучение которых имеет большое диагностическое значение в клинике. Он содержит стволовые кроветворные клетки (СКК) и диффероны гемопоэтических клеток эритроидного, гранулоцитарного и мегакариоцитарного ряда, а также предшественники В- и Т-лимфоцитов. Стромой костного мозга является ретикулярная соединительная ткань, образующая микроокружение для кроветворных клеток. В настоящее время к элементам микроокружения относят также остеогенные, жировые, адвентициальные, эндотелиальные клетки и макрофаги. Ретикулярные клетки благодаря своей отростчатой форме выполняют механическую функцию, секретируют компоненты основного вещества - преколлаген, гликозаминогликаны, проэластин и микрофибриллярный белок и участвуют в создании кроветворного микроокружения, специфического для определенных направлений развивающихся гемопоэтических клеток, выделяя ростовые факторы. Остеогенными клетками называют стволовые клетки опорных тканей, остеобласты и их предшественники. Остеогенные клетки входят в состав эндоста и могут быть в костномозговых полостях. Остеогенные клетки также способны вырабатывать ростовые факторы, индуцировать родоначальные гемопоэтические клетки в местах своего расположения к пролиферации и дифференцировке. Наиболее интенсивно кроветворение происходит вблизи эндоста, где концентрация стволовых клеток примерно в 3 раза больше, чем в центре костномозговой полости. Адипоциты (жировые клетки) являются постоянными элементами костного мозга. Адвентициальные клетки сопровождают кровеносные сосуды и покрывают более 50% наружной поверхности синусоидных капилляров. Под влиянием гемопоэтинов (эритропоэтин) и других факторов они способны сокращаться, что способствует миграции клеток в кровоток. Эндотелиальные клетки сосудов костного мозга принимают участие в организации стромы и процессов кроветворения, синтезируют коллаген IV типа, гемопоэтины. Эндотелиоциты, образующие стенки синусоидных капилляров, непосредственно контактируют с гемопоэтическими и стромальными клетками благодаря прерывистой базальной мембране. Эндотелиоциты способны к сократительным движениям, которые способствуют выталкиванию клеток крови в синусоидные капилляры. После прохождения клеток в кровоток поры в эндотелии закрываются. Эндотелиоциты выделяют колониестимулирующие факторы (КСФ) и белок фибронектин, обеспечивающий прилипание клеток друг к другу и субстрату. Макрофаги в костном мозге представлены неоднородными по структуре и функциональным свойствам клетками, но всегда богатыми лизосомами и фагосомами. Некоторые из популяций макрофагов секретируют ряд биологически активных веществ (эритропоэтин, колониестимулирующие факторы, интерлейкины, простагландины, интерферон и др.). Макрофаги при помощи своих отростков, проникающих через стенки синусов, улавливают из кровотока железосодержащее соединение (трансферрин) и далее передают его развивающимся эритроидным клеткам для построения геминовой части гемоглобина. Межклеточное вещество - В костном мозге это вещество содержит коллаген II, III и IV типа, гликопротеины, протеогликаны и др. Гемопоэтические клетки или кроветворные диффероны составляют паренхиму красного костного мозга. Рассмотрим подробнее образование эритроцитов, гранулоцитов и тромбоцитов в красном костном мозге. Эритроцитопоэз Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических островков. Эритробластический островок состоит из макрофага, окруженного эритроидными клетками. Эритроидные клетки развиваются из колониеобразующей эритроидной клетки (КОЕ-Э), вступившей в контакт с макрофагом костного мозга. КОЕэ и образующиеся из нее клетки - от проэритробласта до ретикулоцита - удерживаются в контакте с макрофагом его рецепторами - сиалоадгезинами. Макрофаги служат своего рода «кормильцами» для эритробластов, способствуют накоплению в непосредственной близости от эритробластов и поступлению в них эритропоэтина, витаминов кроветворения (витамина D3), молекул ферритина. Макрофаги островков фагоцитируют ядра, вытолкнутые эритробластами при их созревании и способны повторно присоединять КОЕэ и формировать вокруг себя новый очаг эритропоэза. По мере созревания эритробласты отделяются от островков и после удаления ядра (энуклеации) проникают через стенку венозных синусов в кровоток. Стенки синусов состоят из эндотелиальных уплощенных клеток, пронизанных щелевидными отверстиями, или порами, в которые проникают форменные элементы крови и плазма. Среди эндотелиальных клеток есть фиксированные макрофаги. Гранулоцитопоэз Гранулоцитопоэтические клетки также образуют островки, главным образом по периферии костномозговой полости. Незрелые клетки гранулоцитарных рядов окружены протеогликанами. В процессе созревания гранулоциты депонируются в красном костном мозге, где их насчитывается примерно в 3 раза больше, чем эритроцитов, и в 20 раз больше, чем гранулоцитов в периферической крови. Тромбоцитопоэз «Гиганты красного костного мозга дают карликов крови» - Мегакариобласты и мегакариоциты располагаются в тесном контакте с синусами так, что периферическая часть их цитоплазмы проникает в просвет сосуда через поры. Отделение фрагментов цитоплазмы в виде тромбоцитов (кровяных пластинок) происходит непосредственно в кровяное русло. Лимфоцитопоэз и моноцитопоэз Среди островков клеток миелоидного ряда встречаются небольшие скопления костномозговых лимфоцитов и моноцитов, которые окружают кровеносный сосуд. В обычных физиологических условиях через стенку синусов костного мозга проникают лишь созревшие форменные элементы крови. Миелоциты и эритробласты попадают в кровь только при патологических состояниях организма. Причины такой избирательной проницаемости стенки сосудов остаются недостаточно ясными, но факт проникновения незрелых клеток в кровяное русло всегда служит верным признаком расстройства костномозгового кроветворения. Васкуляризация. Иннервация. Возрастные изменения. Регенерация. Васкуляризация. Костный мозг снабжается кровью посредством сосудов, проникающих через надкостницу в специальные отверстия в компактном веществе кости. Войдя в костный мозг, артерии разветвляются на восходящую и нисходящую ветви, от которых радиально отходят артериолы. Сначала они переходят в узкие капилляры (2-4 мкм), а затем в области эндоста продолжаются в широкие тонкостенные с щелевидными порами синусы (диаметром 10-14 мкм). Из синусов кровь собирается в центральную венулу. Постоянное зияние синусов и наличие щелей в эндотелиальном пласте обусловливаются тем, что в синусах гидростатическое давление несколько повышено, так как диаметр выносящей вены меньше по сравнению с диаметром артерии. К базальной мембране с наружной стороны прилежат адвентициальные клетки, которые, однако, не образуют сплошного слоя, что создает благоприятные условия для миграции клеток костного мозга в кровь. Меньшая часть крови проходит со стороны периоста в каналы остеонов, а затем в эндост и синус. По мере контакта с костной тканью кровь обогащается минеральными солями и регуляторами кроветворения. Кровеносные сосуды составляют половину (50%) массы костного мозга, из них 30% приходится на синусы. В костном мозге разных костей человека артерии имеют толстую среднюю и адвентициальную оболочки, многочисленные тонкостенные вены, причем артерии и вены редко идут вместе, чаще врозь. Капилляры бывают двух типов: узкие 6-20 мкм и широкие синусоидные (или синусы) диаметром 200-500 мкм. Узкие капилляры выполняют трофическую функцию, широкие являются местом дозревания эритроцитов и выхода в кровоток разных клеток крови. Капилляры выстланы эндотелиоцитами, лежащими на прерывистой базальной мембране. Иннервация. В иннервации участвуют нервы сосудистых сплетений, нервы мышц и специальные нервные проводники к костному мозгу. Нервы проникают в костный мозг вместе с кровеносными сосудами через костные каналы. Далее покидают их и продолжаются как самостоятельные веточки в паренхиме в пределах ячеек губчатого вещества кости. Они ветвятся на тонкие волоконца, которые либо вновь вступают в контакт с костномозговыми сосудами и оканчиваются на их стенках, либо заканчиваются свободно среди клеток костного мозга. Возрастные изменения. Красный костный мозг в детском возрасте заполняет эпифизы и диафизы трубчатых костей и находится в губчатом веществе плоских костей. Примерно в 12-18 лет красный костный мозг в диафизах замещается желтым. В старческом возрасте костный мозг (желтый и красный) приобретает слизистую консистенцию и тогда называется желатинозным костным мозгом. Следует отметить, что этот вид костного мозга может встречаться и в более раннем возрасте, например при развитии костей черепа и лица. Регенерация. Красный костный мозг обладает высокой физиологической и репаративной регенерационной способностью. Источником образования гемопоэтических клеток являются стволовые клетки, находящиеся в тесном взаимодействии с ретикулярной стромальной тканью. Скорость регенерации костного мозга в значительной мере связана с микроокружением и специальными ростстимулирующими факторами гемопоэза. Чувствительность к цитостатикам и излучению Клетки нормального костного мозга, подобно другим незрелым клеткам - клеткам злокачественных опухолей, а также стволовым клеткам кожи и слизистых, - обладают повышенной по сравнению с другими, более зрелыми, клетками организма чувствительностью к ионизирующим излучениям и цитостатическим противоопухолевым химиопрепаратам. Но чувствительность клеток костного мозга все же ниже чувствительности клеток злокачественных опухолей, что и позволяет применять химиотерапию и облучение, уничтожая злокачественные опухоли или тормозя их размножение и метастазирование при сравнительно меньшем (хотя во многих случаях и весьма значительном) повреждении костного мозга. Особенно высокой, более высокой, чем у клеток нормального костного мозга, чувствительностью к химиотерапии обладают лейкозные клетки. Те цитотоксические химиопрепараты, которые уничтожают или повреждают полипотентные клетки, обладают кумулятивным, то есть накапливающимся, повреждающим воздействием на костномозговое кроветворение. Ибо они приводят к исчерпанию невозобновимого костномозгового резерва первичных клеток-предшественников. Подобный кумулятивный угнетающий эффект на костномозговое кроветворение характерен, в частности, для бусульфана и производных нитрозомочевины. Передозировка любого из цитостатических агентов, обладающих кумулятивным действием на клетки-предшественники, вызывает необратимую аплазию костного мозга - апластическую анемию. И напротив, химиопрепараты, в основном повреждающие или уничтожающие более поздние промежуточные стадии развития кроветворных клеток, например мультипотентные клетки, почти не обладают кумулятивным угнетающим действием на костномозговое кроветворение - после прекращения химиотерапевтического воздействия численность костномозговых клеточных популяций полностью или почти полностью восстанавливается за счет костномозгового резерва первичных клеток-предшественников. Таким свойством - относительно мало уничтожать невозобновимую популяцию первичных полипотентных клеток - обладает большинство противоопухолевых препаратов, например, циклофосфамид, цитозин-арабинозид. Именно это позволяет применять эти лекарства при опухолях и лейкозах. История исследований костного мозга В 1963 году полномасштабное исследование красного костного мозга провела исследовательская группа кафедры гистологии и эмбриологии Педиатрического факультета РГМУ под руководством М.И.Пекарского. КОСТНЫЙ МОЗГ Пересадка костного мозга Пересадка костного мозга — относительно новая медицинская процедура, которая используется для лечения болезней, ранее считавшихся неизлечимыми. Со времени ее первого успешного использования в 1968 году, трансплантация костного мозга используется для лечения пациентов, страдающих лейкозом (раком крови), апластической анемией, лимфомами (такими, как имфогрануоматоз или лимфома Ходжкина, множественной миеломой, серьезными нарушениями иммунитета и некоторыми злокачественными опухолями, как например, раком груди или яичников. В 1991 году в США более 7500 пациентов подверглись процедуре пересадки костного мозга. Хотя трансплантация сегодня спасает тысячи жизней ежегодно, 70 процентов нуждающихся в пересадке не проходят ее из-за невозможности найти совместимого донора. ЧТО ТАКОЕ КОСТНЫЙ МОЗГ Костный мозг - это губчатая ткань, которая находится внутри крупных костей. Косный мозг в грудине, костях черепа, бедренных костях, ребрах и в позвоночнике содержит стволовые клетки, из которых вырабатываются клетки крови. Это белые кровяные клетки — лейкоциты, защищающие организм от инфекций, красные кровяные клетки- эритроциты, переносчики кислорода, и тромбоциты, позволяющие крови сворачиваться. |
