Биохимия слюны. Слюна. Слюна ее значение и роль в развитии заболеваний полости рта
 Скачать 5.73 Mb. Скачать 5.73 Mb.
|
Методики определения скорости секреции смешанной слюныСмешанная слюна может быть собрана и количественно измерена рядом объемнометрических (волюмометрических) и гравиметрических методик (Леус П.А., 2004, 2007). Эти методики включают сбор слюны при самопроизвольном истечении из полости рта, при сплевывании или сбором на тампон. В стоматологической клинике традиционно используют комбинацию волюмометрического метода с методикой сбора самоистечения и сплевывания слюны (Леус П.А., 2004). В качестве измерительного устройства также применяют «сиалометр» или хорошо калиброванный мерный цилиндр. Сбор нестимулированной смешанной слюны (в состоянии покоя) Пациента усаживают, просят опустить голову и сидеть в таком положении, не глотать слюну и не двигать губами и языком во время всего периода сбора слюны. Слюна накапливается в полости рта в течение 2 мин, затем пациента просят сплюнуть все содержимое полости рта в приемный сосуд. Процедуру сбора проводят еще два раза так, чтобы общее время сбора составило 10 мин. Для расчета скорости слюноотделения в мл/мин общий объем собранной слюны делят на 10. Сбор стимулированной смешанной слюны Метод с парафином. Пациенту дают подержать кусочек парафина (Orion Diagnostia, Espoo., Финляндия; Леус П.А., 2004) в полости рта 30 сек (до тех пор, пока парафин не станет мягким). Затем предлагают проглотить всю накопившуюся в полости рта слюну. Далее просят пожевать кусочек парафина в своей обычной манере в течение 2 мин, точно засекая время. Накопленную слюну сплевывают в приемный сосуд (пробирку). Процедуру повторяют еще два раза. Объем слюны определяют по делениям сосуда и вычисляют скорость в мл/мин или за 10 мин. Метод с лимонной кислотой. Приготовленный в аптеке 2 %-ный раствор лимонной кислоты наносят на дорсолатеральную поверхность языка каждые 30 сек в течение 2 мин (с помощью тампона или аппликаторной кисточки). Слюну накапливают, а затем сплевывают в приемный сосуд (пробирку). Как в методе с парафином, процедуру повторяют несколько раз, так что общее время сбора составляет 10 мин. Рассчитывают скорость слюноотделения, также выраженную в мл/мин и за 10 мин. Сбор слюны из больших слюнных желез (дифференцированно) Слюну из околоушной слюнной железы традиционно собирают, используя модифицированную двухкамерную капсулу Carlson-Crittenden (Леус П.А., 2004). Внутреннюю камеру капсулы помещают над входным отверстием стенного протока; внешняя камера соединена с помощью резиновой трубки с резиновой грушей, которая при сжимании создает небольшое отрицательное давление и позволяет всей капсуле зафиксироваться на окружающей слизистой оболочке. Это устройство позволяет собрать чистую слюну из околоушной слюнной железы неинвазивным методом. Чтобы собрать слюну подчелюстных и (или) подъязычных желез, область Вартоновых протоков изолируется марлей, а устья Степановых протоков закрываются. Стимулированная слюна или слюна в состоянии покоя, собирающаяся в течение известного периода времени, аспирируется пластмассовой микропипеткой. Скорость слюноотделения выражается мл/мин/пар подчелюстных и (или) подъязычных желез (Леус П.А., 2004). Определение скорости отделения слюны малыми слюнными железами Слюна может быть получена и из малых слюнных желез нижней губы или неба. Малые железы просушиваются и изолируются валиками из марли или ваты. Через 2 мин (при сборе слюны в состоянии покоя) жидкость, выделенную из отверстия одной или нескольких желез, собирают полоской фильтровальной бумаги (Perio-Paper). Затем эту полоску помещают в устройство «Periotron», которое электронным способом определяет объем жидкости, адсорбированной на полоске. Для сбора стимулированной слюны малых желез язык смазывают 2 %-ным раствором лимонной кислоты, как описано выше. Результаты выражают в мкл/мин. Поскольку количество желез и площадь поверхности, с которой производится забор, варьируют, величина скорости отделения секрета является величиной полуколичественной. Ромачева И. Ф. с соавторами (1987) предложила использовать метод подсчета функционирующих слюнных желез на слизистой оболочке нижней губы, окрашенной метиленовым синим, в пределах рамки 2 х 2 см после стимуляции секреции раствором пилокарпина гидрохлорида. В норме функционирует 21 ± 0,9 малой слюнной железы. Рабинович И.М. также исследовал клинико-функциональную характеристику малых слюнных желез слизистой оболочки полости рта (1991). 8. Роль слюны в образовании биофильма (биопленки) на тканях полости рта Все поверхности и твердых, и мягких тканей полости рта покрыты пелликулой, в основном состоящей из компонентов слюны (Барер Г.М., Денисов А.Б., Уварова Л.В., 2010; Вавилова Т.П., Медведев А.Е., 2016). Пелликула обеспечивает смазку, увлажнение тканей и регуляцию состава микробиоты. В состав пелликулы входят слюнные белки и пептиды и другие молекулы, экспрессируемые эпителиальными клетками. Часть из них, а также гликолипиды могут служить рецепторами адгезии для бактерий и обеспечивать их прикрепление (Коленбрандер, 2009). В ее составе присутствуют антимикробные пептиды (3-дефензины и кальпротектин, препятствующие внедрению микроорганизмов в мягкие ткани). Осаждение клеток и остатков пищи из слюны на пелликулу приводит к формированию зубного налета (К03.66 dental plaque; относится к разделу «Отложения на зубах» МКБ-10 – ICD-DA, WHO, 1995) – рыхлого белого биоматериала, образующегося на поверхностях зубов из бактерий, слущенного эпителия, лейкоцитов и остатков пищи. Согласно современной концепции, бактерии могут прикрепляться к пелликуле зуба путем соединения толерантных молекулярных терминалов с обеих сторон (цит. по: Леус П.А., 2007) (рис. 16). 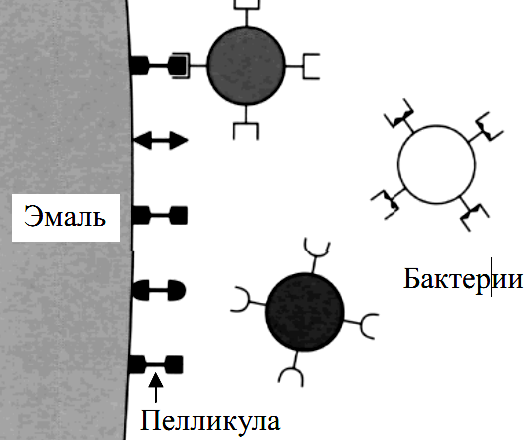 Рис. 16. Концепция механизма прикрепления бактерий к пелликуле. Состав зубного налета меняется со временем. По мере старения зубного налета начинает преобладать анаэробная микрофлора, для которой характерны высокая ферментативная активность и образование органических кислот. Зубной налет примерно на 80% состоит из воды, в которой растворены микро- и макроэлементы, белки и углеводы (20%). Содержание неорганических веществ варьирует. По мере старения зубного налета количество кальция и фосфора продолжает расти. Помимо макроэлементов, в зубном налете присутствуют и микроэлементы – Sr, Fe, Mg, Mn, F и др. Содержание фтора может быть в десятки и даже сотни раз больше, чем в слюне, и достигать 6–180 мкг/г, что в значительной мере зависит от уровня фтора в воде. Фтор присутствует в виде фторида кальция CaF2, связывается с белками матрикса зубного налета и проникает внутрь бактерий, вызывая их гибель. В незрелом зубном налете присутствуют глицерофосфолипиды, триацилглицеролы и холестерол. По мере созревания зубного налета появляются гликолипиды (Леус П.А., 2007). Бактерии способны прилипать и к эмали зуба, и к разным поверхностям полости рта. Адгезия микроорганизмов происходит за счет ван-дер-ваальсовых сил, образования «сшивок» с помощью ионов кальция (Са2+), гидрофобных взаимодействий и водородных связей. На образованной первичной колонии происходит коадгезия, т.е. фиксация нового слоя бактерий, и формируется вторичная колонизация (рис. 17) (Уварова Л.В., 2010). 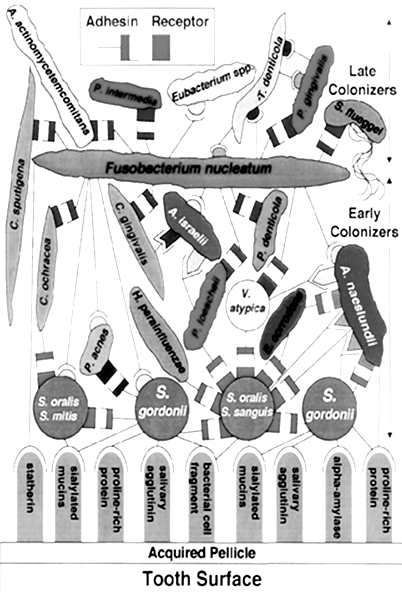 Рис. 17. Первичная и вторичная колонии бактерий (микробного биофильма). Взаимодействие первичной и вторичной колоний осуществляется зачастую с использованием белково-углеводных (лектиноподобных) связей, и в результате формируются пространственно-ориентированные группы микроорганизмов. Расположение бактерий обеспечивает метаболические взаимодействия между ними. Например, стрептококки после утилизации глюкозы освобождают из клетки лактат, который утилизируют вейлонеллы, поэтому вблизи клеток микроорганизмов среда защелачивается, что способствует расщеплению еще большего количества углеводов с последующим ростом количества молочной кислоты, т.е. активация метаболических процессов в анаэробных условиях в S. Mutarts и других бактериях неизбежно приводит к развитию патологии в твердых тканях зубов или воспалению в тканях пародонта. Зубной налет отличается высокой метаболической активностью. По мере роста зубного налета на порядок увеличивается активность гликозидаз и других ферментов. При участии бактериальных гликозилтрансфераз образуются липкие полисахариды (гликаны), которые адсорбируются на поверхности зуба. В прилипании микроорганизмов участвуют гликаны – леваны и декстраны – и гликансвязывающий белок (Вавилова Т.П. Медведев А.Е., 2016; рис. 18). В синтезе леванов осуществляют бактериальные фруктозилтрансферазы, а декстрана – глюкозилтрансферазы. Они переносят остатки глюкозы от сахарозы. 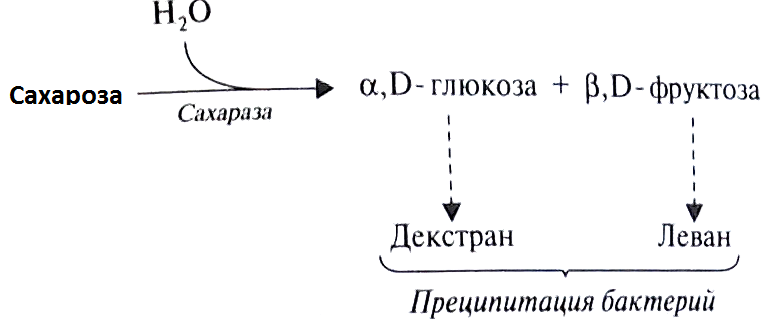 Рис. 18. Схема образования липких полисахаридов в зубном налете. Леван – полисахарид, состоящий из остатков фруктозы, связанных В (2->6)–гликозидными связями, и соединенный с молекулой сахарозы. Молекула декстрана — разветвленный полисахарид, образованный остатками α-D-глюкозы, соединенный с молекулой сахарозы. Молекулы декстрана достаточно долго сохраняются в зубном налете, в то время как молекулы левана легко растворимы и быстро гидролизуются леваназой некоторых стрептококков. Липкие полисахариды помогают бактериям занять определенное место в зубном налете и обеспечивают их адгезию к эмали. Связь поверхности апатитов эмали с полисахаридами бактерий обеспечивают водородные связи, ионы кальция и белки адгезины. К белкам адгезинам относится гликопротеин с молекулярной массой 200 кДа, который выделяется стрептококками. Бактерии способны утилизировать углеводы, аминокислоты с образованием короткоцепочечных органических кислот – уксусной, пропионовой, масляной, молочной. Их накопление, особенно масляной кислоты, является одним из этиопатогенетических факторов развития пародонтита. Зубной камень. Обызвествление зубного налета приводит к образованию зубного камня. В зависимости от расположения различают над- и поддесневой зубной камень. Они по своему составу сходны, но различаются по источникам поступления фосфорно-кальциевых соединений. В наддесневой камень минералы поступают из слюны («слюнный камень»), а в поддесневой из десневой жидкости («сывороточный камень»). В зубном камне определяется до 50% кальция, до 30% неорганического фосфата и около 0,5% магния. В следовых количествах присутствуют свинец, молибден, кремний, алюминий, стронций, кадмий, фтор и другие химические элементы (Вавилова Т.П. с соавт., 2016). Кальций и неорганический фосфат осаждаются на органической матрице в виде солей, и на начальных этапах в основном образуется брушит (СаНРО4 • 2Н2О). Помимо брушита образуются витлокит, монетит, октокальцийфосфат, гидроксиапатит и другие кристаллы. В структуре витлокита определяются безводный фосфат кальция (Са3РО4)2 и ионы Mg2+, Mn2+, Fe3+. Октокальцийфосфат – Са8Н2(РО4)4 • 5Н2О является промежуточным связующим звеном между кислыми солями – монетитом, брушитом и гидроксиапатитом. Кристаллы октакальцийфосфата растут в форме тонких пластинок, содержат кислый фосфатный ион и не имеют гидроксильных групп. В зубном камне нередко присутствует и указанный выше другой кристалл – витлокит (CaMg)3(P04)2. 9. Микрокристаллизация смешанной слюны Как указано выше, слюна может стимулировать или подавлять рост микробов и процесс отложения зубного налета. Это, в свою очередь, изменяет бляшкообразование и процесс кальцификации (Барер Г.М., Денисов А.Б., 2003; Еловикова Т.М. с соавт, 1999, 2000, 2005, 2015; Молвинских В.С. с соавт., 2016; Вавилова Т.П., Медведев А.Е., 2016). Органические и неорганические компоненты смешанной слюны влияют на аккумуляцию бляшки и ее микробный состав. Биологические жидкости организма, в том числе смешанная слюна, имеют способность кристаллизоваться при высушивании и образовывать узоры в виде древовидного рисунка или листа папоротника (Барер Г.М. с соавт., 2003, 2008). Структура этих узоров значительно меняется в зависимости от различных условий: углеводной нагрузки, хронических бронхолегочных заболеваний, эстрогенной (андрогенной) насыщенности организма, воздействий постоянного магнитного поля, множественного кариеса зубов и т.д. Показано влияние искусственного магнитного поля на состояние биологических жидкостей организма, выражающееся в изменении их физико-химических свойств. При этом происходит изменение ионного состава и кристаллической структуры биожидкостей организма, в частности слюны. Данные параметры, безусловно, влияют на скорость накопления зубного налета, аккумуляцию бляшки, ее микробный состав и процесс кальцификации (Барер Г.М., Денисов А.Б., 2003; Еловикова Т.М. с соавт, 1999, 2000, 2005, 2015; Молвинских В.С. с соавт, 2016 и др.). Вышесказанное свидетельствует о значении микрокристаллизации слюны и целесообразности изучения изменений ее под действием различных факторов. Так, в качестве диагностического теста, а также для оценки эффективности профилактических мероприятий при кариесе зубов может быть применена методика Леуса П.А. (1977). Микрокристаллизация смешанной слюны исследуется методом микроскопии высохшей капли слюны обследованных пациентов. С этой целью со дна полости рта пипеткой собирают 0,2–0,3 мл смешанной слюны, 3 капли ее наносят на стерильное стекло, которое затем помещают на час в термостат (370С). По прошествии этого времени высохшие капли смешанной слюны исследуют с помощью стереомикроскопа в отраженном свете при малом увеличении. Различают три типа микрокристаллизации смешанной слюны: I тип (рис. 19) — крупные древовидные кристаллоподобные образования, расположенные в центре, II тип (рис. 20) — единичные кристаллоподобные конгломераты или игольчатые кристаллы, расположенные по всему полю зрения, III тип — разрозненные, единичные мелкие кристаллы, без ориентации (рис. 21). 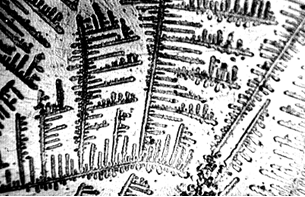 Рис.19. Микрокристаллизация ротовой жидкости I типа.  Рис. 20. Микрокристаллизация ротовой жидкости II типа. 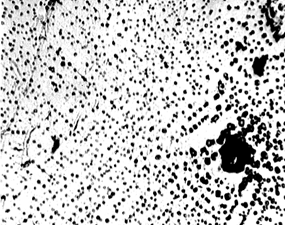 Рис. 21. Микрокристаллизация ротовой жидкости III типа. Исследования морфологической картины смешанной слюны (ротовой жидкости) у санированных пациентов и у лиц с природной санацией представлены в публикациях Разумовой С.Н., Булгакова В.С., Шатохиной С.Н., Шабалина В.Н. Авторами установлены типы морфологической картины смешанной слюны указанного контингента в зависимости от соотношения органического и минерального компонентов в ней. Получение структур смешанной слюны достигалось методом клиновидной дегидратации. Смешанную слюну забирали в пластиковую пробирку в количестве 1,5—2 мл натощак, после чистки зубов, центрифугировали в течение 10 мин при 3000 об/мин. Полуавтоматическим дозатором брали надоса-дочную жидкость в количестве 0,01—0,02 мл и наносили на специальную пластиковую поверхность тест-карты диагностического набора «Литос-система», который разрешен к применению в клинической практике. Капля высушивалась при температуре 20—25 °С, относительной влажности 65-70% и минимальной подвижности окружающего воздуха. Продолжительность периода высыхания составляла 3-4 часа. При завершении дегидратации получали фацию смешанной слюны, представлявшую собой высушенную пленку. Все фации подвергали морфологическому анализу с помощью стереомикроскопа MZ12 фирмы «Leica» (Германия) и фиксировали видеоизображение (рис.22).  Рис. 22. Типы фаций ротовой жидкости: а – I тип, б – II тип, в – III тип Фации смешанной слюны пациентов с природной санацией и у санированных в пробах «после сна» характеризовались наибольшей площадью, занятой кристаллами солей. Фации смешанной слюны II типа в течение суток распределялись у обследованных пациентов следующим образом: наибольший пик выявляемости отмечен в обеих сравниваемых группах в пробе «после обеда». Поскольку прием пищи вызывает активацию пищеварительных ферментов в полости рта, это закономерно отразилось на увеличении доли органического компонента в фациях смешанной слюны. Наибольший пик фаций смешанной слюны III типа встречался только у санированных пациентов в пробе «до обеда» у 23 (40%), что свидетельствует об активизации органической составляющей смешанной слюны, связанной либо с недостаточным очищением полости рта после завтрака, либо с активностью пищеварительных ферментов. Морфологическая картина смешанной слюны у пациентов без патологии полости рта характеризовалась наличием двух компонентов: неорганического (минерального) в виде кристаллов солей и органического – в виде аморфной (бесструктурной) субстанции. В зависимости от соотношения минерального и органического компонента смешанной слюны авторами условно предложено выделять три типа морфологической картины: от наименьшей доли органической составляющей (I тип) к наибольшей (III тип). У лиц с природной санацией в течение суток картина фаций смешанной слюны была представлена только двумя типами – I и II, в то время как у санированных – тремя. Результаты проведенных исследований показали, что маркером здорового пародонта (природная санация) является I тип морфологической картины смешанной слюны с максимальной площадью, занятой кристаллами солей в пробе, полученной сразу после сна. У пациентов с природной санацией в течение суток отмечено гармоничное изменение соотношения минерального и органического компонентов, связанное с приемом пищи. У санированных пациентов доля органического компонента в ротовой жидкости выше, по сравнению с пациентами с природной санацией. Кроме того, по данным Разумовой С.Н., наличие в фации смешанной слюны участков пигментации, то есть маркера интоксикации, свидетельствовало о высоком уровне распространенности и интенсивности кариозных поражений (рис.23). 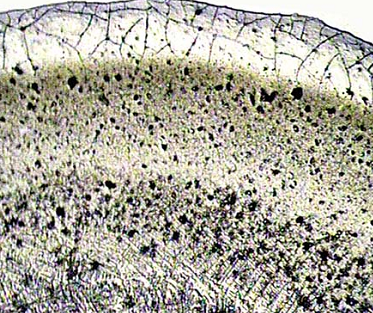 Рис.23. Маркер застойных явлений (трехлучевые трещины в краевой зоне), интоксикации (пигментация). Ув. 60.(цит. по: Разумова С.Н., Королев А.В., Шатохина С.Н., Шабалин В.Н., 2007). Представлены маркеры застойных явлений в виде трехлучевых трещин в краевой зоне и интоксикации в виде пигментации. Выделен феномен патологической кристаллизации солей в белковой среде (маркер деструкции) в виде складчатости в краевой зоне фации. Его наличие свидетельствует о признаках защитной биоминерализации, т.е. связывании органического детрита кристаллами солей и перевода токсических продуктов в инертный органно-минеральный агрегат гриба (рис. 24). 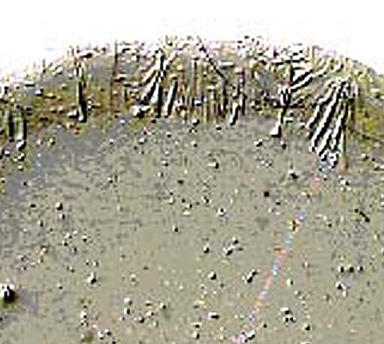 Рис.24. Складчатость в краевой зоне фации. Ув. 60. Следует отметить, что структуры типа «морщин» – постоянный признак патологии полости рта у пациентов, страдающих сахарным диабетом, и являются маркером деструкции тканей (феномен патологической кристаллизации и наличие мицелия гриба в фации смешанной слюны, рис. 25).  Рис. 25. Фрагмент краевой зоны фации смешанной слюны пожилого пациента с феноменом патологической кристаллизации и наличием мицелия гриба. Ув. 50. Кроме того, при патологических состояниях ткани полости рта также выявлены маркеры: маркер деструкции твердых тканей зуба (высокое содержание микрочастиц гидроксилапатита в краевой зоне фации ротовой жидкости), маркер атрофического процесса слизистой полости рта (широкие ломаные трещины в краевой зоне фации), маркер применения лекарственных препаратов (содержание в фации ротовой жидкости химических элементов, отсутствующих в норме – серебро, цинк и др.). Исследования Разумовой С.Н. доказали, что тип фации смешанной слюны характеризует качественный состав бактериальной флоры ротовой полости пациента. Для первого и второго типа фаций характерны бактериологические показатели здоровой полости рта (Str. oralis, Str. salivarius – не более 5x103), при третьем типе фаций имеет место сдвиг в сторону увеличения более агрессивной микрофлоры (Str. haemolyticus (α -гемолиз), Str. haemolyticus (ф-гемолиз), S. aureus, Candida albicans) при средних величинах титра ее высеваемости (не более 5х103 ТО4'). Разумовой С.Н. также выявлена четкая корреляция между некоторыми видами локальных структур фации смешанной слюны, состоянием тканей пародонта и зубов, показателями местного иммунитета полости рта. Феномен патологической кристаллизации в фациях смешанной слюны имеет место при повышенном уровне иммуноглобулина А, маркеры застойных явлений и интоксикации указывают на сниженный уровень иммуноглобулина А в смешанной слюне. Полученные результаты целесообразно использовать в клинической практике, в том числе при скрининговых исследованиях, а также с целью прогнозирования, ранней диагностики и оценки эффективности профилактики и лечения различных стоматологических заболеваний (Разумова С.Н., 2007). |
