Краткий справочник гальванотехника - 1993 - Ильин. Справочник гальванотехника санктПетербург " политехника"
 Скачать 3.02 Mb. Скачать 3.02 Mb.
|
33. Травление медиТравление меди является одной из основных операций в производстве печатных плат. Травильные растворы, с помощью которых осуществляется эта операция, должны удовлетворять следующим требованиям; в состав раствора должны входить дешевые и доступные материалы; раствор должен допускать возможность его регенерации и утилизации меди из отработанных растворов; величина бокового подтравливания проводников должна быть минимальной; травильные растворы не должны воздействовать на диэлектрическое основание печатной платы и на защитный рисунок. В производственной практике получили распространение растворы хлорной меди, кислые растворы для негативного способа и аммиачные (щелочные) для позитивного. Хлорид меди окисляет и растворяет медь по реакции CuCl2 + Сu Образующаяся CuCl нерастворима и может служить источником засорения форсунок и травильных установок. В присутствии ионов хлора в виде НС1, NaCl, NH4C1 образуются хорошо растворимые комплексы CuCl2. Окисление образующихся соединений одновалентной меди (хлористой меди) можно осуществить различными способами, например, воздействием газообразного хлора или перекисью водорода: 2СuС1 + Cl2 2CuCl + Н2O2 + 2НС1 Частично хлористую медь окисляет и кислород воздуха в кислой среде: 2СuС1 + ½ O2 + 2НС1 Таким образом, отработанный кислый раствор хлорной меди можно легко регенерировать в исходное состояние. Состав раствора (г/л): CuCl — 150—300; НС1 — 70—90, рН 1—0,8. Основные характеристики: боковое подтравливание 40—60 мкм; емкость по меди 10—20 г/л. Максимальная скорость травления 35 мкм/мин. Корректирование раствора возможно как в ручном исполнении, так и в автоматическом режиме. В первом случае сливают примерно 1/7 часть отработанного раствора, а оставшуюся часть подкисляют НС1 до рН 1—2 (20—25 г/л НCl). Разбавленную в отношении 1 : 6 перекись водорода вводят в регенерируемый раствор в количестве 110—115 г/л. Раствор перемешивают сжатым воздухом и через 20—30 мин можно приступить к работе. Слитый раствор подлежит обработке для утилизации меди электрохимическим способом. При автоматическом корректировании раствора все его параметры контролируются с помощью датчиков, имеющихся в автоматической линии ГГМ1.240.007. Датчики дают информацию о следующих параметрах раствора: температуре, кислотности рН плотности ρ, окислительно-восстановительном потенциале (Е), уровне раствора h. Момент регенерации определяется по накоплении хлорной меди более 10 г/л сверх установленного содержания по норме, при этом датчики указывают значения: Е = 390 ÷ 395 Мв; ρ = 1,12 г/см3; рН 2. По сигналу датчиков дозирующие устройства введут в раствор компоненты: НCl до рН 0,4; Н2O2 до E = 550 ÷ 600 мВ; NH4C1 до уровня, который снизился вследствие откачки 1/6—1/7 части раствора. Способ электрохимической регенерации отработанного медно-хлоридного раствора травления является весьма перспективным, гак как помимо регенерации раствора он обеспечивает возможность утилизации меди в виде катодного осадка. Указанный способ заключается в пропускании постоянного тока через электро- лизер с графитовыми электродами, разделенными катионитовой мембраной. На рис. 16 представлена схема процесса регенерации меди из кислого раствора. Отработанный травильный раствор, охлажденный в теплообменнике, из установки травления направляется в анодное пространство электролизера, где половина ионов Сu+ окисляется на графитовом аноде до Cu2+ а вторая половина вследствие электродиализа через катионитовую мембрану проникает в катодное пространство и на графитовом катоде происходит восстановление Сu+ до металла (Сu0). Разряд ионов Сu2+ на катоде менее вероятен, 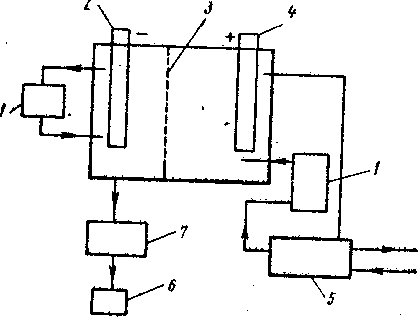 Рис. 16. Установка для электрохимической регенерации травильного раствора: 1 — теплообменники; 3 — катод; 3 — катионитовая мем- брана; 4 — анод; 5 — сборник травильного раствора; 6 — сборник медного порошка; 7 — сепаратор так как он происходит при более отрицательных потенциалах, чем разряд ионов Сu+. Раствор, обогащенный ионами Сu2+, через теплообменник возвращается в травильную установку. Циркуляция раствора в католите осуществляется лишь для его охлаждения. Медь на графитовом катоде осаждается в виде порошка чистотой 99,8% и периодически сбрасывается в сепаратор, а затем и в лоток, откуда выгружается для утилизации. В установке фирмы FSL режим электролиза следующий: сила тока 2000 А, напряжение 12 В. Производительность установки 2,5 кг/ч меди. Электрохимическая регенерация более рациональна, чем химическая, так как она не требует затрат материалов на окисление Сu+ и на последующее выделение солей меди, накапливающихся в растворе при травлении. Таким образом, электрохимическая регенерация осуществляется по реакции 2Cu+ которая является строго обратной реакции травления. Раствор хлорной меди, несмотря на малую емкость по меди, является наиболее перспективным при выполнении операции травления в производстве односторонних плат из гетинакса. Аналогичным является так называемый перекисный хлоридный раствор, применяемый некоторыми предприятиями. Раствор приготавливается из перекиси водорода и соляной кислоты, взятых в соотношении 1 : 3. В процессе травления меди происходят реакции: Сu +Н2О2 СuО + 2НС1 СuС12 + Сu По мере накопления в растворе солей меди этот раствор практически ничем не отличается от приведенного выше меднохлоридного. В аммиачной среде соли меди образуют комплекс: CuCl2 + 4NH4OH Аммиачная комплексная соль двухвалентной меди является окислителем и растворяет медь по реакции Сu(NН3)4Cl2 + Сu Отработанный раствор, содержащий одновалентную медь, легко регенерируется в результате окисления одновалентной меди кислородом воздуха: 2Cu(NH3)2Cl + ½ O2 + 2NH4C1 + 2NH4OH Составы травильных растворов приведены в табл. 148. Корректирование раствора можно осуществить в ручном исполнении или автоматически. В первом случае при накоплении стравленной меди до 60 г/л сливают 1/2 раствора. В оставшуюся Таблица 148. Состав растворов и режим травления меди
часть вводят NH4C1 (100—115 г/л), доводят до рабочего уровня разбавленным NH4OH до рН 8,5—8,8. Слитый раствор направляют на утилизацию меди. Во втором случае с помощью датчиков температуры плотности и кислотности раствора на дозирующие устройства подается сигнал, по которому раствор автоматически корректируется. Окисление Сu+ в Сu2+ происходит непрерывно вследствие воздействия кислорода воздуха при струйном методе обработки. По достижении ρ = 1,17 г/см3 подается сигнал на насос, который откачивает половину раствора и подкачивает порцию свежего раствора, состоящего из смеси NH4C1 и (NН4)2СO3. При снижении рН до 8,5 по сигналу датчика рН открывается вентиль баллона с газообразным аммиаком и происходит насыщение раствора аммиаком, которое прекращается по достижении рН 8,5÷8,8. Корректирование раствора газообразным аммиаком приводит к его повышенному расходу вследствие большой летучести аммиака. На ряде предприятий освоен метод корректирования травителя раствором следующего состава, г/л: хлористый аммоний — 150; аммиак водный 25%-ный— 400—500. Раствор вводится по сигналу датчика величины рН. Автоматический цикл регенерации предусмотрен в линии щелочного травления ДМУМ.240.001. Способ электрохимической регенерации раствора в установке УЭХР, разработанный Горьковским политехническим институтом, заключается в пропускании травильного раствора через электролизер, в котором анод — графитовый, катод — полированная коррозионно-стойкая сталь. На катоде при плотности тока 12 А/дм2 происходит восстановление меди до металла, а на аноде вследствие окислительных процессов выделяется смесь газов: N2, CO2, О2. Газообразный хлор не выделяется, так как он сразу же расходуется на окисление NH3 до N2. По аналогичному принципу действует установка «Урмат», разработанная Московским ГСПИ. Электрохимический процесс осуществляется при ik = 20 А/дм2. Установка снабжена датчиками травильной способности раствора, который дает информацию о концентрации Сu2+. Через 20А∙ч/л блок дозирования включает корректировку солями аммония. Недостатком медно-аммиачных травителей является загрязнение атмосферы и сточных вод аммонийными солями, которые, попадая в систему очистных сооружений, могут образовать комплексные соединения тяжелых металлов (никеля, меди и др.) и утечку их из нейтрализаторов в очистные стоки. Аммиачный медно-сульфатный раствор является аналогом аммиачно-медного хлоридного раствора и основным компонентом раствора служит комплексная соль Cu(NH3)4SO4. Процесс травления протекает по реакции: Сu(NH3)4SO4 + Сu Травильный раствор имеет состав, г/л: медь сернокислая — 90—100, сульфат аммония —160—180; аммиак водный 25%-ный — 400. Температура раствора 45—50 °С. Травление меди в этом растворе протекает более медленно, чем в аналогичном хлоридном, поэтому он рекомендуется для использования в полуаддитивной технологии при травлении тонких (5—7 мкм) слоев меди. С целью ускорения процесса вводится бромистый аммоний в количестве 4—5 г/л. Промывка плат после травления вначале производится в аммиачном растворе, а затем проточной холодной водой. Образовавшийся травильный шлам на проводящем рисунке удаляется осветлением в растворе состава (г/л): тиомочевина — 80—90; кислота соляная 50—60; спирт этиловый 5—6; препарат ОС-20 — 8—10. Температура раствора 18—25 °С: продолжительность 1— 1,5 мин. | ||||||||
