Сульфаниламидные препараты
 Скачать 1.69 Mb. Скачать 1.69 Mb.
|
Furaginum (Фурагин)N-(5-Нитро-2-фурил)-аллилиденаминогидантоин. 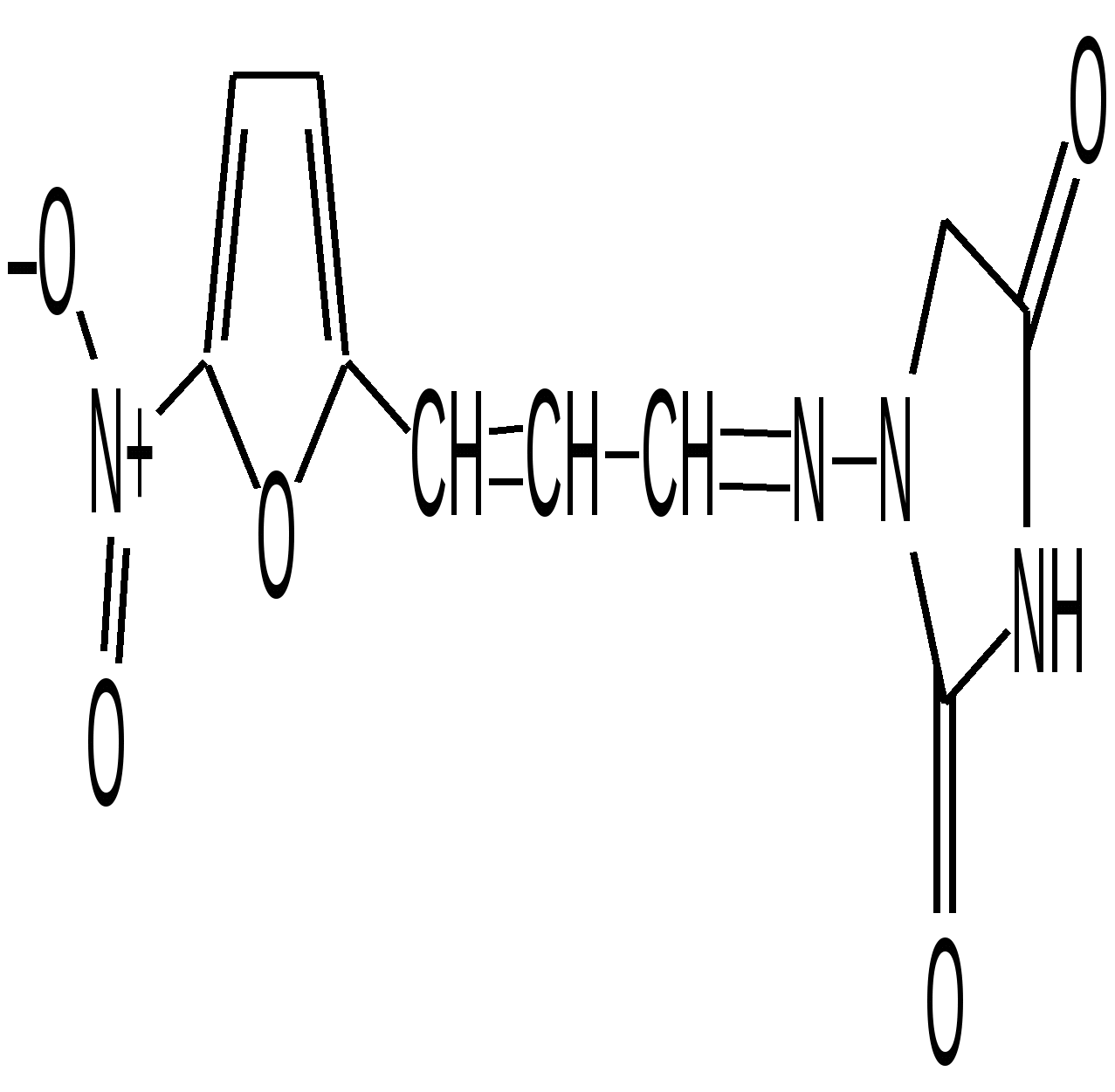 Описание: Желтый или оранжево-желтый мелкокристаллический порошок, без запаха, горький на вкус. Растворимость: Практически нерастворим в воде и спирте. Хранение: список Б. В сухом, защищенном от света месте. Применение: Применяют внутрь и местно. Внутрь назначают главным образом при заболеваниях мочевых путей (острые и хронические пиелонефриты, циститы, уретриты, инфекции после оперативных вмешательств на органах мочеполовой системы и др.). Форма выпуска: порошок; таблетки по 0, 05 г в упаковке по 100 штук. Азотосодержащие пятичленные гетероциклы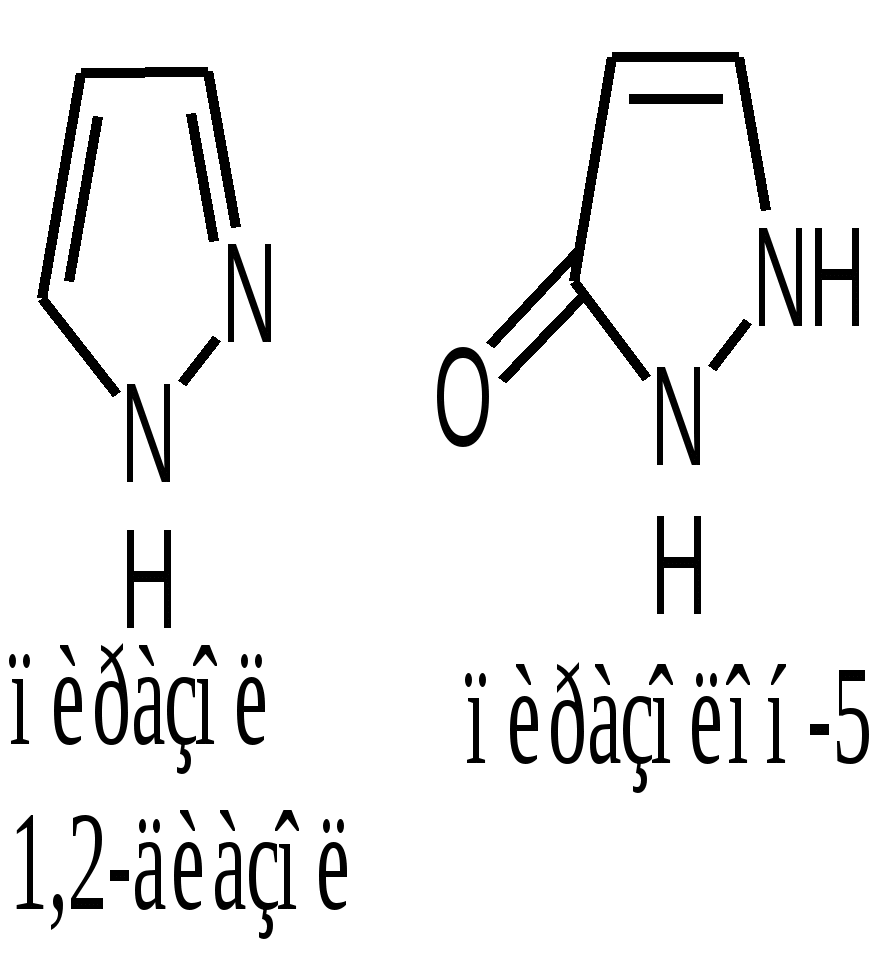 Antipyrinum (Антипирин)1-Фенил-2, 3-диметилпиразолон-5. 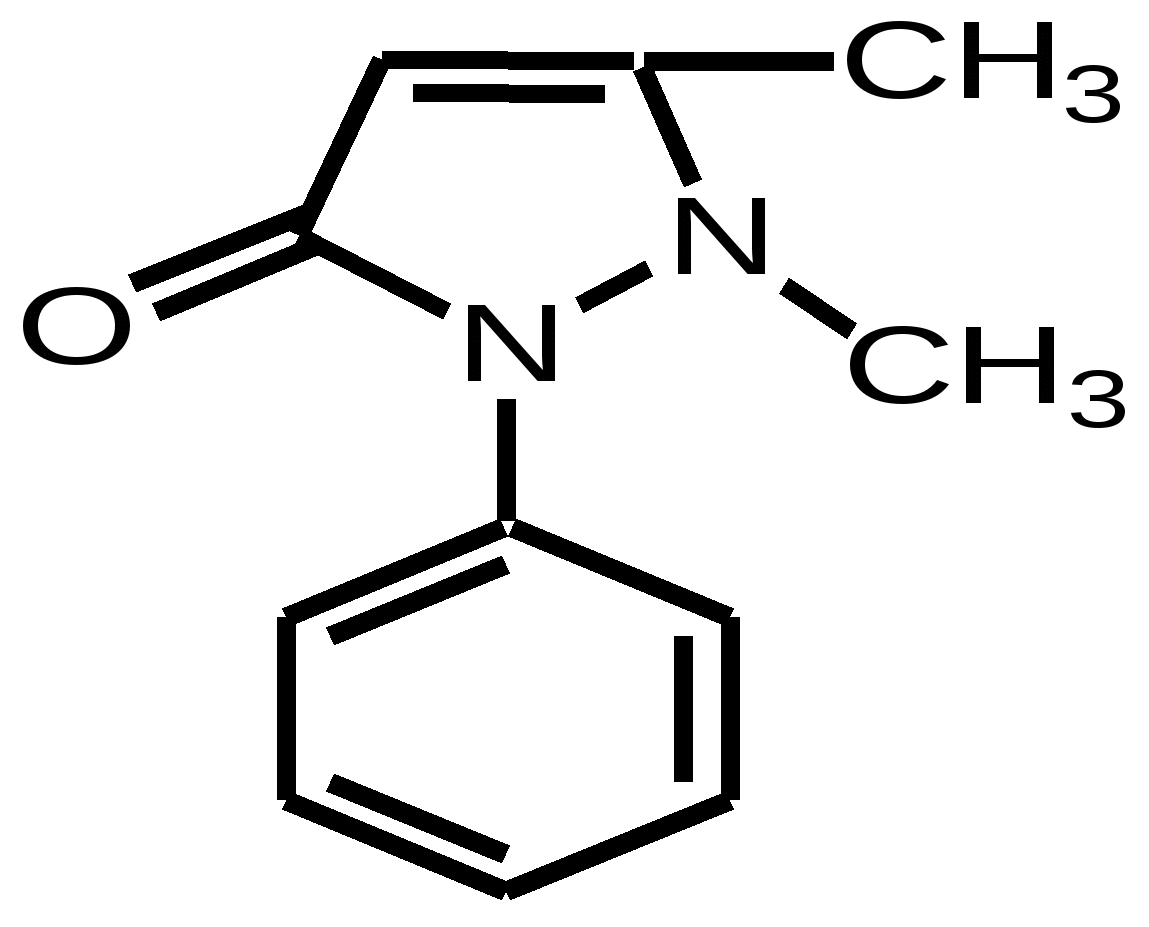 Получение: Синтез антипирина был осуществлен впервые Кнорром в 1883 г. Сырьём служат: фенилгидразин и ацетоуксусный эфир (реакция Кляйзена). 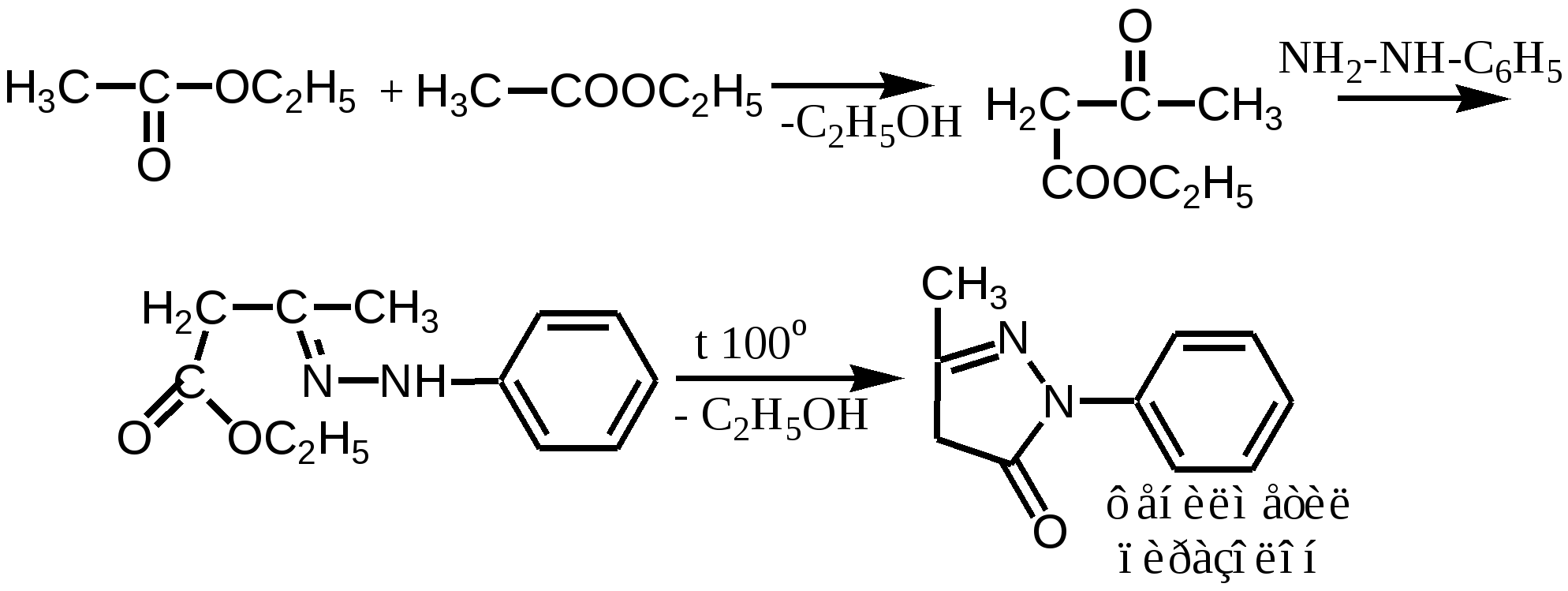 Реакцию ведут в нейтральной среде, т.к. в кислой фенилгидразин вступает в рекацию в другой таутомерной форме, в результате чего при циклизации получается побочный продукт снижающий выход и качество основного продукта – антипирина. Щелочная среда также непригодна, т.к. в этом случае образуется сильное осмоление. Полученный фенилметилпиразолон метилируют, затем обрабатывают щёлочью и выделяют свободный антипирин: 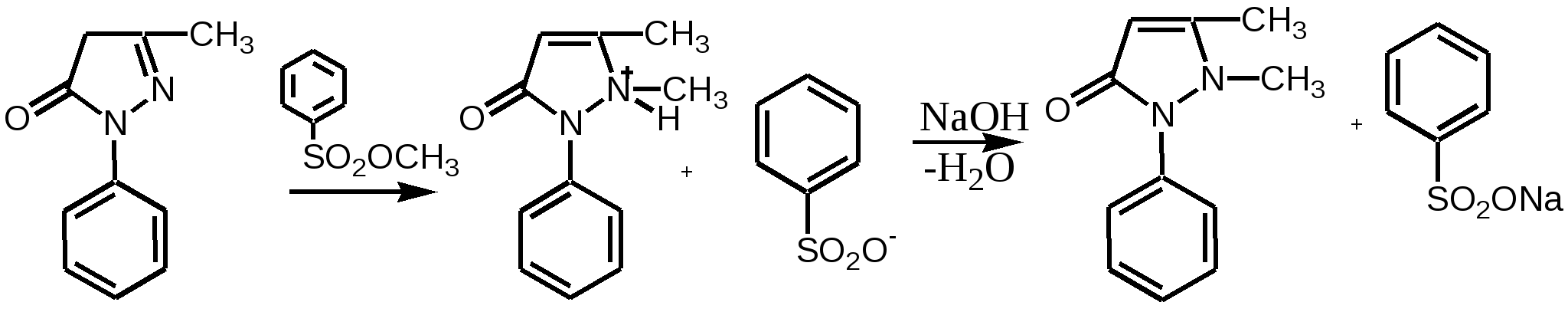 Описание: Бесцветные кристаллы или белый кристаллический порошок без запаха, слабогорького вкуса. Температура плавления = 110 – 113°С. Растворимость: Очень легко растворим в воде (1:1), легко - в спирте, хлороформе, трудно растворим в эфире . Подлинность: 1. Нитрозирование – образование нитрозоантипирина (изумрудно-зелёного цвета): 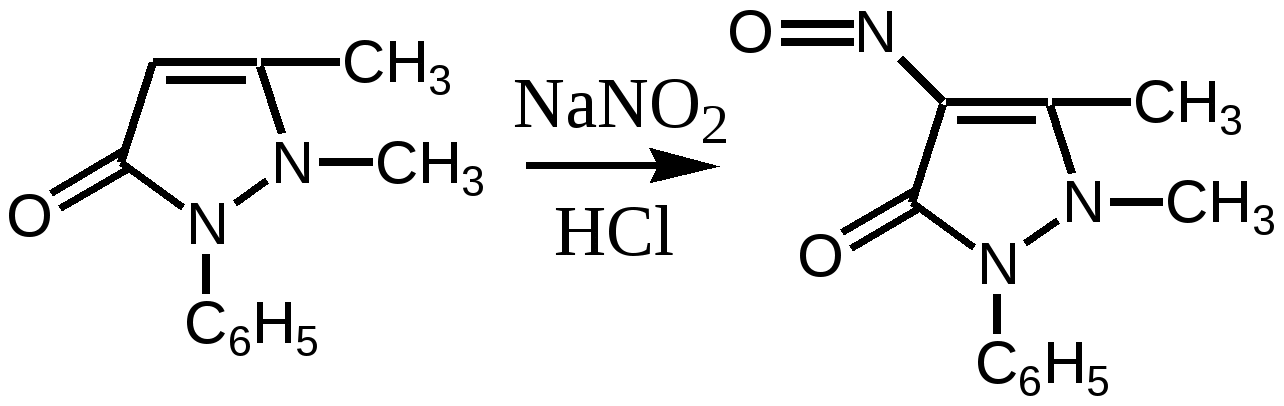 2. С FeCl3 – интенсивно красное окрашивание (у Татьяны Юрьевны в лекциях – коричневое), обусловленное образованием комплексной соли феррипирина: 3C11H12ON2•2FeCl3. Нефармакопейная: 1. (В ГФ10 нет, но в лекциях отнесена к фармакопейным) Образование фиолетово-красного пиразолонового красителя (в отличие от амидопирина). Для этой цели сначала нитрозируем антипирин в присутствии уксусной кислоты (см. реакцию выше, вместо HCl тут будет уксусная кислота). Избыток HNO2 разрушают азидом натрия, после чего вводят α-нафтиламин – образуется азокраситель: 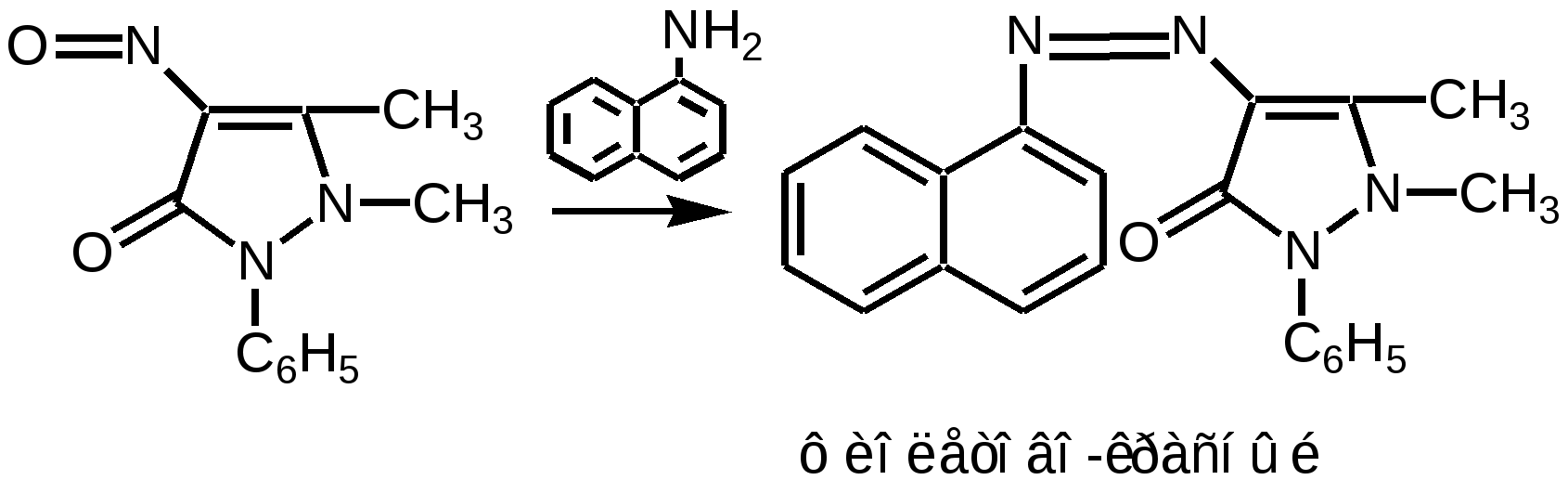 реакция является специфичной для антипирина! 2. Обрабатываем разбавленный раствор антипирина конц. раствором 2-нитроиндандиона в результате образуется оранжевая окраска, исчезающая при добавлении аммиака. Эта реакция специфична для антипирина. 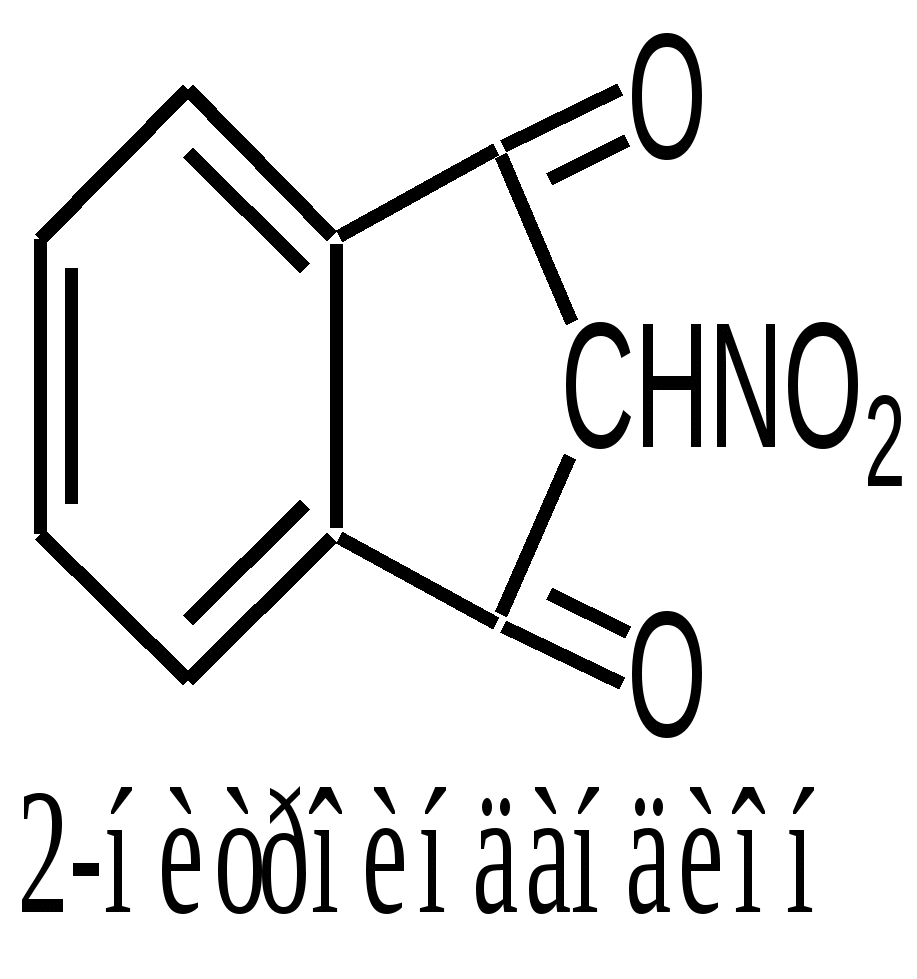 Чистота: 1. Температура плавления = 110 – 113°С. 2. Прозрачность и цветность. 3. Общие допустимые примеси: хлориды, сульфатная зола, органические примеси. 4. Специфические недопустимые: бензосульфонат натрия – раствор в 10 мл дихлорэтана должен быть бесцветным и прозрачным. Количественное определение: Используют обратную йодометрию в слабокислой среде: 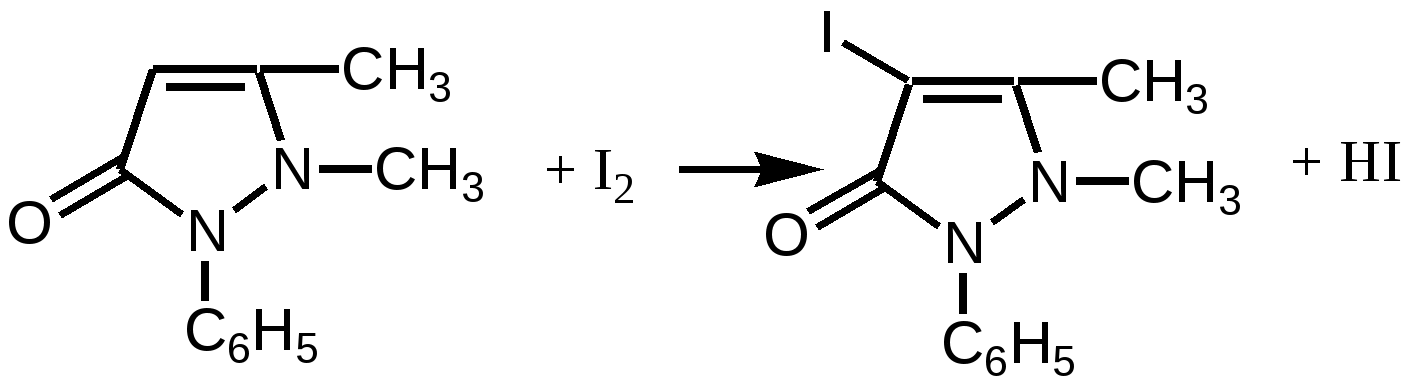 I2 + 2Na2S2O3 2NaI + Na2S4O6 HI + CH3COONa -> NaI + СН3СООН Реакцию ведут в присутствии ацетата натрия, чтобы связать выделяющийся HI и предотвратить обратимость процесса. Образующийся в процессе реакции йодопирин может адсорбировать на своей поверхности некоторое количество йода, поэтому добавляют спирт или хлороформ, которые растворяют образующийся йодопирин. Нефармакопейные: 1. Броматометрия в кислой среде: 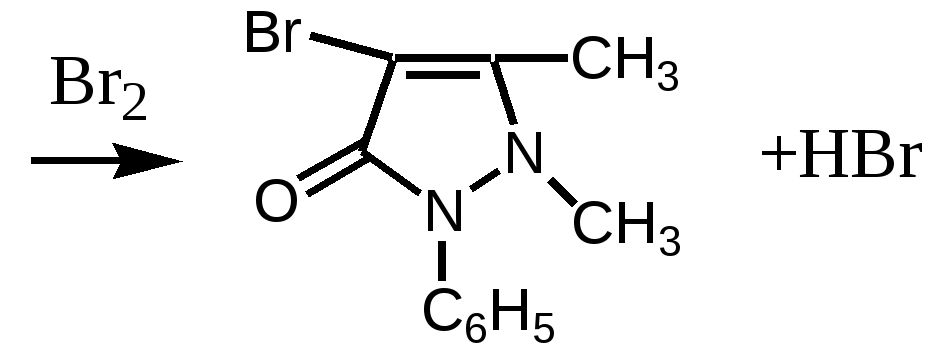 2. Йодхлорметрия: 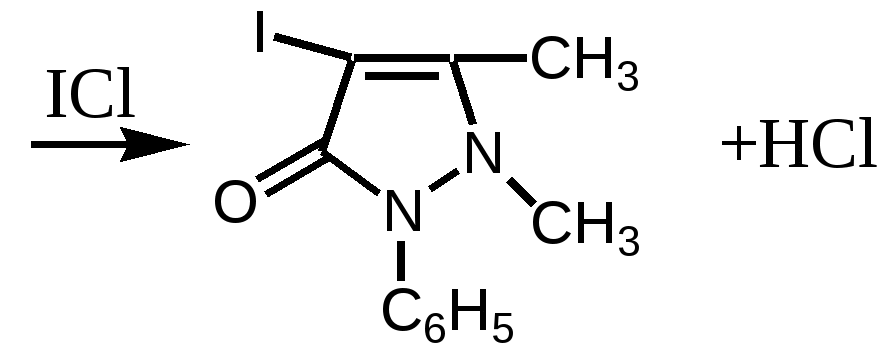 Хранение: список Б. В хорошо укупоренной таре, предохраняющей от действия света. Применение: Как и другие производные пиразолона, антипирин оказывает болеутоляющее, жаропонижающее и в той или иной степени противовоспалительное действие. По анальгезирующей и жаропонижающей активности препараты этой группы близки к производным салициловой кислоты. Производные пиразолона уменьшают проницаемость капилляров и препятствуют развитию воспалительной реакции. Форма выпуска: порошок и таблетки по 0,25 г. |
