Тест. Химия(тест с +). Тесты по неорганической, физической и коллоидной химии 1516 Учение о растворах Для какого вещества фактор эквивалентности
 Скачать 426.71 Kb. Скачать 426.71 Kb.
|
|
Кинетика химических реакций 1. Что такое скорость химической реакции? изменение концентрации реагирующих веществ в единицу времени ++ число молекул, принимающих участие в элементарном акте химической реакции число молекул субстрата, превращающихся под действием одной молекулы фермента сумма показателей степеней в кинетическом уравнении реакции изменение концентрации катализатора в единицу времени 2. Какое уравнение выражает зависимость скорости прямой реакции 2NO + O2 = 2NO2 от концентрации реагентов? w = [NO]2 + [O2] w = 2[NO][O2] w = 2[NO2]2 w = k[NO][O2] w = k[NO]2[O2] ++ 3. Какое уравнение выражает зависимость скорости обратной реакции 2NO + O2 = 2NO2 от концентрации реагентов? w = [NO2]2 w = 2[NO2] w = k[NO2]2 ++ w = k[NO][O2] w = k[NO]2[O2] 4. Какое уравнение соответствует закону действующих масс для прямой реакции A + B + B AB2? w = k[B][B] w = k[A][B] w = k[A][B]2 ++ w = k[AB2] w = k[A][B2] 5. ОСОБЕННОСТЯМИ КАТАЛИТИЧЕСКОГО ДЕЙСТВИЯ ФЕРМЕНТОВ ЯВЛЯЮТСЯ каталитическая активность, сопоставимая с неорганическими катализаторами независимость каталитического действия от температуры исключительно высокая каталитическая активность ++ независимость каталитического действия от рН сверхчувствительность к изменению рН ++ отсутствие температурного оптимума высокая специфичность действия ++ 6. Каким уравнением выражается скорость реакции первого порядка? w=k w=k. ca. cb. cс w=k. c ++ w=k. c2 w=k. ca .cb 7. В чем заключается функция ферментов в живом организме? транспорт оксигенов катализ биохимических реакций ++ обеспечение иммунитета обеспечение энергией перенесение кислорода к тканям и органам 8. СКОРОСТЬ РЕАКЦИИ ВЫРАЖАЕТСЯ КАК w = kC(O2) ДЛЯ РЕАКЦИЙ 1) 4Cu(т) + O2(г) 2Cu2O(т) ++ 2) 2SO2(г) + O2(г) 2SO3(г) 3) O2(г) + 2H2(г) 2H2O(ж) 4) 2NO(г) + O2(г) 2NO2(г) 5) CO(г) + O2(г) 2CO2(г) 6) 2C(т) + O2(г) 2CO(г) ++ 7) N2(г) + O2(г) 2NO(г) 9. Как изменится скорость прямой химической реакции СаСО3(т) = СаО(т) + CO2(г), если давление в системе увеличить в 5 раз? 1) увеличится в 5 раз 2) уменьшится в 25 раз 3) уменьшится в 5 раз 4) увеличится в 25 раз 5) не изменится ++ 10. Какая реакция является тримолекулярной? 1) H2 + J2 = 2HJ 2) J2 = 2J 3) 2NO + O2 = 2NO2 ++ 4) CO + Cl2 = COCl2 5) Ca(HCO3)2 H2O + CO2 + CaO 11. Какая формула соответствует константе равновесия реакции 2NO(г) + Cl2(г) 2NOCl(г)? 1) K = C2(NOCl) / C2(NO) . C(Cl2) ++ 2) K = C2(NO) . C(Cl2) 3) K = C2(NO) . C(Cl2) / C2(NOCl) 4) K = C2(NOCl) / C2(NO) + C(Cl2) 5) K = C2(NO) + C(Cl2) / C2(NOCl) 12. Какая формула соответствует выражению закона действующих масс для прямой реакции CaCO3(т) CO2(г) + CaO(т)? 1) w = k C(CaCO3) 2) w = k C(CaO) . C(CO2) 3) w = k ++ 4) w = k ( C(CaO) + C(CO2)) 5) w = k C(CO2) 13. Температурный коэффициент реакции γ=2. Как изменится скорость химической реакции при увеличении температуры с 35оС до 65оС? 1) увеличится в 8 раз ++ 2) уменьшится в 8 раз 3) не изменится 4) увеличится в 6 раз 5) уменьшится в 6 раз 14. Чему равна константа скорости химической реакции? произведению концентраций реагирующих веществ в степенях, равных их стехиометрическим коэффициентам числу молекул, участвующих в элементарном акте химической реакции сумме показателей степеней при концентрациях скорости химической реакции при концентрациях реагирующих веществ, равных единице ++ скорости химической реакции в любой момент времени 15. Как количественно выражается влияние концентрации реагирующих веществ на скорость химической реакции? правилом Вант-Гоффа законом действующих масс ++ уравнением Аррениуса уравнением Михаэлиса-Ментен уравнением Гендерсона-Гассельбаха 16. Как количественно может быть описана зависимость константы скорости химической реакции от температуры? правилом Панета-Фаянса законом действующих масс уравнением Аррениуса ++ уравнением Михаэлиса-Ментен уравнением Гендерсона-Гассельбаха 17. ФЕРМЕНТАТИВНУЮ РЕАКЦИЮ ХАРАКТЕРИЗУЮТ УТВЕРЖДЕНИЯ ферменты проявляют каталитическую активность в узком интервале температур ++ каталитическая активность ферментов зависит от кислотности или рН среды ++ энергия активации реакции при участии фермента не изменяется фермент не образует промежуточное соединение с субстратом ферменты обладают высокой специфичностью ++ один фермент ускоряет все биохимические реакции ферменты повышают энергию активации 18. ГОМОГЕННЫМИ РЕАКЦИЯМИ ЯВЛЯЮТСЯ FeO(т) + H2(г) Fe(т) + H2O(ж) C(т) + H2O(ж) H2(г) + CO(г) 2NO(г) + Cl2(г) 2NOCl(г) ++ 2H2(г) + O2(г) 2H2O(г) ++ SO2(г) + O2(г) 2SO3(г) ++ C(т) + 2H2(г) CH4(г) C(т) + O2(г) CO2(г) 19. ГЕТЕРОГЕННЫМИ РЕАКЦИЯМИ ЯВЛЯЮТСЯ FeO(т) + H2(г) Fe(т) + H2O(ж) CO(г) + H2O(г) CO2(г) + H2(г) NO(г) + O2(г) NO2(г) 2SO2(г) + O2(г) 2SO3(г) C(т) + CO2(г) 2CO(г) ++ C(т) + 2H2(г) CH4(г) ++ C(т) + O2(г) CO2(г) ++ Окислительно-восстановительные процессы 1. Как называется скачок потенциала, возникающий на границе раздела фаз раствор – раствор? потенциал покоя мембранный потенциал электродный потенциал диффузионный потенциал ++ электродвижущая сила 2. Какая система обладает самыми высокими окислительными свойствами? φ (Au3+/Au+) = 1,40 B φ (Fe3+/Fe2+) = 0,77 B φ (Co3+/Co2+) = 1,81 B ++ φ (Mn3+/Mn2+) = 1,51 B φ (Pb4+/Pb2+) = 1,70 B 3. Как рассчитывают электродвижущую силу гальванического элемента? 1) Е = φ1 + φ2 2) Е = φ1 – φ2 ++ 3) Е = φ1 φ2 4) Е = φ1 / φ2 5) Е = φ2 / φ1 4. ЭЛЕКТРОДАМИ ПЕРВОГО РОДА ЯВЛЯЮТСЯ Hg, Hg2Cl2│KCl Ag, AgCl│KCl Pt│Sn4+, Sn2+ Pt│Fe2+, Fe3+ Ag│AgNO3 ++ Cu│CuSO4 ++ Zn│ZnSO4 ++ 5. ЭЛЕКТРОДАМИ ВТОРОГО РОДА ЯВЛЯЮТСЯ Hg, Hg2Cl2│KCl ++ Ag, AgCl│KCl ++ Pt│Sn4+, Sn2+ Pt│Fe2+, Fe3+ Ag│AgNO3 Cu│CuSO4 Zn│ZnSO4 6. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫМИ ЭЛЕКТРОДАМИ ЯВЛЯЮТСЯ Hg, Hg2Cl2│KCl Ag, AgCl│KCl Pt│Sn4+, Sn2+ ++ Pt│Fe3+, Fe2+ ++ Ag│AgNO3 Cu│CuSO4 Zn│ZnSO4 7. Система (+) Ag│AgNO3(0,1н)║AgNO3(0.01н)│Ag(-) 1) электрод определения 2) электрод сравнения 3) электрод второго рода 4) концентрационный элемент ++ 5) окислительно-восстановительный элемент 8. Чему равен потенциал водородного электрода (В) при [H +]=10-2? -0,059 В +0,059 В -0,118 В ++ +0,118 В 0 В 9. Чему равен потенциал водородного электрода (В) при рН=10? 1) 0,59 2) -0,59 ++ 3) 0,30 4) -0,30 5) 0 10. ПРИ ПОТЕНЦИОМЕТРИЧЕСКОМ ОПРЕДЕЛЕНИИ рН БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ ИСПОЛЬЗУЮТ ЭЛЕКТРОДЫ 1) стандартный водородный 2) хлорсеребряный ++ 3) каломельный 4) водородный 5) стеклянный ++ 6) цинковый 7) медный 11. Какую пару электродов используют при потенциометрическом определении рН биологических жидкостей? 1) цинковый-медный 2) хлорсеребряный-стеклянный ++ 3) медный-водородный 4) цинково-водородный 5) каломельный-хлорсеребряный 12. Какая реакция протекает в гальваническом элементе ( -) Fe / FeSО4 // CuSО4 / Сu (+ ), (φ0 Fe / Fe2+ = - 0,44 В ; φ0 Сu / Сu2+ = +0,34 В)? 1) Fe0 + Cu2+ Fe2+ + Cu0 ++ 2) Cu0 + Fe2+ Fe0 + Cu2+ 3) Fe2+ + 2e Fe0 4) Cu0 - 2e Cu2+ 5) реакция не идет 13. Какая реакция протекает в гальваническом элементе (-) Zn/ZnS04 //CuS04 /Сu (+) (φ0Zn/Zn2+ = -0,76 B ; φ0Cu/Cu2+ = +0,34 B)? 1) Cu0 + Zn2+ Zn0 + Cu2+ ++ 2) Сu2+ + Zn0 Сu0 + Zn2+ 3) Сu0 - 2е Сu2+; 4) Zn2+ + 2e Zn0 5) реакция не идет 14. Какая реакция протекает в гальваническом элементе (-)Zn /ZnS04 // NiS04 /Ni (+) (φ0 Zn/Zn2+ = -0,76 B ; φ0 Ni/Ni2+ = -0,25 B)? 1) Ni0 + Zn2+ Zn0 + Ni2+ 2) Ni2+ + Zn0 Ni0 + Zn2+ ++ 3) Ni0 - 2е Ni2+ 4) Zn2+ + 2e Zn0 5) реакция не идет 15. Как называется скачок потенциала, возникающий на границе раздела фаз металл - раствор его соли? потенциал стандартного водородного электрода мембранный потенциал электродный потенциал ++ диффузионный потенциал электродвижущая сила 16. Как называется скачок потенциала, возникающий на границе раздела фаз мембрана - раствор вследствие избирательной проницаемости мембраны? потенциал стандартного водородного электрода мембранный потенциал ++ электродный потенциал диффузионный потенциал электродвижущую силу 17. Что такое электродвижущая сила гальванического элемента? отношение потенциалов электродов, составляющих гальванический элемент произведение потенциалов электродов, составляющих гальванический элемент потенциал положительно заряженного электрода сумму потенциалов электродов, составляющих гальванический элемент разность потенциалов электродов, составляющих гальванический элемент ++ 18. Как называется электрод, представляющий собой металл, погруженный в насыщенный раствор трудно растворимой соли этого металла и хорошо растворимой соли, имеющий общий анион с анионом трудно растворимой соли? электродом сравнения электродом определения электродом I рода электродом II рода ++ мембранным электродом 19. У какой системы наиболее высокие окислительные свойства? φ (Fe3+/Fe2+) = 0,77 B φ (2Hg2+/Нg22+) = 0,92 В ++ φ (Sn4+/Sn2+) = 0,15 B φ (Ti4+/Ti3+) = 0,06 B φ (Сu2+/Сu+) = 0,16 В Поверхностные явления 1. По какой формуле рассчитывают величину поверхностной активности?  ++ ++  Г = Г . C /(K + C)  2. По какой формуле рассчитывают величину адсорбции растворенного вещества на подвижной границе раздела фаз? 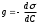 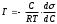 ++ ++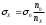 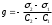 Г = Г . C /(K + C) 3. СОСТОЯНИЕ АДСОРБЦИОННОГО РАВНОВЕСИЯ ХАРАКТЕРИЗУЮТ УТВЕРЖДЕНИЯ процессы адсорбции и десорбции протекают одновременно ++ скорость адсорбции больше, чем скорость десорбции скорость адсорбции меньше, чем скорость десорбции процессы адсорбции и десорбции не протекают скорость адсорбции равна скорости десорбции ++ происходит только процесс адсорбции происходит только процесс десорбции 4. Как называется состояние системы, при котором скорость адсорбции равна скорости десорбции? положительная адсорбция отрицательная адсорбция удельная адсорбция капиллярная конденсация адсорбционное равновесие ++ 5. Какой процесс может быть использован для регенерации катионитов? нагревание замораживание обработка раствором щелочи обработка раствором хлорида натрия обработка раствором сильной кислоты ++ 6. Какой метод может быть использован для удаления ионов Са2+с целью предотвращения свертываемости крови при ее консервировании? диализ электрофорез хроматография молекулярная адсорбция ионообменная адсорбция ++ 7. ПОВЕРХНОСТНОЙ АКТИВНОСТЬЮ ОБЛАДАЮТ ВЕЩЕСТВА NH2CH2COOH C6H13COOH ++ С12Н22О11 С5Н11ОН ++ С6Н12О6 Н2SO4 HCl 8.У какого иона способность к адсорбции самая высокая? Na+ Ca2+ Al3+ Th4+ ++ K+ 9. Какое вещество будет адсорбироваться на поверхности активированного угля в виде молекулы? 1) CH3COONa 2) CH3COOH ++ 3) KOH 4) CaCl2 5) H2SO4 10. Какое уравнение описывает адсорбцию на границе раздела твердое тело – жидкость? 1) 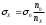 2) Г = Г . C /(K + C) ++ 3) 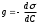 4) 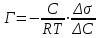 5) х = nx / n(H2O) 11. Как изменяется поверхностная активность водных растворов веществ одного гомологического ряда при удлинении углеводородной цепи на одну –СН2– группу согласно правилу Дюкло-Траубе? 1) увеличивается в 3-3,5 раза ++ 2) увеличивается в 2-4 раза 3) не изменяется 4) уменьшается в 2-4 раза 5) уменьшается в 3-3,5 раза 12. ГИДРОФИЛЬНЫМИ СВОЙСТВАМИ ОБЛАДАЮТ ГРУППЫ 1) – CH2–C6H5 2) – COOH ++ 3) – C2H5 4) – C6H5 5) –С4Н9 6) – NO2 ++ 7) –OH ++ 13. ГИДРОФОБНЫМИ СВОЙСТВАМИ ОБЛАДАЮТ ГРУППЫ 1) – CH2–C6H5 2) – COOH 3) – SO3H 4) – C5H11 ++ 5) – C6H5 6) – NH2 7) – С4Н9 ++ 8) – OH 14. НА ПОВЕРХНОСТИ БРОМИДА СЕРЕБРА СОГЛАСНО ПРАВИЛУ ПАНЕТА-ФАЯНСА АДСОРБИРУЮТСЯ ИОНЫ 1) NH4+ 2) NO3- 3) SO42- 4) Ca2+ 5) Al3+ 6) Ag+ ++ 7) Br- ++ 15. Какое вещество является поверхностно-активным? 1) серная кислота 2) карбонат натрия 3) изоамиловый спирт ++ 4) пероксид водорода 5) сахароза 16. Изотерма поверхностного натяжения показывает зависимость величины поверхностного натяжения σ от полярности растворенного вещества от полярности растворителя от температуры от концентрации растворенного вещества ++ от концентрации растворителя 17. У какого вещества величина поверхностной активности максимальна? СН3СООН С2Н5СООН НСООН С4Н9СООН ++ С3Н7СООН 18. У какого вещества величина поверхностной активности минимальна? С3Н7ОН С5Н11ОН С7Н15ОН С4Н9ОН С2Н5ОН ++ 19. Изотерма адсорбции представляет собой графическую зависимость величины адсорбции Г от полярности растворенного вещества от полярности растворителя от температуры от концентрации растворенного вещества ++ от концентрации растворителя 20. «На твердом адсорбенте адсорбируются те ионы, которые входят в состав адсорбента и могут достраивать его кристаллическую решетку» правило Ребиндера правило Гиббса правило Вант-Гоффа правило Панета-Фаянса ++ правилоЛе-Шателье 21. Как называется накопление одного вещества в объеме другого? адсорбция абсорбция ++ сорбция десорбция хемосорбция 22. Чем характеризуется явление хемосорбции? обратимостью легкой десорбируемостью малой прочностью образованием химических связей между адсорбентом и адсорбтивом ++ наличием слабых межмолекулярных сил ван-дер-ваальса между молекулами адсорбтива и поверхностью адсорбента Дисперсные системы Что характеризует изоэлектрическое состояние гранулы? высокий заряд гранулы отсутствие заряда гранулы ++ увеличение ζ-потенциала увеличение диффузионного слоя увеличение расклинивающего давления Как называется процесс оседания крупных агрегатов под действием силы тяжести? диффузия коагуляция коалесценция седиментация ++ пептизация Раствор какого электролита обладает наибольшим коагулирующим действием на золь с отрицательно заряженными частицами? K2SO4 NaNO3 CaCl2 AlCl3 ++ NaCl Раствор какого электролита обладает наибольшим коагулирующим действием на золь с положительно заряженными частицами? FeCl2 Na2SO4 CaCl2 K3PO4 ++ Al(NO3)3 Раствор какого электролита обладает наибольшим коагулирующим действием на золь с отрицательно заряженными частицами? AlCl3 ++ Ca(NO3)2 CaCl2 FeSO4 NaCl Раствор какого электролита обладает наибольшим коагулирующим действием на золь сульфата бария, полученного в избытке хлорида бария? AlCl3 FeSO4 ++ BaCl2 NaNO3 AgNO3 Раствор какого электролита обладает наибольшим коагулирующим действием на золь хлорида серебра, полученного в избытке нитрата серебра? FeCl2 Na2SO4 ++ CaCl2 KNO3 Al(NO3)3 С наибольшей скоростью коагулируют частицы с большим положительным зарядом с небольшим положительным зарядом электронейтральные ++ с небольшим отрицательным зарядом с большим отрицательным зарядом ДЛЯ ОЧИСТКИ КОЛЛОИДНЫХ РАСТВОРОВ ОТ НИЗКОМОЛЕКУЛЯРНЫХ ПРИМЕСЕЙ ИСПОЛЬЗУЮТ МЕТОДЫ электродиализ ++ электроосмос седиментация электрофорез коагуляция диализ ++ осмос 10.Как называется метод очистки коллоидных растворов, осуществляемый за счет разницы давлений по обе стороны полупроницаемой мембраны? диализ ++ осмос электрофорез ультрафильтрация ультрацентрифугирование 11. В какой дисперсной системе будет наблюдаться конус Тиндаля? 0,9% раствор NaCl раствор глюкозы золь серебра ++ суспензия глины в воде раствор нитрата серебра 12. Какой ион является потенциалопределяющим ионом при получении золя берлинской лазури Fe4[Fe(CN)6]3 действием на FeCl3 избытка К4[Fe(CN)6]? K+ 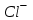 Fe3+ [Fe(CN)6]4 - ++  13. Какой ион является потенциалопределяющим ионом при получении золя берлинской лазури Fe4[Fe(CN)6]3 добавлением к К4[Fe(CN)6] избытка FeCl3? K+  Fe3+ ++ [Fe(CN)6]4 –  14. Как называется процесс объединения коллоидных частиц в более крупные агрегаты? коагуляцией ++ седиментацией тиксотропией синерезисом электрофорезом 15. Какая формула соответствует мицелле золя сульфата бария стабилизированного избытком K2SO4? 1)  2)  3)  ++ ++4)  5)  16. Какой ион быстрее вызывает коагуляцию отрицательно заряженного золя? Na+ K+ Mg2+ Fe3+ ++ Li+ 17. ПОТЕНЦИАЛОПРЕДЕЛЯЮЩИМИ ДЛЯ ЗОЛЯ СУЛЬФИДА ЖЕЛЕЗА МОГУТ БЫТЬ ИОНЫ HS- ++ Сl- Н+ АgO- K+ Fe3+ ++ SO42- 18.Какая мицеллярная формула соответствует золю бромида серебра стабилизированного нитратом серебра? 1) {m(АgВr)n К+(n-х)Cl-}x+ хСl- 2) {m(АgВr)n Br-(n-х)K+}x- хK+ 3) {m(АgВr)n SO42- 2(n-х)Na+}2x- хNa+ 4) {m(АgВr)n Ag+(n-х)NO3-}x+ хNO3- ++ 5) {m(АgВr)n J-(n-х)K+}x- хK+ 19. Как называется непрерывное хаотическое движение коллоидных частиц? осмосом диализом диффузией броуновским движением электроосмосом 20. Как называется самопроизвольное выравнивание концентрации коллоидных частиц по всему объему? 1) осмосом 2) диализом 3) диффузией 4) броуновским движением ++ 5) электроосмосом 21. В каких растворах наблюдается наиболее интенсивное броуновское движение? грубодисперсных коллоидных ++ истинных суспензиях эмульсиях 22. Для частиц каких растворов не характерно броуновское движение? грубодисперсных ++ коллоидных истинных молекулярно-дисперсных ионно-дисперсных 23. Для частиц дисперсной фазы каких растворов скорость диффузии максимальна? грубодисперсных коллоидных истинных ++ суспензий эмульсий 24. Для частиц дисперсной фазы каких растворов диффузия практически не наблюдается? грубодисперсных ++ коллоидных истинных молекулярно-дисперсных ионно-дисперсных 25. Для частиц дисперсной фазы каких растворов скорость седиментации максимальна? грубодисперсных ++ коллоидных истинных молекулярно-дисперсных ионно-дисперсных 26. ЯВЛЕНИЕ СЕДИМЕНТАЦИИ НАБЛЮДАЕТСЯ ДЛЯ РАСТВОРОВ молекулярно-дисперсных ионно-дисперсных грубодисперсных ++ коллоидных ++ истинных суспензий 27. Как называется движение заряженных коллоидных частиц к противоположно заряженному электроду? диализ электродиализ электроосмос электрофорез ++ вивидиализ 28. К МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИМ СВОЙСТВАМ КОЛЛОИДНЫХ СИСТЕМ ОТНОСЯТСЯ 1) образование конуса Тиндаля 2) броуновское движение ++ 3) светорассеяние 4) седиментация ++ 5) электрофорез 6) электроосмос 7) коацервация 8) диффузия ++ 29. К ОПТИЧЕСКИМ СВОЙСТВАМ КОЛЛОИДНЫХ СИСТЕМ ОТНОСЯТСЯ 1) образование конуса Тиндаля ++ 2) броуновское движение 3) светорассеяние ++ 4) седиментация 5) электрофорез 6) электроосмос 7) коацервация 8) диффузия Высокомолекулярные соединения 1. ПРИ ОГРАНИЧЕННОМ НАБУХАНИИ ОБРАЗЦА ПОЛИМЕРА ПРОИСХОДЯТ ПРОЦЕССЫ уменьшение объема до определенного значения уменьшение массы до определенного значения увеличение объема до определенного значения ++ увеличение массы до определенного значения ++ разрыв межмолекулярных связей растворение образца полимера 2. Как называется негидролитическое нарушение уникальной структуры нативного белка, сопровождающееся изменением его физико-химических и биологических свойств? коацервация денатурация ++ коалесценция тиксотропия коагуляция 3. Как называется самопроизвольный процесс поглощения низкомолекулярного растворителя высокомолекулярным веществом, сопровождающееся увеличением массы и объема? осмос коалесценция коацервация набухание ++ седиментация 4. СТЕПЕНЬ НАБУХАНИЯ ПОЛИМЕРА РАССЧИТЫВАЕТСЯ ПО ФОРМУЛАМ 1) 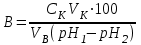 2) 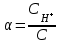 3) 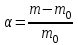 ++ ++4) 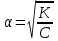 5) 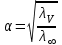 6) 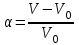 ++ ++7) 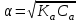 5.Как называется значение pH, при котором суммарный заряд белковой молекулы равен нулю? точка эквивалентности изоэлектрическая точка ++ точка равновесия константа равновесия константа диссоциации 6. Что является результатом неограниченного набухания полимера? 1) увеличение плотности 2) растворение полимера ++ 3) перемещение сетки полимера 4) увеличение массы полимера 5) уменьшение объема Что является количественной мерой набухания? масса сухого полимера масса набухшего полимера количество поглощенного растворителя степень набухания ++ степень полимеризации При каком рН наблюдается наименьшее набухание белков? рН < 0 рН = 7 рН = 4 pH = 0 рН = pI ++ Как называется процесс выпадения в осадок высокомолекулярных соединений под действием растворов электролитов? осаждение коагуляция фильтрация высаливание ++ коацервация Как называется процесс слияния гидратных оболочек молекул высокомолекулярных соединений без объединения самих частиц? фильтрация осаждение коагуляция коацервация ++ высаливание 11. Изоэлектрическая точка белка альбумина находится при рН=4,8. При каком зничении рН раствора молекулы белка альбумина заряжены положительно и при электрофорезе перемещаются к катоду? 1) 12 2) 8 3) 7,4 4) 5 5) 3 ++ 12. В растворе содержится смесь белков: γ-глобулин крови (pI=6,40); альбумин сыворотки крови (pI=4,64); цитохром С (pI=10,70). При каком значении рН можно электрофоретически разделить эти белки? 1) 3,55 2) 4,64 3) 6,40 ++ 4) 7,40 5) 10,70 13. Что такое онкотическое давление? 1) это осмотическое давление плазмы крови 2) это часть осмотического давления плазмы крови, обусловленная наличием в ней ионов натрия и хлорид-ионов 3) это часть осмотического давления плазмы крови, обусловленная только наличием в ней ионов натрия 4) это часть осмотического давления плазмы крови, обусловленная только наличием в ней хлорид-ионов 5) это часть осмотического давления плазмы крови, обусловленная наличием в ней молекул белка ++ 14. Как называются реакции образования ВМС, сопровождающиеся выделением побочных низкомолекулярных веществ (NH3, H2O, CO2, HCl) ? полимеризации поликонденсации ++ изомеризации соединения замещения 15. В результате каких реакций образуются белки? изомеризации полимеризации обмена поликонденсации ++ соединения 16. Как называется способность гелей под влиянием механического воздействия разжижаться, а затем в состоянии покоя вновь застудневать? коацервация тиксотропия ++ коалесценция синерезис синергизм 17. Как называется процесс разделения студня на две фазы с образованием уплотненного геля и разведенного золя? коацервация тиксотропия коалесценция синерезис ++ синергизм 18. В каком случае происходит наименьшее набухание желатина? в кислой среде в щелочной среде в ИЭТ ++ при рН = 0 в нейтральной среде 19. Как изменяется вязкость растворов ВМВ при повышении температуры? не изменяется увеличивается уменьшается ++ сначала увеличивается, потом уменьшается сначала уменьшается, потом увеличивается Тесты по правовой компетенции 1. Что является основным правилом при оказании помощи в случае острого отравления ядовитыми веществами независимо от тяжести отравления и состояния пострадавших? 1) вынести пострадавшего из зоны отравления 2) сделать искусственное дыхание, массаж сердца 3) дать пострадавшему противоядие 4) сделать пострадавшему промывание желудка 5) немедленно вызвать скорую помощь ++ 2. Что запрещено делать при поражении человека электрическим током? 1) прикасаться голыми руками к обнаженным частям тела пострадавшего, находящегося под действием тока ++ 2) отключить электроэнергию общим рубильником 3) отключить от сети прибор, вызвавший поражение 4) сделать пострадавшему искусственное дыхание и массаж сердца 5) немедленно вызвать врача 3. Какие емкости с реактивами и химическими веществами разрешено использовать в лаборатории? 1)емкости, снабженные этикетками с исправленными надписями 2)емкости, снабженные новыми этикетками, наклеенными поверх старых 3) емкости, снабженные легко стирающимися надписями 4) емкости без этикеток или с неясными надписями 5) емкости, снабженные разборчивыми надписями (название, химическая формула) ++ 4. Как называется вещество или смесь, добавляемое в материал органического происхождения для снижения его горючести? 1) антикоагулянт 2) антидепрессант 3) адсорбент 4) антипирен ++ 5) дегазатор 5. При химических ожогах пораженное место промывают струей воды из под крана в течение длительного времени (не менее 15 минут). Раствором какого вещества необходимо обработать место ожога в случае его поражения кислотой? 1) 2%-ным раствором виннокаменной кислоты 2) 2%-ным раствором лимонной кислоты 3) 2%-ным раствором уксусной кислоты 4) 2%-ным раствором бикарбоната натрия ++ 5) 2%-ным раствором гидроксида натрия Экзаменационные тесты по органической химии |
