Учебник по микробиологии. Учебник для товаровед, и технол фак торг вузов. 5е изд., перераб. М. Экономика, 1985. 256 с
 Скачать 2.41 Mb. Скачать 2.41 Mb.
|
|
Глава 2 ФИЗИОЛОГИЯ МИКРООРГАНИЗМОВ Физиология микроорганизмов изучает процессы их роста, развития, питания, способы получения энергии для осуществления этих процессов, а также происходящие при этом превращения веществ в клетке. Знания физиологии позволяют управлять жизнедеятельностью микроорганизмов, эффективно использовать их в практических целях – в сельском хозяйстве и в промышленности, а также найти средства борьбы с ними, когда это необходимо. ПОНЯТИЕ ОБ ОБМЕНЕ ВЕЩЕСТВ Основу жизнедеятельности микроорганизмов, как и всех живых существ, составляет обмен веществ (метаболизм) с окружающей средой. «Жизнь есть способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка»1. Обмен веществ представляет собой сложный комплекс разнообразных химических превращений веществ пищи, поступающей в организм из внешней среды (из субстрата). Поступившие в клетку питательные вещества подвергаются «переработке» и из образующихся простых соединений синтезируются сложные клеточные вещества. Этот процесс называют анаболизмом2 или строительным· (конструктивным) обменом. Для осуществления его и других жизненных функций (движения, размножения и др.) необходима энергия. Организм получает ее в результате окислительно-восстановительных превращений поступивших в него с пищей органических и неорганических веществ. Этот процесс называют катаболизмом3 или энергетическим обменом. 1 Энгельс Ф. Диалектика природы.– Маркс К., Энгельс Ф. Соч., т. 20, с. 616. 2 Ранее применялся термин «ассимиляция». 3 Ранее применялся термин «диссимиляция». Оба этих процесса (анаболизм и катаболизм) в совокупности составляют обмен веществ организма в целом. Они находятся в тесном взаимодействии и взаимозависимости, неотделимы один от другого, обусловливают рост, развитие и размножение организма. В этом проявляется один из законов диалектики – закон развития как борьбы противоположностей. Многочисленные химические реакции обмена веществ, управляемые ферментами, протекают в определенной последовательности; они согласованы между собой и гармонично сочетаются. Многие промежуточные продукты процессов энергетического обмена участвуют в реакциях процессов строительного обмена. Одно и то же вещество может служить и источником энергии, и материалом для синтеза компонентов тела, но нередко используют для этих целей разные вещества. Конечные продукты обмена веществ выделяются во внешнюю среду. - Особенностью микроорганизмов является большое разнообразие обменных процессов: различны потребности в питательных веществах для синтеза веществ тела, различны способы добывания энергии и, кроме того, у микробов необычайно интенсивный обмен веществ. За сутки при благоприятных условиях одна клетка потребляет пищу, масса которой в 30–40 раз больше массы тела микроба. Основная часть пищи расходуется в энергетическом обмене, при котором выделяется в среду большое количество продуктов обмена: кислот, спиртов, углекислого газа, водорода и др. Эта особенность микроорганизмов широко используется в практике переработки растительного и животного пищевого и непищевого сырья; она же обусловливает явление быстрой порчи пищевых продуктов. ХИМИЧЕСКИЙ СОСТАВ МИКРООРГАНИЗМОВ Для понимания процессов обмена веществ у микроорганизмов и их потребностей в пище необходимо знать химический состав их тела. Состав веществ микроорганизмов в принципе мало отличается от химического состава тела животных и растений. Важнейшими компонентами клетки являются белки, нуклеиновые кислоты, липиды. Универсальны многие ферменты строительного и энергетического обменов. Потребность микроорганизмов в питательных веществах определяется в основном элементарным составом их клеток. Важнейшими химическими элементами, преобладающими в клетках микроорганизмов, являются углерод, кислород, водород, азот, сера, фосфор, калий, магний, кальций и железо. Первые четыре из указанных элементов составляют основу органического вещества, поэтому называются органогенными элементами. Они составляют 90–97% сухого вещества. Другие элементы называют зольными или минеральными, на долю которых приходится 3–10%. Из них больше всего содержится фосфора, который входит в состав важных веществ клетки (нуклеиновых кислот, АТФ и др.). В клетках микроорганизмов находятся, хотя и в крайне малых количествах, микроэлементы: медь, цинк, марганец, молибден и многие другие. Некоторые микроэлементы входят в состав ферментов. Соотношение отдельных химических элементов заметно колеблется в зависимости от вида микроорганизма и условий его роста. Среднее количество отдельных элементов в клетках микроорганизмов приведено в табл. 1. Все элементы связаны в клетках в различные соединения, среди которых преобладает вода. Вода. Вода составляет 75–85 % массы клеток. Она имеет важное значение в жизни организма. Все вещества поступают в клетку только с водой, с ней же удаляются и продукты обмена. Часть воды в клетке находится в связанном состоянии (с белками, углеводами и другими веществами) и входит в клеточные структуры. Остальная вода находится в свободном состоянии: она служит дисперсной средой для коллоидов и растворителем различных органических и минеральных соединений, образующихся в клетке при обмене веществ. Вода – участник многих химических реакций, протекающих в клетке. Содержание свободной воды в клетке изменяется в зависимости от условий внешней среды, физиологического состояния клетки, ее возраста и т. п. Так, в спорах бактерий и грибов значительно меньше воды, чем в вегетативных клетках, ввиду низкого содержания в них свободной воды. Потеря свободной воды влечет за собой высыхание клетки и более или менее глубокие изменения обмена веществ. С потерей связанной воды нарушаются клеточные структуры и наступает смерть клетки. Органические вещества. Сухое вещество клеток микроорганизмов не превышает 15–25% и состоит преимущественно (до 85–95 %) из органических соединений – белков, нуклеиновых кислот, углеводов, липидов и др. Таблица 1
Белковые вещества являются основными компонентами клетки. Содержание их у бактерий достигает 40–80 % сухого вещества, у дрожжей – 40–60, у грибов–15–40%. Белкам принадлежит важнейшая роль в жизни организма. Аминокислотный состав белков микроорганизмов сходен с белками других организмов. Различное сочетание аминокислот создает огромное количество белков, обусловливающих все разнообразие организмов. Некоторые белки выполняют каталитические функции, катализируют различные биохимические реакции, протекающие постоянно в микробной клетке. Такие белки называют ферментами (подробно см. с. 48). Многие микроорганизмы накапливают большое количество белков в клетке. Считают, что микроорганизмы можно рассматривать в качестве возможных продуцентов пищевого и кормового белка. Рентабельность промышленного производства таких белковых продуктов определяется быстротой накопления биомассы микроорганизмов и использованием для их выращивания дешевого недефицитного сырья. Сырьем может служить гидролизат древесины или других растительных материалов, отходы пищевой, нефтеперерабатывающей и других отраслей промышленности. В СССР такой белок получают из дрожжей, некоторых бактерий, водоросли хлореллы и используют его в животноводстве и птицеводстве. В последние годы внимание микробиологов обращено на цианобактерии (сине-зеленые водоросли), некоторые из которых синтезируют большое количество белка. Многие страны мира получают в промышленном масштабе биомассу цианобактерии спирулины для использования в питании человека. Такие работы ведутся и в СССР. В клетке микроорганизмов содержатся нуклеиновые кислоты (ДНК и РНК). Молекула нуклеиновой кислоты представляет собой длинную цепь, которая состоит из многих элементарных единиц, называемых нуклеотидами. В состав каждого нуклеотида входят молекула фосфорной кислоты, молекула углеводного компонента (пентозы или дезоксипентозы) и одного азотистого основания (пуринового или пиримидинового). ДНК (дезоксирибонуклеиновая кислота) содержит дезоксирибозу и азотистые основания: аденин, гуанин, цитозин, тимин. В молекуле ДНК закодирована вся наследственная информация клетки, «записаны» все особенности будущего организма, выработанные в процессе длительной эволюции и свойственные данному виду. Через ДНК наследственные особенности передаются потомкам. ДНК сосредоточена главным образом в ядре клеток или в его аналоге – нуклеоидах бактериальных клеток. РНК (рибонуклеиновая кислота) содержит рибозу и азотистые основания: аденин, гуанин, цитозин и урацил. РНК преимущественно сосредоточена в цитоплазме и в рибосомах. РНК рибосом участвует в синтезе белка. Углеводы входят в состав различных мембран клеток микроорганизмов. Они используются для синтеза различных веществ в клетке и в качестве энергетического материала. Углеводы могут откладываться в клетке в виде запасных питательных веществ. В клетках большинства бактерий углеводы составляют 10–30% сухого вещества, у грибов – 40 – 60%. В теле микроорганизмов углеводы встречаются преимущественно в виде полисахаридов – гликогена, гранулезы (углевод, близкий к крахмалу), декстрина, клетчатки или близких ей соединений. Полисахариды находятся и в связанном состоянии с белками, липидами. Липиды в клетках большинства микроорганизмов составляют 3–10 % сухого вещества. Лишь у некоторых дрожжей и плесеней количество липидов может быть значительно выше – до 40–60%· Липиды входят в состав цитоплазматиче-ской мембраны и в состав других мембран, а также откладываются в виде запасных гранул. В клетках микроорганизмов часто обнаруживают пигменты, витамины и другие органические вещества. Пигменты, или красящие вещества, у некоторых микроорганизмов составляют значительную долю сухого вещества клетки. Пигменты обусловливают окраску микроорганизмов, а иногда выделяются в окружающую среду. Фотосинтезирующие бактерии содержат особые пигменты типа хлорофилла растений – бактериохлорофилл, который отличается по строению от хлорофилла растений. В настоящее время известно четыре типа бактериохлорофилл а: а, Ь, с, d. Фототрофные микроорганизмы и некоторые дрожжи образуют, кроме того, пигменты каротиноиды. Каротиноиды, как и бактериохлорофилл, участвуют в ассимиляции углекислого газа. У некоторых дрожжей в значительных количествах образуются желто-розовые и оранжевые каротиноиды, которые являются провитаминами витамина А. Производство таких дрожжей перспективно для получения белково-витаминных кормовых продуктов. Минеральные вещества составляют не более 5– 15 % сухого вещества клетки. Они представлены сульфатами, фосфатами, карбонатами, хлоридами и др. Фосфаты могут быть в свободном виде и входить в состав различных соединений. Минеральные соединения играют большую роль в регуляции внутриклеточного осмотического давления и коллоидного состояния цитоплазмы. Они влияют на скорость и направление биохимических реакций, являются стимуляторами роста, активаторами ферментов. ФЕРМЕНТЫ МИКРООРГАНИЗМОВ Общая характеристика Все разнообразные и многочисленные биохимические реакция, протекающие в живом организме в связи с его обменом веществ, ростом и развитием, совершаются при участии ферментов – биологических катализаторов, вырабатываемых клетками организма. Ферменты «есть в полном смысле возбудители жизни»,– писал академик И. П. Павлов. Структура и свойства ферментов. Ферменты представляют собой белки простые (протеины) или сложные (протеиды), состоящие из белка и небелкового компонента, называемого π ρ о -стетической (активной) группой. Таким образом, есть ферменты однокомпонентные и двухкомпонентные. В состав простетической группы ферментов входят витамины или их производные, различные металлы (Fe, Co, Си), азотистые основания и др. Простетическая группа ферментов обусловливает их каталитическую способность, а белковая часть – специфические свойства, избирательную способность действовать на определенный субстрат. Прочность связи простетической группы с белком у разных ферментов неодинакова. У некоторых простетическая группа легко может отделяться от белковой части и вступать во временную связь с другими белками. Такие простетические группы называют коферментами. В однокомпонентных ферментах роль активной группы выполняют определенные химические группировки в молекуле белка, составляя активный центр фермента. Такими группировками могут быть SH-группа, остатки отдельных аминокислот и др. Ферменты обладают очень высокой активностью. Ничтожно малого количества фермента достаточно, чтобы вовлечь в реакцию значительную массу реагирующего вещества (субстрата). Например, грамм амилазы при благоприятных условиях может превратить в сахар тонну крахмала. Ферменты действуют чрезвычайно быстро, резко ускоряя реакцию. Молекула фермента за минуту может вызвать превращение десятков и сотен тысяч молекул соответствующего субстрата. Характерной особенностью ферментов, отличающей их от неорганических катализаторов, является субстратная специфичность и специфичность действия – каждый фермент взаимодействует лишь с одним определенным веществом и катализирует лишь одно из тех превращений, которым может подвергаться данное вещество. Например, фермент лактаза вызывает расщепление только молочного сахара (лактозы) на глюкозу и галактозу и не действует на другие углеводы; фермент каталаза – только перекись водорода с образованием воды и свободного кислорода и т. д. Специфичность ферментов обусловлена структурными особенностями молекул фермента и субстрата. Субстрат и фермент подходят друг к другу, как ключ к замку. Катализируемая ферментом реакция начинается со связывания субстрата с белковой частью фермента в определенном участке ее – активном центре. Образуется комплекс фермент-субстрат. По окончании реакции образовавшийся комплекс фермента с продуктами реакций распадается с освобождением исходного фермента и конечных продуктов ферментативного процесса (рис. 18). Ферменты отличаются неустойчивостью (лабильностью) к воздействию ряда факторов внешней среды. Эта неустойчивость во многом объясняется белковой природой ферментов и выражается в том, что они теряют свою активность (инактивируются). 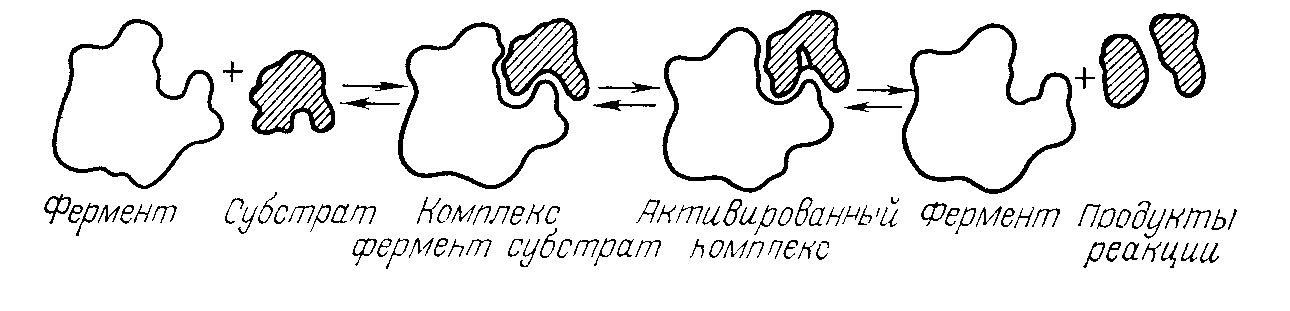 Рис. 18. Схема взаимодействия фермента с субстратом Условия действия ферментов. Важнейшим фактором, определяющим активность ферментов, является температура. По мере повышения температуры возрастает начальная скорость ферментативной реакции. Однако при достижении известного предела дальнейшее повышение температуры вызывает денатурацию ферментного белка. Концентрация активного фермента в субстрате непрерывно уменьшается, и чем выше температура, тем быстрее происходит деструкция фермента. Эта сложная зависимость ферментных реакций от температуры показана на рис. 19. Ход ферментативной реакции при различных значениях температуры практически характеризуется кривой ОМС, как некоторой результирующей двоякое действие повышения температуры: с одной стороны, ускорение химической реакции, с другой – повышение скорости инактивации фермента. Оптимальная температура, при которой данный фермент наиболее активен, для разных ферментов различна и в известной мере характеризует каждый фермент. У холодолюбивых микроорганизмов температурный оптимум ферментов значительно ниже, чем у теплолюбивых. Однако оптимальная температура действия каждого фермента не является постоянной величиной и зависит от условий, в частности от продолжительности реакции. Некоторые ферменты после тепловой инактивации восстанавливают свою каталитическую активность (в случае обратимого процесса денатурации белка). Уровень температуры, вызывающий денатурацию различных ферментов, неодинаков. Для одних ферментов это 40– 50 °С, для других (термоустойчивых) – только 70 °С, но при температуре около 100 °С почти все ферменты полностью инак-тивируются. При температуре ниже оптимальных пределов скорость ферментативных процессов уменьшается. В условиях температур, близких к нулю, и особенно ниже нуля, эти реакции значительно замедляются, а некоторые приостанавливаются, хотя при таких температурах ферменты заметно не разрушаются. Имеются исследования, показывающие, что ферменты сохраняют свою активность в замороженных продуктах. Лучистая энергия (ультрафиолетовые лучи, радиоактивные излучения) инактивирует ферменты. Большое влияние на ход ферментативных процессов оказывает pH среды. Для одних ферментов лучшей является среда со слабокислой реакцией, для других – со слабощелочной реакцией. Для действия каждого фермента имеется свое оптимальное значение рН среды. При значении pH выше или ниже оптимальной величины активность ферментов снижается. На активность ферментов влияет и присутствие в среде некоторых химических веществ. Одни из них ускоряют ферментативную реакцию (активаторы), другие способны снижать ее или полностью приостановить (ингибиторы). Действие многих активаторов и ингибиторов специфично. Активаторами ферментов являются металлы (Си, Ni, Mg, Co) и некоторые органические вещества, например витамины. Ингибиторами ферментов служат соли тяжелых металлов, антибиотики, H2S и др. Сущность действия ингибиторов состоит в том, что они соединяются с активными группами или активными центрами ферментов, парализуя тем самым связывание с ними субстрата. Концентрация субстрата, т. е. вещества, на которое действует фермент, и концентрация фермента также влияют в известной мере на скорость процессов. При малых концентрациях субстрата, когда фермент оказывается в избытке, скорость ферментативной реакции падает; уменьшение скорости реакции наблюдается и при избытке субстрата. 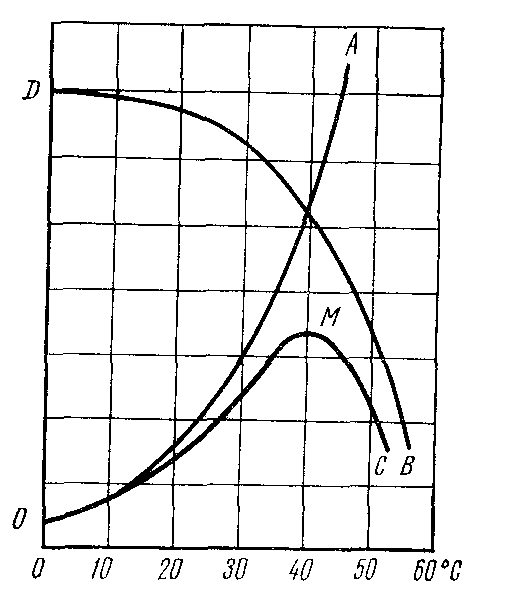 Рис. 19. Действие температуры на активность ферментов: 0А – скорость реакции; DB– скорость инактивирования ферментов; ОМС – ход ферментативной реакции Биохимические процессы, протекающие в микробных клетках,- регулируются ферментами, поэтому любой фактор, действующий на активность фермента, будет действовать и на микроорганизм. Каждый микроорганизм обладает комплексом разнообразных ферментов, своеобразием и активностью которых определяется их биохимическая деятельность, избирательность в отношении питательных веществ, роль микроорганизмов в круговороте веществ в природе, в процессах порчи пищевых продуктов. Многие ферменты микроорганизмов аналогичны ферментам растений и животных, но существуют и такие, которые не встречаются ни в растениях, ни у животных. Ферменты, присущие данному микроорганизму, входящие в число компонентов его клетки, называют конститутивными. Существуют ферменты индуцируемые (адаптивные), которые вырабатываются клеткой только при добавлении к среде вещества (индуктора), стимулирующего синтез данного фермента. Например, микроорганизм, не ассимилирующий мальтозу, можно приучить к использованию ее, культивируя в среде с этим сахаром как единственным источником углерода. В этих условиях микроорганизм синтезирует фермент мальтазу, которым ранее он не обладал. В живой клетке действие ферментов происходит упорядочение, строго согласованно. Ферменты локализованы в различных клеточных структурах (в мезосомах, митохондриях, цито-плазматической мембране и др.). Некоторые ферменты выделяются микроорганизмами наружу (в среду); их принято называть экзоферментами. Они играют большую роль в подготовке пищи к ее поступлению в клетку. Происходит внеклеточное «переваривание» пищи – расщепление сложных веществ субстрата (крахмала, белков и др.) на более простые, способные проникать в клетку. Ферменты, не выделяющиеся при жизни клетки в окружающую среду, называют эндоферментами (внутриклеточными). Они участвуют во внутриклеточных процессах обмена веществ. Хотя ферменты вырабатываются клеткой, но и после ее смерти временно остаются в активном состоянии и может произойти автолиз (от греч. autos – сам, lysis – растворение) – саморастворение, или самопереваривание, клетки под влиянием внутриклеточных ферментов. При разрушении клеток ферменты поступают в среду – в субстрат, в котором развивались микроорганизмы. При хранении пищевых продуктов, значительно обсемененных микроорганизмами, даже в условиях, исключающих их развитие, возможно снижение качества продуктов за счет ферментов автолизированных микробных клеток. | ||||||||||||||||||
