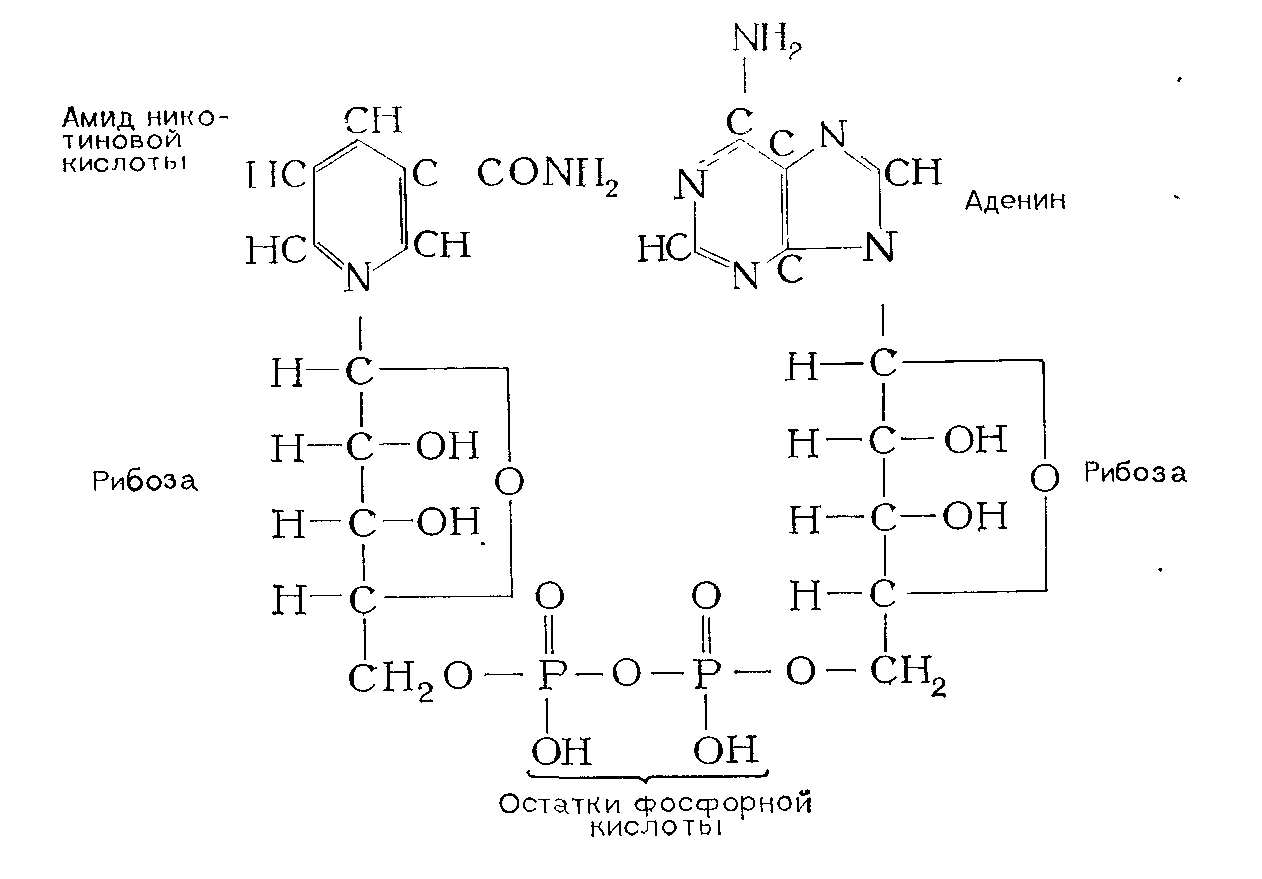|
|
Учебник по микробиологии. Учебник для товаровед, и технол фак торг вузов. 5е изд., перераб. М. Экономика, 1985. 256 с
Классификация ферментов
Номенклатура ферментов складывалась постепенно, по мере их открытия и изучения. Названия ферментов вначале носили случайный характер. Например, фермент, расщепляющий крахмал, был назван диастазом, а фермент желудочного сока, расщепляющий белки, – пепсином. Позднее название фермента стали составлять из корня слова, обозначающего вещество, на которое действует фермент, добавляя к нему окончание «аза». Фермент, расщепляющий крахмал (амилум), стали называть амилазой, фермент, разлагающий мальтозу, – мальтазой и т. п. Наряду с этим ферменты называют и по функции – по химическим процессам, которые они катализируют. Например, ферменты, катализирующие отщепление водорода от субстрата (дегидрогенерирование), называют дегидрогеназами, а расщепляющие сложные органические соединения путем гидролиза – гидролазами и т. д.
В соответствии с принятой в настоящее время классификацией ферментов (Правила номенклатуры ферментов, 1972) все ферменты делят на 6 классов: 1–оксидоредуктазы; 2 – транс-феразы; 3 – гидролазы; 4 – лиазы; 5 – изомеразы; 6 – лигазы. Классы подразделяют на подклассы, которые делят на под-подклассы. Каждый фермент имеет название и шифр из четырех цифр. Первая цифра обозначает класс, вторая – подкласс, третья – подподкласс, четвертая – порядковый номер данного фермента.
В настоящее время известно более 1000 ферментов.
Ниже рассматриваются только некоторые наиболее распространенные ферменты микроорганизмов.
Оксидоредуктазы – окислительно-восстановительные ферменты. В этот класс входят многочисленные ферменты, катализирующие окислительно-восстановительные реакции процессов дыхания и брожения микроорганизмов. Среди оксидоредуктаз различают следующие ферменты.
Дегидрогеназы – ферменты, катализирующие реакцию де-гидрогенерирования органических соединений: отщепление водорода. Отнятый водород передается дегидрогеназой какому-либо другому веществу (промежуточному – временному или конечному акцептору водорода). Одновременно одно вещество окисляется, а другое восстанавливается.
Дегидрогеназы специфичны по отношению к донору водорода (веществу, подвергающемуся дегидрогенерированию) и к акцептору водорода. Их делят на анаэробные и аэробные.
Анаэробные (первичные) дегидрогеназы передают отнятый от окисляемого субстрата водород другим дегид-рогеназам или молекулам каких-либо органических веществ. Эти дегидрогеназы являются двухкомпонентными ферментами. Их простетическая группа при диализе легко отделяется в виде кофермента.
Коферменты анаэробных дегидрогеназ построены по типу динуклеотидов. Каждый нуклеотид содержит органическое основание (чаще гетероциклическое), которое через пентозу соединено с фосфорной кислотой. Коферментом многих анаэробных дегидрогеназ является никотинамидадениндинуклеотид (сокращенно НАД).
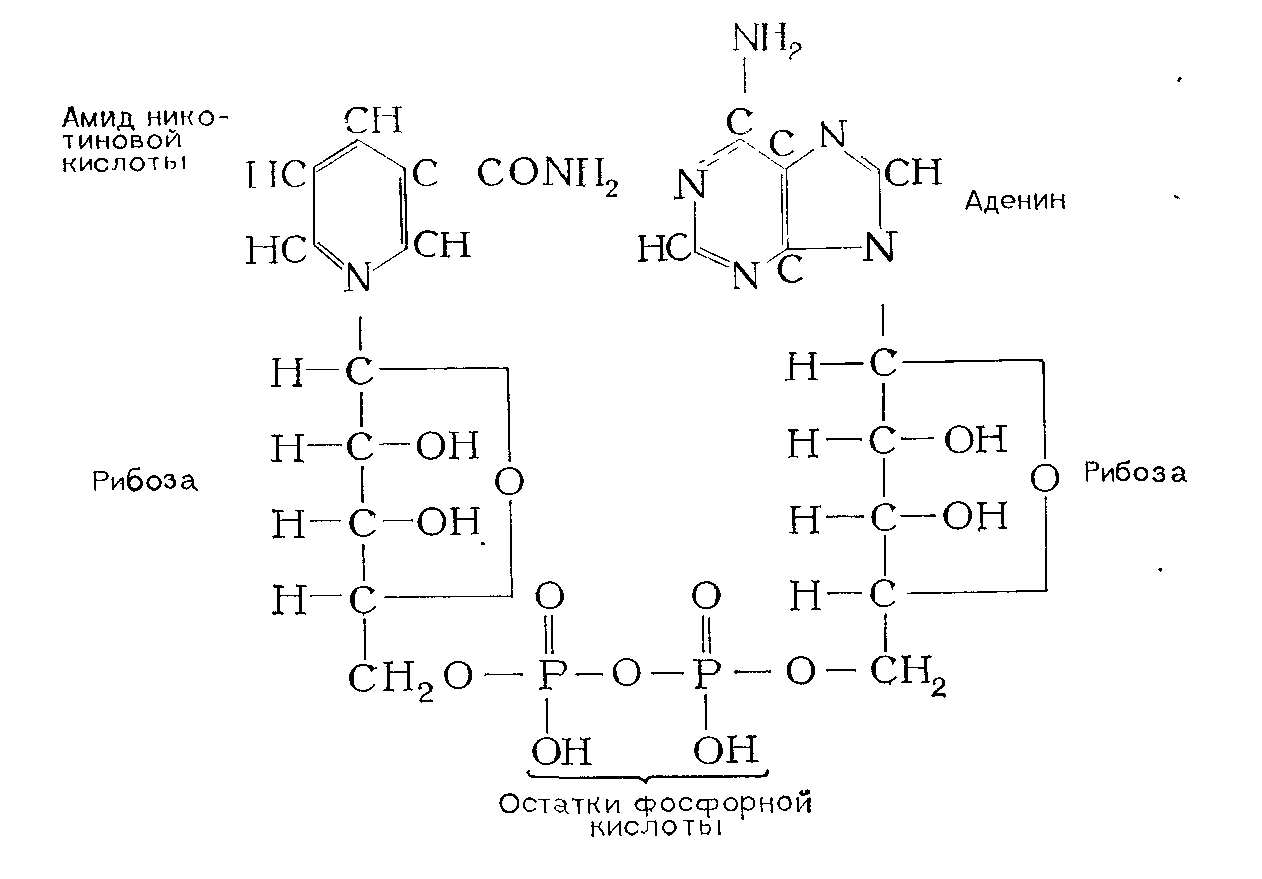
Кофермент, присоединяя водород от окисляемого вещества, превращается в восстановленную форму – НАД·Н2. Передавая затем водород другому веществу, он восстанавливает его, а НАД · Нг снова превращается в НАД (окисляется).
Анаэробные дегидрогеназы имеются как у анаэробов, так и у аэробов (см. с. 65).
Аэробные (вторичные) дегидрогеназы передают активированный водород, отнятый у окисляемого вещества или от восстановленной анаэробной^ дегидрогеназы, кислороду воздуха непосредственно либо через промежуточных переносчиков.
Аэробные дегидрогеназы, передающие водород субстрата только непосредственно кислороду, называют оксидазами. К оксидазам относится, например, полифенолоксидаза, катализирующая реакцию окисления полифенолов с образованием темноокрашенных соединений меланинов. Этот фермент имеется у многих плесневых грибов. Действие полифенолоксидазы проявляется в потемнении тканей плодов и овощей, пораженных этими плесенями.
К аэробным дегидрогеназам относятся флавиновые ферменты, коферментом которых является флавин-аденин-дину-клеотид (ФАД). Поскольку в состав кофермента входит рибофлавин (витамин В2), флавиновые ферменты окрашены в желтый цвет. Одни флавиновые ферменты могут переносить водород непосредственно на кислород, т. е. являются оксидазами; другие передают водород от окисляющихся веществ кислороду через ряд промежуточных переносчиков. В таких случаях участвуют системы ферментов, а водород многократно переносится от одного вещества к другому, пока не достигнет своего конечного акцептора – кислорода. Последний подвергается восстановлению с образованием воды или перекиси водорода.
Особо важное значение в процессах аэробного дыхания имеет цитохромная ферментная система, состоящая из цитохро-мов и фермента цитохромоксидазы.
Цитохромы представляют собой гемопротеиды. В состав простетической группы (гема) входит двухвалентное железо. Роль цитохромов в процессе дыхания заключается в последовательном переносе электронов от водородного атома восстановленной дегидрогеназы на цитохромоксидазу.
Цитохромоксидаза – двухкомпонентный гемосодержа-щий фермент, катализирует окислительно-восстановительную реакцию между восстановленным цитохромом (последним в цепи цитохромов) и кислородом (см. с. 69).
Цитохромная система содержится в клетках всех микроорганизмов, за исключением облигатно-анаэробных бактерий.
Пероксидаза – железосодержащий двухкомпонентный фермент, катализирующий окисление органических веществ с помощью перекиси водорода или каких-либо органических перекисей. Перекиси действуют как акцепторы водорода.
Каталаза – двухкомпонентный фермент, простетическая группа которого аналогична таковой у пероксидазы. Каталаза расщепляет перекись водорода на воду и молекулярный кислород. В процессе дыхания нередко образуется перекись водорода – вещество, ядовитое для клетки.
Трансферазы – ферменты переноса. Ферменты этой группы катализируют перенос атомных группировок от одного соединения к другому. Известно много таких ферментов; их различают по тем группам, перенос которых они катализируют.
Наиболее важное значение в обмене веществ имеют фосфо-трансферазы и аминотрансферазы.
Фосфотрансферазы (киназы) катализируют перенос остатков фосфорной кислоты с одного вещества на другое вещество.
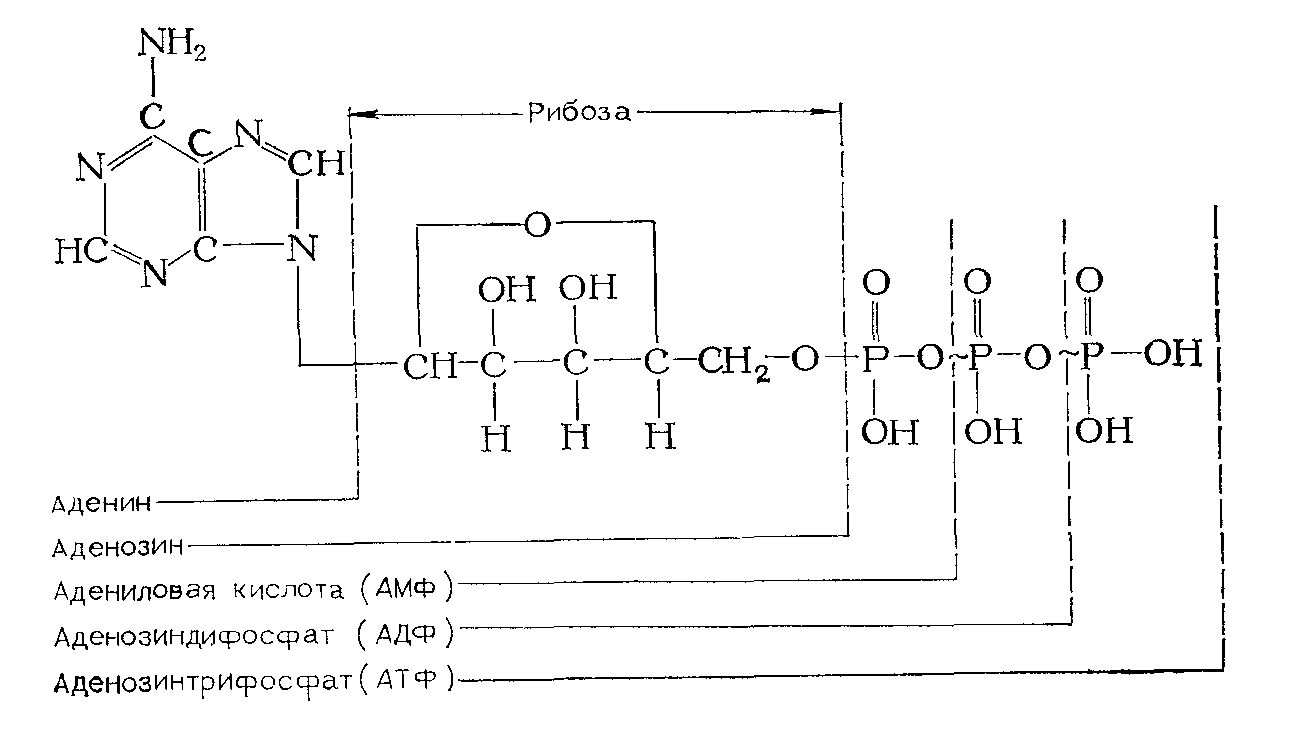
Большинство реакций переноса фосфатных групп протекает с участием аденозинтрифосфата (АТФ) и аденозиндифос-фата (АДФ). Эти реакции имеют большое значение, благодаря им осуществляется перенос энергии с одного вещества на другое.
Из приведенной ниже формулы АТФ видно, что это соединение имет одну простую связь (–) и две макроэргических (богатых энергией), обозначаемых значком (
). При гидролизе обычной фосфатной связи освобождается 8,4·103–12,6·103 Дж на грамм-молекулу отщепленного фосфата, а при гидролизе макроэргической связи – около 4,2 • 104 Дж.
Примером фосфотрансфераз может служить гексоки-н а з а – фермент, катализирующий перенос остатка фосфорной кислоты с АТФ на глюкозу. При этом образуются фосфорный эфир глюкозы и АДФ:
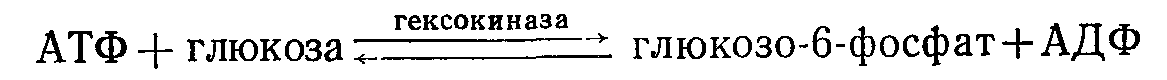
Фосфатная группа с АТФ может быть перенесена и на другие органические вещества.
Фосфотрансферазы участвуют в процессах дыхания и брожения.
Аминотрансферазы – ферменты, осуществляющие реакции переаминирования, т. е. межмолекулярный перенос аминогруппы (–NH2) с аминокислот на кетокислоты. Эти ферменты обладают специфичностью: каждый катализирует реакцию переноса аминогруппы от определенной аминокислоты. Они являются двухкомпонентными ферментами, в состав кофермента входит витамин Вб. В обмене веществ аминоферазы играют большую роль, участвуют в образовании новых аминокислот в клетке.
Гидролазы. К гидролазам относятся ферменты,катализирующие процессы расщепления сложных органических веществ по типу гидролитических реакций с присоединением воды.
Большинство гидролаз являются однокомпонентными ферментами.
Гидролазы подразделяют на подгруппы в зависимости от веществ, на которые они действуют.
Карбогидразы – это ферменты, катализирующие гидролиз и синтез глюкозидов, ди-, три- и полисахаридов.
Примерами карбогидраз, расщепляющих дисахариды, распространенных у Микроорганизмов, являются следующие ферменты.
Мальтаза (α-глюкозидаза) расщепляет мальтозу (солодовый сахар) на две молекулы глюкозы.
Сахараз а (инвертаза, β-фруктофуранозидаза) расщепляет сахарозу на глюкозу и фруктозу.
Лакта за (β-галактозидаза) расщепляет молочный сахар (лактозу) на галактозу и глюкозу.
Из гидролаз, действующих на полисахариды, наибольшее значение имеют следующие.
Амилазы – ферменты, катализирующие гидролиз крахмала. Известно три типа амилаз: а-амилаза, β-амилаза и глюкоамилаза. Они отличаются между собой по свойствам и способу действия на крахмал. Амилазы находятся в плесневых грибах и многих бактериях. Дрожжи не содержат амилаз.
α-Амилаза расщепляет крахмал преимущественно на сравнительно низкомолекулярные декстрины. Мальтозы получается мало.
β-Амилаза расщепляет крахмал с образованием главным образом мальтозы и небольшого количества декстринов (высокомолекулярных) .
Глюкоамилаза расщепляет крахмал, образуя преимущественно глюкозу и небольшое количество декстринов.
Целлюлаза – фермент, гидролизующий целлюлозу (клетчатку) с образованием дисахарида целлобиозы, который в дальнейшем при участии фермента целлобиазы (β-глюкозидазы) расщепляется на две молекулы глюкозы. Целлюлаза встречается в грибах и некоторых бактериях.
Пектолитические ферменты – это комплекс ферментов, гидролизующих пектиновые вещества. Пектиновые вещества в виде нерастворимого протопектина находятся в растениях в качестве межклеточного вещества и входят в состав клеточных оболочек. При участии пектолитических ферментов (протопектиназы, пектинэстеразы, полигалактуроназы) протопектин и растворимый пектин гидролизуются с образованием метилового спирта, галактуроновых кислот, пентоз, гексоз.
Пектолитические ферменты имеются у многих плесеней и у некоторых бактерий. Развитие этих микроорганизмов в растительном пищевом сырье (плодах, овощах) приводит к мацерации (размягчению) их тканей.
Пептидазы (протеолитические ферменты) катализируют гидролиз белков, пептидов, расщепляя пептидные связи. Пептидазы обладают специфичностью, которая обусловлена структурой молекулы белка, наличием и расположением определенных химических групп. Каждая пептидаза разрывает пептидные связи между определенными аминокислотами.
Дезаминазы и амидазы – ферменты, катализирующие гидролитическое расщепление аминокислот и амидов с отщеплением азота в виде аммиака.
Из амидаз существенную роль в азотном обмене микроорганизмов играют аспарагиназа, катализирующая гидролиз ас-парагина на аспарагиновую кислоту и аммиак, а также глу-таминаза, вызывающая гидролиз глутамина с образованием аммиака и глутаминовой кислоты.
Эстеразы – ферменты, катализирующие реакции расщепления и синтеза сложных эфиров(эстеров). Они широко распространены у микроорганизмов. Важную роль в обмене веществ микроорганизмов играют следующие эстеразы.
Липазы – ферменты, вызывающие гидролиз жиров на глицерин и высокомолекулярные жирные кислоты.
Фосфатазы – многочисленные ферменты, расщепляющие эфироподобные фосфорсодержащие органические соединения с освобождением фосфорной кислоты.
Лиазы. К классу лиаз относятся ферменты, которые катализируют реакции негидролитического расщепления органических веществ, сопровождаемые отщеплением от субстрата тех или иных групп: СО2, Н2О, NH3.
Альдолаза – фермент, обратимо расщепляющий шести-углеродную молекулу фруктозодифосфата на два трехуглерод-ных соединения: фосфодиоксиацетон и фосфоглицериновый альдегид. Этот фермент участвует в начальной стадии превращения сахара в процессе дыхания и брожения.
Декарбоксилазы – ферменты, катализирующие декарбоксилирование (отщепление СО2) органических кислот.
Во многих микроорганизмах содержится, например, пируватдекарбоксилаза, катализирующая отщепление СО2 от пировиноградной кислоты с образованием уксусного альдегида. В состав кофермента этой декарбоксилазы входит витамин B1.
Декарбоксилазы аминокислот участвуют в отщеплении СО2 от аминокислот с выделением аминов.
Микроорганизмы, особенно гнилостные бактерии, богаты декарбоксилазами аминокислот.
Изомеразы. Ферменты этого класса катализируют превращение органических соединений в их изомеры – внутримолекулярное перемещение радикалов, атомов, атомных группировок.
Примерами могут служить следующие ферменты.
Триозофосфатизомераза катализирует взаимное превращение фосфотриоз: фосфодиоксиацетона и фосфоглицеринового альдегида.
Глюкозофосфатизомераза катализирует обратимое превращение глюкозо-6-фосфат во фруктозо-6-фосфат.
Оба этих фермента участвуют на первых стадиях превращения сахара в процессах дыхания и брожения.
Лигазы (синтетазы). В этот класс входят ферменты, катализирующие реакции синтеза сложных органических соединений из более простых. Эти реакции требуют затрат энергии и обычно протекают одновременно с расщеплением пирофосфатной (мак-роэргической) связи в АТФ.
Примерами таких ферментов являются следующие.
Карбоксилазы катализируют при участии AT Φ присоединение СОг к'органическим кислотам.
Глутаминсинтетаза и аспарагинсинтетаза – ферменты синтеза глутамина и аспарагина из NH3 и соответствующих аминокислот.
Лигазы играют большую роль в углеводном и азотном обмене микроорганизмов.
Использование микробных ферментов
Человек издавна использовал ферментативную активность микроорганизмов. Широкое применение микроорганизмов в пищевых производствах основано на использовании их ферментативной деятельности в перерабатываемом пищевом сырье. Культуры микроорганизмов можно заменить ферментами, выделив их в виде препаратов из клеток или культуральной среды. Применение ферментов в пищевой и легкой промышленности позволяет значительно интенсифицировать технологический процесс, повысить выход и улучшить качество готовой продукции.
Использование микроорганизмов для получения ферментов имеет ряд преимуществ по сравнению с растительным и животным сырьем:
1. Микроорганизмы обладают богатым «ассортиментом» ферментов. Среди них есть такие, которые отсутствуют у животных и в растениях.
2. Микроорганизмы быстро размножаются и в течение короткого времени дают огромную массу клеток, из которых (или из культуральной среды) можно выделить большое количество фермента.
3. Микроорганизмы растут на относительно дешевых субстратах, например на отходах различных промышленных производств.
4. Управлять развитием микроорганизмов при современном аппаратурном оформлении таких производств значительно легче и проще, чем выращивать растения и животных.
В настоящее время во многих отраслях народного хозяйства ферменты микробного происхождения вытесняют ферменты растительного и животного происхождения.
Отечественное производство микробных ферментных препаратов в последние годы интенсивно развивается. В настоящее время десятки различных ферментов в виде индивидуальных ферментных белков и технических препаратов разной степени очистки уже производятся в промышленном масштабе с использованием культур плесневых грибов, бактерий, дрожжей.
Препараты грибных амилолитических ферментов применяют при производстве этилового спирта из крахмалсодержащего сырья вместо зернового солода; в хлебопекарной промышленности – взамен солода при изготовлении заварного ржаного хлеба; добавляют грибные амилазы и в пшеничное тесто. Поскольку в этом препарате помимо амилазы имеются, хотя и в небольшом количестве, другие ферменты (мальтаза, пептидазы), процесс изготовления теста ускоряется: увеличивается объем и пористость хлеба, улучшаются его внешний вид, аромат, вкус.
Применение этих ферментных препаратов в пивоварении позволяет частично заменить солод несоложенным (не подвергшимся прорастанию) ячменем. С помощью грибной глюкоами-лазы получают глюкозную патоку и кристаллическую глюкозу из крахмала.
Пектолитические грибные ферментные препараты используют в соко-морсовом производстве и виноделии. В результате разрушения пектина этими ферментами ускоряется процесс выделения сока, повышается его выход, улучшается фильтрация и осветление соков.
Ферментные препараты, содержащие микробные пептидазы, применяют для повышения стойкости (предохранения от белкового помутнения) вина и пива; в сыроделии взамен (частично) сычужного фермента. Целесообразно применять микробные пептидазы для размягчения мяса, ускорения созревания мяса и сельди, получения из отходов рыбной и мясной промышленности пищевых гидролизатов и в других технологических процессах переработки животного и растительного сырья.
В Основных направлениях экономического и социального развития СССР на 1981–1985 годы и на период до 1990 года, принятых XXVI съездом КПСС, предусмотрено значительно увеличить производство ферментов микробного происхождения.
КОНСТРУКТИВНЫЙ ОБМЕН – ПИТАНИЕ МИКРООРГАНИЗМОВ
Поступление питательных веществ в клетку
Поступление питательных веществ и воды в клетку, а также выделение продуктов обмена в окружающую среду происходят у микроорганизмов через всю поверхность их тела.
Возможность проникновения веществ извне в клетку обусловлена многими факторами: величиной и структурой их молекул; способностью растворяться в компонентах цитоплазматической мембраны; концентрацией веществ в клетке и в среде; свойствами клеточной стенки и цитоплазматической мембраны, являющихся барьерами, через которые должны проникнуть в клетку питательные вещества, и др.
Вещества питательной среды могут поступать в клетку только в растворенном состоянии. Нерастворимые сложные органические соединения должны подвергнуться расщеплению на более простые вне клетки, что происходит с помощью экзоферментов микроорганизмов.
Клеточная стенка (оболочка) проницаема и задерживает лишь макромолекулы. Цитоплазматическая мембрана обладает полупроницаемостью, она является осмотическим барьером; проницаемость ее для различных веществ неодинаковая.
Ранее (см. с. 44) указывалось, что до 90 % и более сухой массы клеток микроорганизмов составляют четыре химических элемента – водород, кислород, углерод и азот, входящие в состав важнейших веществ клетки.
Кислород и водород все микроорганизмы получают из воды. Потребности различных микроорганизмов в отношении источников углерода и азота весьма разнообразны.
Источники углерода. В зависимости от используемого в конструктивном обмене источника углерода микроорганизмы делят на две группы: автотрофы и гетеротрофы.
Автотрофы1 в качестве единственного источника углерода для синтеза органических веществ тела используют углекислоту (СO2).
Гетеротрофы2 не могут использовать в качестве источника углерода только углекислый газ; они нуждаются в готовых органических соединениях.
Соответственно по источнику углерода различают и типы питания: автотрофный и гетеротрофный.
Автотрофы для превращения не имеющей энергетической ценности углекислоты в органические вещества нуждаются в постороннем источнике энергии.
Одни автотрофы в этих целях используют световую энергию – этот процесс называется фотосинтезом.
Другие используют химическую энергию, высвобождающуюся при окислении простых неорганических соединений, – этот процесс называется хемосинтезом. Открыт он был С. Н. Виноградским.
Таким образом, учитывая природу основного источника углерода и природу источника энергии, используемой при синтезе органических веществ, микроорганизмы по типам питания можно подразделить на следующие группы.
Фотоавтотрофы для синтеза органических веществ используют световую энергию и неорганический источник углерода (СO2). К ним относятся цианобактерии (см. с. 19), пурпурные и зеленые серные бактерии. Это преимущественно водные бактерии, в них содержатся различные пигменты (каротиноидные, бактериохлорофиллы), поглощающие свет.
Фотогетеротрофы для синтеза органических веществ используют световую энергию и простые органические соединения. Это живущие в водоемах пурпурные несерные бактерии.
Хемоавтотрофы в качестве источника углерода для синтеза органических веществ используют углекислоту, а в качестве источника энергии – реакции окисления неорганических соединений. Относящиеся к этой группе бактерии живут в водоемах, в почве: они специфичны в отношении окисляемого ими вещества.
1 Автотроф – питающийся самостоятельно (autos – сам, trophe – пища).
2 Гетеротроф – питающийся другими (heteros – другой).
Известно Несколько путей проникновения питательных веществ в клетку.
Пассивная диффузия, которая подчиняется законам осмоса.
При осмотическом проникновении веществ через полупроницаемую мембрану движущей силой является разность осмотических давлений (концентраций веществ) в растворах по обе стороны мембраны, т. е. между средой и клеткой. Такой пассивный перенос веществ – по градиенту концентрации (от более высокой к более низкой) – протекает до уравнивания концентрации и не требует затрат энергии клеткой.
Вода – основное вещество, которое проникает в клетку и выделяется из нее путем пассивной диффузии.
Большинство питательных веществ поступает в клетку путем переноса их через мембрану специфическими переносчиками– пермеазами (от англ. permeable – проницаемый), локализованными в цитоплазматической мембране. Пермеазы сходны с ферментами; они обладают субстратной специфичностью – каждая транспортирует определенное вещество. На внешней стороне цитоплазматической мембраны пермеаза адсорбирует вещество – вступает с ним во временную связь и диффундирует комплексно через мембрану, отдавая на внутренней стороне ее транспортируемое вещество в цитоплазму.
В клетку из питательной среды могут поступать только те вещества, для которых в цитоплазматической мембране имеются соответствующие пермеазы. Таким образом, мембрана является не только осмотическим барьером, но обладает и избирательной проницаемостью.
Перенос веществ с помощью пермеаз может протекать, как при пассивной диффузии, по законам осмоса – по градиенту концентрации. Эта так называемая облегченная диффузия, протекает без затрат энергии.
Перенос веществ из питательной среды в клетку может осуществляться пермеазами и против градиента концентрации. Такой активный перенос требует затрат энергии.
При этом концентрация транспортируемого вещества в клетке может значительно превысить его концентрацию в питательной среде.
Типы питания микроорганизмов
Пища должна содержать такие вещества, которые удовлетворяли бы потребность микроорганизма в химических элементах, необходимых для синтеза веществ и структур клетки.
В зависимости от того, какие химические элементы поступают из веществ питательной среды, последние называют их источниками (источник углерода, фосфора и т. д.).
Это бактерии, окисляющие водород с образованием воды (водородные бактерии), аммиак до нитратов (нитрифицирующие бактерии), сероводород до серной кислоты (бесцветные серобактерии), а также окисляющие закисное железо в окисное (железобактерии).
Хемоорганотрофы (хемегетеротрофы) в качестве источников энергии и углерода используют органические соединения. Таким типом питания обладают многочисленные бактерии, грибы, дрожжи.
Одни хемогетеротрофы непритязательны в отношении питательных веществ источников углерода, другие проявляют большую специфичность.
Наиболее специфичными являются микробы-паразиты, живущие в теле другого организма – хозяина, питающиеся веществами его тела. К паразитам относятся возбудители заболеваний человека, животных, растений.
Большинство хемогетеротрофных микроорганизмов живет за счет использования органических веществ различных субстратов животного и растительного происхождения. Такие микроорганизмы называют сапрофитами. К ним относятся микроорганизмы, которые разлагают различные органические вещества в природе (в почве, воде), вызывают порчу пищевых продуктов или используются в процессах переработки растительного и животного сырья.
Однако резкую грань между этими подгруппами хемогетеротрофов не всегда можно установить. Отдельные виды микробов-паразитов могут существовать во внешней среде как сапрофита, и наоборот, некоторые сапрофита в определенных условиях вызывают заболевания у людей, животных и растений.
Многие сапрофита всеядны, т. е. способны использовать в качестве источника углерода разнообразные органические соединения; некоторые проявляют выраженную специфичность (избирательность) в отношении источника углерода. Так, гриб Oidium lactis усваивает изобутиловый спирт и не усваивает бутиловый. Последний является хорошим источником углерода для гриба Aspergillus niger, а изобутиловый спирт этот гриб не потребляет. Существуют и такие, которые используют только определенное вещество, их называют субстрат-специфичными микроорганизмами. Примером могут служить целлюлозные бактерии, для которых клетчатка является единственным источником углерода.
Сапрофита наряду с органическими соединениями используют и СО2, вовлекая его в обмен веществ. Углекислый газ служит дополнительным источником углерода для биосинтеза веществ тела.
Источники азота. Все автотрофные микроорганизмы усваивают азот из неорганических соединений.
У хемогетеротрофов по отношению к источнику азота, как и по отношению к источнику углерода, проявляется избирательность. Паразиты используют органические азотсодержащие вещества клеток хозяина. Источником азота для сапрофитов могут служить как органические, так и неорганические азотсодержащие соединения. Одни способны расти только на субстратах, содержащих сложные азотсодержащие вещества (азотистые основания, пептиды, большой набор аминокислот), так как сами синтезировать их из более простых соединений не способны.
Другие могут развиваться при ограниченном числе органических соединений азота, например, в субстратах, содержащих только некоторые аминокислоты и даже одну-две из них, а все остальные необходимые для синтеза белков клетки синтезируют сами. Они дезаминируют взятые аминокислоты, а образующийся аммиак используют в реакциях аминирования оксикислот или чаще кетокислот, например:
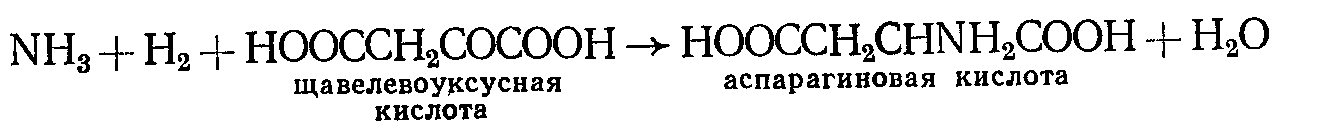
Синтез новых аминокислот может протекать и без дезамини-рования взятых из субстрата аминокислот (без промежуточного образования аммиака) путем перестройки их (переаминирования) – переноса аминогруппы с аминокислоты на кетокислоты при участии ферментов аминотрансфераз:
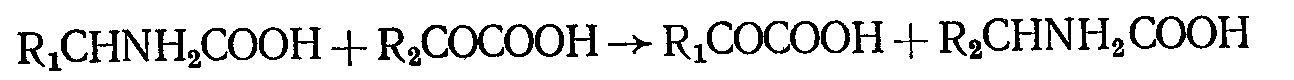
Многие сапрофита (бактерии, грибы, дрожжи) вообще не нуждаются в органических соединениях азота, используя неорганические его соединения, лучшими из которых являются соли аммония.
Азот в состав компонентов клетки входит главным образом в восстановленной форме. Используя в качестве источника азота нитраты или нитриты, микроорганизмы восстанавливают эти окисленные формы азота с образованием аммиака, который и используется в биосинтетических процессах.
Существуют сапрофита, которые используют свободный азот атмосферы. Они переводят его в связанное состояние – восстанавливают в аммиак. Эти микроорганизмы называют азот-фиксаторами или азотсобирателями (см. с. 140).
Специфичностью отношений микроорганизмов к источникам углерода и азота определяется круговорот этих элементов в природе. Эта особенность гетеротрофов проявляется и при порче многих пищевых продуктов, при смене развития одних форм
другими.
Источники зольных элементов. Для синтеза клеточных веществ нужны и различные зольные элементы: сера, фосфор, калий, кальций, магний, железо. Хотя потребность в них незначительна, но при недостатке в питательной среде даже одного из этих элементов микроорганизмы не будут развиваться и могут погибнуть.
Для большинства микроорганизмов источниками зольных элементов являются минеральные соли. Немногие микроорганизмы лучше усваивают серу и фосфор из органических соединений.
Микроэлементы, необходимые для роста микроорганизмов, могут быть использованы ими также из минеральных солей.
Потребность микроорганизмов в витаминах. В составе каждой микробной клетки имеются различные витамины. Они необходимы для нормальной жизнедеятельности. Некоторые витамины входят в состав простетических групп ферментов.
Одни микроорганизмы должны получать витамины в готовом виде, и при отсутствии того или иного витамина в среде у них резко нарушается обмен веществ. Добавление в питательную среду недостающего витамина ликвидирует задержку роста, поэтому витамины нередко называют ростовыми веществами.
Другие микроорганизмы, наоборот, хорошо развиваются при отсутствии витаминов в среде. Они способны сами синтезировать витамины из веществ питательной среды, накапливать их и выделять из клетки наружу. Некоторые микроорганизмы синтезируют витамины в количествах, значительно превышающих собственные потребности. Такие микроорганизмы используют для промышленного производства витаминов. Так, с помощью гриба эремотециум (Eremothecium ashbyii) получают витамин Вг. Некоторые актиномицеты, пропионовокислые бактерии, метанооб-разующие (перерабатывающие различные органические вещества в метан) бактерии применяются для получения витамина B12.
ЭНЕРГЕТИЧЕСКИЙ ОБМЕН У МИКРООРГАНИЗМОВ
Описанные выше процессы конструктивного обмена – синтез веществ клетки из поступивших в нее извне питательных веществ, активный перенос этих веществ через цитоплазматиче-скую мембрану и многие другие процессы жизни – протекают с затратой энергии.
Источники энергии у микроорганизмов разнообразны.
У фотоавтотрофов источником энергии служит видимый свет. Световая энергия, улавливаемая фотоактивными пигментами клетки в процессе фотосинтеза, трансформируется в химическую энергию, обеспечивающую энергетические потребности клетки.
Источником энергии для биосинтеза клеточных веществ из СО2 у хемоавтотрофов является химическая энергия, высвобождаемая в результате окисления кислородом воздуха неорганических соединений (NH3, H2S и др.).
Хемоорганотрофы (хемогетеротрофы) получают энергию в процессах окисления органических соединений.
Любое природное органическое вещество и многие синтетические могут быть использованы гетеротрофами, но не всеми. Одни окисляют многие органические вещества, другие – лишь небольшой набор их, имеются и такие, которые проявляют большую специфичность по отношению к энергетическому материалу.
Поскольку возбудители порчи пищевых продуктов и используемые при переработке пищевого сырья обносят к хемооргано-трофам, их энергодающие процессы и рассматриваются ниже.
Окисление органических веществ может происходить различными путями:
1. Прямым, т. е. присоединением к веществу кислорода.
2. Непрямым, т. е. дегидрогенерированием (отнятием водорода). Отнятый от окисляемого вещества водород переносится на другое вещество, которое при этом восстанавливается.
3. Путем переноса электронов (е
) от одного вещества к другому. Вещество, теряющее электроны, окисляется, а присоединяющее их – восстанавливается.
Вещество, отдающее водород (электроны), называется донором, а вещество, присоединяющее их, – акцептором.
Биологическое окисление (в клетках) органических веществ происходит чаще путем дегидрогенерирования. Так как атом водорода состоит из протона (Н+) и электрона (е
), перенос водорода с одного вещества на другое включает и перенос электрона.
Перенос водорода (электрона) от подвергающегося окислению вещества к акцептору осуществляется различными окислительно-восстановительными ферментами.
Реакцию окисления – восстановления можно изобразить следующим образом:
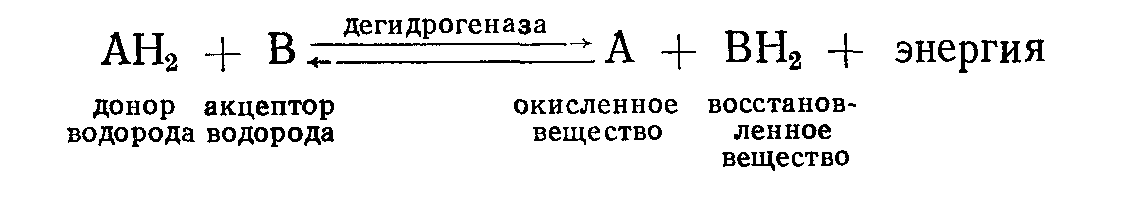
Конечным акцептором водорода может быть кислород воздуха или другое вещество, способное восстанавливаться.
В зависимости от конечного акцептора водорода хемоорганотрофные микроорганизмы делят на две группы:
аэробы, окисляющие органические вещества с использованием молекулярного кислорода, который и является конечным акцептором водорода;
анаэробы, которые в энергетических процессах не используют кислород. Конечными акцепторами водорода служат органические или неорганические соединения.
Аэробные микроорганизмы
Многие аэробные микроорганизмы, к которым относят грибы, некоторые дрожжи и многие бактерии, подобно высшим организмам (растениям, животным), окисляют органические вещества полностью до минеральных веществ – углекислого газа и воды. Процесс этот называется дыханием.
В качестве энергетического материала в процессе дыхания микроорганизмы часто используют углеводы. При этом сложные (ди-, три- и полисахариды) ферментативным путем гидролизу-ются до моносахаров, которые и подвергаются окислению.
Этот процесс в общем виде может быть представлен следующим уравнением: 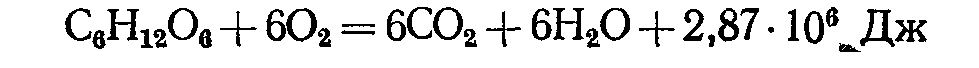
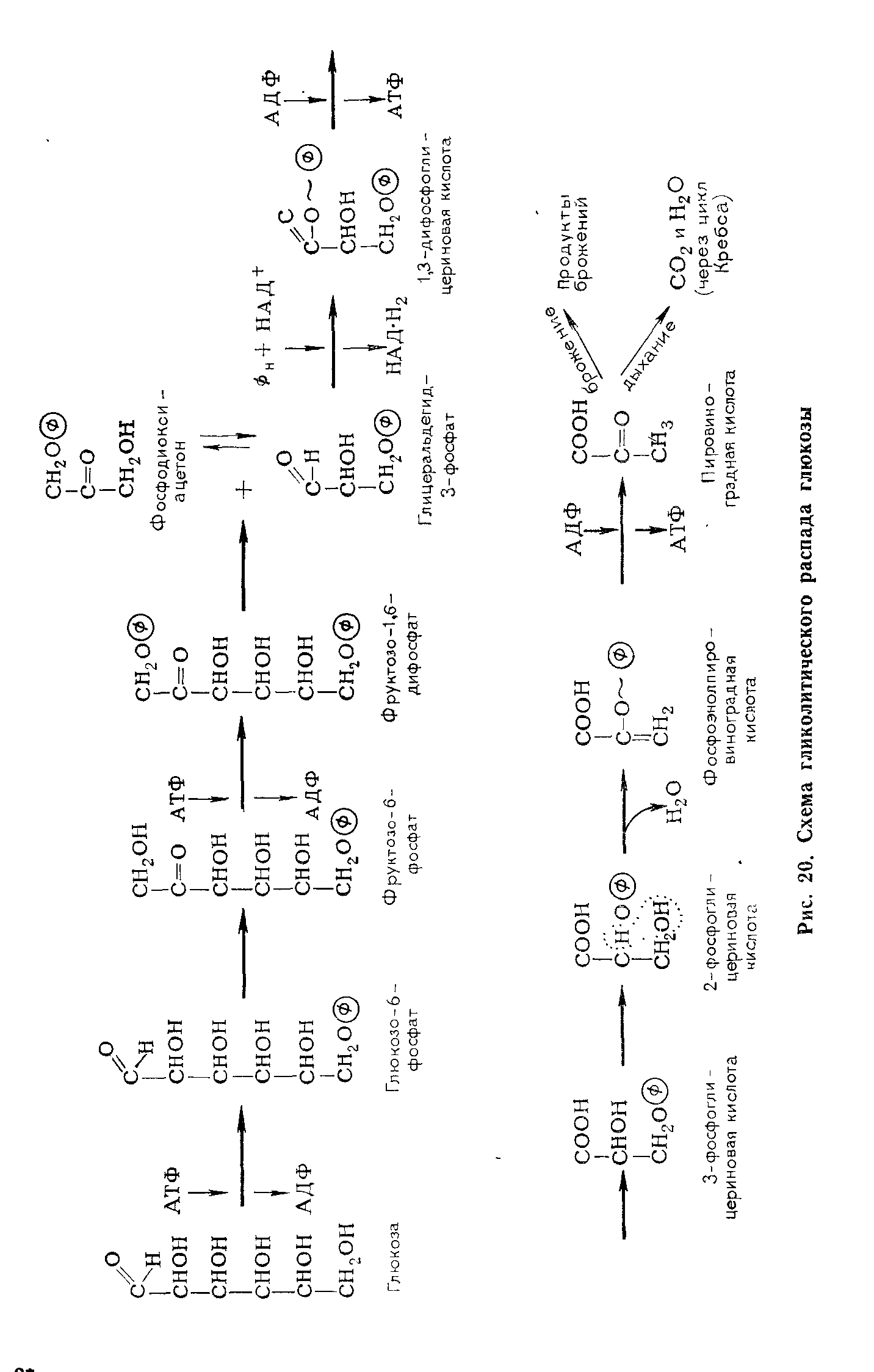
Как видно из уравнения, при полном окислении глюкозы освобождается вся потенциальная (свободная) энергия молекулы глюкозы.
Приведенное уравнение характеризует процесс в суммарном виде, показаны лишь исходный и конечные продукты окисления.
Однако процесс этот многоэтапный и протекает при участии многих ферментов с образованием различных промежуточных продуктов. Обязательным промежуточным продуктом в процессе биологического окисления глюкозы является пировиноградная кислота.
Известно несколько путей расщепления глюкозы до этого важнейшего промежуточного продукта. Одним из таких путей является распад глюкозы, называемый гликолитическим. Он довольно универсален и свойствен многим аэробным и анаэробным микроорганизмам (рис. 20).
1. Первым этапом является активирование глюкозы путем φ о с φ ο ρ и -лирования при участии АТФ и фермента фосфотрансферазы (гексоки-назы). К молекуле глюкозы от молекулы аденозинтрифосфорной кислоты (АТФ) присоединяется концевой фосфатный остаток, обладающий макроэргической (со) связью. Образуется глюкозо-6-фосфат, а АТФ превращается в аденозиндифосфорную кислоту (АДФ).
2. Глюкозо-6-фосфат путем изомеризации при участии фермента глюкозофосфатизомеразы переходит во фруктозо-6-фосфат.
3. Фруктозо-6-фосфат затем фосфорилируется за счет АТФ при участии соответствующей фосфотрансферазы (фосфофруктокиназы). Образуется фруктозо-1,6-дифосфат, а АТФ превращается в АДФ. Вторичное фос-форилирование молекулы гексозы приводит к ее дальнейшему активированию.
4. Фруктозо-1,6-дифосфат расщепляется при участии фермента альдо-лазы на две молекулы фосфотриоз. Одна из них — фосфодиоксиацетон, другая — фосфат глицеринового альдегида. Оба эти вещества легко могут превращаться друг в друга.
Дальнейшему превращению подвергаются две молекулы 3-фосфоглицери-нового альдегида, так как фосфат диоксиацетона под действием фермента триозофосфатизомеразы превращается в 3-фосфоглицериновый альдегид.
5. Следующим этапом является окисление 3-фосфоглицеринового альдегида. Эта реакция катализируется дегидрогеназой, коферментом которой является НАД (см. с. 53). В окислении участвует фосфорная кислота.
Молекула 3-фосфоглицеринового альдегида присоединяет фосфат, а водород переносится на кофермент НАД, который восстанавливается в НАД·Н2. Освобождающаяся при окислении фосфоглицеринового альдегида энергия сосредоточивается в, макроэргической связи (∞) образующейся 1,3-дифосфоглицериновой кислоты.
6. В дальнейшем фосфатная группа 1,3-дифосфоглицериновой кислоты, имеющая макроэргическую связь, при участии фермента фосфоглицератки-назы переносится на молекулу аденозиндифосфорной кислоты. Образуется 3-фосфоглицериновая кислота, а АДФ превращается в АТФ. Таким образом свободная энергия окисления альдегидной группы запасается в молекуле
7. З-Фосфоглицериновая кислота под влиянием фермента фосфоглицеромутазы превращается в 2-фосфоглицериновую кислоту.
8. Под действием фермента энолазы 2-фосфоглицериновая кислота, теряя воду, переходит в энольную форму фвсфопировиноградной кислоты. При этом происходит перераспределение внутримолекулярной энергии, большая часть которой сосредоточивается в форме макроэргической фосфатной связи фосфоэнолпировиноградной кислоты.
В процессе дыхания аэробных микроорганизмов пировино-градная кислота в дальнейшем подвергается полному окислению до СO2 и Н2O, вступая в сложный цикл превращений (цикл Кребса) с образованием три- и дикарбоновых кислот, последовательно окисляющихся (отщепляется Н2) и декарбоксилирую-щихся (отщепляется СO2).
Из рис. 21 видно, что окисление одной молекулы пировино-градной кислоты сопровождается выделением трех молекул углекислого газа и пяти пар водородных атомов.
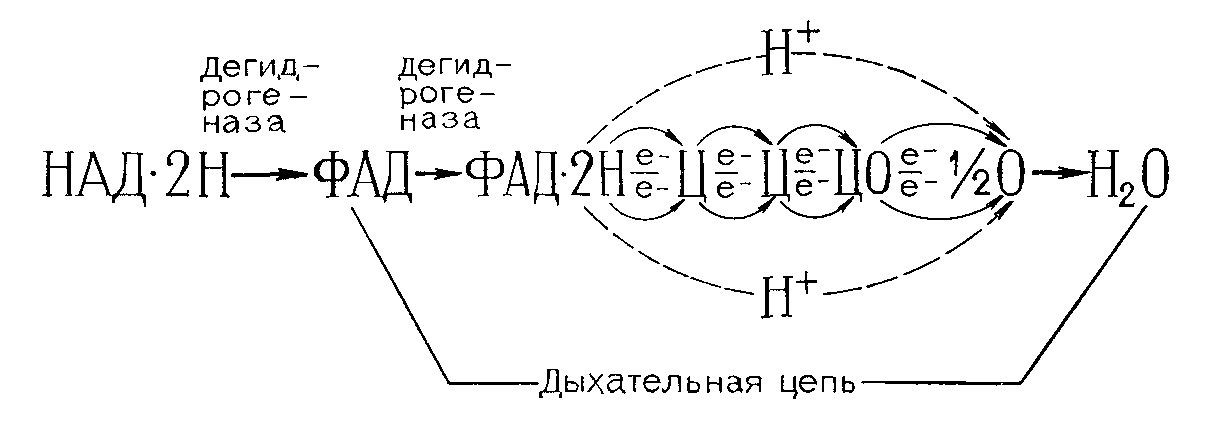
Водород, отщепленный от окисляемых в цикле Кребса кислот, посредством коферментов (НАД и НАДФ) соответствующих дегидрогеназ передается по так называемой «дыхательной цепи», состоящей из комплекса ферментов, к конечному акцептору – молекулярному кислороду.
Из приведенной ниже схемы (с. 69) видно, что водород восстановленного НАД · 2Н передается на кофермент (ФАД) фла-винового фермента, который восстанавливается в ФАД · 2Н. С восстановленной флавиновой дегидрогеназы водород передается на цитохром цитохромной системы, при этом атом водорода расщепляется на ион водорода (Н+) и электрон (е
), Цитохром из окисленной формы превращается в восстановленную. Восстановленный цитохром передает электроны следующему ци-тохрому и т. д.
Цитохромы попеременно то восстанавливаются, то окисляются, что связано с изменением валентности железа, содержащегося в их простетической группе. Последний цитохром передает электроны цитохромоксидазе, восстанавливая ее кофер-. мент. Завершающей реакцией является окисление восстановленной цитохромоксидазы молекулой кислорода. Кислород за счет передачи ему (с цитохромоксидазы) электронов активируется и приобретает способность соединяться с ионами водорода (Н+), в результате чего образуется вода. На этом и заканчивается у аэробов полное окисление исходного органического вещества.
9. Фосфоэнолпировиноградная кислота дефосфорилируется. При этом богатая энергией фосфатная группа при участии фермента пируваткиназы передается на молекулу АДФ. В результате образуется пировиноградная кислота, а АДФ превращается в АТФ.
Из изложенного и рис. 20 видно, что гликолитическое расщепление глюкозы до пировиноградной кислоты происходит без участия кислорода (анаэробная стадия) и заканчивается выходом двух молекул пировиноградной кислоты, двух молекул НАД · Н2 и двух молекул АТФ. Синтезируются четыре молекулы АТФ, но две расходуются на фосфорилирование новой молекулы глюкозы.
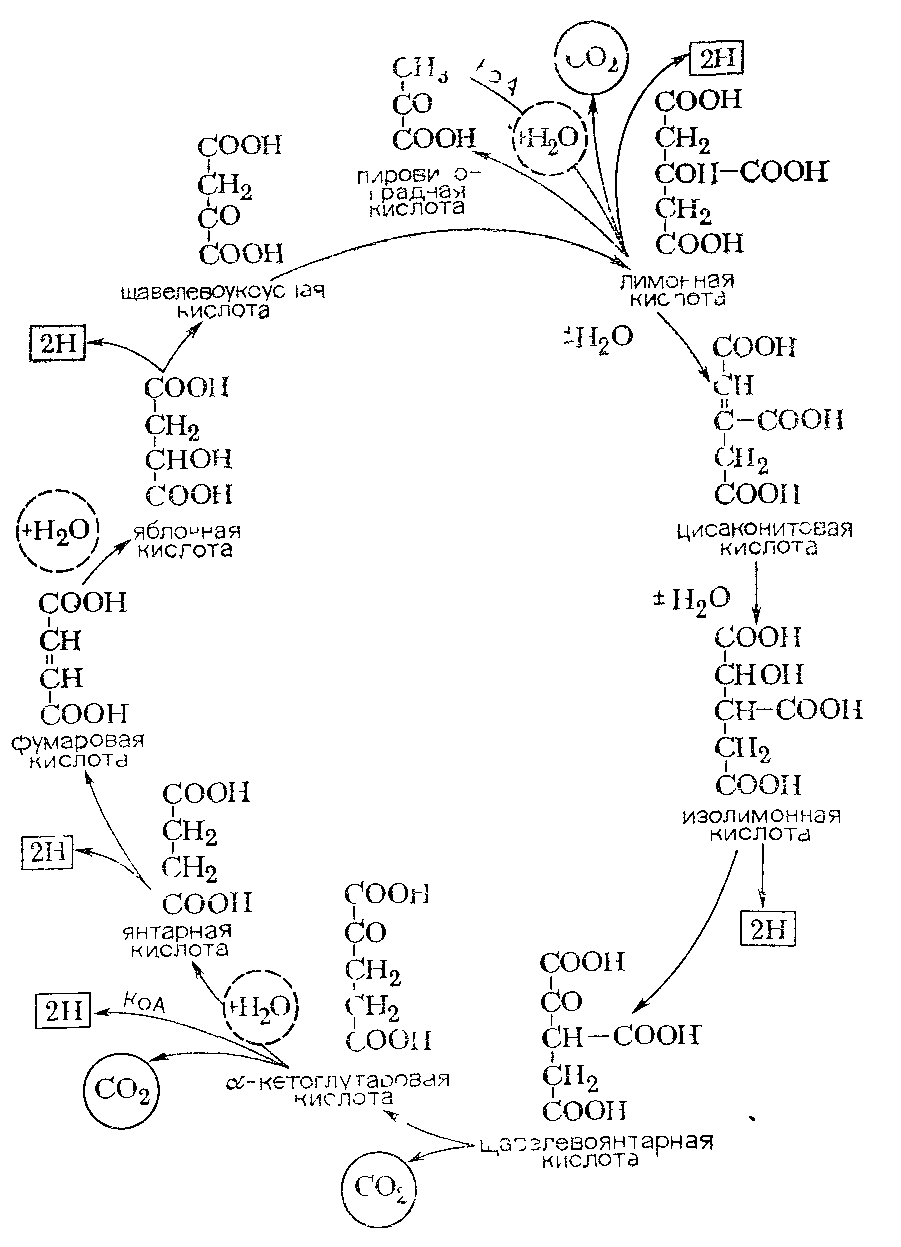
Рис. 21. Цикл Кребса
Освобождающаяся при переносе электронов в дыхательной цепи энергия затрачивается на син
тез АТФ из АДФ и неорганического фосфата, т. е. запасается в форме энергии фосфатной связи АТФ. Этот процесс называется окислительным фосфорилированием.
Некоторые аэробные гетеротрофные микроорганизмы получают энергию за счет неполного окисления органических веществ; при этом в среде накапливаются промежуточные недоокисленные продукты, преимущественно органические кислоты.
При неполном окислении энергетического материала высвобождается соответственно меньшее количество энергии. Часть потенциальной энергии окисляемого вещества остается в продуктах неполного окисления. Например, некоторые плесневые грибы в определенных условиях окисляют сахар с образованием воды и различных органических кислот – глюконовой, лимонной, яблочной, щавелевой, янтарной и др. Уксуснокислые бактерии окисляют этиловый спирт до уксусной кислоты и воды:
Дальнейшее превращение образующихся пировиноградной кислоты и восстановленного промежуточного переносчика водорода НАД · Н2 у анаэробов иное, чем у аэробов. Пировиноград-ная кислота в бродильных процессах является исходным материалом для разнообразных продуктов брожения (спиртов, органических кислот).
У одних анаэробов она непосредственно служит конечным акцептором водорода от НАД · Н2 и восстанавливается в продукт брожения – молочную кислоту; НАД · Н2 при этом окисляется в НАД.
У других анаэробов из пировиноградной кислоты образуются различные промежуточные продукты, которые служат затем акцепторами водорода от НАД · Н2. Последний регенерируется, а акцептировавшие водород восстановленные органические соединения, являющиеся конечными продуктами брожения, выделяются в окружающую среду. В зависимости от того, какой основной продукт накапливается в среде, процесс брожения имеет соответствующее название.
Примерами такого типа получения энергии могут служить следующие виды брожения.
Спиртовое брожение осуществляется многими дрожжами в анаэробных условиях. Молекула глюкозы (энергетический материал) в этом процессе превращается в две молекулы этилового спирта и две молекулы углекислого газа с выделением энергии:
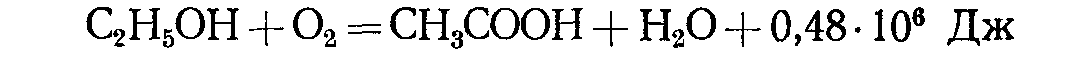
В молекуле спирта заключено энергии 1,37-106 Дж. Как видно из уравнения, освобождается только часть энергии, много ее остается в уксусной кислоте.
Некоторые из этих окислительных процессов используют в промышленности, например, при производстве уксуса, лимонной и глюконовой кислот. Условия, химизм и возбудители этих процессов описаны в гл. 4.
Анаэробные микроорганизмы
Анаэробные микроорганизмы, к которым относят многие бактерии и некоторые дрожжи, получают необходимую для жизнедеятельности энергию в процессе брожения. Этот энерго-дающий процесс протекает также путем сопряженного окисления-восстановления, но без участия кислорода воздуха.
Конечным акцептором водорода, отнятого от окисляемого органического вещества, служат органические вещества – промежуточные продукты распада используемого субстрата.
Анаэробные микроорганизмы подразделяют на облигатные, или безусловные, анаэробы, для которых кислород не только не нужен, но и вреден, и факультативные, или условные, анаэробы, которые могут жить как при доступе воздуха, так и без него.
Степень анаэробности у факультативных анаэробов различна. Одни из них лучше развиваются в анаэробных условиях или при ничтожно малом содержании кислорода в среде (микроаэрофилы), другие – при доступе воздуха. Известны факультативные анаэробы (например, некоторые дрожжи), способные в зависимости от условий развития переключаться с анаэробного на аэробный тип получения энергии.
Энергетическим материалом при брожении чаще служат углеводы, из них наиболее используемый – глюкоза.
Превращение глюкозы до образования пировиноградной кислоты протекает так же, как и у аэробов по гликолитическому пути (см. с. 66, рис. 20).
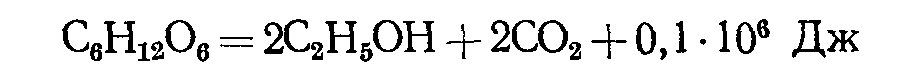
Молочнокислое брожение – это процесс получения энергии молочнокислыми бактериями, заключающийся в превращении молекулы сахара в две молекулы молочной кислоты с выделением энергии:
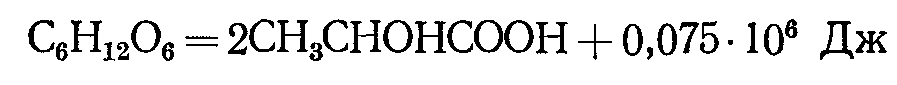
Как видно из уравнений, среди конечных продуктов брожения всегда имеются продукты неполного окисления – органические вещества, заключающие в себе значительное количество потенциальной энергии.
Известно много других брожений, отдельные типы которых различаются составом конечных продуктов, что зависит от комплекса ферментов возбудителя брожения.
Многие бродильные процессы применяют в промышленности; они могут являться причиной порчи пищевых продуктов. Подробнее эти процессы рассматриваются в гл. 4.
Маслянокислое брожение вызывается облигатно анаэробными маслянокислыми бактериями. Глюкоза в этом энерго-дающем процессе превращается в масляную кислоту, водород и углекислый газ:
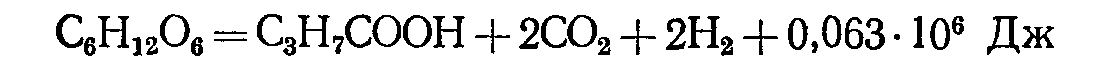
В анаэробных условиях некоторые микроорганизмы могут при окислении органических веществ использовать неорганические акцепторы водорода (электроны), которые при этом восстанавливаются. Эти микроорганизмы используют, следовательно, в качестве окислителя не свободный, а связанный кислород неорганических веществ, богатых этим элементом.
Такой способностью обладают, например, денитрифицирующие бактерии, восстанавливающие нитраты до свободного азота. Этот способ получения энергии называют нитратным дыханием.
Десульфатирующие бактерии используют в качестве конечного акцептора электронов (водорода) сульфаты, восстанавливая их до сероводорода, – сульфатное дыхание.
Таким образом, различие между аэробным и анаэробным процессом получения энергии у гетеротрофов заключается в природе конечного акцептора водорода (окислителя).
Рассмотренные процессы (дыхание, брожение) следует расценивать не только как процессы, обеспечивающие организм энергией. Многие промежуточные продукты распада углеводов служат исходным материалом для синтеза важнейших компонентов клетки (белков, нуклеиновых кислот, липидов и др.).
Важным поставщиком промежуточных продуктов для биосинтетических процессов является цикл Кребса. Многие кето-кислоты, образующиеся в этом цикле превращений ди- и три-карбоновых кислот, путем аминирования и переаминирования превращаются в различные аминокислоты, из которых далее синтезируются белки.
Использование энергии микроорганизмами
Освобождаемая в процессах дыхания и брожения свободная энергия не может быть непосредственно использована клеткой. Энергия должна быть преобразована в биологически полезную форму – в химическую энергию макроэргических фосфатных связей фосфорорганических соединений, главным из которых является АТФ. Только часть энергии окисления органических веществ переводится в доступную для клетки форму (резервируется в АТФ). Значительное количество, преимущественно в виде тепловой энергии, теряется – рассеивается во внешней среде.
АТФ является универсальным переносчиком химической энергии между реакциями как с выделением энергии, так и с ее затратой. АТФ называют «энергетической валютой» клетки. Из этого своеобразного аккумулятора организм черпает энергию для удовлетворения своих потребностей.
В энергетическом отношении дыхание – значительно более выгодный процесс, чем брожение.
У анаэробов в процессе брожения энергодающим этапом является гликолитический распад глюкозы до образования пировиноградной кислоты. Полезный эффект, как указывалось ранее (см. с. 68), состоит в образовании двух молекул АТФ из АДФ. Макроэргическая фосфатная связь АТФ содержит энергии около 4,2-104 Дж.
Следовательно, при использовании одного моля глюкозы (потенциальный запас энергии 2,87· 106 Дж) в клетках анаэробов запасается всего лишь около 0,09- 106 Дж. Большая часть энер-' гии остается в выделяемых в среду органических веществах – конечных продуктах брожения, много теряется и в форме тепловой энергии.
У аэробов в процессе дыхания при полном окислении одного моля глюкозы синтезируется значительно больше молей АТФ.
Установлено, что при продвижении по дыхательной цепи пары атомов водорода (пары электронов) к атому кислорода – при образовании молекулы воды – синтезируются три моля АТФ.
Из приведенной схемы цикла Кребса (см. рис. 21) видно, что окисление одного моля пировиноградной кислоты сопровождается отнятием пяти пар атомов водорода. В процессе окисления участвуют два моля пировиноградной кислоты. Кроме того, до образования пировиноградной кислоты, при окислении глицеринового альдегида, образуется 2НАД · Н2, следовательно, в дыхательную цепь поступают 12 пар атомов водорода, образуются 12 молекул воды и синтезируются 36 молей АТФ. Два моля АТФ образуются еще при гликолитическом распаде глюкозы до ππρο-ν виноградной кислоты. Всего, таким образом, синтезируются 38 молей АТФ, т. е. резервируются около 1,6· 106 Дж.
Следовательно, аэробами полезно используется около 50 % энергии и около 50 % теряется в виде тепла. Этим объясняется явление самосогревания навоза, силосных кормов, зерна, клубней картофеля, когда вследствие повышенной влажности в них обильно развиваются различные микроорганизмы.
При самосогревании зерновая масса приобретает несвойственные здоровому зерну запах и цвет. Происходит потеря массы, значительно снижаются всхожесть, технологические качества зерна и может быть полностью потеряна потребительная стоимость продукта.
Самосогревание торфа, недостаточно просушенного сена, хлопка и других материалов, возникающее при массовом разви-• тии сначала мезофильных, а затем термофильных микроорганизмов, иногда приводит к самовозгоранию. Это явление обусловливается тем, что при повышении температуры материала до 60–70 °С начинают развиваться автокаталитические химические окислительные процессы, которые вызывают еще большее нагревание материала, вплоть до воспламенения.
У некоторых микроорганизмов наблюдается выделение неиспользованной энергии в форме световой. Такой способностью обладают некоторые бактерии, грибы, протисты. Свечение морской воды, сгнившего дерева, рыбы обусловлено присутствием в них светящихся микроорганизмов.
|
|
|
 Скачать 2.41 Mb.
Скачать 2.41 Mb.