8 класс. Уметь выделять главное
 Скачать 0.76 Mb. Скачать 0.76 Mb.
|
|
Тема: «Первый закон термодинамики. Работа газа и пара при расширении» Цели: - Образовательная: познакомить с первым законом термодинамики, сформировать общие представления о работе газа и пара при расширении; - Развивающая: развивать коммуникабельные способности по теме, уметь выделять главное; сопоставлять факты, результаты, анализировать, высказывать свою точку зрения по проблеме урока. - Воспитательная: воспитание стремления к учению, умения напряженно трудиться; развивать культуру речи, взаимоотношения, взаимопомощь и сотрудничество. Тип рассматриваемого урока: изучение нового материала Методы: словесные, наглядные, практические Програм. дидактическое обеспечение : учебник, рабочая тетрадь, интерактивная доска Ход урока: Этап организации начала урока Этап актуализации знаний (работа над ошибками). Проверка домашнего задания Этап усвоения новых знаний Теория (Параллельно демонстрация на интерактивной доске flash - объекта) Термодинамика- раздел физики, в котором изучаются тепловые явления и различные свойства тел без использования представлений об их внутреннем молекулярном строении В термодинамике мы имеем дело не с отдельными молекулами, а с макроскопическими телами, состоящими из огромного числа частиц. Эти тела называются термодинамическими системами. В термодинамике тепловые явления описываются макроскопическими величинами: давление (p), температура (t), объем (V), которые не применимы к отдельным молекулам и атомам Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Он формулируется следующим образом: Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами. ΔU = Q – A Соотношение, выражающее первый закон термодинамики, часто записывают в другой форме: Q = ΔU + A Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами. Первый закон термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Важным следствием первого закона термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины. Такая гипотетическая машина получила название вечного двигателя (perpetuum mobile) первого рода. Многочисленные попытки создать такую машину неизменно заканчивались провалом. Любая машина может совершать положительную работу A над внешними телами только за счет получения некоторого количества теплоты Q от окружающих тел или уменьшения ΔU своей внутренней энергии. Количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра называют ГАЗОВЫМИ ЗАКОНАМИ. С помощью уравнения состояния идеального газа можно исследовать процессы, в которых масса газа и один из трех параметров – давление, объем или температура – остаются неизменными. Процессы, протекающие при неизменном значении одного из параметров, называют ИЗОПРОЦЕССАМИ (от греческого слова « изос» - равный). ИЗОПРОЦЕССЫ ИЗОТЕРМИЧЕСКИЙ ИЗОБАРНЫЙ ИЗОХОРНЫЙ Применим первый закон термодинамики к изопроцессам в газах. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно, Q = ΔU = U(T2) – U(T1) Здесь U(T1) и U(T2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0). ИЗОХОРНЫЙ ПРОЦЕСС – это процесс, происходящий в системе при постоянном объеме. Для осуществления изохорного процесса газ помещают в герметичный сосуд, не меняющий своего объема. Изохора – это линия на диаграмме состояния, являющаяся графиком изохорного процесса. ЗАКОН ШАРЛЯ – при неизменном объеме и массе газа отношение давления газа к его абсолютной температуре является величиной постоянной. В современной физике закон Гей-Люссака рассматривается как одно из следствий уравнения состояния идеального газа (уравнения Менделеева–Клапейрона). Из закона Гей-Люссака следует, что при постоянном объеме давление газа прямо пропорционально его абсолютной температуре.  В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением A = p(V2 – V1) = pΔV Первый закон термодинамики для изобарного процесса дает: Q = U(T2) – U(T1) + p(V2 – V1) = ΔU + pΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T2 < T1; внутренняя энергия убывает, ΔU < 0. ИЗОБАРНЫЙ ПРОЦЕСС – это процесс, происходящий в системе при постоянном давлении. Изобара – линия на диаграмме состояния, являющаяся графиком изобарного процесса. ЗАКОН ГЕЙ-ЛЮССАКА - при неизменном давлении и массе газа отношение объема газа к его абсолютной температуре является величиной постоянной. В современной физике закон Шарля рассматривается как одно из следствий уравнения состояния идеального газа (уравнения Менделеева–Клапейрона). 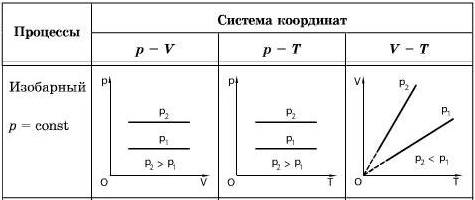 В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС – это процесс, происходящий в системе при постоянной температуре. Изотерма – кривая на диаграмме состояния газа, отражающая ход изотермического процесса. ЗАКОН БОЙЛЯ–МАРИОТТА – при неизменной температуре произведение объема данной массы газа на его давление является величиной постоянной. В современной физике закон Бойля–Мариотта рассматривается как одно из следствий уравнения состояния идеального газа (уравнения Менделеева–Клапейрона). Из закона Бойля–Мариотта следует, что при постоянной температуре газа его давление обратно пропорционально объему. 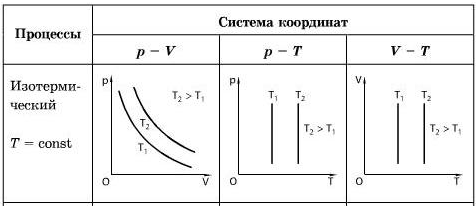 Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими. В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид A = –ΔU т. е. газ совершает работу за счет убыли его внутренней энергии. 4. Подведение итогов 5. Домашнее задание Тема: «Необратимость тепловых процессов. Второй закон термодинамики. Тепловые двигатели» Цели: - Образовательная: познакомить со вторым законом термодинамики; сформировать общие представления о тепловых двигателях; - Развивающая: развивать коммуникабельные способности по теме, уметь выделять главное; сопоставлять факты, результаты, анализировать, высказывать свою точку зрения по проблеме урока. - Воспитательная: воспитание стремления к учению, умения напряженно трудиться; развивать культуру речи, взаимоотношения, взаимопомощь и сотрудничество. Тип рассматриваемого урока: изучение нового материала Методы: словесные, наглядные, практические Програм. дидактическое обеспечение : учебник, рабочая тетрадь, интерактивная доска Ход урока: Этап организации начала урока Этап актуализации знаний (письменная работа). Проверка домашнего задания Этап усвоения новых знаний Теория (Параллельно демонстрация на интерактивной доске flash - объекта) Первый закон термодинамики представляет собой закон сохранения и превращения энергии для тепловых процессов. Однако 1 - ый закон термодинамики не накладывает никаких ограничений на направление превращения энергии из одного вида в другой и на направление перехода теплоты от одного тела к другому. Однако существуют определенные ограничения, связанные с направлением протекания процессов в природе. Например, энергия путем теплообмена самопроизвольно переходит от горячего тела к более холодному, а обратный процесс сам по себе не происходит т.е. он не обратим. Положение о необратимости тепловых явлений, односторонней направленности энергетических превращений в макроскопических системах представляет собой второй закон (второе начало) термодинамики: теплота не может переходить сама собой от более холодного тела к более теплому, т.е. теплота самопроизвольно переходит лишь от горячего тела к холодному Второй закон термодинамики накладывает ограничения на превращение внутренней энергии в механическую. Это означает что невозможно построить машину, которая совершила бы работу только лишь за счет получения теплоты из окружающей среды. Поэтому второй закон термодинамики часто формулируют так: «Вечный» двигатель второго рода невозможен. Внутреннюю энергию газа можно повысить: - если над газом совершить работу по его сжатию -если передать ему некоторое количество теплоты Превращение внутренней энергии в механическую очень важно для практической деятельности людей, для развития техники. Осуществляется такое превращение с помощью тепловых машин (тепловых двигателей) Тепловые машины (тепловые двигатели) – устройства, с помощью которых часть внутренней энергии системы можно превратить в механическую энергию за счет нее совершить работу Принцип действия тепловых двигателей: энергия топлива сначала переходит во внутреннюю энергию газа или пара, нагретых до высокой температуры. Расширяясь, газ совершает работу против внешних сил и при этом охлаждается. При этом уменьшается его внутренняя энергия. Это означает , что часть его внутренней энергии превращается в механическую работу, оставшаяся часть внутренней энергии газа, не превращенная в механическую энергию передается окружающей среде, которая играет роль охладителя и называется холодильником. Конструкция теплового двигателя: рис.54 стр 91 1) Нагреватель – освобождается энергия топлива 2) Рабочее тело – пар или газ 3) Холодильник – забирает неиспользованное кол –во теплоты 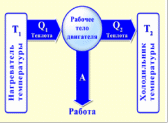 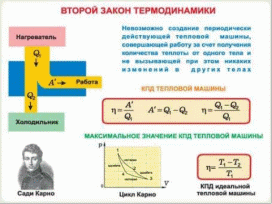 Подведение итогов Домашнее задание Тема: «Двигатель внутреннего сгорания» Цели: - Образовательная: сформировать общие представления о ДВС; - Развивающая: развивать коммуникабельные способности по теме, уметь выделять главное; сопоставлять факты, результаты, анализировать, высказывать свою точку зрения по проблеме урока. - Воспитательная: воспитание стремления к учению, умения напряженно трудиться; развивать культуру речи, взаимоотношения, взаимопомощь и сотрудничество. Тип рассматриваемого урока: изучение нового материала Методы: словесные, наглядные, практические Програм. дидактическое обеспечение : учебник, рабочая тетрадь, интерактивная доска Ход урока: Этап организации начала урока Этап актуализации знаний (устный опрос). Проверка домашнего задания Этап усвоения новых знаний Теория (Параллельно демонстрация на интерактивной доске flash - объекта) Рассмотрим наиболее распространенный вид теплового двигателя – ДВС. Так он называется потому, что жидкое топливо (бензин, керосин, дизельное топливо) или горючий газ сгорают прямо в цилиндре, внутри самого двигателя. Задание: работа в группах 1 группа: ДВС 2 группа: 4-х тактный двигатель 3 группа: 4-х тактный дизельный двигатель По мере выступлений учащихся заполн. Таблицу:
Подведение итогов Домашнее задание Тема: «Паровые и газовые турбины. Реактивные двигатели. Холодильные машины. КПД. Рль тепловых двигателей» Цели: - Образовательная: сформировать общие представления о паровых и газовых турбинах, реактивных двигателях, холодильных машинах; познакомить с КПД; - Развивающая: развивать коммуникабельные способности по теме, уметь выделять главное; сопоставлять факты, результаты, анализировать, высказывать свою точку зрения по проблеме урока. - Воспитательная: воспитание стремления к учению, умения напряженно трудиться; развивать культуру речи, взаимоотношения, взаимопомощь и сотрудничество. Тип рассматриваемого урока: изучение нового материала Методы: словесные, наглядные, практические Програм. дидактическое обеспечение : учебник, рабочая тетрадь, интерактивная доска Ход урока: Этап организации начала урока Этап актуализации знаний (устный опрос). Проверка домашнего задания Этап усвоения новых знаний Теория (Параллельно демонстрация на интерактивной доске flash - объекта) Подведение итогов Домашнее задание Тема: «Термодинамические условия на Луне, Венере, Марсе» Цели: - Образовательная: сформировать общие представления о термодинамических условиях на Луне, Венере, Марсе; - Развивающая: развивать коммуникабельные способности по теме, уметь выделять главное; сопоставлять факты, результаты, анализировать, высказывать свою точку зрения по проблеме урока. - Воспитательная: воспитание стремления к учению, умения напряженно трудиться; развивать культуру речи, взаимоотношения, взаимопомощь и сотрудничество. Тип рассматриваемого урока: изучение нового материала Методы: словесные, наглядные, практические Програм. дидактическое обеспечение : учебник, рабочая тетрадь, интерактивная доска Ход урока: Этап организации начала урока Этап актуализации знаний (тест). Проверка домашнего задания Этап усвоения новых знаний Задание: заполнить таблицу
Подведение итогов Домашнее задание Контрольная работа №2 Цели: - Образовательная: закрепление знаний по пройденным темам - Развивающая: уметь выделять главное; сопоставлять факты, результаты, анализировать - Воспитательная: воспитание стремления к учению, умения напряженно трудиться; развивать взаимоотношения, взаимопомощь и сотрудничество. Тип рассматриваемого урока: контроль знаний Методы: практические Програм. дидактическое обеспечение : учебник, рабочая тетрадь, интерактивная доска Ход урока: Этап организации начала урока Домашнее задание |
