Вопрос Белки. Разнообразие. Функции
 Скачать 362.81 Kb. Скачать 362.81 Kb.
|
|
ВОПРОС № 21 Иммуноглобулины, или антитела, - специфические белки, вырабатываемые В-лимфоцитами в ответ на попадание в организм чужеродных структур, называемых антигенами. Все иммуноглобулины характеризуются общим планом строения, который мы рассмотрим на примере строения IgG. Молекула IgG состоит из четырёх полипептидных цепей: двух идентичных лёгких (L), содержащих около 220 аминокислотных остатков, и двух тяжёлых (Н), состоящих из 440 аминокислот каждая. Все 4 цепи соединены друг с другом множеством нековалентных и четырьмя дисульфидными связями. Поэтому молекулу IgG относят к мономерам. Лёгкие цепи IgGсостоят из 2 доменов: вариабельного (VL), находящегося в N-концевой области полипептидной цепи, и константного (CL), расположенного на С-конце. Каждый из доменов состоит из 2 слоев с β-складчатой структурой, где участки полипептидной цепи лежат антипараллельно. β-Слои связаны ковалентно дисульфидной связью примерно в середине домена. Тяжёлые цепи IgGимеют 4 домена: один вариабельный (VH), находящийся на N-конце, и три константных (СН1, СН2, СH3). Домены тяжёлых цепей IgG имеют гомологичное строение с доменами лёгких цепей. Между двумя константными доменами тяжёлых цепей СH1, и СН2 есть участок, содержащий большое количество остатков пролина, которые препятствуют формированию вторичной структуры и взаимодействию соседних Н-цепей на этом отрезке. Этот участок называют "шарнирной областью"; он придаёт молекуле гибкость. Между вариабельными доменами тяжёлых и лёгких цепей находятся два идентичных участка, связывающих два одинаковых специфических антигена; поэтому такие антитела часто называют"биваленты".В связывании антигена с антителом участвует не вся аминокислотная последовательность вариабельных доменов обеих цепей, а всего лишь 20-30 аминокислот, расположенных в гипервариабельных областях каждой цепи. Именно эти области определяют уникальность взаимодействия с соответствующим (комплементарным) антигеном. 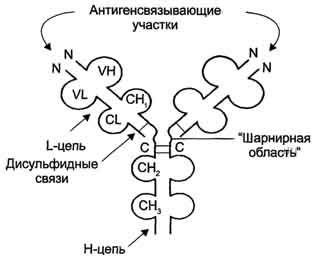 Основные функции антител - обнаружение и связывание чужеродных антигенов, находящихся в организме вне его клеток (в крови, лимфе, межклеточной жидкости, в слизистых секретах). Это происходит с помощью специфических антигенсвязывающих участков разных клонов иммуноглобулинов. Кроме, того, благодаря связыванию антигена с антителом облегчается процесс дальнейшего разрушения чужеродных веществ. Специфичность пути разрушения комплекса антиген-антитело зависит от класса антител. ВОПРОС № 22 Ферменты (энзимы, Е) – биокатализаторы белковой природы. Ферменты, как было установлено ещё в 1922 г., являются белками. В отличие от катализаторов неживой природы, они обычно более специфичны. Биороль – каталитическая и регуляторная. Ферменты присутствуют во всех живых клетках и способствуют превращению одних веществ (субстратов) в другие (продукты). Ферменты выступают в роли катализаторов практически во всех биохимических реакциях, протекающих в живых организмах — ими катализируется более 4000 разных биохимических реакций. Ферменты играют важнейшую роль во всех процессах жизнедеятельности, направляя и регулируя обмен веществ организма. Действие ферментов в клетке, как правило, строго упорядочено: продукт одной ферментативной реакции является субстратом другой, образуя таким образом "метаболические пути". Среди множества ферментов практически каждого метаболического пути различают ключевые, или регуляторные, ферменты, активность которых может изменяться в зависимости от потребности клетки в конечном продукте метаболического пути. Регуляторные ферменты расположены, как правило, в начале и/или в месте разветвления метаболического пути. Особенности ферментативного катализа: - высокая эффективность действия - специфичность - способность к регуляции - мягкие условия протекания ферментативных реакций (t = 37º С, нормальное атмосферное давление, рН близкое к 7,0). Большинство катализируемых ферментами реакций высокоэффективны, они протекают в 108-1014 раз быстрее, чем некатализируемые реакции. Каждая молекула фермента способна за секунду трансформировать от 100 до 1000 молекул субстрата в продукт. Количество молекул субстрата, превращённых в продукт с помощью одной молекулы фермента за 1 с, называют числом оборотов фермента, или молярной активностью. Специфичность - наиболее важное свойство ферментов, определяющее биологическую значимость этих молекул. Различают субстратную и каталитическую специфичности фермента, определяемые строением активного центра. Под субстратной специфичностью понимают способность каждого фермента взаимодействовать лишь с одним или несколькими определёнными субстратами. Различают:
Активный центр ферментов, обладающих абсолютной субстратной специфичностью, комплементарен только одному субстрату. Следует отметить, что таких ферментов в живых организмах мало. Другой пример фермента с абсолютной субстратной специфичностью - уреаза, катализирующая гидролиз мочевины до диоксида углерода и аммиака. Большинство ферментов катализирует однотипные реакции с небольшим количеством (группой) структурно похожих субстратов. Так, фермент панкреатическая липаза катализирует гидролиз жиров в двенадцатиперстной кишке человека, катализируя превращение любой молекулы жира (триацилглицерола) до молекулы моноацилглицерола и двух молекул высших жирных кислот. При наличии у субстрата нескольких стерео-изомеров фермент проявляет абсолютную специфичность к одному из них. В организме человека наблюдают специфичность ферментов к следующим стереоизомерам. Каталитическая специфичность Фермент катализирует превращение присоединённого субстрата по одному из возможных путей его превращения, Это свойство обеспечивается строением каталитического участка активного центра фермента и называется каталитической специфичностью, или специфичностью пути превращения субстрата. Так, молекула глюкозо-6-фосфата в клетках печени человека - субстрат 4 различных ферментов; фос-фоглюкомутазы, глюкозо-6-фосфатфосфатазы, фосфоглюкоизомеразы и глюкозо-6-фосфатдегидрогеназы. Однако из-за особенностей строения каталитических участков этих ферментов происходит различное превращение этого соединения с образованием 4 различных продуктов. Если стерерокаталитическая специфичность – субстрат просто не должен иметь стереоизомеры. ВОПРОС № 23 Субстрат (S) – лиганд, взаимодействующий с активным центром фермента; вещество, на которое действует фермент. Продукт реакции (Р) – вещество, образующееся из субстрата под влиянием фермента. В составе фермента, являющегося сложным белком – апофермент (белковая часть) и небелковая часть (низкомолекулярные органические соединения, кроме аминикислот, – коферменты или неорганические частицы – кофакторы). Комплекс апофермента и кофермента – холофемент. Вещества, которые оказывают влияние на активность ферментов, называют эффекторами. Это могут быть ингибиторы – соединения, тормозящие каталитический процесс, или активаторы – вещества, которые этот процесс ускоряют. Фермент – ЛДГ. Субстрат – лактат, продукт – пируват. Кофермент – НАД. Фермент – альфа-амилаза. Субстрат – крахмал, продукт – мальтоза. Кофактор – ион кальция. Фермент – пируваткиназа. Субстрат – фосфоенолпируват, продукт – пируват. Ингибитор – АТФ, активатор – фруктозо-1,6-фосфат. Фермент – сукцинатдегидрогеназа. Ингибитор – малоновая кислота. Фермент – ацетилхолинэстераза. Ингибиторы – прозерин и эндрофоний. Коферменты: в трансаминазах – пиридиксальфосфат, в дегидрогеназах – НАД, в оксидоредуктазах – ФАД. ВОПРОС № 24 Структура ферментов. Ферменты делятся на простые и сложные. Простые ферменты являются белками и состоят только из аминокислот (например, ферменты 3 класса гидролазы). Сложные ферменты состоят из белкового компонента (апофермента) и небелкового (кофак тора или кофермента). В целом сложный фермент (апофермент + кофактор) называется холоферментом. Активный центр (АкЦ) – уникальная комбинация АК остатков в молекуле фермента, обеспечивает связывание её с молекулой S и участие в акте катализа, расположен в узком гидрофобном углублении (щели) молекулы фермента, образуется на уровне третичной структуры. В линейной последовательности полипептидной цепи радикалы, формирующие активный центр, могут находиться на значительном расстоянии друг от друга. Активный центр фермента - относительно изолированный от окружающей среды участок, сформированный аминокислотными остатками. Объединение таких аминокислот в единый функциональный комплекс изменяет реакционную способность их радикалов. Часто активный центр формируется таким образом, что доступ воды к функциональным группам его радикалов ограничен, т.е. создаются условия для связывания субстрата с радикалами аминокислот. В АкЦ Е различают:
В активном центре фермента субстраты располагаются таким образом, чтобы участвующие в реакции функциональные группы субстратов находились в непосредственной близости друг к другу. Это свойство активного центра называют эффектом сближения и ориентации реагентов. Активный центр фермента также способствует дестабилизации межатомных связей в молекуле субстрата, что облегчает протекание химической реакции и образование продуктов. Это свойство активного центра называют эффектом деформации субстрата ВОПРОС № 25 S- связывающий участок по форме соответствует S (геометрическое соответствие), между АК остатками активного центра и S образуются связи (Н, гидрофобные, ионные), т.е. устанавливается электронное или химическое соответствие. Таким образом, S комплементарен активному центру. В общем виде все сводится к комплементарному взаимодействию E и S. При этом функциональные группы субстрата взаимодействуют с соответствующими им функциональными группами фермента. Наличие субстратной специфичности объясняют две гипотезы:
ВОПРОС № 26 Ферменты, катализирующие одну и ту же химическую реакцию, но отличающиеся по первичной структуре белка, называют изоферментами, или изоэнзимами. Они катализируют один и тот же тип реакции с принципиально одинаковым механизмом, но отличаются друг от друга первичной структурой, физико-химическими свойствами (кинетическими параметрами, условиями активации, молекулярной массой, сродством к субстрату), особенностями связи апофермента и кофермента, локализацией в организме. Природа появления изоферментов разнообразна, но чаще всего обусловлена различиями в структуре генов, кодирующих эти изоферменты. Следовательно, изоферменты различаются по первичной структуре белковой молекулы и, соответственно, по физико-химическим свойствам. На различиях в физико-химических свойствах основаны методы определения изоферментов. Значение – возможность действовать в разных тканях и органах, где есть разные условия – pH, температура, эффекторы, наличие кислорода, химический состав) По своей структуре изоферменты в основном являются олигомерными белками. Причём та или иная ткань преимущественно синтезирует определённые виды протомеров. В результате определённой комбинации этих протомеров формируются ферменты с различной структурой - изомерные формы. Обнаружение определённых изоферментных форм ферментов позволяет использовать их для диагностики заболеваний. Изоформы лактатдегидрогеназы. Фермент лак-татдегидрогеназа (ЛДГ) катализирует обратимую реакцию окисления лактата (молочной кислоты) до пирувата (пировиноградной кислоты) Лактатдегидрогеназа - олигомерный белок с молекулярной массой 134 000 Д, состоящий из 4 субъединиц 2 типов: М (от англ, muscle - мышца) и Н (от англ, heart - сердце). Комбинация этих субъединиц лежит в основе формирования 5 изоформ лактатдегидрогеназы (рис. 2-35, А). ЛДГ1 и ЛДГ2 наиболее активны в сердечной мышце и почках, ЛДГ4 и ЛДГ5 - в скелетных мышцах и печени. В остальных тканях имеются различные формы этого фермента. Изоформы ЛДГ отличаются электрофоретической подвижностью, что позволяет устанавливать тканевую принадлежность изоформ ЛДГ При ряде заболеваний исследуют активность ЛДГ в плазме крови. В норме активность ЛДГ составляет 170-520 ЕД/л. Повышение активности наблюдают при острых поражениях сердца, печени, почек, а также при мегалобластных и гемолитических анемиях. Однако это указывает на повреждение лишь одной из перечисленных тканей. Для постановки диагноза необходимо исследование изоформ ЛДГ в плазме крови методом электрофореза. Изоформы креатинкиназы. Креатинкиназа (КК) катализирует реакцию образования креатинфосфата. Молекула КК - димер, состоящий из субъединиц двух типов: М (от англ, muscle - мышца) и В (от англ, brain - мозг). Из этих субъединиц образуются 3 изофермента - ВВ, MB, MM. Изофермент ВВ находится преимущественно в головном мозге, ММ - в скелетных мышцах и MB - в сердечной мышце. Изоформы КК имеют разную электрофоретическую подвижность Активность КК в норме не должна превышать 90 МЕ/л. Определение активности КК в плазме крови имеет диагностическое значение при инфаркте миокарда (происходит повышение уровня МВ-изоформы). Количество изоформы ММ может повышаться при травмах и повреждениях скелетных мышц. Изоформа ВВ не может проникнуть через гематоэнцефалический барьер, поэтому в крови практически не определяется даже при инсультах и диагностического значения не имеет. ВОПРОС № 27 Кинетика ферментативных реакций - раздел энзимологии, изучающий зависимость скорости химических реакций, катализируемых ферментами, от химической природы реагирующих веществ, а также от факторов окружающей среды. Математически скорость ферментативной реакции выражается в изменении концентрации субстрата (уменьшение) или продукта (увеличение) за единицу времени: V= D[S]/t = D[P]/t. Повышение температуры до определённых пределов оказывает влияние на скорость ферментативной реакции, подобно влиянию температуры на любую химическую реакцию. С повышением температуры ускоряется движение молекул, что приводит к повышению вероятности взаимодействия реагирующих веществ. Однако скорость химической реакции, катализируемая ферментами, имеет свой температурный оптимум, превышение которого сопровождается понижением ферментативной активности, возникающим из-за термической денатурации белковой молекулы. Наличие E-S-комплекса повышает для некоторых молекул фермента температуру денатурации Активность ферментов зависит от рН раствора, в котором протекает ферментативная реакция. Для каждого фермента существует значение рН, при котором наблюдается его максимальная активность. Отклонение от оптимального значения рН приводит к понижению ферментативной активности. При проведении ферментативной реакции в условиях избытка субстрата скорость реакции будет зависеть от концентрации фермента. Графическая зависимость такой реакции имеет вид прямой линии Если концентрацию ферментов оставить постоянной, изменяя только количество субстрата, то график скорости ферментативной реакции описывают гиперболой 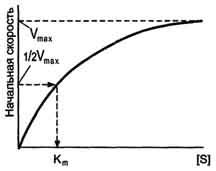 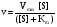 Уравнение имеет вид: где
Выражение в знаменателе — (k-1+k2)/k1 — называется константой Михаэлиса (Km). k1 — константа скорости реакции образования фермент-субстратного комплекса из фермента и субстрата. k2 — константа скорости реакции превращения фермент-субстратного комплекса в фермент и продукт Vmax и Кm — кинетические характеристики эффективности Е. Vmax (при ней – фермент полностью насыщен субстратом) позволяет оценить эффективность действия Е, определяет максимальную возможность образования Р при данной [E] и в условиях избытка S. Кm характеризует сродство данного фермента к данному субстрату и является величиной постоянной, не зависящей от концентрации фермента. Чем меньше Кm, тем больше сродство фермента к данному субстрату, тем выше начальная скорость реакции и наоборот, чем больше Кm, тем меньше начальная скорость реакции, тем меньше сродство фермента к субстрату. |
