Зачем врачу нужна биологическая химия
 Скачать 6.47 Mb. Скачать 6.47 Mb.
|
Дыхательная цепь включает множество белков-переносчиковВсего цепь переноса электронов (англ. electron transport chain) включает в себя около 40 разнообразных белков, которые организованы в 4 больших мембраносвязанных мульферментных комплекса. Также существует еще один комплекс, участвующий не в переносе электронов, а синтезирующий АТФ. 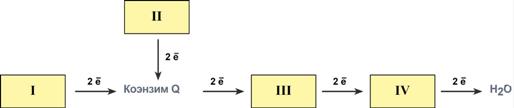 Блок-схема дыхательной цепиСтроение ферментативных комплексов дыхательной цепи1 комплекс. НАДН-КоQ-оксидоредуктазаЭтот комплекс также имеет рабочее название НАДН-дегидрогеназа, содержит ФМН, 22 белковых молекулы, из них 5 железосерных белков с общей молекулярной массой до 900 кДа.Функция
2 комплекс. ФАД-зависимые дегидрогеназыДанный комплекс как таковой не существует, его выделение условно. Он включает в себя ФАД-зависимые ферменты, расположенные на внутренней мембране – например, ацил-SКоА-дегидрогеназа (окисление жирных кислот), сукцинатдегидрогеназа (цикл трикарбоновых кислот), митохондриальная глицерол-3-фосфат-дегидрогеназа (челночный механизм переноса НАДН в митохондрию). Функция
3 комплекс. КоQ-цитохром с-оксидоредуктазаДанный комплекс включает цитохромы b и c1. Кроме цитохромов в нем имеются 2 железо-серных белка. Всего насчитывается 11 полипептидных цепей общей молекулярной массой около 250 кDа. Функция
4 комплекс. Цитохром с-кислород-оксидоредуктазаВ этом комплексе находятся цитохромы а и а3, он называется также цитохромоксидаза, всего содержит 6 полипептидных цепей. В комплексе также имеется 2 иона меди. Функция
5 комплексПятый комплекс – это ферментАТФ-синтаза, состоящий из множества белковых цепей, подразделенных на две большие группы:
Упрощенно считают, что для синтеза 1 молекулы АТФ необходимо прохождение приблизительно 3-х протонов Н+. Каким образом энергия водорода преобразуется в энергию АТФ?Механизм окислительного фосфорилированияНа основании строения и функций компонентов дыхательной цепи предложен механизм окислительного фосфорилирования: 1. Ферменты дыхательной цепи расположены в строго определенной последовательности: каждый последующий белок обладает большим сродством к электронам, чем предыдущий (он более электроположителен, т.е. обладает более положительным окислительно-восстановительным потенциалом). Это обеспечивает однонаправленное движение электронов. 2. Все атомы водорода, отщепленные дегидрогеназами от субстратов в аэробных условиях, достигают внутренней мембраны митохондрий в составе НАДНили ФАДН2. 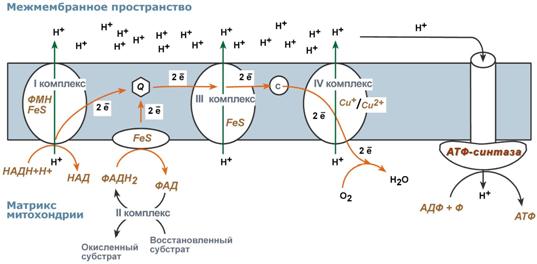 Строение дыхательной цепи и механизм окислительного фосфорилирования3. Здесь атомы водорода (от НАДН и ФАДН2) передают свои электроныв дыхательную ферментативную цепь, по которой электроны движутся (50-200 шт/сек) к своему конечному акцептору – кислороду. В результате образуется вода. 4. Поступающие в дыхательную цепь электроны богаты свободной энергией. По мере их продвижения по цепи они теряют энергию. 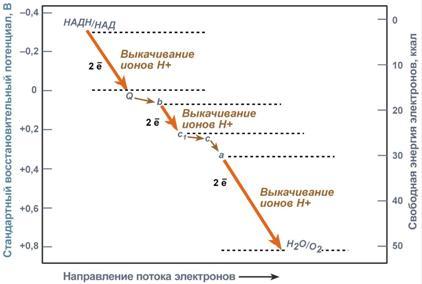 Энергетические соотношения в дыхательной цепи митохондрий и |
