Зачем врачу нужна биологическая химия
 Скачать 6.47 Mb. Скачать 6.47 Mb.
|
Откуда в клетке АТФ?Способы получения энергии в клеткеВ клетке существуют четыре основных процесса, обеспечивающих высвобождение энергии из химических связей при окислении веществ и ее запасание: 1. Гликолиз(2 этап биологического окисления) – окисление молекулы глюкозы до двух молекул пировиноградной кислоты, при этом образуется 2 молекулы АТФи НАДН. Далее пировиноградная кислота в аэробных условиях превращается в ацетил-SКоА, в анаэробных условиях – в молочную кислоту. 2. β-Окисление жирных кислот (2 этап биологического окисления) – окисление жирных кислот до ацетил-SКоА, здесь образуются молекулы НАДНи ФАДН2. Молекулы АТФ "в чистом виде" не появляются. 3. Цикл трикарбоновых кислот (ЦТК, 3 этап биологического окисления) – окисление ацетильной группы (в составе ацетил-SКоА) или иных кетокислот до углекислого газа. Реакции полного цикла сопровождаются образованием 1 молекулы ГТФ(что эквивалентно одной АТФ), 3 молекул НАДНи 1 молекулы ФАДН2. 4. Окислительное фосфорилирование (3 этап биологического окисления) – окисляются НАДН и ФАДН2, полученные в реакциях катаболизма глюкозы, аминокислот и жирных кислот. При этом ферменты дыхательной цепи на внутренней мембране митохондрий обеспечивают образование большейчасти клеточного АТФ. Два способа синтеза АТФОсновным способом получения АТФ в клетке является окислительное фосфорилирование, протекающее в структурах внутренней мембраны митохондрий. При этом энергия атомов водорода молекул НАДН и ФАДН2, образованных в гликолизе, ЦТК, окислении жирных кислот, преобразуется в энергию связей АТФ. Однако также есть другой способ фосфорилирования АДФ до АТФ – субстратное фосфорилирование. Этот способ связан с передачей макроэргического фосфата или энергии макроэргической связи какого-либо вещества (субстрата) на АДФ. К таким веществам относятся метаболиты гликолиза (1,3-дифосфоглицериновая кислота, фосфоенолпируват), цикла трикарбоновых кислот (сукцинил-SКоА) икреатинфосфат. Энергия гидролиза их макроэргической связи выше, чем 7,3 ккал/моль в АТФ, и роль указанных веществ сводится к использованию этой энергии для фосфорилирования молекулы АДФ до АТФ. Пируват окисляется до уксусной кислотыПировиноградная кислота (ПВК, пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробныхусловиях она восстанавливается до молочной кислоты. В аэробныхусловиях пируват симпортом с ионами Н+, движущимися по протонному градиенту, проникает в митохондрии. Здесь происходит его превращение доуксусной кислоты, переносчиком которой служит коэнзим А. Пируватдегидрогеназный мульферментный комплексСуммарное уравнение отражает окислительное декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-SKoA. 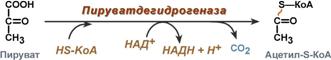 Суммарное уравнение окисления пировиноградной кислотыПревращение состоит из пятипоследовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса насчитывают 3 фермента и 5 коферментов:
Помимо указанных коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД. Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению пирувата до ацетила и переносу ацетила на коэнзим А (катализируется дигидролипоамид-ацетилтрансферазой, Е2). 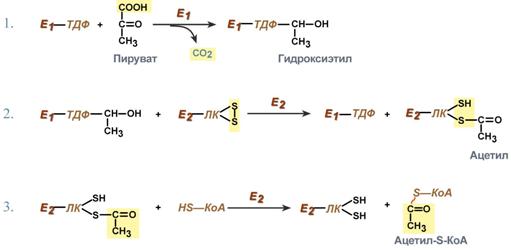 Реакции синтеза ацетил-SКоАОставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются дигидролипоат-дегидрогеназой, Е3). При этом образуется НАДН. 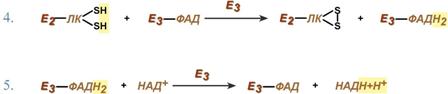 Реакции образования НАДНРегуляция пируватдегидрогеназного комплексаРегулируемым ферментом ПВК-дегидрогеназного комплекса является первый фермент –пируватдегидрогеназа (Е1). Два вспомогательных фермента – киназаи фосфатаза обеспечивают регуляцию активности пируватдегидрогеназы путем ее фосфорилированияи дефосфорилирования. Вспомогательный фермент киназаактивируется при избытке конечного продукта биологического окисленияАТФи продуктов ПВК-дегидрогеназного комплекса – НАДНи ацетил-S-КоА. Активная киназа фосфорилирует пируватдегидрогеназу, инактивируя ее, в результате первая реакция процесса останавливается. Фермент фосфатаза, активируясь ионами кальцияили инсулином, отщепляет фосфат и активирует пируватдегидрогеназу. 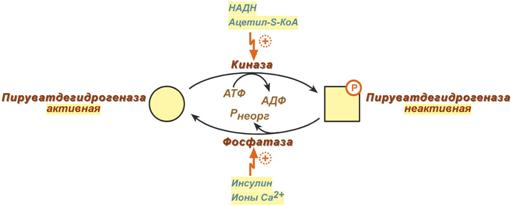 Регуляция активности пируватдегидрогеназыТаким образом, работа пируватдегидрогеназы подавляется при избыткев митохондрии (в клетке) АТФиНАДН, что позволяет снизить окисление пирувата и, следовательно, глюкозы в случае когда энергии достаточно. ЕслиАТФ мало или имеется влияние инсулина, то образуется ацетил-SКоА. Последний в зависимости от условий будет направляться либо в цикл трикарбоновых кислот с образованием энергии АТФ, либо на синтезхолестерина и жирных кислот. |
