Закон Авогадро. В равных vах всех газов при одинаковых давлении и температуре содержится одинаковое число молекул
 Скачать 0.77 Mb. Скачать 0.77 Mb.
|
|
60.Составные части системы и компоненты. Правило фаз.Составные части системы – химически индивидуальные вещества, составляющие данную систему и способные к самостоятельному существованию.В равновесной системе | ||
| 55.Химическая и концентрационная поляризация при электролизе. Понятие перенапряжения.В процессе электролиза всегда возникает некоторая разность потенциалов, направленная противоположно той, которая накладывается извне. Это явление носит название поляризации. Различают химическую и концентрационную.Химическая обусловлена химическими изменениями на поверхности электрода.Концентрационная поляризация: концентрация потенциалопределяющих ионов у анода и катода в процессе электролиза будет различаться, у катода она меньше равновесной, у анода – больше. Возникает концентрационный элемент, ЭДС которого направлена навстречу внешней ЭДС, она может быть уменьшена путем перемешивания раствора. Напряжение разложения – наименьшее значение внешней ЭДС, при достижении которого начинается длительный электролиз (с выделением его продуктов). Перенапряжение – это разность между напряжением разложения, фактически необходимым для протекания электролиза в данной электрохимической системе, и ЭДС гальванического элемента, отвечающего этой системе. Вред перенапряжения: добавочный расход электроэнергии, польза: удается получать электролизом водных растворов металлы, потенциалы которых отрицательны. | 56.Классификация химических источников тока.Существуют 3 типа ХИТ: первичные - гальванические элементы, вторичные – аккумуляторы и топливные элементы.В гальванических элементах активные вещества, необходимые для работы элемента, закладываются в него при монтаже, после израсходования веществ элемент утилизируется.В основу аккумулятора положена высоко-обратимая хим реакция окисления-восстановления, которую можно проводить в обоих направлениях.Топливный элемент – это ХИТ длительного действия, начинающий и прекращающий работу с началом и прекращением подачи активных веществ в электродам.Достоинства ХИТ: высокий КПД, экологическая чистота, бесшумность, автономность действия.Недостаток – низкие удельные характеристики. Марганцево-цинковый элемент: наиболее широко применяется среди первичных ХИТ. Электрохимическая цепь: (-)Zn|NH4Cl|MnO2(+). Электролит – 20% раствор NH4Cl, загущенный до студнеобразного состояния, для предотвращения высыхания и загнивания вводят специальные добавки. MnO2 спрессован с добавкой сажи – для увеличения электроемкости. ЭДС от 1,48 до 1,8 в зависимости от кристаллической модификации MnO2, начальное напряжение 1,1-1,25В. Процессы при разряде: (-) Zn-2ē+2H2O>Zn(OH)2+2H+, (+)2MnO2+2ē+2H+>2MnO.OH, Zn+2MnO2+2H2O=Zn(OH)2+2MnO.OH. Вторичная реакция: Zn(OH)2+2NH4Cl=[Zn(NH3)2]Cl2+2MnO.OH | 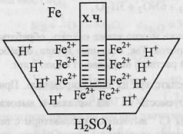 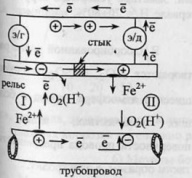 57.Коррозия металлов. Химическая и электрохимическая коррозия.Коррозия – самопроизвольно протекающий процесс поверхностного окисления металла в результате его химического или электрохимического взаимодействия с окружающей средой.В результате коррозии металл из свободного состояния переходит в связанное. Потери от коррозии велики: десятки миллиардов долларов в индустриально-развитых странах.Химическая коррозия (газовая и жидкостная).Газовая – разрушение происходит в атмосфере сухого газа – окислителя (кислород, галогены). 57.Коррозия металлов. Химическая и электрохимическая коррозия.Коррозия – самопроизвольно протекающий процесс поверхностного окисления металла в результате его химического или электрохимического взаимодействия с окружающей средой.В результате коррозии металл из свободного состояния переходит в связанное. Потери от коррозии велики: десятки миллиардов долларов в индустриально-развитых странах.Химическая коррозия (газовая и жидкостная).Газовая – разрушение происходит в атмосфере сухого газа – окислителя (кислород, галогены). |
| 58.Основные методы борьбы с коррозией.Коррозия – самопроизвольно протекающий процесс поверхностного окисления металла в результате его химического или электрохимического взаимодействия с окружающей средой.В результате коррозии металл из свободного состояния переходит в связанное. Потери от коррозии велики: десятки миллиардов долларов в индустриально-развитых странах.Методы борьбы различны: -антикоррозийное легирование металла – введение в металл добавок, чтобы повысить стойкость основного металла.защитные покрытия (металлические и неметаллические).металлические наносятся под давлением сжатого воздуха. характерно покрытие листового материала тонким слоем другого материала.неметаллические – лаки ,краски, битум, солидол.-ингибиторы коррозии.вещества, замедляющие процесс разрушения металла.Пример. | 59.Кристаллическое состояние вещества. Химическая связь в кристаллах.Твердые вещества могут находиться в аморфном или кристаллическом состояниях.Вещества в аморфном состоянии не имеют четкой структуры, их иногда называют «переохлажденными жидкостями с аномально высокой вязкостью».Кристаллические структуры.Наименьшая структурная единица – элементарная ячейка. В зависимости от решеток и углов между характеристическими осями различают 7 основных видов (кубическая, ромбоэдрическая и пр.).Тип кристаллической системы определяется природой и размерами частиц, видом химических связей между ними, температурой и другими факторами.Многие соединения могут существовать в двух и более кристаллических структурах. Это явление – полиморфизм.Все кристаллы можно разделить по видам химической связи. Стоит отметить, что существуют кристаллы со смешанными связями.1. Молекулярная связь.В узлах кристаллических решеток находятся молекулы, между которыми дейтсвуют вандерваальсовы силы, имеющие невысокую энергию.Для кристаллов с молекулярными связями характерны низкие температуры плавления и высокая сжимаемость.2. Ковалентная связь.В узлах кристаллов располагаются атомы, образующие прочные ковалентные связи.Это обуславливает высокую энергию решетки.Кристаллы с ковалентной связью - диэлектрики или полупроводники. Типичными примеры: алмаз и кремний.3. Ионная связь.Структурные единицы – положительно и отрицательно заряженные ионы, между которыми происходит электростатическое взаимодействие, характеризуемое высокой энергией.Кристаллы с ионной связью при низких температурах являются диэлектриками. При температурах близких к температуре плавления они становятся проводниками электричества.4. Металлическая связь.Специфические свойства металлов (высокая проводимость, теплопроводность, ковкость, пластичность, металлический блеск) можно объяснить особым типом связи – металлическая.Во всех узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно движутся валентные электроны, отщепившиеся от атомов при образовании ионов. Эти электроны удерживают вместе положительные ионы, в противном случае решётка распалась бы под действием сил отталкивания между ионами. 5. Смешанная связь.Тот или иной вид связи встречается редко, обычно – наложение двух или более связей. | |
| 6 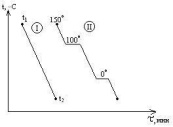 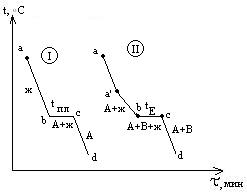 1.Сущность термографического анализа. Кривые нагревания и охлаждения.Термографический анализ – кривые нагревания или кривые охлаждения системы. Диаграммы плавкости (частный вид диагарамм состояния) строят исходя из кривых охлаждения, которые изображаются в координатах: температура(Оу), время(Ох). Рассмотрим кривые охлаждения двух систем. Система I в интервале t1-t2 не испытывает никаких фазовых превращений, температура меняется монотонно. Кривая II отвечают охлаждению воды от 150 o C (пар при атмосферном давлении) до 0 o C и ниже. При 100 o C наблюдается горизонтальный участок, отвечающий фазовому переходу – процессу конденсации пара, температура поддерживается низменной, пока не исчезнет весь пар. Постоянство температуры обеспечивается за счёт выделения в процессе конденсации пара теплоты испарения воды. От 100 o C до 0 o C наблюдается монотонный ход кривой охлаждения – остывает жидкая вода. При 0 o C наблюдается второй горизонтальный участок, отвечающий фазовому переходу – процессу кристаллизации. Температура поддерживается постоянной за счет выделения теплоты плавления.Рассмотрим кривые охлаждения чистого металла (I) и сплава с так называемой эвтектикой (II). На кривой охлаждения (I) чистого металла А наблюдается одна площадка bc, отвечающая процессу кристаллизации металла. При tпл в равновесии находятся жидкая и твердая фазы одинакового состава. Образование твердой фазы сопровождается выделением теплоты плавления.Кривая II отвечает охлаждению сплава А-В. От “а” до “a’ “ температура меняется монотонно, остывает жидкая фаза. При достижении точки a’ из жидкой фазы начинают выпадать кристаллы А – одного из компонентов сплава, при этом жидкая фаза за счет этого начнет обогащаться компонентом В. Таким образом, в интервале a’-b в равновесии находятся жидкая и твердая фазы различного состава, площадки на кривой охлаждения не наблюдается. За счет выделения при кристаллизации А теплоты плавления этого компонента темп охлаждения сплава замедляется, и на кривой наблюдается перелом. Выпадение кристаллов А продолжается до тех пор, пока жидкая фаза не достигнет так называемого “эвтектического состава”. Основной особенностью эвтектического сплава является то, что он кристаллизуется подобно чистому компоненту – на кривой охлаждения наблюдается площадка. Из жидкой фазы одновременно выпадают кристаллы А и В и, таким образом при tЕ (отрезок bc) в равновесии находятся жидкая и твердая фазы одинакового состава. Отрезок cd отвечают охлаждению твердого сплава.Остановки в падении температуры могут наблюдаться и на кривой охлаждения уже твердого металла, указываю на переходы металла из одной аллотропной формы в другую. 1.Сущность термографического анализа. Кривые нагревания и охлаждения.Термографический анализ – кривые нагревания или кривые охлаждения системы. Диаграммы плавкости (частный вид диагарамм состояния) строят исходя из кривых охлаждения, которые изображаются в координатах: температура(Оу), время(Ох). Рассмотрим кривые охлаждения двух систем. Система I в интервале t1-t2 не испытывает никаких фазовых превращений, температура меняется монотонно. Кривая II отвечают охлаждению воды от 150 o C (пар при атмосферном давлении) до 0 o C и ниже. При 100 o C наблюдается горизонтальный участок, отвечающий фазовому переходу – процессу конденсации пара, температура поддерживается низменной, пока не исчезнет весь пар. Постоянство температуры обеспечивается за счёт выделения в процессе конденсации пара теплоты испарения воды. От 100 o C до 0 o C наблюдается монотонный ход кривой охлаждения – остывает жидкая вода. При 0 o C наблюдается второй горизонтальный участок, отвечающий фазовому переходу – процессу кристаллизации. Температура поддерживается постоянной за счет выделения теплоты плавления.Рассмотрим кривые охлаждения чистого металла (I) и сплава с так называемой эвтектикой (II). На кривой охлаждения (I) чистого металла А наблюдается одна площадка bc, отвечающая процессу кристаллизации металла. При tпл в равновесии находятся жидкая и твердая фазы одинакового состава. Образование твердой фазы сопровождается выделением теплоты плавления.Кривая II отвечает охлаждению сплава А-В. От “а” до “a’ “ температура меняется монотонно, остывает жидкая фаза. При достижении точки a’ из жидкой фазы начинают выпадать кристаллы А – одного из компонентов сплава, при этом жидкая фаза за счет этого начнет обогащаться компонентом В. Таким образом, в интервале a’-b в равновесии находятся жидкая и твердая фазы различного состава, площадки на кривой охлаждения не наблюдается. За счет выделения при кристаллизации А теплоты плавления этого компонента темп охлаждения сплава замедляется, и на кривой наблюдается перелом. Выпадение кристаллов А продолжается до тех пор, пока жидкая фаза не достигнет так называемого “эвтектического состава”. Основной особенностью эвтектического сплава является то, что он кристаллизуется подобно чистому компоненту – на кривой охлаждения наблюдается площадка. Из жидкой фазы одновременно выпадают кристаллы А и В и, таким образом при tЕ (отрезок bc) в равновесии находятся жидкая и твердая фазы одинакового состава. Отрезок cd отвечают охлаждению твердого сплава.Остановки в падении температуры могут наблюдаться и на кривой охлаждения уже твердого металла, указываю на переходы металла из одной аллотропной формы в другую. | 62.Диаграмма плавкости однокомпонентной системы на примере воды. | 63.Основные принципы построения диаграммы плавкости бинарных систем.Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.Диаграммы плавкости – частный вид диаграмм состояния.Курнаков сформулировал 2 принципа, устанавливающих связь геометрических образов диаграммы с химическим состоянием системы.1. Принцип непрерывности.При непрерывном изменении температуры, давления, концентрации свойства отдельных фаз системы меняются также непрерывно. Свойства системы в целом изменяются непрерывно лишь до тех пор, пока не изменится число или характер ее фаз. При появлении новых или исчезновении имеющихся фаз свойства системы в целом меняются скачком.2. Принцип соответствия.Каждой совокупности фаз, находящихся в равновесии в данной системе, отвечает на диаграмме определенный геометрический образ.В двухкомпонентной системе одной фазе на диаграмме соответствует участок плоскости, кристаллизации твердой фазы- кривая начала кристаллизации, равновесию между тремя фазами - точка пересечения кривых, и т.д. |
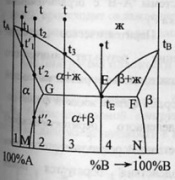 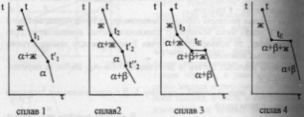 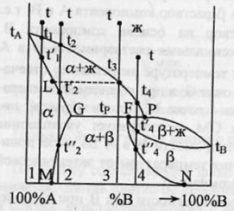 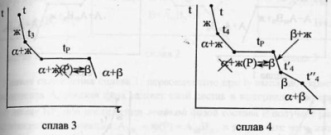 65. Диаграмма плавкости бинарной системы с ограниченными твердыми растворами. Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.Диаграммы плавкости – частный вид диаграмм состояния.Для данных систем характерны полная взаимная растворимость компонентов в жидком состоянии и ограниченная - в твердом. Если твердые растворы образуют эвтектику, то точка нонвариантного равновесия Е лежит ниже t плавления чистых компонентов,если же перитектику,то нонвариантная точка P лежит между t плавления чистых компонентов.Пример. Cu-Ag,Pb-Sn; Hg-Cd.Рассмотрим первый случай.Система А-В с ограничен.тв.р-рами- с эвтектикой. В системе имеется 2 твердых раствора: α - р-р компонентов В в А и β- р-р компонента А в В.Max растворимость В в А при t эвтектики tЕ отвечает точке G, а при комнат.t – точке M. Линия GM характеризует уменьшение растворимости В в А по мере понижения t от эвтектич-й до комнат-й.Линия FN-снижение растворимости А в В при понижении t от tЕ до комнат-й.Кривые охлаждения 4 сплавов:1,2,3,4.На кривой охлаждения сплава 1 имееются 2 перегиба,отвечающих началу и концу выделения кристаллов тв.р-ра α.На кривой охлаждения сплава 2 дополнительно наблюдается слабо выраженный перегиб при t”2,отвечающий частичному распаду в тв.состоянии кристаллов α с выделением кристаллов тв.р-ра β. Кривая охлаждения сплава 3: при t3 из жид.фазы выделяются кристаллы тв.р-ра α,жид.фаза при понижении от t3 до tЕ меняет свой состав по линии t3Е,т.е.обогащается компонентом В.Как только жид.фаза достигнет состава Е,начинается кристаллизация эвтектики-мех.смеси 2 тв.фаз-тв.р-ра α состава G и тв.р-ра β состава F,на кривой охлаждения наблюдается площадка.Сплав 4 точно отвечает эвтектич.составу,кривая охлаждения его подобна кривой охлаждения чистого компонента. Система А-В с ограничен.тв.р-рами- с перитектикой(т.Р). Перитектическое превращение-результат химического взаимодействия ранее выпавшей тв.фазы с жид.фазой определенного (перитектического) состава.В результате этого взаимодействия образуется новая тв.фаза.Кривые охлаждения 4 сплавов-1,2,3,4. Кривые охлаждения 1 и 2 полностью похожи на эвтектические.Кривая охлаждения 3:в интервале t от t до t3 идет охлаждение жид.фазы,и t изменяется монотонно.При t3 из жид.фазы выпадают кристаллы тв.р-ра α, на кривой охлаждения-перегиб.В интервале t3-tP жид.фаза меняет свой состав по линии t3Е,а тв.фаза по линии LG.Как только жид.фаза достигнет состава P(перитектического),получает развитие перитектическая реакция.В результате этой реакции исчезает жид.фаза и ниже tP наблюдается смесь 2 тв.фаз-тв.р-ров α и β.На кривой охлаждения наблюдается площадка,т.к. имеет место нонвариантное превращение:С=К-Ф+1=2-3+1=0.Для сплава 4 при tP в результате перитектической реакции исчезает тв.р-ра α.В интервале tP –t’4 из жид.фазы выпадают кристаллы тв.р-ра β. От t’4 до t”4 происходит охлпждение тв.фазы β, а при t”4 тв.р-р β частично распадается-с выделением кристаллов тв.р-ра α. 65. Диаграмма плавкости бинарной системы с ограниченными твердыми растворами. Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.Диаграммы плавкости – частный вид диаграмм состояния.Для данных систем характерны полная взаимная растворимость компонентов в жидком состоянии и ограниченная - в твердом. Если твердые растворы образуют эвтектику, то точка нонвариантного равновесия Е лежит ниже t плавления чистых компонентов,если же перитектику,то нонвариантная точка P лежит между t плавления чистых компонентов.Пример. Cu-Ag,Pb-Sn; Hg-Cd.Рассмотрим первый случай.Система А-В с ограничен.тв.р-рами- с эвтектикой. В системе имеется 2 твердых раствора: α - р-р компонентов В в А и β- р-р компонента А в В.Max растворимость В в А при t эвтектики tЕ отвечает точке G, а при комнат.t – точке M. Линия GM характеризует уменьшение растворимости В в А по мере понижения t от эвтектич-й до комнат-й.Линия FN-снижение растворимости А в В при понижении t от tЕ до комнат-й.Кривые охлаждения 4 сплавов:1,2,3,4.На кривой охлаждения сплава 1 имееются 2 перегиба,отвечающих началу и концу выделения кристаллов тв.р-ра α.На кривой охлаждения сплава 2 дополнительно наблюдается слабо выраженный перегиб при t”2,отвечающий частичному распаду в тв.состоянии кристаллов α с выделением кристаллов тв.р-ра β. Кривая охлаждения сплава 3: при t3 из жид.фазы выделяются кристаллы тв.р-ра α,жид.фаза при понижении от t3 до tЕ меняет свой состав по линии t3Е,т.е.обогащается компонентом В.Как только жид.фаза достигнет состава Е,начинается кристаллизация эвтектики-мех.смеси 2 тв.фаз-тв.р-ра α состава G и тв.р-ра β состава F,на кривой охлаждения наблюдается площадка.Сплав 4 точно отвечает эвтектич.составу,кривая охлаждения его подобна кривой охлаждения чистого компонента. Система А-В с ограничен.тв.р-рами- с перитектикой(т.Р). Перитектическое превращение-результат химического взаимодействия ранее выпавшей тв.фазы с жид.фазой определенного (перитектического) состава.В результате этого взаимодействия образуется новая тв.фаза.Кривые охлаждения 4 сплавов-1,2,3,4. Кривые охлаждения 1 и 2 полностью похожи на эвтектические.Кривая охлаждения 3:в интервале t от t до t3 идет охлаждение жид.фазы,и t изменяется монотонно.При t3 из жид.фазы выпадают кристаллы тв.р-ра α, на кривой охлаждения-перегиб.В интервале t3-tP жид.фаза меняет свой состав по линии t3Е,а тв.фаза по линии LG.Как только жид.фаза достигнет состава P(перитектического),получает развитие перитектическая реакция.В результате этой реакции исчезает жид.фаза и ниже tP наблюдается смесь 2 тв.фаз-тв.р-ров α и β.На кривой охлаждения наблюдается площадка,т.к. имеет место нонвариантное превращение:С=К-Ф+1=2-3+1=0.Для сплава 4 при tP в результате перитектической реакции исчезает тв.р-ра α.В интервале tP –t’4 из жид.фазы выпадают кристаллы тв.р-ра β. От t’4 до t”4 происходит охлпждение тв.фазы β, а при t”4 тв.р-р β частично распадается-с выделением кристаллов тв.р-ра α. | 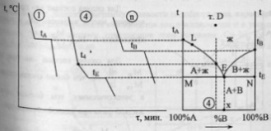 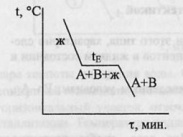 64.Эвтектическая диаграмма плавкости (без образования твердых растворов).Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.Диаграммы плавкости – частный вид диаграмм состояния.Для систем, дающих диаграмму плавкости такого типа, характерна полная взаимная растворимость компонентов в жидком состоянии и нерастворимость – в твердом. Пример. Системы Pb-Ag, Cd-Bi, Tl-Au, KCl-LiCl и т.д.Чтобы построить диаграмму плавкости системы А-В, необходимо приготовить несколько сплавов – от 100% А, через каждые 64.Эвтектическая диаграмма плавкости (без образования твердых растворов).Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.Диаграммы плавкости – частный вид диаграмм состояния.Для систем, дающих диаграмму плавкости такого типа, характерна полная взаимная растворимость компонентов в жидком состоянии и нерастворимость – в твердом. Пример. Системы Pb-Ag, Cd-Bi, Tl-Au, KCl-LiCl и т.д.Чтобы построить диаграмму плавкости системы А-В, необходимо приготовить несколько сплавов – от 100% А, через каждые | |
