Ответы на Экзаменационные вопросы - 2005 год. 1. 1 Квантовомеханическая модель атома. Характеристики энергетического состояния электрона системой квантовых чисел. Основное и возбужденное состояние атома
 Скачать 0.82 Mb. Скачать 0.82 Mb.
|
|
Изоморфизм - свойство химически и геометрически близких атомов, ионов и их сочетаний замещать друг друга в кристаллической решетке, образуя кристаллы переменного состава; т.е. изоморфизм – это изменение химического состава минерала при сохранении его кристаллической структуры. Изоморфны, например, кристаллы дигидрофосфатов и арсенатов щелочных металлов: KH2PO4 (KDP), NH4H2PO4 (ADP), RbH2PO4, CsH2PO4, KH2AsO4, PbH2AsO4 и др. Все они при комнатной температуре кристаллизуются в одном классе с сходной внешней формой и близкими параметрами решетки, все имеют сегнето- и параэлектрические фазы, Этот изоморфный ряд интересен тем, что здесь ни замена катиона (например, K+ на NH4+), ни замена аниона (например, PO4- на AsO4-) не меняет морфологию кристалла. Ураты - соли мочевой кислоты, накапливаются в крови при некоторых болезнях, например при подагре, нефритах, лейкемиях; могут откладываться в тканях. Оксалаты (от греч. oxalís — щавель), кислые и средние соли щавелевой кислоты, например HOOC—COOK, NaOOC—COONa. Карбонаты - соли и эфиры угольной кислоты Н2СО3. Различают нормальные (средние) соли с анионом CO32- (напр., К2СО3) и кислые (гидрокарбонаты) с анионом НСО3- (напр., КНСО3). | ||
| | ||
| | ||
| № 7.3 Лигандообменные равновесия и процессы. Конкуренция за лиганд или за комплексообразователь: изолированное и совмещенное лигандообменные равновесия. Константа нестойкости комплекса. Инертные и лабильные комплексы. Представления о строении металлоферментов и других биокомплексных соединений (гемоглобин, цитохромы, кобаламины). Физико-химические принципы транспорта кислорода гемоглобином. Металло-лигандный гомеостаз и причины его нарушения. Механизм токсического действия тяжелых металлов и мышьяка на основе теории жестких и мягких кислот и оснований (ЖМКО). Термодинамические принципы хелатотерапии. Механизм цито-токсического действия соединении платины. Если в системе несколько лигандов с одним ионом металла или несколько ионов металла с одним лигандом способных к образованию комплексных соединений, то наблюдаются конкурирующие процессы: в первом случае лигандообменное равновесие - конкуренция между лигандами за ион металла, во втором случае металлообменное равновесие - конкуренция между ионами металла за лиганд. Преобладающим будет процесс образования наиболее прочного комплекса. Нарушения металлолигандного гомеостаза вызывают нарушения процесса обмена веществ, ингибируют активность ферментов, разрушают важные метаболиты, такие как АТФ, клеточные мембраны, нарушают градиент концентрации ионов в клетках. Поэтому создаются искусственные системы защиты. Должное место в этом методе занимает хелатотерапия (комплексонотерапия). Хелатотерапия – это выведение токсичных частиц из организма, основанное на хелатировании их комплексонатами s–элементов. С практическими целями часто пользуются величиной, обратной константе устойчивости - константой нестойкости Кн: Чем меньше константа нестойкости, тем прочнее комплекс. Константы нестойкости позволяют прогнозировать направление процессов комплексообразования. Основные термодинамические принципы хелатотерапии можно сформулировать в двух положениях. 1. Детоксикант (Lg): должен эффективно связывать ионы токсиканты (Мт, Lт), вновь образующиеся соединения (МтLg),должны быть прочнее, чем те, которые существовали в организме. Ку(МтLg) > Ку (МбLт), Ку(МбLтLg) > Ку (МбLт), где Ку – константа устойчивости; 2. Детоксикант не должен разрушать жизненно необходимые комплексные соединения (МбLб); соединения, которые могут образовываться при взаимодействии детоксиканта и ионов биометаллов (MбLq), должны быть менее прочными, чем существующие в организме. Гемоглобин - дыхательный пигмент, придающий крови красный цвет. Гемоглобин состоит из белка и железопорфирина и переносит кислород от органов дыхания к тканям тела и углекислый газ от них к дыхательным органам. Цитохромы - сложные белки (гемопротеиды), осуществляющие в живых клетках ступенчатый перенос электронов и/или водорода от окисляемых органических веществ к молекулярному кислороду. При этом образуется богатое энергией соединение АТФ. Кобаламины - природные биологически активные кобальторганические соединения. Структурной основой К. является корриновое кольцо, состоящее из 4 пиррольных ядер, у которых атомы азота связаны с центральным атомом кобальта. Физико-химические принципы транспорта кислорода гемоглобином - Атом (Fe (II)) (один из компонентов гемоглобина) способен образовывать 6 координационных связей. Из них четыре используются для закрепления самого атома Fe(II) в геме, пятая связь - для связывания гема с белковой субъединицей, а с помощью шестой связи происходит связывание молекулы О2 или СО2. Реакция, лежащая в основе переноса кислорода гемоглобином. HHb+ + O2 <=> HbO2 + H+ Токсичность солей тяжелых металлов. Хорошо известно, что загрязнение окружающей среды соединениями токсичных элементов — тяжелых металлов: ртути, свинца, кадмия, хрома, никеля — может приводить к отравлениям. Ядовитость или токсичность таких соединений во многих случаях объясняется взаимодействием катионов тяжелых металлов Мт с бионеорганическими комплексами. Реакция, описывающая это взаимодействие, может быть записана в виде Здесь MбL — комплекс иона биогенного металла Мб (Fe, Zn, Сu, Со) с биоорганическим лигандом L (например, порфирином); Мт — ион тяжелого металла. | № 7.4 Редокс-равновесия и процессы. Механизм возникновения электродного и редокс-потенциалов. Уравнения Нернста - Петерса. Сравнительная сила окислителей и восстановителей. Прогнозирование направления редокс-процессов по величинам редокс-потенциалов. Влияние лигандообменного окружения центрального атома на величину редокс - потенциала. Физико-химические принципы транспорта электронов в электронотранспортной цепи митохондрий. Общие представления о механизме действия редокс-буферных систем. Токсическое действие окислителей (нитраты; нитриты, оксиды азота). Обезвреживание кислорода, пероксида водорода и супероксид-иона. Применение редокс-реакций для детоксикации. Окислителями называются вещества или частицы, принимающие электроны от других веществ или частиц — восстановителей. Окисленную и восстановленную форму одного и того же вещества называют редокс-системой (редокс-парой). Для протекания окислительно-восстановительной реакции (редокс-реакции) необходимо наличие как минимум двух веществ, относящихся к разным редокс-системам. В общем виде реакции такого типа можно представить уравнением: Потенциал, возникающий на границе раздела металл — раствор соли этого металла, называют электродным. Его величина φ определяется уравнением Нернста: Количественной характеристикой редокс-систем, в которых и окислитель, и восстановитель находятся в растворенном состоянии, является редокс-потенциал. Для его вычисления используется следующая форма уравнения Нернста: Чем больше величина редокс-потенциала, тем сильнее окислитель и слабее сопряженный ему восстановитель. Сильный окислитель вступает в реакции с большим числом восстановителей, чем слабый, и/или вызывает более глубокое окисление восстановителей. Токсическое действие оксидов азота связано с их высокой окислительно-восстановительной способностью. Токсическое действие нитратов связано с восстановлением их до нитритов, аммиака, гидроксиламина под влиянием микрофлоры пищеварительного тракта и тканевых ферментов. Если в организм человека поступают высокие дозы нитратов, через 4–6 ч появляются тошнота, одышка, посинение кожных покровов, диарея. В зависимости от дозы нитратов, поступающих в организм, отмечают патоморфологические изменения разной степени: некроз или зернистая дистрофия в сильной степени в печени, почках, миокарде. Биологическое окисление протекает по сложным механизмам при участии большого числа ферментов. В митохондриях окисление происходит в результате переноса электронов от органических субстратов- интермедиатов на элементный кислород, который при этом восстанавливается до воды: 1/2O2 + 2H+ +2e- = H2O В качестве переносчиков электронов в дыхательную цепь митохондрий входят различные белки, содержащие, разнообразные функциональные группы, которые предназначены для переноса электронов. По мере продвижения по цепи от одного интермедиата к другому электроны теряют свободную энергию. На каждую пару электронов, переданных по дыхательной цепи кислороду, синтезируются три молекулы АТФ. Значительная часть свободной энергии, выделяющейся при переносе одной пары электронов, запасается в молекулах АТФ. | № 7.5 Совмещенные равновесия и конкурирующие процессы разных типов. Константа совмещенного равновесия. Совмещенные равновесия и конкурирующие процессы разных типов, протекающие в организме в норме, при патологии и при корреции патологических состояний. Одним из видов совмещения разнотипных равновесий является протолитическое — гетерогенное — равновесие. В лабораторной практике с ним встречаются, изучая растворимость осадков при разных значениях рН. Растворимость труднорастворимых солей, образованных анионами слабых кислот, значительно зависит от рН раствора, т.е. от кислотности. Объясняется это возникающими конкурирующими процессами за анион слабой кислоты между ионом металла и протоном: В этом совмещенном равновесии объектом конкуренции является анион слабой кислоты (В"), а конкурирующими частицами - ион металла (М+) и протон (Н+). Выигрывает конкуренцию ион металла — образуется осадок, выигрывает протон — осадок растворяется. Преобладание того или иного процесса определяется общей константой совмещенного равновесия, которая определяется через частные константы равновесия, чаще всего диссоциативного типа (константы кислотности для протолитических равновесий, константы растворимости для гетерогенных, константы нестойкости для лиган-дообменных). Общая константа равновесия равна отношению произведения частных констант диссоциативного типа веществ, стоящих в левой части уравнения, к произведению частных констант диссоциативного типа веществ, стоящих в правой части уравнения. При наличии стехиометрических коэффициентов, отличных от 1, их необходимо учитывать, возводя частные константы равновесия в соответствующие степени. |
| | ||
| | ||
| № 8.1 Адсорбционные равновесия и процессы на подвижной границе раздела фаз. Поверхностная энергия Гиббса и поверхностное натяжение. Адсорбция. Уравнение Гиббса. Поверхностно-активные и поверхностно-неактивные вещества. Изменение поверхностной активности в гомологических рядах (правило Траубе). Изотерма адсорбции. Ориентация молекул в поверхностном слое и структура биомембран. Адсорбция - поглощение к.-л. вещества из газообразной среды или раствора поверхностным слоем жидкости или твёрдого тела. Например, если поместить в водный раствор уксусной кислоты кусочек угля, то произойдёт А. — количество кислоты в растворе уменьшится, молекулы кислоты сконцентрируются на поверхности угля. Адсорбция и абсорбция — поглощение в объёме тела, объединяются общим термином сорбция. Явление А. тесно связано с особыми свойствами вещества в поверхностном слое. Например, молекулы, лежащие на поверхности раздела фаз жидкость — пар, втягиваются внутрь жидкости, т. к. испытывают большее притяжение со стороны молекул, находящихся в объёме жидкости, чем со стороны молекул пара, концентрация которых во много раз меньше концентрации жидкости. Это внутреннее притяжение заставляет поверхность сокращаться и количественно характеризуется поверхностным натяжением. По той же причине молекулы какого-либо другого вещества, оказавшиеся вблизи поверхности, притянутся к ней и произойдёт А. После А. внутреннее притяжение частично компенсируется притяжением со стороны адсорбционного слоя и поверхностное натяжение уменьшается. Гиббс вывел формулу, связывающую значение А. с изменением поверхностного натяжения. Те вещества, А. которых сильно уменьшает поверхностное натяжение, принято называть поверхностно-активными (дифильные и ассиметричные, одноатомные спирты, одноосновные карбоновые кислоты, амины, эфиры). Изотерма адсорбции - зависимость адсорбции от равновесной концентрации растворенного вещества при постоянной температуре. П 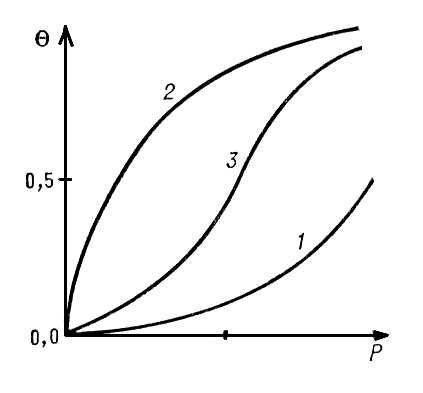 оверхностно-неактивные вещ-ва (адсорбирующие отрицательно) либо не изменяют коэффициент поверхностного натяжения водной фазы, либо незначительно его увеличивают.(большинство неорганический вещ-в: кислоты, щелочи, соли) Мера адсорбции-Г(гамма)ед. изм.-моль\м2. оверхностно-неактивные вещ-ва (адсорбирующие отрицательно) либо не изменяют коэффициент поверхностного натяжения водной фазы, либо незначительно его увеличивают.(большинство неорганический вещ-в: кислоты, щелочи, соли) Мера адсорбции-Г(гамма)ед. изм.-моль\м2.Уравнение Гиббса: Г=-Сср/RT Х ср.ро/ср.С При малых концентрациях пав углеводородные радикалы лежат на поверхности полярной жидкости, а полярные группировки погружены в нее. С увеличением конц. Пав в растворе число молекул, находящихся в поверхностном слое, возрастает. Это приводит в пределе к образованию на граничной поверхности насыщенного мономолекулярного адсорбционного слоя, а котором молекулы пав предельно ориентированы.-это слой Ленгмюра. Биологическая мембрана (Даниэли и Давсон): основной элемент мембранных структур клетки явл. Биомолекулярный слой из молекул липидов, полярные(взаимодействуют с белками) группировки направлены наружу, а неполярные углеводородные радикалы – внутрь. Белки образуют симметричные и ассиметричные распределия белков в клеточных мембранах. Среди мембранных есть способные взаимодействовать с гидрофобными радикалами и проникать вглубь мембраны(интегральные белки) наиболее принятая – мозаичная модель.поры- ионные каналы(облад. Избирательной проницаемостью) Правило Дюкло-Траубе: с ростом длины углеводородного радикала адсорбция уменьшается. Т.е. с ростом длины углеводородной цепочки растет растворимость пав в неполярных растворителях. | № 8.2 Адсорбционные равновесия на неподвижных границах раздела фаз. Физическая адсорбция и хемосорбция. Адсорбция из растворов. Уравнение Ленгмюра. Зависимость величины адсорбции от различных факторов. Правило выравнивания полярностей. Избирательная адсорбция. Значение адсорбционных процессов для жизнедеятельности. Физико-химические основы адсорбционной терапии, гемосорбции, применения в медицине ионитов. Вещество, на поверхности которого происходит Адсорбция, называется адсорбентом, а поглощаемое из объёмной фазы — адсорбатом. В зависимости от характера взаимодействия между молекулой адсорбата и адсорбентом А. принято подразделять на физическую А. и хемосорбцию. Менее прочная физическая А. не сопровождается существенными изменениями молекул адсорбата. Она обусловлена силами межмолекулярного взаимодействия, которые связывают молекулы в жидкостях и некоторых кристаллах и проявляются в поведении сильно сжатых газов. При хемосорбции молекулы адсорбата и адсорбента образуют химические соединения. Часто А. обусловлена и физическими и химическими силами, поэтому не существует чёткой границы между физикой А. и хемосорбцией. Адсорбированные молекулы рано или поздно покидают поверхность молекулы — десорбируются. Время, в течение которого молекула находится на поверхности, называется временем Адсорбции Времена А. могут колебаться в очень широких пределах. Скоростью А. (соответственно скоростью десорбции) называется количество молекул, адсорбирующихся (или десорбирующихся) за единицу времени, оба значения величин относят к единице поверхности или массы адсорбента. Скорость хемосорбции, как и скорость любого химического процесса, чаще всего увеличивается с повышением температуры. Если скорости А. и десорбции равны друг другу, то говорят, что установилось адсорбционное равновесие. В состоянии равновесия количество адсорбированных молекул остаётся постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и др.). |
