1. Аналитическая часть
 Скачать 1.26 Mb. Скачать 1.26 Mb.
|
2. Технологическая часть2.1 Технология деструкции резины концентрированной серной кислотойКак было показано в аналитическом обзоре, в настоящее время нет экологически чистой технологии утилизации отработанных резинотехнических изделий, в частности автомобильных шин. Наши исследования позволили теоретически обосновать и подтвердить в лабораторных экспериментах принципиально новую технологию утилизации отработанных резинотехнических изделий, основанную на процессе деструкции резины под действием концентрированной серной кислоты. Последняя вызывает разрыв связей C-C, C-H, C-S-C, что в итоге приводит к образованию сыпучей углеродистой массы, т.е. имеет место модификация исходного материала с разрушением углеводородных цепей. При сжигании такого материала исключается возможность образования полициклических углеводородов (ПАУ), полихлорированных дибензодиоксинов (ПХДД) и полихлорированных дибензофуранов (ПХДФ), что имеет место при сжигании отработанных шин. 2.2 Теоретические основы химической деструкции резины под действием концентрированной серной кислотыОкислительное действие концентрированной серной кислоты хорошо известно, в том числе и на органические вещества (в частности деструкция целлюлозы и клетчатки, т.е. высокомолекулярных соединений). Нами были проведены термодинамические расчеты для реакций взаимодействия предельных и ароматических углеводородов и некоторых их замещенных с концентрированной серной кислотой. Расчеты сделаны по первому приближению Улиха. 2.2.1 Термодинамика деструкции предельных углеводородовВеличины изобарно-изотермических потенциалов (ΔGт) были рассчитаны для следующих реакций деструкции предельных углеводородов: С2Н6 + 3H2SO4 = 2С + 3SO2 + 6Н2О (1) С3Н8 + 4H2SO4 = 3С + 4SO2 + 8Н2О (2) С4Н10 + 5H2SO4 = 4С + 5SO2 + 10Н2О (3) С5Н12 + 6H2SO4 = 5С + 6SO2 + 12Н2О (4) С6Н14(ж) + 7H2SO4 = 6С + 7SO2 + 14Н2О (5) С7Н16(ж) + 8H2SO4 = 7С + 8SO2 + 14Н2О (6) или в общем виде: СnН2n+2 + (n+1) H2SO4 = nС + (n+1) SO2 + (2n+2) Н2О (7) Полученные результаты приведены в таблице 5 и на рисунке 1. Таблица 5 - Значение величины ΔG при Т=373 К для реакций (1-6)
Из таблицы 5 и рисунка 1 видно, что для реакций (1-6) величина ΔG<0, т.е. все они термодинамически возможны. Поскольку с повышением мольной массы углеводорода наблюдается последовательное уменьшение изобарно-изотермического потенциала, можно считать, что реакции деструкции высокомолекулярных углеводородов, протекающие по уравнению (7) также термодинамически возможны, что давало основания для проведения исследований по кинетике процесса деструкции высокомолекулярных компонентов резины. 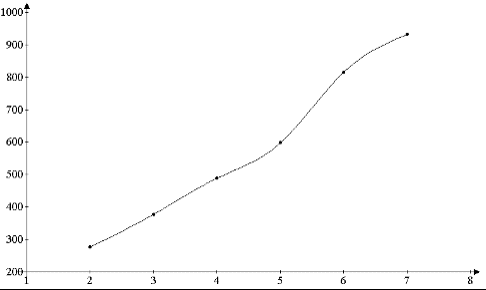 Рисунок 1 - Изменение ΔG в зависимости от числа атомов углерода в молекулах 2.2.2 Термодинамика деструкции ароматических углеводородовСреди каучуков, используемых для производства резины, используется и бутадиен-стирольный каучук, имеющий в своей цепи бензольное кольцо. Известно [3], что при сжигании полимерных материалов, в частности твердых бытовых отходов, образуются чрезвычайно ядовитые соединения ароматического типа - бензпирены, 3,12 - диметилбензантрацен и другие полициклические ароматические соединения (ПАУ), а также различные диоксины - полихлорированные дибензо-n-диоксины (ПХДД) и полихлордибензофураны (ПХДФ). Все эти соединения являются приоритетными в списках Европейского союза и России. Поэтому было целесообразно рассчитать термодинамическую возможность деструкции ароматических углеводородов. Расчеты были сделаны для следующих реакций: С6Н6 + 3H2SO4 = 6С + 3SO2 + 6Н2О (8) С6Н5СН3 + 4H2SO4 = 7С + 4SO2 + 8Н2О (9) С6Н4(СН3)2 + 5H2SO4 = 8С + 5SO2 + 10Н2О (10) С10Н8 + 4H2SO4 = 10С + 4SO2 + 8Н2О (11) С14Н10 + 5H2SO4 = 14С + 5SO2 + 10Н2О (12) Полученные результаты приведены в таблице 6. Таблица 6 - Значение величин ΔG при Т=373 К для реакций (8-12)
Как видно из таблицы 6, для всех ароматических углеводородов, использованных в расчетах, величины ΔG<0 при Т=373 К. В ряду бензол - его замещенные величина ΔG последовательно уменьшается. То же самое наблюдается по мере увеличения цикличности углеводородов (бензол - антрацен). Это позволяет сделать заключение, что полициклические углеводороды, о которых было сказано выше, также термодинамически могут подвергаться деструкции под действием концентрированной серной кислоты. 2.2.3 Термодинамика деструкции некоторых замещенных углеводородовПри изготовлении технических резин используют не только чисто углеводородные каучуки, но также их замещенные, в частности хлоропреновый и винилпиридиновый каучуки (последний для изготовления протекторов шин). Другими компонентами шин являются стабилизаторы (в частности фенил-β-нафтиламин) и активаторы - соли жирных кислот. Кроме того, при изготовлении корда используют нити из полимерных материалов - полиамидные, полиакрилонитрильные и другие волокна. Поэтому было целесообразно рассмотреть термодинамику деструкции замещенных алкил- и арилуглеводородов. Были рассмотрены следующие реакции: 2C5H5N + 5H2SO4 = 10C + N2 + 5SO2 + 10H2O (13) 2C6H5NН2 + 7H2SO4 = 12C + N2 + 7SO2 + 14H2O (14)6H5ОН + 2H2SO4 = 6C + 2SO2 + 5H2O (15)6H5Cl + 2H2SO4 = 6C + HCl + 2SO2 + 4H2O (16)2H5Сl + 2H2SO4 = 2C + HCl + 2SO2 + 4H2O (17) NH2CH2COOH + H2SO4 = 4C + N2 + SO2 + 6H2O (18) Полученные результаты приведены в таблице 7. Таблица 7 - Значения величин ΔG при Т=373 К для реакций (13-18)
Как видно из таблицы 7, азот- и хлорпроизводные алкил- и арилуглеводородов термодинамически неустойчивы по отношению к действию концентрированной серной кислоты при t=100˚С и эта неустойчивость должна возрастать с увеличением температуры, т.к. во всех рассматриваемых случаях величины ΔS˚ положительны. Проведенные расчеты показывают, что при действии концентрированной серной кислоты на технические резины деструкции должны подвергаться все ее органические компоненты, что делало целесообразным проведение соответствующих экспериментов. |
