Билеты Микробиология. 1. Бактериофаги (фаги)
 Скачать 0.53 Mb. Скачать 0.53 Mb.
|
|
Генные рекомбинации Бактериальный геном состоит из генетических элементов, способных к самостоятельной репликации (воспроизведению), т.е репликонов. Репликонами являются: -Бактериальная хромосома -Плазмиды. Наследственная информация хранится у бактерий в форме последовательности нуклеотидов ДНК, которые определяют последовательность аминокислот в белке. Каждому белку соответствует свой ген,т.е дискретный участок на ДНК, отличающийся числом и специфичностью последовательности нуклеотидов. Бактериальная хромосома представлена одной двуцепочечной молекулой ДНК кольцевой формы. Она формирует компактный нуклеоид бактериальной клетки и имеет гаплоидный набор генов. Бактериальная хромосома кодирует жизненно важные для бакт.клетки функции. Плазмиды представляют собой двуцепочечные молекулы ДНК. Они кодируют не основные для жизнедеятельности клетки функции, но придающие бактерии преимущества при попадании в неблагоприятные условия существования. (Такие фенотипические признаки, как устойчивость к антибиотикам, продукцию факторов патогенности, расщепление сложных орг.в-в и тд). Репликацию плазмидной ДНК осуществляет тот же набор ферментов, что и репликацию бактериальной хромосомы. Изменения бактериального генома, а, следовательно, и свойств бактерий могут происходить в результате мутаций и рекомбинаций. Генетическая рекомбинация – это взаимодействие между двумя геномами, т.е. между двумя ДНК, обладающими различными генотипами, которое приводит к образованию рекомбинантной ДНК, формированию дочернего генома, сочетающего гены обоих родителей. Особенности рекомбинации у бактерий определяют отсутствие полового размножения и гаплоидный набор генов. В процессе рекомбинации бактерии условно делятся на клетки-доноры, которые передают генетический материал, и клетки-реципиенты, которые воспринимают его. В клетку-реципиент проникает только часть хромосомы клетки-донора, что приводит к формированию неполной зиготы – мерозиготы. В результате рекомбинации в мерозиготе образуется только один рекомбинант, генотип которого представлен в основном генотипом реципиента, с включенным в него фрагментом хромосомы донора. Реципроктные (взаимные) рекомбинанты не образуются. По молекулярному механизму рекомбинация у бактерий делится на: 1. Гомологичную 2. Сайт-специфическую 3. Незаконную. Гомологичная рекомбинация. В процессе разрыва и воссоединения ДНК происходит обмен между участками ДНК, обладающими высокой степенью гомологии. Гомологичная рекомбинация происходит через образование промежуточного соединения, крестообразной структуры Холидея или полухиазмы. В полухиазме осуществляется комплементарное спаривание между одноцепочечными участками , принадлежащими к разным родительским молекулам ДНК. Процесс гомологичной рекомбинации находится под контролем генов, объединенных в REC – систему, состоящих из генов recA,B,C,D. Продукты этих генов производят расплетание нитей ДНК и их переориентацию с образованием структуры Холидея, а также разрезают структуру Холидея для завершения процесса рекомбинации. Сайт-специфическая рекомбинация. Происходит в определенных участках генома и не требует высокой степени гомологии ДНК. Не зависит от функционирования генов recABCD. Примером данного типа рекомбинации является встраивание плазмиды в хромосому бактерий, которое происходит между идентичными вставочными последовательностями (Встав.последовательности ,IS – элементы – участки ДНК,способные как целое перемещаться из одного участка репликона в другой, а так же между репликонами.) хромосомы и плазмиды, интеграция ДНК фага в хромосому E.coli. Сайт-специфическая рекомбинация, происходящая в пределах одного репликона, участвует также в переключении активности генов. Например, у сальмонелл последствием этого процесса является фазовые вариации жгутикового H-антигена. Незаконная (репликативная) рекомбинация. Впервые она была описана Л.Б. Борисовым в 1965 г. между неродственными коли-фагами, лизирующими энтеропатогенные эшерихии серогрупп 0III и 026. Не зависит от функционирования генов recABCD. Примером ее является транспозиция подвижных генетических элементов по репликону или между репликонами, при этом транспозиция подвижного генетического элемента сопровождается репликацией ДНК. Рекомбинация у бактерий является конечным этапом передачи генетического материала, которая осуществляется тремя механизмами: 1.Конъюгацией (при контакте бактерий, одна из которых несет конъюгативную плазмиду) 2. Трансдукцией (при помощи бактериофага) 3. Трансформацией (при помощи высокополимеризованной ДНК). А. Трансформация – непосредственная передача генетического материала от донорской к реципиентной клетке. В бактериальной популяции в результате аутолиза клеток всегда присутствует внеклеточная ДНК. Некоторые клетки обладают соответствующими рецепторами для ее адсорбции и ферментами для ее транспорта внутрь своей клетки и последующей рекомбинации экзогенной ДНК с ДНК бактериальной хромосомы. Такие клетки называются компетентными. Б. Трансдукция – передача генетического материала от донорской к реципиентной клетке с помощью дефектных бактериофагов. 1. При неспецифической (общей) трансдукции может передаваться любой, случайный признак, который присутствует у всего клона, образованного рекомбинантной клеткой. 2. При абортивной трансдукции также передается любой, случайный признак, но он скоро теряется, так как при каждом делении клеток экзогенная ДНК не рекомбинирует с бактериальной хромосомой, как в случае с общей трансдукцией, а остается в цитоплазме и переходит только в одну из двух разделившихся клеток. 3. При специфической трансдукции каждый бактериофаг передает только ему присущий признак, который, как и в случае с общей трансдукцией, присутствует у всего клона, образованного рекомбинантной клеткой. В. Конъюгация – передача генетического материала от донорской к реципиентной клетке с помощью конъюгационных пилей. 1. Если конъюгация обусловлена плазмидой, находящейся в автономном состоянии, то донорской клетке передается сама эта плазмида, в том числе несущая в своем составе или другую, неконъюгационную, плазмиду или участок бактериальной хромосомы. 2. Если конъюгация обусловлена плазмидой, находящейся в интегрированном состоянии, то донорской клетке передается не эта плазмида, а участок бактериальной хромосомы. Г. Лизогенизация по определению является видом рекомбинационной изменчивости у бактерий, так как при ней в геном реципиентной клетки внедряется экзогенный генетический материал – геном умеренного фага . Изменения генома при этом виде рекомбинационной изменчивости не сопровождаются фенотипическими изменениями. Д. Фаговая конверсия – отличается от лизогенизации лишь тем, что фенотип донорской клетки изменяется . 2. Местный иммунитет (колонизационная резистентность) — это сложный комплекс защитных приспособлений различной природы, сформировавшийся в процессе эволюционного развития и обеспечивающий защиту слизистых тех органов, которые непосредственно сообщаются с внешней средой. Основная его функция — сохранение гомеостаза внутренней среды макроорганизма, т.е. он является первым барьером на пути микроорганизма и любого антигена.Местная защитная система слизистой оболочки полости рта слагается из факторов неспецифической защиты и специфических механизмов иммунитета; антител и Т-лимфоцитов, направленных против определенного антигена. Функции секрета ротовой полости и его состав. Ротовая жидкость (смешанная слюна) состоит из секрета, выделяемого слюнными железами, и кревикулярной (щелевой) десневой жидкости, которая составляет до 0,5% объема смешанной слюны. Этот процент может увеличиваться у пациентов с гингивитом. Защитные факторы слюны формируются в ходе активных процессов, протекающих местно.Смешанная слюна имеет целый комплекс функций: пищеварительную, защитную, трофическую, буферную. Слюна обладает бактериостатическими и бактерицидными свойствами благодаря наличию различных факторов: лизоцима, лактоферрина, пероксидазы и т.д. Защитные функции слюны определяются неспецифическими факторами и некоторыми показателями специфического иммунитета. Значение комплемента, калликреина и лейкоцитов в поддержании колонизационной резистентности ротовой полости. Комплемент представляет собой сложную многокомпонентную систему белков, включающую 9 фракций. В слюне в незначительных количествах находится лишь фракция СЗ системы комплемента. Остальные отсутствуют или выявляются в следовых количествах. Ее активация происходит лишь при наличии воспалительных процессов в слизистых оболочках. Весьма существенным компонентом слюны являются лейкоциты, которые в большом количестве поступают из десневых щелей и миндалин; причем 80% их состава представлены полиморфно-ядерными нейтрофилами и моноцитами. Часть их, попадая в ротовую полость, погибает, выделяя лизосомальные ферменты (лизоцим, пероксидазу и др.), способствующие обезвреживанию патогенной и условно-патогенной флоры. Оставшиеся лейкоциты в слизистой, обладая фагоцитарной активностью, создают мощный защитный барьер на пути развития инфекционного процесса. Незначительная фагоцитарная активность необходима и достаточна для того, чтобы захватить оставшиеся в ротовой полости пищевые частицы, попавшие вместе с ними микроорганизмы и тем самым очистить ротовую полость. Вместе с тем при возникновении в полости рта очагов воспаления местная активность лейкоцитов слюны может значительно возрастать, осуществляя таким образом защитное действие, направленное непосредственно против возбудителя. Так, известно, что фагоциты и система комплемента вовлекаются в защитные механизмы при таких заболеваниях, как пульпит, периодонтит. В слюне обнаружены тромбопластин, идентичный тканевому, антигепариновая субстанция, факторы, вхо-дящие в протромбиновый комплекс, фибриназа и др. Они играют важную роль в обеспечении местного гомеостаза, участвуя в развитии воспалительных, регенеративных процессов. При травмах, местных аллергических и воспалительных реакциях происходит поступление из сыворотки различных классов иммуноглобулинов, что поддерживает местный иммунитет. Специфические защитные факторы слюны и слизистой оболочки. Специфическим фактором антибактериальной и антивирусной защиты являются антитела — иммуноглобулины. Наиболее значимыми в специфическом иммунитете ротовой полости из известных пяти классов иммуноглобулинов (IgA, IgM, IgG, IgD, IgE) являются антитела класса А, причем в секреторной форме (slgA). Секреторный IgA в отличие от сывороточного IgA является димером. Он имеет две молекулы мономера IgA, соединенные J-цепью и гликопротеином SC (секреторный компонент), который обеспечивает устойчивость slgA к протеолитическим ферментам слюны, так как блокирует точки их приложения, экранируя уязвимые участки. Ведущую роль в образовании sIgA играют подcлизистые скопления лимфоидных клеток типа пейеровых бляшек, покрытых особым кубоидальным эпителием.Показано, что sIgA и SC присутствуют в слюне у детей с момента рождения. Концентрация sIgA отчетливо нарастает в раннем постнатальном периоде. К 6-7 дню жизни уровень sIgA в слюне увеличивается почти в 7 раз. Нормальный уровень синтеза sIgA является одним из условий достаточной устойчивости детей первых месяцев жизни к инфекциям, поражающим слизистую полости рта. К факторам, способным стимулировать синтез slgA, следует отнести лизоцим, витамин А, полноценное сбалансированное питание (витамины, микроэлементы и т.д.). IgG и IgA, проникающие из кровяного русла в секрет ротовой полости, быстро инактивируются под действием протеаз слюны и, таким образом, не способны выполнить свою защитную функцию, а антитела классов М, Е и D выявляются в незначительных количествах. Уровень IgE отражает аллергическую настроенность организма, повышаясь в основном при аллергических заболеваниях. Подавляющее большинство плазматических клеток слизистых оболочек и всех желез внешней секреции продуцируют IgA, так как в клетках слизистых преобладают Т-хелперы, которые получают информацию для В-лимфоцитов, предназначенных для синтеза slgA. SC-гликопротеин синтезируется в аппарате Гольджи эпителиальных клеток слизистой оболочки органов, сообщающихся с внешней средой. На базальной мембране этих клеток происходит связывание SC-компонента с двумя молекулами IgA. J-цепь инициирует процесс дальнейшей миграции, а гликопротеин способствует транспорту антител через слой эпителиальных клеток и последующей секреции slgA на поверхность слизистой. Секреторный иммуноглобулин А в секрете ротовой полости может находиться в свободной форме (связывает антиген Fab-фрагментом) или быть зафиксированным Секреторный IgA обладает следующими защитными функциями: 1) связывает антигены и вызывает их лизис; 2) подавляет адгезию бактерий и вирусов к клеткам СОПР, что препятствует возникновению воспалительного процесса, а также их адгезию к зубной эмали (т.е. оказывает противокариозное действие) 3)препятствует проникновению аллергенов через слизистую. slgA, связанные со слизистой, образуют с антигеном иммунные комплексы, которые при участии макрофагов элиминируются. Благодаря этим функциям sIgA являются ведущими факторами первой линии защиты организма от инфекционных и других чужеродных агентов. Антитела этого класса препятствуют возникновению патологических процессов на слизистой оболочке, не вызывая ее травматизации. Из защитных функций sIgA вытекает перспективность мeтодов создания местного пассивного иммунитета, в том числе, против кариеса. 3. Сибирская язва известна с глубокой древности. Возбудитель ее — Вacillis anthracis — впервые был описан Поллендером (1849) и Давеном (1850). Большой вклад в изучение сибирской язвы внесли Кох (1876), Пастер (1881) и Л. С. Ценковский (1883). Морфология и биологические свойства. Возбудитель сибирской язвы (В. anthracis) представляет собой крупную палочку с обрубленными концами (в среднем 1,5X8 мкм). В окрашенном препарате палочки располагаются одиночно, попарно или цепочкой (рис. 38, 1). 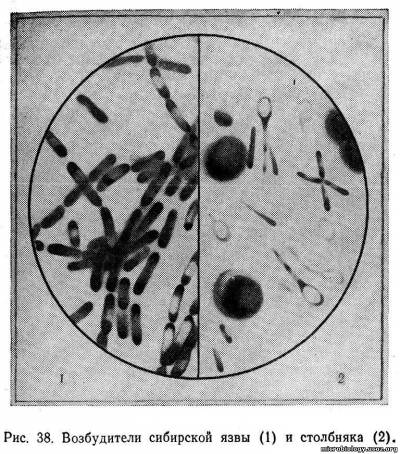 Грамположительны. Микроб неподвижен, окружен прозрачной капсулой, образование которой характерно для вирулентных штаммов. Капсула образуется как в организме больных людей и животных, так и при культивировании на специальных питательных средах. В неблагоприятных условиях внешней среды при доступе кислорода и температуре от 15 до 42°С микроб образует спору, которая располагается центрально и имеет овальную форму. Диаметр ее не превышает поперечника клетки. При попадании в благоприятную среду споры прорастают в течение нескольких часов. Возбудитель сибирской язвы относится к факультативным аэробам. Оптимальная температура роста 35— 37°С и рН 7,4—8,0. Микроб нетребователен к питательным средам, поэтому может расти даже на таких субстратах, как настой соломы, сырой и вареный картофель, экстракты злаков, гороха и др. На мясо-пептонном агаре рост настолько характерен, что имеет диагностическое значение. Через 24 ч роста появляются колонии: серебристо-серые, зернистые, диаметром 3—5 мм, с бахромчатыми краями и отходящими от них пучками нитей, напоминающими голову медузы или львиную гриву. Такой рост (R-форма) характерен для вирулентных штаммов. В старых культурах появляются гладкие S-формы колоний, авирулентные. В бульоне через 18—24 ч образуется осадок в виде хлопьев, а сам бульон остается прозрачным. Биохимическая активность невелика: разлагает глюкозу, мальтозу, сахарозу с образованием кислоты, молоко медленно свертывает и пептонизирует. Характерен рост в столбике желатина: в виде «опрокинутой елочки», позже желатин воронкоооразно разжижается; на кровяном агape не дает гемолиза, чем отличается от сходных с ним почвенных и ложносибиреязвенных бацилл. Патогенетическими факторами возбудителя сибирской язвы являются его способность продуцировать экзотоксин и образовывать капсулу. С экзотоксином связывают воспалительное и летальное действие возбудителя. Обнаружено, что токсин также подавляет фагоцитарную активность лейкоцитов. Капсула препятствует фагоцитозу бацилл, способствуя проявлению действия основного патогенетического фактора — токсина. Токсин вызывает в организме повышение проницаемости сосудов, расстройство дыхания вследствие поражения центральной нервной системы, изменяет клеточный и химический состав крови. Устойчивость. Вегетативные формы малоустойчивы: в трупе погибают в течение 1—3 сут, при 60°С — через 15 мин, а при 75°С — через минуту. Споры сибиреязвенных бацилл отличаются большой устойчивостью. Они сохраняются во внешней среде длительнее, чем все другие известные патогенные спорообразующие микробы. Выдерживают сухой жар 120—140°С в течение 2—3 ч, автоклавирование при 120°С — 5—10 мин. Дезинфицирующие растворы (сулема 1 : 1000, 5% раствор карболовой кислоты, 5—10% раствор хлорамина) убивают их только за несколько часов, а этиловый спирт в концентрациях от 25% до абсолютного — за 50 дней. Антигенная структура. Возбудитель сибирской язвы содержит в клеточной стенке полисахаридный антиген и капсульный протеиновый антиген. К обоим антигенам в организме вырабатываются антитела, но защитными свойствами они не обладают. В организме животных и человека микроб образует особый протективный антиген, который обусловливает состояние иммунитета. Патогенность. Сибирской язвой болеют преимущественно домашние травоядные животные. Заражение животных происходит главным образом через инфицированный корм, что приводит к развитию кишечной формы сибирской язвы и сопровождается выделением большого количества микробов с испражнениями. В лабораторных условиях наиболее чувствительны к сибирской язве морские свинки, белые мыши и кролики. При подкожном введении даже небольших доз микроба животные погибают через 2—4 дня. На вскрытии сибиреязвенные бациллы обнаруживаются в крови и различных органах. Патогенез и клиника. Инкубационный период при сибирской язве длится 2—3 дня. Различают несколько клинических форм заболевания в зависимости от способа заражения: кожную, легочную и кишечную. Наиболее часто (в 98% случаев) встречается кожная форма болезни. На месте внедрения бацилл сибирской язвы появляется красное пятнышко, которое затем превращается в папулу, пустулу и при усилении воспалительного процесса — в сибиреязвенный карбункул. Чаще всего он располагается на лице, руках и других открытых частях тела. Общее состояние больного тяжелое: температура 0°С сильная головная боль, увеличение регионарных лимфатических узлов. Обычно кожная форма при своевременном лечении заканчивается выздоровлением. Однако при неблагоприятном течении возбудитель может попасть в кровь, что приводит к развитию сепсиса и заканчивается, как правило, летально. Легочная форма возникает только у человека и характеризуется высокой температурой, развитием бронхопневмонии, тяжелой одышкой и другими симптомами. При кишечной форме наблюдаются боли в животе, вздутие, диспепсические явления. При легочной и кишечной формах прогноз неблагоприятный — заболевание заканчивается смертью больного. В очень редких случаях при массивном заражении вирулентными штаммами сибиреязвенных бацилл развивается (первично) септическая форма, приводящая к летальному исходу. Иммунитет. При сибирской язве нестойкий, возможны повторные заболевания. Основная роль в защите организма принадлежит фагоцитарной реакции, обусловленной образованием протективного антигена. Микробиологическая диагностика. В лабораторию направляют патологический материал, взятый у больного: отделяемое карбункула, мокроту, испражнения, кровь, материал от животных (шерсть, кожа, мясо, трупный материал и др.), воду, почву, смывы с различных объектов внешней среды. Лабораторная диагностика сибирской язвы складывается из микробиологического исследования, биопробы, кожно-аллергической пробы, реакции термопреципитации по Асколи. При микробиологическом исследовании готовят мазок из патологического материала, окрашивают по Граму, микроскопируют. Затем материал засевают на мясо-пептонный агар и мясо-пептонный бульон и выращивают сутки в термостате при 37°С. Выделенную культуру идентифицируют по морфологическим и культуральным свойствам. Для выделения чистой культуры сибиреязвенных бацилл, исследуемый материал можно вводить подкожно морским свинкам или белым мышам (биопроба). Животные погибают обычно через 1—2 дня. Характерная патологоанатомическая картина при вскрытии и микроскопия мазков из различных органов (наличие капсульных сибиреязвенных бацилл) помогают поставить диагноз. Применяют также кожно-аллергическую пробу, положительную уже с первых дней заболевания. Метод основан на способности организма больного отвечать местной аллергической реакцией на введение сибиреязвенного аллергена (антраксин). С целью обнаружения сибиреязвенного антигена в различных объектах (кожевенное, меховое сырье и др.) используют реакцию термопреципитации Деколи с преципитирующей противосибиреязвенной сывороткой. Реакция эта высокочувствительна, отрицательный результат исключает наличие сибирской язвы. Профилактика и лечение. Поскольку источником инфекции являются животные, основные профилактические мероприятия проводит ветеринарная служба. Специфическая профилактика — введение живой сибиреязвенной вакцины СТИ, полученной из бескапсульного штамма бацилл сибирской язвы. Вакцинацию проводят по эпидемиологическим показаниям лицам, связанным с животноводством. Иммунитет после прививки сохраняется до года. Для лечения используют антибиотики, специфическую противосибиреязвенную сыворотку и глобулин. 23 билет( но не точно) 1 вопрос: защита бактерий от действия лекарственный средств. 2 вопрос: 1 тип аллергической реакции. 3 вопрос: возбудитель чумы, морфология, а.г структура, б.х и т.д 1. Известно два типа устойчивости микроорганизмов к антимикробным средствам — естественная (природная) и приобретённая. Естественная резистентность относится к видовым признакам микроба. Она в основном связана с отсутствием мишеней на клеточной стенке либо непроницаемостью последней для определённых ЛС. |
