3.0_Ответы на экзамен (хзхз) Патфиз. 1. Предмет и задачи патологической физиологии. Ее место в системе высшего медицинского образования. Патофизиология как теоретическая основа клинической медицины
 Скачать 1.5 Mb. Скачать 1.5 Mb.
|
|
84.Виды и функции клеточных онкогенов, роль онкобелков в нарушении функции трансформированных клеток. Понятие об антионкогенах. Продукты деятельности онкогенов — онкобелки в следовых количествах синтезируются и в нормальных клетках, функционируя в них как регуляторы чувствительности их рецепторов к факторам роста или как синергисты послед них. Многие онкобелки гомологичны или родственны ростовым факторам: тромбоцитарному (ТФР), эпидермальному (ЭФР), инсулинподобному и др. На ходясь под контролем регуляторных механизмов целостного организма, фактор роста, действуя прерывисто, обеспечивает процессы регенерации. Выйдя из-под контроля, он «работает» перманентно, вызывая безудержную пролифера цию и подготавливая почву для процесса малигнизации (теория «самозатяги вающейся петли»). Так, добавление ТФР в культуру нормальных клеток, имеющих соответствующие рецепторы, может вызывать обратимые фенотипи-ческие изменения, сходные с трансформацией: круглые клетки превращаются в веретенообразные, растут многослоем. Большая часть онкобелков принадлежит к протеинкиназам. Известно, что рецепторы факторов роста на своей внутрен ней, погруженной в цитоплазму стороне несут каталитическую часть протеин-киназы или гуанилат-циклазы. Механизмы действия онкогенов и их продуктов — онкобелков можно подразделить на три основные категории (рис. 5). Онкобелки могут имитировать действие факторов роста, оказывая влияние на синтезирующие их клетки по аутокринному пути (синдром «самозатягивающейся петли»; рис. 5, Б). Онкобелки могут модифицировать рецепторы факторов роста, имитируя ситуацию, характерную для взаимодействия рецептора с соответствующим фактором роста, без его действия (рис. 5, В). Продукты онкогенов могут действовать на ключевые внутриклеточные процессы, участвующие в контроле роста клеток без внешней их стимуляции. Так, продукт гена sre, являющийся тирозинпротеинкиназой, может воздействовать на митотическую активность клетки и тем самым влиять на фосфори лирование ключевых регуляторных белков. Аналогичный эффект возможен при действии продукта гена ras, стимулирующего (опосредованно) активность аденилатциклазы. Многоэтапность процесса онкогенеза 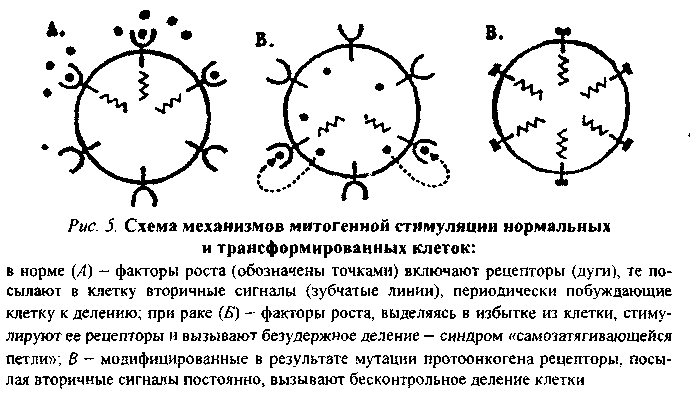 В становлении неопластического фенотипа принимает участие не один онкоген а последовательно включающиеся в данный процесс несколько (по меньшей мере два) онкогена. Этот феномен лежит в основе еще одного явле ния характерного для канцерогенеза, — многоэтапное™, многоступенчато сти процесса, причем два этапа решающие. На первом этапе происходит им-мортелизация популяции клеток, т.е. процесс, формирующий их способность беспредельно размножаться. В нем принимают участие ядерные онкогены, он-кобелки которых поступают в ядро. На втором этапе совершается процесс, ме няющий характер роста клетки, определяющий ее агрессивность. К этому причастны в основном мембранные онкогены, онкобелки которых накаплива ются в мембранах. Предполагается, что непрерывное деление клеток — функ ция ядра, а агрессивный (инфильтрирующий) их рост— функция мембран. Антионкогены и их роль в онкогенезе 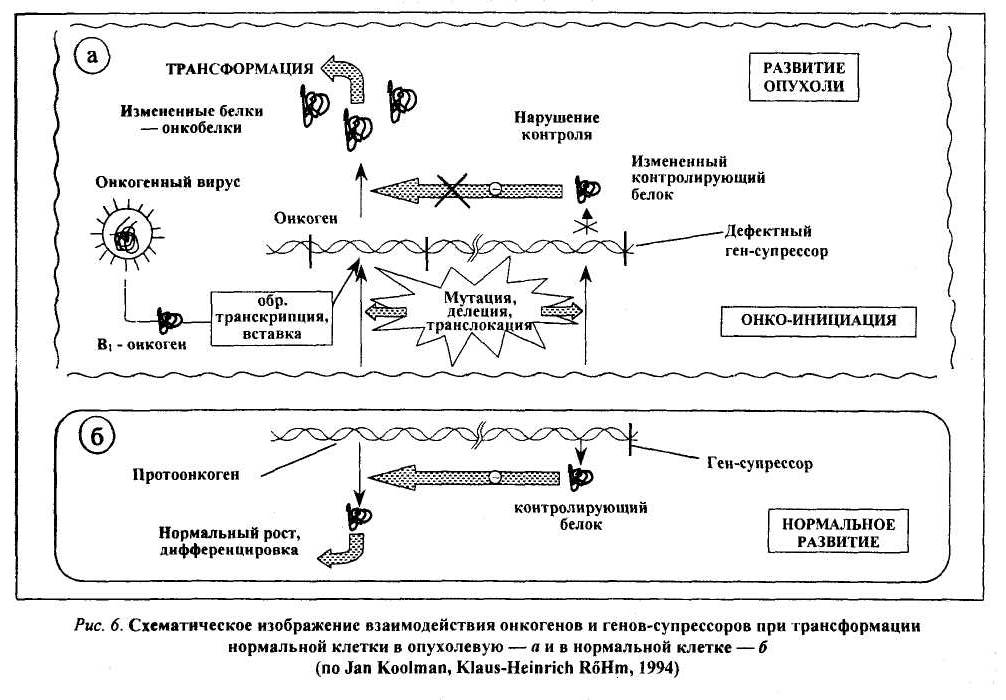 В геноме клетки имеется и второй класс опухолеродных генов — гены-супрессоры (антионкогены). В отличие от онкогенов, они контролируют синтез не стимуляторов роста, а его ингибиторов (подавляют активность онкогена и соответственно — размножение клеток; стимулируют их дифференцировку). Нарушение баланса процессов синтеза стимуляторов и ингибиторов роста и лежит в основе трансформации клетки в опухолевую (рис. 6). Впервые ген-супрессор был обнаружен в 1985 году при исследовании ретинобластомы — злокачественной опухоли сетчатки глаза у детей. Выяснилось, что в клетках опухоли ген, локализующийся в нормальных клетках в длинном плече 13-й хромосомы, отсутствует или в результате мутации утратил функциональную активность. Кодируемый этим геном (РБ) белок (р 100) регулирует активность генов (в частности, онкогенов), вызывающих опухолевую трансформацию клеток сетчатки глаза. С помощью методов генной инженерии он был выделен и перенесен в безудержно размножающиеся клетки культуры ретинобластомы. Раковые клетки, получив отсутствующий ген, стали вырабатывать белок р100, который блокировал действие онкогена. В результате опухолевые клетки превратились в нормальные, жили положенный им срок, старели и погибали. В последующем было установлено, что РБ-ген отсутствует в 40 % случаях рака мо чевого пузыря, почти во всех случаях рака легких, молочной железы, саркомы костей. При других формах злокачественных новообразований отсутствуют другие гены (возможно, супрессоры) различных хромосом. 85. Взаимосвязь нарушений функций нервной и эндокринной систем с возникновением и развитием опухолей. Гормонально-зависимые опухоли. Патогенез опухолевого роста не ограничивается механизмами опухоле вой трансформации клетки. Появление опухолевой клетки - лишь начальный этап онкогенеза. Дальнейшая судьба такой клетки во многом зависит от регуляторных систем организма (нервной, эндокринной, иммунной), состояние кото рых во многом определяет как сам факт возникновения опухоли, так и характер течения опухолевой болезни. Нервная система и развитие опухоли О важной роли в онкогенезе состояния нервной системы организма убе дительно свидетельствуют экспериментальные и клинические данные. Так, у собак с экспериментальным неврозом значительно выше процент самопроиз вольно возникающих опухолей. У них легче вызвать химический канцерогенез. Введение экспериментальным животным средств, угнетающих ЦНС, облегчает, а возбуждающих - затрудняет перевивку и индуцирование опухоли. Перевивку и индуцирование опухолей намного легче осуществить у животных со слабым типом высшей нервной деятельности, чем у животных с сильным уравновешенным подвижным типом ее. Локализация очагов опухоли может определять ся нарушением иннервации органа: узлы опухоли развиваются после введения опухолевых клеток в кровь кролика на фоне денервации селезенки — в селе зенке; после денервации почки - в почке; после денервации желудка — в же лудке. Из этого следует, что повреждение периферических образований нерв ной системы может иметь определенное значение в усилении метастазирования, которое иногда происходит после хирургических вмешательств. Анализ клинических наблюдений позволяет считать, что хронические стрес совые ситуации, длительная депрессия являются предрасполагающими факторами, заметно увеличивающими риск развития рака при прочих равных условиях. Развивающаяся опухоль в свою очередь оказывает влияние на неврологи ческий статус организма: вначале у больного преобладает возбуждение, затем на заключительном этапе болезни нарастает угнетение. Эндокринная система и развитие опухоли По степени участия эндокринных факторов в онкогенезе различают дисгармональные опухоли, в происхождении которых решающую роль играет на рушение гормонального фона организма, и опухоли неэндокринного происхождения, в возникновении и развитии которых нарушения гормонального фона организма играют дополнительную, хотя иногда и весьма существенную роль. Из дисгормональных опухолей человека и животных наиболее часто встречаются опухоли молочной железы, матки, предстательной железы. Веду щая роль в развитии опухоли (в том числе рака) грудной железы, матки при надлежит гиперэстрогенизации организма. В основе канцерогенного действия эстрогенов лежит их физиологическая способность стимулировать процесс пролиферации в указанных органах. Такое же действие оказывает фоликулостимулирующий гормон гипофиза. Он не только стимулирует процесс проду цирования эстрогенов, но и сам активизирует процессы пролиферации в матке и грудных железах. Антитиреоидная терапия по поводу хирургического вмешательства в свя зи с развивающейся опухолью благоприятствует рецидивам и метастазирова-нию последней. Назначение онкологическим больным тиреоидных гормонов в послеоперационный период способствует более благоприятному исходу лече ния. Тиреоидные гормоны, как и эстрогены, усиливают клеточную пролифера цию, однако они, в отличие от последних, способствуют дифференцировке клеток и повышают неспёцифическую резистентность организма, его защитные силы. Длительная стимуляция клеточной пролиферации, развивающаяся по принципу обратной связи в той или иной железе внутренней секреции при по нижении ее функции, иногда способствует развитию опухолевого роста в самих эндокринных железах, как в гиперплазированной периферической железе, так и в железе-хозяйке — гипофизе. Следовательно, способность некоторых гормо нов стимулировать клеточную пролиферацию может при определенных усло виях иметь отрицательное для организма значение. Растущая опухоль в свою очередь часто меняет гормональный фон орга низма. Так, при опухолях эндокринных желез возможны и угнетение, и активи зация процесса выработки гормонов, а также эктопический синтез их (паранеоэндокринный синдром). К примеру, раковая опухоль щитовидной железы не редко синтезирует адренокортикотропный гормон гипофиза (АКТГ), хорион-эпителиома — тиреотропный гормон и антидиуретический гормон гипофиза (ТТГ и АДГ). Опухоли, исходящие из островкового аппарата поджелудочной железы, могут синтезировать до 7 различных гормонов. В ряде опухолей неэн докринных органов синтезируются гормоноподобные вещества. Например, не которые формы бронхогенного рака нередко синтезируют вещества, подобные АКТГ, АДГ и т.д. Такого рода явления называются паранеоэндокринным синдромом (одна из разновидностей паранеопластического синдрома). Последний представляет собой совокупность клинических симптомов, проявляющихся в результате действия специфических и неспецифических продуктов обмена опу холи на организм, исчезающих при ее удалении и возобновляющихся при рецидиве и метастазировании опухоли. Паранеопластический синдром может про являться в виде нейротрофических, аутоиммунных и эндокринных изменений. 86.Взаимосвязь нарушений функций иммунной системы с возникновением и ростом опухолей. Основные причины и проявления иммуносупрессии при раке. Иммунная атака (иммунологический надзор) организма выполняет очень важную роль в предотвращении возможности перехода предопухолевой ситуации в опухолевую. У людей с наследственно детерминированной неполноцен ностью иммунной системы опухоли возникают в 10000 раз чаще, чем у лиц с нормальной иммунной системой. Среди реципиентов, которым с целью профи лактики отторжения пересаженного по жизненным показаниям органа (почки) назначались иммунодепресанты, в 80-100 раз чаще возникали злокачественные новообразования. Доказано, что в ответ на развивающуюся опухоль вырабаты ваются и клеточные, и гуморальные реакции иммунитета. Причем решающая „ роль, как правило, принадлежит первым. Роль первого «эшелона» защиты от опухоли выполняют естественные киллеры — ЕК, имеющие с Т-киллерными клетками общую клетку-предшест венницу и отличающиеся от последних тем, что не проходят «обучения» в ти мусе и реагируют на клетки с чужеродной информацией (инфицированные ви русом, опухолевые) без предварительной сенсибилизации. Реакция ЕК на появ ление опухолевых клеток осуществляется в 4 стадии: распознавание антигенов мишени, усиленное размножение ЕК, контакт их с клеткой-мишенью и собст венно лизис последней — «летальный удар» (рис. 7). Гранулы ЕК, перемещаясь к месту контакта, высвобождают содержащиеся в них цитотоксические вещества Под влиянием последних в мембране клетки-мишени образуется множество дыр и она становится проницаемой. Поступающая в клетку вода раздувает ее, и она, поте ряв большинство своих микроворсинок, лопается, а ЕК поражает новую мишень. Второй «эшелон» защиты от опухоли инициируется макрофагами - антигенпредставляющими клетками. Прилипнув к чужеродному объекту - опухо левой клетке (адгезия), — макрофаг образует псевдоподии, захватывает ими эту клетку и переносит ее в цитоплазму (эндоцитоз). После этого чужеродный бе лок расщепляется в клетке (процессинг) и на поверхности макрофага образуется комплекс опухолевых антигенов с молекулами своих антигенов совместимо сти II класса. Такое сочетание распознается Т-хелперами, что и служит сигналом для иммунологических реакций. В ответ на синтезируемый макрофагами интерлейкин-1 (ИЛ-I) Т-хелперы ативно размножаются и продуцируют другой цитокин — ИЛ-2. Под влиянием последнего покоящиеся Т-клетки уже через 6 часов превращаются в Т-киллеры и оказывают на опухолевые клетки цитоток-сическое действие, аналогичное таковому естественных киллеров (рис. 7). Существует немало гипотез, объясняющих причину развития опухоли, несмотря на иммунную реакцию организма. Некоторые исследователи полага ют, например, что опухолевые клетки вследствие «эмбрионализации» приобретают супрессорные потенции, препятствующие действию как ЕК, макрофагов, так и генерализованного Т-иммунитета. В клетках злокачественной опухоли синтезируются простагландины группы Е3 (заметно подавляющие иммунитет) и хорионический гонадотропин (гормон периода беременности, оказывающий \ иммуносупрессорный эффект). В результате при опухолевом росте иммунная :: реакция организма не заканчивается (как это имеет место при инфекционном процессе) супрессией, а начинается с нее. В ответ на «гипогликемическое давление» опухоли на организм, в результате чего он переходит на гликолитический путь получения энергии, надпочечники интенсивно синтезируют глюкокортикоиды (стимулируют процессы глюконеогенеза), избыток которых ведет к нарастающей иммунодепрессии. 87. Системное действие опухоли на организм. Паранеопластический синдром, его патогенез, основные проявления. Патогенез раковой кахексии. Опухоль — не местный изолированный процесс; ее развитие затрагивает весь организм. В.А. Шапот (1974) сформулировал положение о системном дей ствии опухоли и выделил две его компоненты. Неспецифическая компонента: успешная конкуренция опухоли с органа ми и тканями, непосредственно не затронутыми опухолевым процессом, за жизненно важные метаболиты (глюкозу, азотистые основания, предшественни ки нуклеиновых кислот, железо, витамины и др.). Инициирующими звеньями ее являются гипогликемическое давление опухоли (опухоль — «ловушка глюкозы») и высокая активность синтетических процессов в ней (опухоль — «ловуш ка азотистых соединений»). Специфическая компонента: постепенное перепрограммирование про цессов, происходящих в органах и тканях, непосредственно не пораженных опухолью, в сторону, характерную для процессов самой опухоли. Паренеоэндокринный синдром - разновидность паренеопластического синдрома - совокупность клинических симптомов, проявляющихся в результате действия на организм специфических и неспецифических продуктов обмена опухоли, исчезающие при ее удалении и возобновляющиеся при рецидивировании и метастазировании опухоли. Он может быть представлен: - нервно-трофические нарушения; - аутоиммунные процессы; - эндокринные нарушения. В растущей опухоли в процессе обмена образуются соединения влияющие на активность желез внутренней секреции. В опухолях могут вырабатываться эндокриноподобные вещества. В опухолях одной эндокринной железы могут вырабатываться гормоны другой эндокринной железы: в опухолях щитовидной железы - синтез АКТГ; в опухолях хорион-эпителиоме - синтез ТТГ. Гормоны, вырабатываемые опухолями часто в неактивном состоянии. Крайним выражением системного действия опухоли на организм является кахексия. К основным патогенетическим слагаемым ее относятся:
88. Учение о предраковых состояниях. Облигатный и факультативный предрак. Стадии развития злокачественных опухолей. Основные принципы терапии и профилактики новообразований. Под предраковыми состояниями понимают такие патологические процессы, которые в большем или меньшем проценте случаев способны подвергаться малигнизации. Различают облигатный (с высоким риском малигнизации) и фа культативный (низкая вероятность малигнизации) предрак. К облигатным предраковым состояниям относят полипоз толстого кишечника, полипоз желудка, пигментную ксеродерму, некоторые формы мастопатии и др. Примерами факультативного предрака являются эррозии шейки матки, ряд форм фиброматозной мастопатии, аноцидный гастрит, язвенная болезнь желудка и др. В развитии злокачественной опухоли принято выделять несколько стадий. Первая стадия — стадия неравномерной диффузной гиперплазии, когда ткань еще полностью сохраняет нормальное строение, но заметно увеличивает ся численность составляющих ее элементов - клеток, волокон. Это увеличение носит диффузный характер, но неодинаково выражено в разных участках тка ни; причем ограниченных участков пролиферации нет. Первая стадия еще не является предраковым состоянием. Она может быть квалифицирована как предопухолевая стадия. Вторая стадия — стадия очаговых пролифератов. На данной стадии ткань в основном еще сохраняет нормальную структуру, но в общей массе ин тенсивно размножающихся клеток появляются отдельные ограниченные очаги особенно бурного размножения. Эта стадия, как и следующая за ней — третья, — стадия относительно доброкачественной опухоли (миомы, аденомы, фиб ромы), относится к предраковому состоянию. Отличительной особенностью третьей стадии является все возрастаю щий атипизм клеток очагов пролиферации, однако, без признаков инвазивного и деструктивного роста. Четвертая стадия — развитие злокачественной опухоли (рак, саркома). Более характерной ее чертой и является наклонность к инвазии и деструкции. Нередко злокачественная опухоль развивается сразу же после стадии очаговых пролифератов, минуя стадию относительно доброкачественной опухоли. |
