3.0_Ответы на экзамен (хзхз) Патфиз. 1. Предмет и задачи патологической физиологии. Ее место в системе высшего медицинского образования. Патофизиология как теоретическая основа клинической медицины
 Скачать 1.5 Mb. Скачать 1.5 Mb.
|
|
78.Опухоли. Определение понятия. Характеристика бластоматозного роста, его отличия от других видов тканевого роста. Особенности распространения опухолей в фило- и онтогенезе. Основные причины роста онкологической заболеваемости. Стремительно растет число опухолевых заболеваний: В Европе каждый год заболеваемость раком возрастает на 3%. Причины роста числа раковых заболеваний: 1. Улучшение диагностики 2. Успехи а области лечения ООИ туберкулеза, полиомиелита 3. Улучшение методов статистики. 4. Увеличение средней продолжительности жизни. 5. Загрязнение окружающей Среды канцерогенами. Опухоли могут быть у животных. У растений - опухолевовидные образования. В филогенезе: 1. Все виды животных организмов в состоянии заболевать опухолевыми болезнями. 2. По мере усложнения животных организмов число спонтанно возникающих опухолей возрастает. 3. По мере усложнения организмов все чаще возникают опухоли эпителиального тканного происхождения (у низших - соединительнотканного). 4. Увеличивается доза злокачественных новообразований. 5. Увеличивается разнообразие видов опухолей. 6. Для каждого вида животных организмов характерен свой спектр опухолей: лошади - лейкоз, человек - рак желудка. В онтогенезе: В 1-й половине беременности не встречаются опухоли у эмбриона Во 2-й половине возможны Далее - чем старше, тем больше вероятность развития опухоли. Опухоли - нерегулируемые избытки клеточного размножения (Петров). Опухоли - эксцессы роста. Опухоли - плюс размножение клеток, минус дифференцировка (Шабад). Опухоль - избыточное, продолжающееся после прекращения действия вызывающих его причин, некоординированное с организмом патологическое разрастание тканей, состоящее из клеток, ставших атипичными в отношении дифференцировки и роста и передающие эти свойства своим производным. Критерии отличия злокачественных и доброкачественных опухолей: 1. Характер роста: экспансивный инфильтрующий (деструктивный) 2. Способность к развитию метастазов 3. Способность к развитию кахексии. 79.Этиология опухолей. Классификация бластомогенных агентов. Канцерогенные вещества экзо- и эндогенного происхождения. Методы экспериментального воспроизведения опухолей. Исторически - концепции: 1. Р.Вирхов - опухоль - избытки, результат избыточного чрезмерного формативного раздражения клетки. По Вирхову 3 вида раздражения клетки: внутритивное (обеспечивающее питание) функциональное нормативное Рак Кангри на коже живота после привязывания к животу горшков с горящими углями. 2. Конгейм - дисонтогенетическая концепция канцерогенеза: недоиспользованные эмбриональные зачатки дают начало опухоли. Плоскоклеточный рак желудка Миксома кишечника (из ткани, похожей на ткань пуповины). 3. Рибберт - любая ткань, оказавшаяся в необычном окружении может дать начало росту опухоли. Но это частные случаи, ошибочно распространенные на все виды опухолей. ПОЛИЭТИОЛОГИЧНОСТЬ ОПУХОЛЕЙ 1) Химические факторы онкогенеза (канцерогенеза) XVIII в. - рак кожи мошонки у трубочистов в Англии - продукты перегонки каменного угля (сажа). Ямагива и Ичикава (1914-1916 гг.) - смазывали уши кролика каменноугольной смолой - возник плоскоклеточный ороговевающий рак кожи уха кролика. Выделены чистые канцерогены (более 1000, 60-70 истинных канцерогенов). Химические канцерогены: 1. Экзогенные: 1. Полициклические ароматические углеводы (ПАУ): фенантрен, бензпирен, бензидин; 3-4 бензпирен - индикатор канцерогенности; анилин и анилиновые красители: азосоединения; нитрозамины и нитрозамиды - образуются в организме при употреблении в пищу продуктов с нитратами: нитраты ---------------------------------------------------и нитраты нитратдедуктаза амины амиды нитрозамины ----------------------------------- нитрозамиды канцерогенез Специфичность канцерогенов относительна: уретан - рак легкого b-нафталамин - опухоль мочевого пузыря при любом пути введения. Факторы, определяющие канцерогенность химического соединения: 1. Химическая структура соединения. 2. Путь метаболических превращений вещества, попавшего в организм b-нафталамин и 2-амино-1-нафтол и опухоль Проканцерогены - вещества, попадая в организм превращаются в канцерогены. 3. Доза вещества. Опухоль возникает через длительный латентный период (1/7 - 1/3 продолжительность жизни, 12-18 лет для человека). Синканцерогенез - усиление эффекта канцерогенеза под влиянием неканцерогенных веществ: кротоновое масло (коканцероген) Трансплацентарный канцерогенез - через плаценту канцерогены проникают от матери к плоду по 2-й половине беременности и вызывают опухоли уже во взрослом состоянии (если в 1-й половине беременности - преждевременные роды, уродство плода). Пути появления экзогенных канцерогенов: 1. Химическое производство, металлургические предприятия 2. Использование нитратов, пестицидов в сельском хозяйстве 3. Выхлопные газы транспорта (от 60 до 80 канцерогенов) Строение большинства канцерогенов близко к строению стероидных гормонов. 2. Эндогенные канцерогены метилхолантрен - из дезоксихолевой кислоты Шабад - бензольный экстракт из рака желудка человека вызывал опухоль у мышей. В животном организме образуются канцерогенные вещества: - продукты расщепления холестерина (холестеридины), продукты расщепления триптофана, тирозина. ФИЗИЧЕСКИЕ КАНЦЕРОГЕНЫ Чахотка горнорабочих Шнейберга - рак легких (радиоактивные изотопы в Саксонских рудах). Рак рентгенолога - проверили кистью жесткость лучей. Торотраст (содержит радиоактивный Th) 0 контрастное вещество и злокачественные опухоли. R-лучи, -лучи; Уф лучи. БИОЛОГИЧЕСКИЕ ФАКТОРЫ КАНЦЕРОГЕНЕЗА Мечников, Роуз - предполагали, что причина опухолей - вирусы. перевивка бесклеточного фильтрата лейкозной ткани вызывала лейкоз (Боурейм). Перевивка фильтрата саркомы кур Онкогенные вирусы передаются вертикально от родителей детям (не исключен и горизонтальный путь). Лимфома Беркитта - 4 узла на челюсти (симметричные) - это уже метастазы опухоли. Рак шейки матки - вирус герпеса. Онкогенные вирусы: 1. РНК-содержащие (Oncornaviridae): лейкозосаркоматозный комплекс обезьян, мышей, крыс... 2. ДНК-содержащие: группа Papovaviridae группа вирусов оспы аденовирусы группа вирусов герпеса Патогенез опухолей один - опухоли монопатогенетичны. Экспериментальное воспроизведение опухолей: 1. Перевивка (трансплантация) опухолей: Новинский в 1876 г. впервые пересадил опухоль от собаки Правила перевивки опухолей: очень малый разрез очень малый кусочек опухоли тщательное соблюдение асептики и антисептики молодое животное живая ткань перевивка животному того вида. аутотрансплантация гомо(алло)трансплантация гетеро(ксено)трансплантация 2. Индуцирование опухолей. 3. Эксплантация - культивирование опухолевых клеток вне организма 1907 г. Харрисон - в течение 2 нед эмбрион клетки лягушки культивировал. 1911 г. Каррель - питательная Среда. 1950 г. - ткань опухоли человека рака шейки матки культивируется до сих пор (культура НеLa) 80.Значение наследственности, возраста, пола, особенностей питания, вредных привычек в возникновении и развитии опухолей. 1. Возраст: чем старше организм, тем более вероятность развития опухоли. 2. Пол: мужчины - рак желудка, легкого; женщины - рак молочной железы, матки. 3. Питание: объем пищи - избыток питания повышает риск заболеть характер пищи - недостаток витаминов, белка; избыток жира - рак прямой кишки; копченые, консервированные - рак пищевода. индолы в капсуле; кумарины в других овощах - противоопухолевые факторы в овощах и фруктах. Роль наследственности в развитии опухолей: Большая наследственная предрасположенность: Ретинобластома сетчатки саркома сосудистой оболочки глаза пигментная ксеродерма нейрофиброматоз полипоз толстого кишечнике Вредные привычки и рак: 1. Курение: в 20 раз чаще рак легкого; рак языка, глотки, пищевода, кишечника, 30 - 40% опухолей связаны с курением. 2. Алкоголь. 3. Загар - увеличение рака кожи у мужчин на 20%, у женщин - на 50% за последние годы. 4. Жевание бетеля. 81.Основные биологические особенности опухолей. Метастазирование опухолей механизмы, стадии. Понятие об опухолевой прогрессии. Биологические особенности злокачественных новообразований: 1. Относительная автономность и нерегулируемость роста (рост не подчиняется регуляторным механизмам). - отсутствуют лимит клеточного деления Хейблига - ослаблены межклеточные контакты - понижены механизмы контактного торможения - расстройство рецепторной поверхности клеток - нарушены синтез и чувствительность к кейлонам (вырабатываются зрелыми клетками и подавляют размножение опухолевых клеток). - нарушена работа аденилатциклазы системы 2. Упрощение структурно-химической организации клеток (анаплазия): - морфологическая анаплазия - биохимическая - энергетическая - функциональная - иммунологическая а) морфологическая тканевая - соотношение стромы и паренхимы нарушены клеточная - разные размеры, форма клеток, миграция ядрышка, нарушение структуры поверхности клеток. б) биохимическая анаплазия: набор изоферментов уменьшен активность ферментов снижена изоферментное упрощение (монотонизация) в) энергетическая анаплазия энергия за счет гликолиза как анаэробного, так и аэробного Превалируют синтетические процессы - снижение белка за счет продуктов разрушения клеток. Нарушение соотношения гистонов и негистоновых белков. Много ферментов синтеза РНК на денатурированной матрице ДНК. г) функциональная анаплазия Функция либо понижена, либо повышена. Гипо- ли гипертиреоз - пример. д) иммунологическая анаплазия: органоспецифические антигены межорганные антигены 1. Антигенное упрощение - резко уменьшено количество органоспецифических антигенов (нем. Вейлер). 2. Антигенная дивергенция - синтез. В опухолевых клетках гетерогенных антигенов (другого органа; Вейлер и Оленов). 3. Антигенная реверсия - синтез в опухолевых клетках эмбриональных антигенов (Абеленов и Татаринов - в гепатоме найден a-феропротеин; эмбриональный преальбумин в гепатоме мыши). 3. Наследуемость изменений - раковая клетка при размножении дает себе подобные. 4. Способность к метастазированию - образование вдали от первичного опухолевого узла вторичного опухолевого зачатка. Этапы метастазирования: 1. Отрыв опухолевых клеток от тканей опухоли 2. Транспортировка клеток по кровеносному или лимфатическому руслу, Лишь 9-11? переходит в 3 стадию. 3. Фиксация клетки к стенке сосуда. Если вызвать повреждение стенки сосуда, то фиксируется 85-90% клеток (атеросклеротическое; дистрофическое поражение стенки сосуда). Дремлющие клетки не проявляют своей активности до воздействия определенных агентов. 4. Пролиферация при действии факторов: гормональные нарушения нейродистрофические изменения хирургические вмешательства 5. Способность к инвазивному и деструктивному росту. 6. Прогрессия опухоли (Фулис) - способность опухоли в процессе ее эволюции менять биологические свойства. Опухоль становится все более и более злокачественной.(повыш. изменчивось генотипа опух. кл., постоянно изменяется генотип опух.кл., возрастание степени приспособл.кл.опухоли, повыш. резистентности кл.опухоли) 7. Системное действие опухоли на организм. Эпидемиология опухолей: Самая высокая заболеваемость раком: среди мужчин - Австрия среди женщин - Чили СССР - самая высокая заболеваемость раком в республиках Прибалтики; самая низкая - Ср. Азия. 82. Виды и основные проявления атипизма опухолевых клеток. Упрощение структурно-химической организации клеток (анаплазия): - морфологическая анаплазия - биохимическая - энергетическая - функциональная - иммунологическая а) морфологическая тканевая - соотношение стромы и паренхимы нарушены клеточная - разные размеры, форма клеток, миграция ядрышка, нарушение структуры поверхности клеток. б) биохимическая анаплазия: набор изоферментов уменьшен активность ферментов снижена изоферментное упрощение (монотонизация) в) энергетическая анаплазия энергия за счет гликолиза как анаэробного, так и аэробного Превалируют синтетические процессы - снижение белка за счет продуктов разрушения клеток. Нарушение соотношения гистонов и негистоновых белков. Много ферментов синтеза РНК на денатурированной матрице ДНК. г) функциональная анаплазия Функция либо понижена, либо повышена. Гипо- ли гипертиреоз - пример. д) иммунологическая анаплазия: органоспецифические антигены межорганные антигены 1. Антигенное упрощение - резко уменьшено количество органоспецифических антигенов (нем. Вейлер). 2. Антигенная дивергенция - синтез. В опухолевых клетках гетерогенных антигенов (другого органа; Вейлер и Оленов). 3. Антигенная реверсия - синтез в опухолевых клетках эмбриональных антигенов (Абеленов и Татаринов - в гепатоме найден a-феропротеин; эмбриональный преальбумин в гепатоме мыши). 3. Наследуемость изменений - раковая клетка при размножении дает себе подобные. 4. Способность к метастазированию - образование вдали от первичного опухолевого узла вторичного опухолевого зачатка. 83. Патогенез опухолей. Современные представления о молекулярно-генетических механизмах неопластической трансформации. Современная трактовка концепции онкогена. Роль мутаций, вирусов и эпигеномных нарушений в механизмах превращения протоонкогена в онкоген. Молекулярно-генетические механизмы опухолевой трансформации клетки Современная концепция канцерогенеза получила название концепции онкогена. Основополагающие положения ее были сформулированы еще в 1981-1985 гг. Этому предшествовали сложные поиски ведущего патогенетиче ского звена в механизме опухолевой трансформации клетки. Все исследователи второй половины 20-го столетия считали, что данный процесс осуществляется на молекулярно-генетическом уровне, но суть его трактовали по-разному. Мутационная концепция канцерогенеза Нормальная клетка превращается в опухолевую в результате структур ных изменений в генетическом материале, т.е. мутаций. В этом заключается суть мутационной концепции. Различают три ее варианта. Первый вариант концепции (Т. Bovery, 1914) касается хромосомных аббераций и геномных му таций, затрагивающих значительную часть генома. Второй вариант (Н.Н. Петров, К.Н. Bayer, 1924) учитывает еще и точечные или генные мутации. Третий вариант касается возможности участия в канцерогенезе мутации регуляторных генов. О возможной роли мутационных механизмов в канцерогенезе свиде тельствуют следующие факты: Мутагенность подавляющей части (90 %) известных канцерогенов и канцерогенность большинства (у 85-87 % исследованных образцов) мутагенов. Обнаружение в клетках ряда опухолей человека и животных так называемых маркерных хромосом (например, филадельфийской хромосомы примиелоцитарном лейкозе человека). Резкое увеличение заболеваемости лейкозом и опухолевой болезнью людей с различного рода генетическими дефектами (при болезни Дауна, синдромах Клайнфельтера, Шерешевского-Тернера и др). Эпигеномная концепция канцерогенеза Согласно этой концепции (Ю.М. Оленов, А.Ю. Броновицкий, B.C. Ша-пот), в основе превращения нормальной клетки в злокачественную лежат стойкие нарушения регуляции генной активности, а не изменения структуры генетического материала. Под влиянием химических и физических канцерогенов, а также онкогенных вирусов происходит сдвиг в строго специфичной для каждой ткани регуляции генной активности: дерепрессируются группы генов, которые в данной ткани должны быть зарепрессированы и (или) блокируются активные гены. В результате клетка в значительной мере утрачивает присущую ей специфику, становится нечувствительной или малочувствительной к регуляторным влияниям целостного организма, неуправляемой. С точки зрения эпигеномной концепции канцерогенеза можно объяснить ряд особенностей неоплазмы: изоферментное упрощение, антигенную ревер сию, выработку некоторыми опухолями гормонов, не присущих клеткам гомо логичной ткани и др. Вирусо-генетическая концепция канцерогенеза Данную концепцию предложил Л.А. Зильбер (1948). Она заключается в следующем. Опухолевая трансформация клетки происходит в результате привнесения в ее генетический материал новой генетической информации онкогенными вирусами. Главным свойством последних является их способность разрывать цепочку ДНК и объединяться с ее обрывками, т.е. с клеточным гено мом. Проникнув в клетку, вирус, освободившись от белковой оболочки, под влиянием содержащихся в нем ферментов встраивает свою ДНК в генетический аппарат клетки. Привнесенная вирусом новая генетическая информация, меняя характер роста и «поведение» клетки, превращает ее в злокачественную. G. Temin (1963) открыл явление обратной транскрипций: списывание генети ческой информации возможно не только в одном направлении (ДНК-РНК-белок), но и в обратном (от РНК к ДНК). Обнаружение в РНК-содержащих ви русах фермента ревертазы, или обратной транскриптазы, обеспечивающего процесс обратной транскрипции, позволило понять механизм действия и РНК-вирусов. Они синтезируют ДНК-овую копию своей РНК, которая и встраивает ся затем в геном клетки. В процессе обратной транскрипции на концах ДНК-вой копии формируются одинаковые последовательности — большие терми нальные повторы (LTR), играющие роль в трансформации нормальной клетки в опухолевую. Современная концепция онкогена Альтернативные точки зрения относительно природы неопластической трансформации в 70-е годы значительно сблизились, поскольку появились не опровержимые факты участия в канцерогенезе и мутационных, и эпигеномных, и вирусно-генетических механизмов, последовательно включающихся в про цесс опухолевой трансформации. Стало аксиомой представление о многоэтапности процесса канцерогенеза, решающей предпосылкой которого является нерегулируемая экспрессия трансформирующего гена - онкогена, предсущест-вующего и геноме. Впервые онкогены были обнаружены с помощью трансфекции («переноса генов») в вирусах, вызывающих опухоли у животных. Затем с помощью данного метода было установлено, что в организме животных и человека содерпотенциальные онкогены – протоонкогены, экспрессия которых и обуславливает трансформацию нормальной клетки в опухолевую. Согласно современной концепции онкогена мишенью для изменений, обусловливающих начаяо опухолевого роста, являются протоонкогены, или потенциальные онкогены, существующие в геноме нормальных клеток и обеспечивающие yсловия для нормальной жизнедеятельности организма. В эмбриональный период они обеспечивают условия для интенсивного размножения клеток и нормального развития организма. В постэмбриональном периоде функциональная их активность в значительной степени снижается — большая часть их оказывается в репрессированном состоянии, а остальные обеспечива ют лишь периодическое обновление клеток. Механизмы превращения протоонкогена в онкоген Превращение протоонкогена в активно действующий онкоген обеспечи вается следующими механизмами. 1. Присоединение к протоонокгену промотора — участка ДНК, с кото рым связывается РНК-полимераза, инициирующая транскрипцию гена, в том числе и онкогена, располагающегося непосредственно за ним (рис.1). Такого рода участки (промоторы) содержатся в больших терминальных повторах (LTR) ДНК-копий РНК-содержащих вирусов. Роль промотора могут выполнять и транспозирующие элементы генома — мобильные генетические элементы, способные перемещаться по геному и встраиваться в различные его участки. 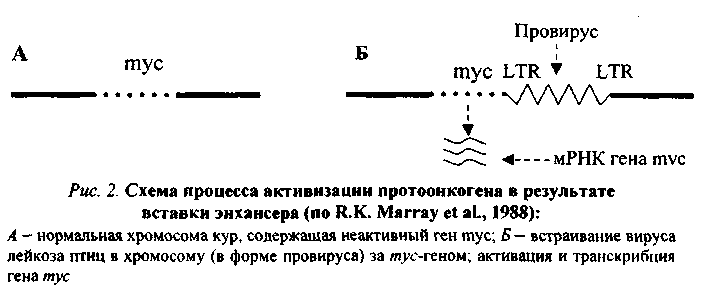 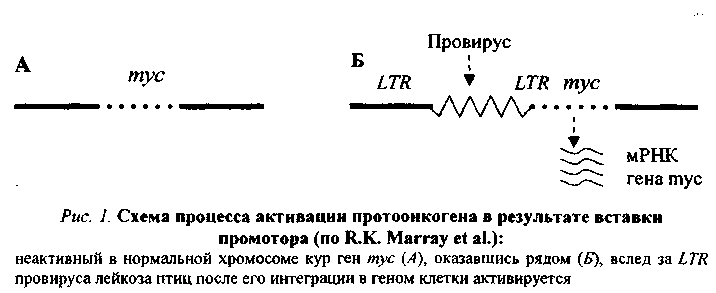 2. Вставка в геном клетки энхансера (enchancer — усилитель) — участка ДНК, способного активизировать работу структурного гена, находящегося не только в непосредственной близости от него, но и на расстоянии многих ты сяч пар нуклеотидов или даже встроенного в хромосому после него. Свойства ми усилителя обладают подвижные гены, LTR ДНК-копий. В случае, проиллюстрированном рис. 2, LTR провируса не может работать как промотор (см. рис. 1, Б) и выступает в роли энхансера, в результате чего ген туе активизируется и транскрибируется. 3. Хромосомные абберации с явлениями транслокации, роль которых в механизмах опухолевой трансформации клетки можно проиллюстрировать следующим примером. При лимфоме Беркитта конец (q-плеча хромосомы 8, отделившись от нее, переходит к хромосоме 14: гомологичный фрагмент последней перемещается к хромосоме 8; а неактивный ген туе (протоонкоген), находившийся в том ее сегменте, который попадает на хромосому 14, встраивается вслед за активными генами, кодирующими тяжелые цепи молекул иммуноглобулинов, и активизи руется (рис. 3, 4). Явления реципрокной транслокации между 9-й и 22-й хромо сомами имеют место в 95 % случаев миелоцитарного лейкоза. Хромосома 22 с укороченным в результате такой транслокации одним плечом получила назва ние Филадельфийской. 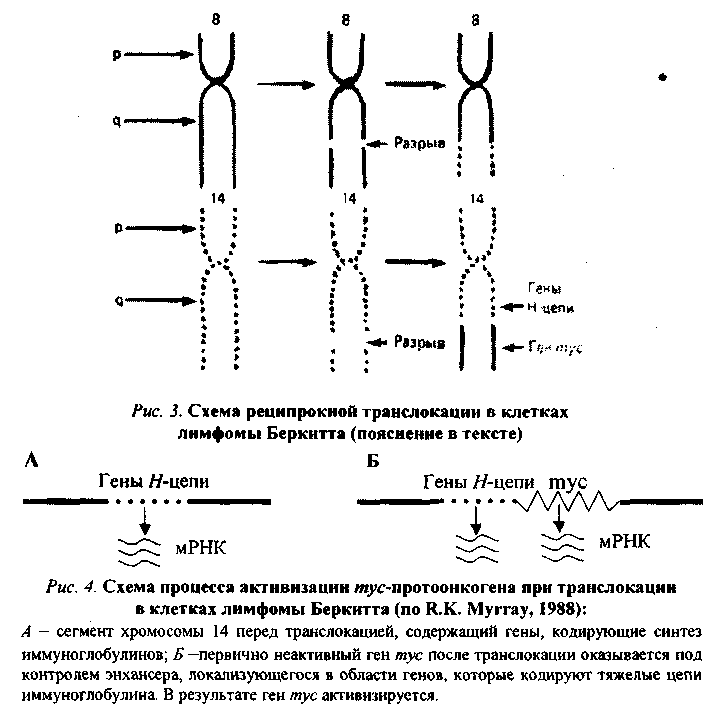 Точечные мутации протоонкогена, к примеру, C-H-raS, согласно имеющимся сведениям, отличается от нормального гена (C-H-raS) всего одной аминокислотой, но тем не менее обусловливает снижение гуанозинтрифосфатазной активности в клетке, что может вызвать рак мочевого пузыря у человека. Амплификация (умножение) прогоонкогенов, обладающих в норме небольшой следовой активностью, обусловливает увеличение их общей актив ности до уровня, достаточного для инициации опухолевой трансформации. Известно, что в икринке шпорцевой лягушки около 5 млн копий гена туc. После оплодотворения и дальнейшего деления яйцеклетки число их прогрессирующе уменьшается. В каждой клетке будущего головастика в эмбриональный период развития содержится не более 20—50 копий тус-гена, обеспечивающих быстрое деление клеток и рост эмбриона. В клетках же взрослой лягушки выявляются лишь единичные гены туc, в то время как в раковых клетках той же лягушки число их вновь достигает 20-50. 6. Трансдукция неактивных клеточных генов (протоонкогенов) в геном ретровируса и последующее их возвращение в клетку: считается, что онкоген опухолеродного вируса клеточного происхождения; при инфицирова нии животных или человека таким вирусом «похищенный» им ген попадает в иной участок генома, что и обеспечивает активизацию некогда «молчавшего» гена. |
