калоиды и кристалоиды. инфузиоона терапия. 2. Приемущества и недостатки коллоидов и кристаллоидов
 Скачать 85.74 Kb. Скачать 85.74 Kb.
|
|
План Введение………………………………………………………………2-3 1. Инфузионные терапия - коллоиды и кристаллоиды……………4-7 2. Приемущества и недостатки коллоидов и кристаллоидов……..8-9 Литература……………………………………………………………..14 Введение Инфузионная терапия является серьезным инструментом анестезиолога-реаниматолога и может дать оптимальный лечебный эффект только при соблюдении двух непременных условий: врач должен четко понимать цель применения препарата и иметь представление о механизме его действия. Нарушение водно-электролитного обмена может привести к тяжелым расстройствам сердечно-сосудистой и центральной нервной систем. В связи с этим рациональной можно считать только ту программу инфузионной терапии, которая основывается на четких знаниях водно-электролитного обмена. Инфузионная терапия при длительных хирургических вмешательствах является неотъемлемой и важной частью анестезиологического пособия. Современное анестезиологическое пособие включает в себя не только введение наркотических анальгетиков, гипнотиков и других средств используемых для подавления болевой импульсации из зоны операции, но и управление функциями организма, в первую очередь дыханием и кровообращением. Эти задачи реализуются применением искусственной вентиляцией легких для обеспечения функции внешнего дыхания и инфузией жидкостей для обеспечения нормального минутного объема кровообращения. Инфузионная терапия во время операции преследует несколько целей в зависимости от объема и длительности оперативного вмешательства и соматического состояния пациента. Во-первых, это обеспечение пациента водой и электролитами с учетом физиологических потребностей до операции и во время нее. Перед операцией больной не ест и не пьет с вечера (12 часов). В таких условиях даже у здорового человека за счет облигатных потерь воды (с мочой, дыханием, перспирацией и стулом) растет дефицит жидкости до 1250 мл и более, в среднем около 15 мл/кг. У многих больных уже перед анестезией имеется относительная гиповолемия, служащая предпосылкой для развития гипотензии после вводного наркоза (1,2,3) . Во-вторых, большие по объему операции сопровождаются более или менее значимой кровопотерей. В-третьих, необходимо учитывать перспирацию жидкости из зоны операции. Открытая лапаротомная рана сама по себе является источником водных потерь. Учитывая вышеизложенное, сбалансированная инфузионная терапия занимает важное место в профилактике и лечении периоперационных осложнений, наиболее грозным из которых считается нестабильная гемодинамика со всеми вытекающими из нее негативными последствиями. Но, даже при малотравматичных и не особо длительных операциях, обходясь без инфузии, при, казалось бы, стабильной анестезии, в послеоперационном периоде могут возникнуть проблемы с заживлением операционного шва, развиться инфекционные осложнения и затянуться реабилитационный период. Такие осложнения не принято связывать с инфузией, однако ее вклад несомненен. Во многом это зависит не только от инфузии, но и от других факторов (адекватность анестезии, кровопотеря, травматичность операции и т.д.). В то же время рациональная инфузионная терапия является компонентом анестезиологического пособия, поддерживающим гомеостаз. Инфузионные терапия - коллоиды и кристаллоиды Инфузионная терапия подразумевает введение в сосудистое русло кристаллоидных и коллоидных растворов. Кристаллоидные растворы - это водные растворы низкомолекулярных ионов, иногда в сочетании с глюкозой. Коллодные растворы содержат не только ионы, но и высокомолекулярные вещества - белки и полимеры глюкозы (полисахариды). Кристаллоидные растворы делятся на: гипотонические, имеющие более низкое осмотическое давление, чем плазма; изотонические - такое же как у плазмы; гипертонические - более высокое осмотическое давление, чем плазма крови. Действие вводимых растворов на осмоляльность зависит от концентрации натрия в растворе относительно его концентрации в сыворотке. Изотонические растворы равномерно распределяются исключительно во внеклеточном секторе, т.е. в плазме и интерстиции. Часть объема гипотонических растворов за счет белее низкой осмоляльности, чем у плазмы перемещается в клетки. Например, раствор Рингер-лактат (осмоляльность 273 мОсм/кг) умеренно гипотоничен по сравнению с плазмой крови. Каждый литр этого раствора содержит 114 мл свободной воды. В противоположность гопотоническим, гипертонические растворы создают гиперосмолярность, тем самым увеличивают ОЦК. Например, 300 мл 7,5% NaCl увеличивает ОЦК на 1000 мл за счет привлечения в сосудистое русло тканевой жидкости (22). Растворы глюкозы являются водными и предназначены в основном для восполнения внутриклеточного сектора и энергообеспечения. После метаболизма глюкозы, вода раствора распределяется между всеми водными секторами равномерно. Но учитывая, что внутриклеточный сектор составляет 2/3 общей воды организма, в плазме крови остается мизерное количество раствора. Применение растворов глюкозы, при нарушениях мозгового кровообращения и хирургических вмешательствах, в настоящее время не рекомендуется, поскольку они усугубляют ацидоз в тканях головного мозга Инфузионные жидкости, не содержащие физиологическое буферное основание бикарбонат, создают дилюционный ацидоз, поскольку вливание подобного раствора уменьшает концентрацию HCO3- (буферного основания) во всем внеклеточном пространстве, тогда как парциальное давление CO2 (буферной кислоты) остается постоянным. Разбавление может быть изоволемическим (нормоволемическим), т. е. HCO3- теряется вместе с кровью, а восстановление крови или внеклеточного жидкостного объема до нормального происходит путем добавления раствора, не содержащего HCO3- , или гиперволемическим, когда внеклеточный жидкостный объем расширяется с помощью раствора без бикарбоната с возникновением гиперволемии. Резюмируя вышесказанное, дилюционный ацидоз предсказуем и определяется как ятрогенное нарушение, вызываемое разбавлением бикарбоната во всем внеклеточном пространстве, которое может быть связано с гиперхлоремией или гипохлоремией в зависимости от того, была ли гемодилюция вызвана вливанием гиперхлоремического или гипохлоремического раствора . Поскольку бикарбонат с трудом можно поддерживать в стабильном состоянии в обычных инфузионных растворах или хранить во флаконах, в большинстве растворов он был заменен так называемыми предшественниками бикарбоната. Кроме того, бикарбонат натрия нельзя использовать в инфузионных растворах, содержащих кальций, или смешивать с ним, поскольку быстро образуется осадок карбоната кальция. Дилюционный ацидоз можно предотвратить, используя адекватные концентрации предшественников бикарбоната - метаболизируемых анионов для замещения HCO3- . В качестве метаболизируемых оснований (носителей резервной щелочности) могут использоваться следующие анионы органических кислот: ацетат (уксусная кислота), лактат (молочная кислота), глюконат (глюкуроновая кислота), малат (яблочная кислота) и цитрат (лимонная кислота). Поглощая в процессе метаболизма ионы H+ и кислород, эти анионы метаболизируются в неповрежденной печени (в основном лактат) или в мышцах (в основном ацетат и малат) с получением HCO3- . При pH 7,40 угольная кислота (H2CO3) является единственным источником ионов H+ для организма (при поступлении в низкой концентрации 1,2 ммоль/л, H2CO3 может свободно синтезироваться из CO2 + H2O). Следовательно, HCO3- высвобождается в эквимолярных количествах. Из каждого моля окисленного ацетата, глюконата или лактата получается один моль бикарбоната, тогда как при окислении каждого моля малата или цитрата получается 2 или 3 моля бикарбоната соответственно. Если инфузионная жидкость содержит метаболизируемые анионы в концентрациях, превышающих недостаток бикарбоната, вероятным последствием будет инфузионно-индуцированный алкалоз, называемый реактивным алкалозом. Метаболический алкалоз всегда ятрогенный. В хирургии посттравматический алкалоз считается ятрогенным (25): из 1414 пациентов в тяжелом состоянии 12,5% имели артериальное pH более 7,55. Алкалоз является достаточно частым нарушением кислотно-основного баланса: 66% всех нарушений кислотно-основного баланса представляют собой метаболический или сочетание метаболического и респираторного ятрогенного алкалоза. При pH 7,58 или выше смертность среди этих пациентов составляет приблизительно 50% (26). Коллоидные растворы хорошо возмещают ОЦП при нормальной проницаемости стенок капилляров. Каждый грамм введенного коллоида добавляет в кровоток примерно 20 мл воды (14-15 мл на 1 грамм альбумина, 16-17 мл на 1 грамм гидроксиэтилированного крахмала, 20-25 мл на 1 грамм декстрана) (27,28,29,30). После уравнивания онкотического давления возмещение ОЦП в первую очередь определяется дозой введенного коллоида в граммах, а не объемом и концентрацией вводимого раствора. Наиболее часто используемые кристаллоидные растворы 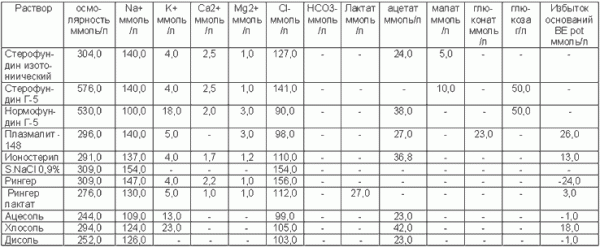 Фармакологические характеристики ГЭК  При назначении препаратов ГЭК необходимо учитывать некоторые физико-химические характеристики. Чем ниже молекулярный вес и чем больше в полидисперсном препарате находится низкомолекулярных фракций, тем выше коллоидно-осмотическое давление. Молярное замещение (Ms) представляет собой среднее число гидроксильных групп, приходящихся на глюкозную единицу (в молекуле ГЭК). Например, Ms рефортана - 0.5. Это означает, что на 10 молекул глюкозы приходится 5 гидроксиэтиловых групп. Чем больше молярное замещение, тем дольше продолжается эффект замещения внутрисосудистого объема. Препараты среднемолекулярные низкозамещенные 130000 Д (степень замещения 0,4) называются тетракрахмалами (Tetrastarch). Препараты со средней молекулярной массой 200000 Д и степенью замещения 0,5 были отнесены к фармакологической группе "Pentastarch", а препараты с высокой молекулярной массой 450000 Д и степенью замещения 0,7 - к фармакологической группе "Hetastarch" (31, 32, 33, 34, 35). Действие ГЭК по возмещению внутрисосудистого объема жидкости основано на выраженной способности связывать воду. В количественном отношении это зависит от концентрации ГЭК. Один грамм 10% ГЭК, способен связать 12-14 мл воды, у 6%-ного ГЭК - 8-10 мл на 1 г. Растворы ГЭК способны "запечатывать" поры в эндотелии, появляющиеся при разных формах его повреждений (36, 37). Коллоиды или кристаллоиды в периоперационном периоде. Единого мнения, какие растворы - коллоидные или кристаллоидные - назначать хирургическим больным, нет. Одни специалисты считают, что коллоидные растворы более эффективно восстанавливают ОЦК и сердечный выброс благадоря поддержанию онкотического давления плазмы (38,39,40,41). Другие утверждают, что кристаллоидные растворы не менее эффективны при инфузии в достаточном объеме (42,43,44,45). Опасения, что при повышенной проницаемости легочных капилляров коллоидные растворы способствуют развитию отека легких, оказались не обоснованными, поскольку онкотическое давление плазмы и легочного интерстиция одинаково. Приемущества и недостатки коллоидов и кристаллоидов  По данным мета-анализа восьми рандомизированных клинических исследований сравнения инфузионной терапии с применением коллоидов или кристаллоидов, выяснилось, что разница в смертности у больных травматологического профиля составила 12.3% (больше в группе где применяли коллоидные растворы), и 7,8% (больше в группе, где применяли кристаллоиды) у больных без травм. Был сделан вывод, что у больных с заведомо повышенной проницаемостью капилляров назначение коллоидов может быть опасным, во всех остальных случаях оно эффективно. На большем количестве экспериментальных моделей и в клинических исследованиях не была получена четкая связь между коллоидно-онкотическим давлением, видом вводимого раствора и количеством внесосудистой воды в легких (46). Основные аргументы в пользу выбора того или иного раствора должны основываться на правильной интерпритации различных показателей, характеризующих данную клиническую ситуацию,и сопоставимость с ней физико-химических свойств препарата: Критерии выбора растворов для инфузионной терапии: проницаемость эндотелия, транспорт кислорода, факторы свертывания, онкотическое давление, отек тканей, баланс электролитов, кислотно-основное состояние, метаболизм глюкозы, мозговые нарушения. В недавних публикациях об использовании кристаллоидов и коллоидов для жидкостной терапии, включая человеческий альбумин, оценивается и пересматривается. В последний год использование альбумина как средства для реанимационной инфузии стало оспариваться. В системном обзоре сообщается, что риск смерти пациента в леченой альбумином группе выше чем в сравниваемой группе. Этот обзор предполагает, что терапия альбумином критических больных пациентов увеличивает летальность. Однако данный мета-анализ имеет ряд методологических слабостей, что ограничивает значение некоторых выводов из его данных. Влияние инфузионных растворов на систему гемостаза При длительных хирургических вмешательствах, когда объем и качество инфузионной терапии имеет принципиальное значение, а так же у пациентов с заболеваниями крови, необходимо считаться с влиянием инфузионных растворов, прежде всего синтетических коллоидов на систему гемостаза. В настоящее время известно несколько механизмов гемостазиологического действия инфузионных растворов: 1. Гемодилюция - или снижение концентрации факторов свертывания, компонентов, определяющих противосвертывающие механизмы, белков системы фибринолиза и форменных элементов крови за счет простого разведения. Действию гемодилюции подвержены все компоненты системы гемостаза, однако, клинически данный механизм наименее значим. 2. Непосредственное взаимодействие с мембранами тромбоцитов, клетками эндотелия сосудов или, так называемый, "силиконизирующий" эффект - механизм, в большей степени характерный для декстрана. Проявляется в образовании пленки из молекул кровезаменителя на поверхности тромбоцитов и эндотелиоцитов. Такая пленка значимо ослабляет межклеточные взаимодействия. 3. Специфическое взаимодействие с факторами свертывания крови и другими компонентами системы гемостаза. Данный механизм, обуславливает наибольшее повреждающее действие синтетических коллоидов на систему гемостаза. Синтетические коллоиды способны активировать фибринолиз за счет угнетения эндогенных антифибринолитиков. На молекулярном уровне плазмозаменители связываются с фибронектином и благодаря образованию подобного комплекса, получают возможность встраиваться в структуру сгустка. При этом, тромбообразование ускоряется, но образующийся тромб получается более рыхлым и легче подвергается деструкции. Т.е. за счет данного механизма, по сути реализуются три эффекта: гипокоагуляционный - за счет снижения активности VIII фактора свертывания, фибринолитический - за счет угнетения эндогенных антифибринолитиков и гиперкоагуляционный - за счет взаимодействия с плазмином. |
