2Техникоэкономическое обоснование
 Скачать 1.69 Mb. Скачать 1.69 Mb.
|
|
4.Теоретические основы физико – химических процессов в производстве ситаллов Технология ситаллов включает стадии варки стекла, формовки изделий специальной термической обработки. Процесс стекловарения протекает в сложной обстановке, создаваемой рядом химических, физических и технологических факторов. реальных производственных условиях отдельные этапы этого процесса трудно выделить изолированно. Однако для ясного освоения процесса стекловарения в целом, знание элементов, из которых он слагается, необходимо и важно. Процесс варки стекла состоит из пяти стадий. Первая стадия - силикатообразование –характеризуется тем, что концу ее: а) в шихте не остается отдельных составляющих ее компонентов (нет отдельно песка, соды, сульфаты, мела и пр.); б) большинство газообразных шихты улетучивается; в) основные химические реакции в твердом состоянии между компонентами шихты закончены. Для обычных натриево- кальциевых стекол эта стадия завершается при 800-9000. Фриттованные шихты, которые практиковалось в древности и рекомендовалось еще в прошлом веке, есть, собственно говоря, осуществление стадии силикатообразования. Вторая стадия– стеклообразование– характеризуется тем, что к ее концу масса становится прозрачной, т. е. в ней отсутствуют не проваренные частицы шихты, однако она пронизана большим количеством пузырей и свилей, т. е. неоднородна. Для обычных стекол эта стадия завершается при 1150-12000. Третья стадия – осветления – характеризуется тем, что к ее концу стекломасса освобождается от видимых газовых включений, и тем, что устанавливается равновесное состояние между стекломассой (жидкой фазой) газами, остающимися в самой стекломассе (газовая фаза). 16 Для обычных стекол этот этап завершается при 1400 – 15000. Вязкость стекломассы составляет около 100 пуаз. Четвертая стадия – гомогенизация – характеризуется тем, что к ее концу стекломасса освобождается от свилей и становится однородной. Колебания в показателях преломления отдельных частей стекломассы минимальные. Так, в оптическом стекле эти колебания не превышают ±0,0005. Для обычных стекол, эта стадия может быть завершена при температурах, более низких, чем это необходимо для завершения этапа дегазации. Пятая стадия – студка – характеризуется тем, что температура стекломассы снижается на 200 – 300 0 для создания необходимо рабочей вязкости, Каждая из пяти перечисленных стадий процесс стекловарения имеет свои особенности, и для проведения каждой из них существуют свои оптимальные условия. Пути, по которым следует вести практическое стекловарения, должны быть основаны на теории стеклообразования. Для того чтобы эта теория полное вскрыла все стороны вопроса, необходимо детально разобрать: Явления химического, физического и физика – химического порядка, происходящие в процессе стеклообразования, т.е.: а) химическая реакция, протекающие при нагревании в отдельных стеклообразующих компонентах и их смеси; б) термофизику процессов, т.е. физические состояние отдельных стеклообразующих компонентов и смесей при их нагревании; в) физика – химические взаимодействия в стекломассе, а также между стекломассой и атмосферной печи и между стекломассой и огнеупором; влияние различных факторов, ускоряющих процесс стеклообразования на отдельных его этапах и в целом. 17 Все явления, происходящие в процессе стеклообразования, классифицируют следующим образом (это классификация было предложна в 1920 г. В. Тернером). Физические изменения: испарения влаги; нагревания шихты; плавление отдельных ее компонентов; растворение веществ в твердом или жидком состоянии в уже образовавшейся жидкости; изменения кристаллической формы; улетучивание некоторых составных частей. Химическая реакции расщепления гидратов; удаление химически связной воды; разложение карбонатов, сульфатов, нитратов и перекисей; взаимодействие различных компонентов и образования силикатов. Физикo – химические процессы взаимодействие между стекломассой и газообразными компонентами атмосферы печи; взаимодействие между стекломассой и включенными в ее газами; взаимодействия между газовой фазой стекломассы и газовой фазой пузырей, включенных ы стекломассу; взаимодействия между газами печи и газами, включенными в стекломассе и пузырях, пронизывающих ее; взаимодействия между стекломассой и огнеупором. Процесс кристаллизации. Главной в технологии ситаллов является стадия кристаллизации. Кристаллизация представляет собой двух стадийный процесс термообработки. Процесс кристаллизации стекла протекает в две стадии: образование центров кристаллизации (зародышей) и рост кристаллов на них. 18 Первая стадия - образования центров кристаллизации - осуществляется для большинства составов шихт выдержкой при температуре, оптимальной для этого процесса. С понижением температуры расплава растет число центров кристаллизации, однако после достижения наибольшего значения при определенной температуре скорость образования кристаллов падает до нуля. Практически температурный интервал кристаллизации расплава стекла ограничивается нижним пределом температур, при котором появляются первые кристаллы, и верхним, при котором кристаллы растворяются.Для фотоситаллов изделия после отжига облучают ультрафиолетовыми, рентгеновскими или - лучами. Проявление скрытого изображения происходит при нагревании стекол в интервале между температурой размягчения и отжига в течение 8 - 60 мин. Далее термообработка продолжается при более высоких температурах для завершения процесса кристаллизации и получения ситалла. На второй стадии изделия отжигают при температуре, наиболее благоприятной для роста кристаллов. При производстве стеклокристаллических материалов важную роль играет правильный выбор вида и количества каталитической добавки. Эффективность действия катализатора кристаллизации во многом зависит от химического состава исходного стекла. Наибольшее применение на практике нашли сульфидные и фторидные катализаторы, а также оксиды хрома. При производстве шлакоситалла белого цвета на основе доменных шлаков в качестве катализатора применяют сульфид цинка ZnS, при условии, что в стекле содержание СаО не превышает 34 - 35 %, а Al2O3 — 8,5 - 9,5 % по массе. При получении темно-серых шлакоситаллов используют комбинированный катализатор FeS + MnS при содержании в стекле СаО до 35 - 36 %, Al2O3 - 14 - 14,5 % по массе. 19 Шлакоситаллы благодаря их высокой прочности, химической стойкости применяют в строительстве, химической, горнорудной, электротехнической и других отраслях промышленности. Фториды применяют как глушители стекла, но фтор может быть использован и в качестве катализатора кристаллизации для стекол, содержание СаО в которых не превышает 21 % и Al2O3 не выше 10 ... 12 % по массе. Оксид хрома Cr2O3 чаще всего применяют в качестве катализатора для стекол, которые наряду с СаО содержат свыше 5 % по массе MgO. Технические ситаллы получают на основе искусственных шихт тех частей силикатных систем, в которых кристаллизуются фазы, обладающие заданными свойствами. Для термостойких ситаллов такими фазами являются кордиерит, сподумен LiAlSi2O6, эвкриптит LiAlSiO4; для высокопрочных - шпинель, муллит; для диэлектриков -кордиерит, диопсид, волластонит и т.д. Такие свойства, как плотность, коэффициент термического расширения, теплопроводность, модуль упругости и диэлектрическая проницаемость зависят от свойств фаз и аддитивно меняются с изменением содержаний этих фаз. Поэтому важнейшую задачу технической петрологии составляет изучение диаграмм состояния соответствующих систем. На фазовый состав ситаллов влияют малые (до 1,5%) добавки модификаторов (Na, K, Ca, Ba и др.), стеклообразователей (В, Р и др.) и окислов промежуточного типа, введение которых не меняет состав основных фаз, но заметно увеличивает или снижает их содержание. Необходимыми добавками являются вещества, служащие катализаторами и центрами кристаллизации стекол. 20 5.Характеристика сырьевых материалов и предъявляемые к ним требования. Характеристика сырьевых материалов, подлежащих входному контролю приведена в таблице 4
21 Расчет материального баланса. Расчёт материального баланса для производства бытового стеклокристаллического материала специального назначения. Для получения кордиеритовых ситаллов в качестве катализатора кристаллизации возможно использование TiO2 в количестве (масс.%) - от 0 до 15, оптимально – более 8; ZrO2 – более 6 или комплексы соединений TiO2 (0-10%) + ZrO2 (0-5 %); TiO2 + ZrO2 + SnO2 – около 6 %. Введение TiO2 менее 8 моль % нецелесообразно, так как при кристаллизации формируется крупнокристаллическая структура. Применение Cr2O3 в количестве до 0,5% приводит к образованию ситаллов энстатитового состава. Для получения ситаллов кордиеритового состава были выбраны местные сырьевые материалы - талько-магнезит Зинельбулакского месторождения и обогащенный каолин АКF-78 Ангренского месторождения. Химический состав сырьевых материалов приведен в таблице 5. Таблица 5. Химический состав сырьевых материалов и стекла.
Теоретический химический состав кордиерита следующий: MgO-13,7; Al2O3-34,9; SiO2 – 51,4 мас.%. Однако кордиерит кристаллизуется при химических составах в диапазоне: MgO-12-14,7; Al2O3-30,00-34,90; SiO2 – 51,40-55,00 мас.%. Рассчитаем количество каждого сырьевого материала, необходимое для обеспечения теоретического химического состава кордиерита. Приведем химический состав талька с 100%. 22
FeO 2.08 – 99.57% х = 2,09% FeO x – 100%
Тальк был приведен к 100%. 23 таблице 6 приведен химический состав сырьевых материалов, приведённый к 100%. Таблица6. Химический состав сырьевых материалов, приведенный к 100%
Задан шихтовый состав материала: Тальк – 41,75%, каолин – 76,61%. Необходимо определить содержание оксидов элементов и сравнить с химический формулы кордиерита. SiO2
x – 41.75%
Na2O 0.50 – 100% x=0.38% Na2O x – 76.61% п.п.п 12,87 – 100% x=9.85% п.п.п x – 76.61% Таблица 7. Химический состав ситалла 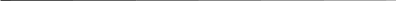   
           Данный химический состав ситалла соответствует составу кордиерита.  Катализатор кристаллизации – TiO2 добавляется свыше 100% в качестве 4%. Для производства 60т стекломассы в сутки необходимы следующие сырьевые материалы: Тальк – 24,96 т каолин – 46,08 т оксид титана – 2,4 т Потери при варки стекла (при расчете на 100%) Тальк – 41,75% Каолин – 76,61% 41,75+76,61=118,4т 118,4 т – 100 т =18,4т Потери при варке 60т стекломассы 100 т – 18,4 т 60 т – х х=11,04 т потери 26 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
