|
|
Окислительно-восстановительной реакцией является
|
Cо щелочами реагирует оксид
|
При взаимодействии Са + Н2О образуется
|
Царская водка – это
|
Химические процессы, протекающие с поглощением теплоты, называются
|
Энтальпия – это
|
Формулировка «энтропия идеального кристалла чистого вещества при 0 К равна нулю» относится к
|
Энергия Гиббса – это термодинамический потенциал в
|
Формулировка «тепловой эффект химической реакции зависит от состояния исходных веществ и продуктов реакции, но не зависит от пути реакции и ее промежуточных стадий» относится к
|
Изобарическим называется процесс, протекающий в системе при постоянном
|
Уравнение Q=dU+W является математическим выражением
|
Изменение энтропии для реакции: NH3 (газ.) + HCl(газ.) = NH4Cl (тв.)
|
Неэлектролитами являются
|
Свойство растворов, являющееся коллигативным
|
Нормальная концен-трация есть отношение
|
Мольная доля есть отношение |
Молярная концентрация есть отношение
|
Процентная концентрация есть отношение
|
50% раствор H2SO4 содержит
|
1 М раствор едкого натра содержит (объем 1 л)
|
1 N раствор соляной кислоты содержит
|
Осмосом называют |
Раствор содержит 10 г Na2SO3 и 90 г воды. Какова процентная концентрация раствора?
|
Дана реакция: H2 + J2 = 2HJ. Написать выражение для скорости прямой реакции.
|
Константа равновесия химической реакции: СО2 + С = 2СО имеет вид
|
Возможные степени окисления Сl
|
Элемент, имеющий степень окисления,равной ( -2 )
|
К группе благородных газов не относится
|
Повышение температуры кипения раствора можно найти как
|
Закон Рауля формулируется следующим образом
|
Жесткость воды обусловлена присутствием ионов:
|
Возможные степени окисления Fe
|
Степень окисления кислорода в молекуле озона
|
Один из продуктов реакции KMnO4+MnSO4+ +H2O=
|
Один из продуктов реакции KMnO4+Na2SO3+ +KOH=
|
Ионное произведение чистой воды при 250 С равно
|
Водородный показатель (рН) - это
|
При взаимодействии концентрированной H2SO4 c Cu образуется
|
На титрование 10 мл кислоты израсходовали 20 мл 0,5 N раствора щелочи. Какова концентрация кислоты?
|
Роданид аммония - это
|
рН раствора серной кислоты:
|
Лакмус в кислой среде
|
Фенолфталеин в щелочной среде
|
Сусальное золото- это
|
Закон сохранения массы гласит, что в ходе химической реакции остается постоянной
|
В первой половине XVIII века увеличение массы металла после прокаливания на воздухе объясняли
|
Гашеная известь - это
|
Эквивалентная масса карбоната натрия в реакции: Na2CO3 + HCl = NaHCO3 + NaCl равна
|
В каком из этих соединений больше доля водорода
|
Максимальная степень окисления железа равна
|
Бор использовал в своей модели атома
|
Главное квантовое число может принимать значения
|
Орбитальное квантовое число может принимать значения
|
Магнитное квантовое число может принимать значения
|
Спиновое квантовое число может принимать значения
|
П
Влад
орядок заполнения электронами орбиталей атома определяется принципами
|
I правило Клечковского правило Клечковского
|
Атом поглощает или излучает энергию при
|
Физический смысл орбитального квантового числа (АО – атомная орбиталь)
|
Правило Хунда
|
Символы только
d – элементов расположены в ряду
|
Для какого металла в основном состоянии имеет место «провал» электрона типа: 1e 4s → 3d
|
Число неспаренных электронов в атоме золота равно
|
Амминокомплексом является
|
Элементом с конфигурацией внешнего слоя 3d104s1 является
|
Невозможна следующая конфигурация в атоме
|
Молекула HF образована следующей химической связью
|
В ряду элементов Li, Be, B, C, N, O, F Электроотрицательность
|
Химическая кинетика – это наука
|
Кинетическое уравнение химической реакции записывается в следующем виде:
|
Термодинамика есть наука, изучающая
|
Закон Гесса необходим для
|
При р, Т = const изменение энергии Гиббса вычисляется по формуле:
|
С увеличением температуры энтропия:
|
Пара следующих ионов может находиться совместно в растворе
|
Соль, гидролизующаяся только по катиону
|
Растворимость – это концентрация раствора
|
Нормальность – это, содержащееся в 1 л раствора количество
|
10 мл 0,2 N H2SO4 реагирует с 5 мл гидроксида натрия. Какова нормальная концентрация щелочи?
|
Моляльная концентрация измеряется в
|
Если смешать 35 г калийной селитры и 65 г воды, какова массовая доля KNO3 в растворе:
|
Константа равновесия равна
|
Константа скорости реакции зависит от
|
Осмос – это проникновение через полупронецаемую перегородку в раствор
|
Следующие электролиты при диссоциации в водном растворе образуют ионы водорода:
|
Равновесие процесса N2 + 3H2 2NH3 при повышении давления сместится в сторону
|
Раствор отличается от химического соединения
|
Растворитель-это компонент раствора
|
Электролиты - это
|
По величине степени диссоциации электролиты делятся
|
Сильной кислотой является
|
Для слабых бинарных электролитов выражение 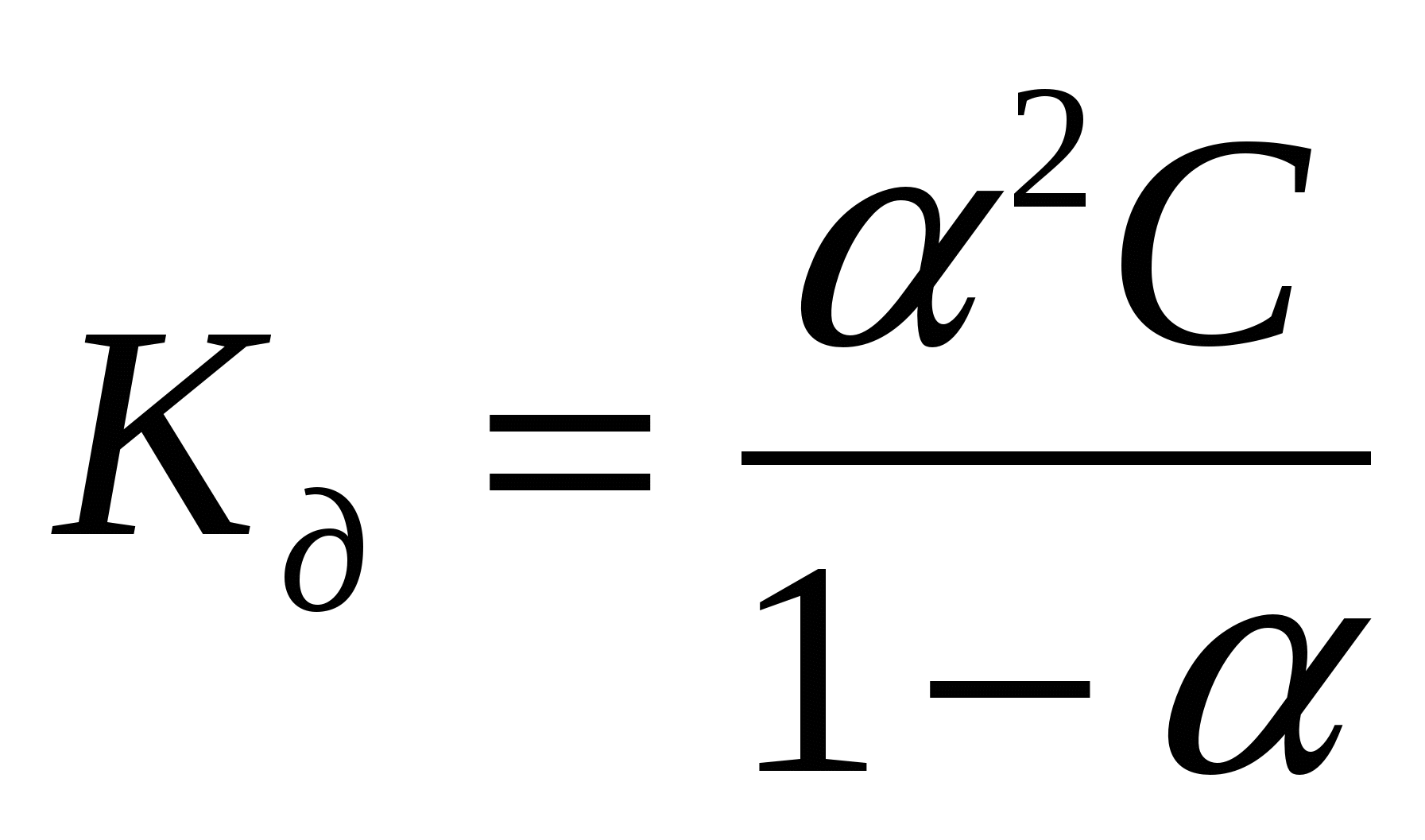 носит название носит название
|
При 250С константа диссоциации уксусной кислоты равна 1,810-5. Степень диссоциации кислоты в 1 N водном растворе равна
|
Из приведенных электролитов выберите самый слабый
|
Ионное произведение воды равно
|
Индикаторы – это
|
Фенолфталеин в щелочной среде имеет цвет
|
Окраска лакмуса в щелочной среде
|
Значение рН щелочного раствора рассчитывают по формуле
|
рН в 0,0001 N растворе гидроксида калия равен:
|
Среда водного раствора, водородный показатель которого рН = 13,0
|
Диссоциация ортофосфорной кислоты по второй ступени описывается уравнением
|
В растворе хлорида цинка среда
|
Электролиз - это
|
Коррозия - это
|
Изменение температуры кипения раствора рассчитывается по формуле:
|
Восстановителем является
|
Марганец восстанавливается по схеме Mn+7+5e=Mn+2
|
Укажите, какие из приведенных процессов представляют собой окисление
|
В нейтральной среде взаимодействие KMnO4 с Na2SO3 приводит к образованию:
|
Из KMnO4 в результате реакции KMnO4+FeSO4+H2SO4 образуется следующее вещество
|
В результате реакции K2Cr2O7+Na2SO3+H2SO4 образуется следующее вещество
|
В результате реакции Cu+HNO3(k) образуется следующее вещество
|
Наиболее характерные степени окисления для железа
|
Уравнение Нернста для электродов I рода
|
Царская водка - это
|
Малахит - это
|
Горная порода доломит, химический состав которого соответствует формуле CaMg(CO3)2, относится к классу:
|
Гидроксосульфат свинца -это
|
Сульфидом Na является соединение
|
Перманганатом калия является соединение
|
Цианидом калия является соединение
|
Ангидридом какой кислоты является Cl2O7 ?
|
Карбонатом Mg является
|
Из перечисленных соединений кристаллогидратом является
|
Эквивалентная масса едкого натра равна
|
Кислотным оксидом является
|
Степень окисления P в ряду соединений P2O5, P, H3PO4 равна
|
Из перечисленных соединений к кислотам относятся
|
Из перечисленных соединений к солям относятся
|
Гидроксохлорид меди (II) – это
|
Эквивалентная масса кислоты зависит от
|
Эквивалентная масса водорода (г/моль)
|
Эквивалентная масса оксида элемента составляет 27. Чему равна эквивалентная масса элемента?
|
Амфотерным не является оксид
|
Жесткость воды обусловлена наличием солей
|
Параметр, характеризующий собственный магнитный момент электрона
|
Формулировка «электрон может вращаться вокруг ядра только по определенным орбитам» относится к
|
Какая из перечисленных электронных конфигураций возможна?
|
Среди перечисленных реакцией гидролиза является
|
Кислую реакцию имеет раствор
|
В присутствии основания лакмус становится
|
Щелочную реакцию имеет раствор
|
Среди перечисленных реакцией нейтрализации является
|
Окислительно-восстановительной реакцией является
|
Cо щелочами реагирует оксид
|
При взаимодействии Са + Н2О→ образуется
|
Царская водка – это
|
Формулировка «энтропия идеального кристалла чистого вещества при 0 К равна нулю» относится к
|
Энергия Гиббса – это термодинамический потенциал в
|
Изобарическим называется процесс, протекающий в системе при постоянном
|
Размерность энтропии
|
Изменение энтропии для реакции: NH3 (газ.) + HCl(газ.) = NH4Cl (тв.) равно:
|
Неэлектролитами являются
|
Нормальная концентрация есть отношение
|
Моляльная концентрация есть отношение
|
Мольная доля есть отношение
|
Молярная концентрация есть отношение
|
1 М раствор едкого натра содержит (объем 1 л)
|
Осмосом называют
|
Раствор содержит 10 г Na2SO3 и 90 г воды. Какова процентная концентрация раствора?
|
К |
 Скачать 3.08 Mb.
Скачать 3.08 Mb.
 правило Клечковского
правило Клечковского