Билет 1 биологическое окисление
 Скачать 1.13 Mb. Скачать 1.13 Mb.
|
|
| название | ферменты | активатор | ингибитор |
| гликолиз | Гексокиназа Фосфофруктокиназа Пируваткиназа | Гл-6-фосф Атф,цитрат Атф,аланин | Амф, фр 2-6-бифосф Фр 1-6 дифосф |
| глюконеогенз | Пируваткарбоксилаза Фосфоенолпируваткарбоксилаза Фруктозо 1-6 дифосфатаза | Адф Адф Амф, фр 2-6 бифосф | Ацитилкоа Ацетилкоа Цитрат, атф |
3(33)
Жирные кислоты - структурные компоненты липидов. В составе триацилглицеролов жирные кислоты выполняют функцию депонирования энергии. В составе фосфолипидов и сфинголипидов жирные кислоты образуют внутренний гидрофобный слой мембран.
ЖК липидов человека представляют собой углеводородную неразветвлённую цепь, на одном конце которой находится карбоксильная группа, а на другом - метальная группа.Большинство жирных кислот в организме содержат чётное число атомов углерода - от 16 до 20). Жирные кислоты, не содержащие двойных связей, называют насыщенными. Основной насыщенной жирной кислотой в липидах человека является пальмитиновая (до 30-35%). Жирные кислоты, содержащие двойные связи, называют ненасыщенными. Ненасыщенные жирные кислоты представлены моноеновыми и полиеновыми. Если в составе жирной кислоты содержатся две и более двойных связей, то они располагаются через СН2-группу. Имеется несколько способов изображения структуры жирных кислот. При обозначении жирной кислоты цифровым символом общее количество атомов углерода представлено цифрой до двоеточия, после двоеточия указывают число двойных связей. Позицию двойной связи обозначают знаком Δ, после которого указывают номер атома углерода, ближайшего к карбоксилу, у которого находится двойная связь. Позиция двойной связи может быть указана по расположению первой двойной связи, считая от метального со-атома углерода жирной кислоты. Например, линоле-вая кислота может быть обозначена как С18:2Δ9,12 или С18:2ω-6. По положению первой двойной связи от метального углерода полиеновые жирные кислоты делят на семейства ω-3 и ω-6. Двойные связи в жирных кислотах в организме человека имеют цис-конфигурацию Большинство жирных кислот синтезируется в организме человека, однако полиеновые кислоты
(линолевая и α-линоленовая) не синтезируются и должны поступать с пищей. Эти жирные кислоты называют эссенциальными.
триацилглицеролы
Ацилглицеролы - сложные эфиры трёхатомного спирта глицерола и жирных кислот. в организме человека приобладаютют триацилглицеролы . У человека с массой тела 70 кг в норме содержится до 10 кг жиров. Они запасаются в адипоцитах и используются при голодании как источники энергии.
в позициях 1 и 3 находятся более насыщенные жирные кислоты, а во второй позиции - полиеновая кислота.
Жиры, содержащие преимущественно насыщенные кислоты, являются твёрдыми (говяжий, бараний жиры), а содержащие большое количество ненасыщенных кислот – жидкими(растительные масла)
Различают простые и смешанные триацилглицерины. Простые — содержат остатки одинаковых ВЖК, а смешанные — остатки различных кислот.
Билет №14
1(4) Дыхательная цепь — система структурно и функционально связанных трансмембранных белков и переносчиков электронов. Она позволяет запасти энергию, выделяющуюся в ходе окисления НАД∙Н и ФАДН2 молекулярным кислородом (в случае аэробного дыхания) или иными веществами (в случае анаэробного) в форме трансмембранного протонного потенциала за счёт последовательного переноса электрона по цепи, сопряжённого с перекачкой протонов через мембрану.
Организация дыхательной цепи в митохондриях
Основные переносчики электронов встроены во внутреннюю мембрану митохондрий и организованы в 4 комплекса, расположенных в определённой последовательности . В этой последовательности их стандартные о-в потенциалы становятся более положительными по мере приближения к кислороду.
Каждое звено этой цепи специфично в отношении донора и акцептора электронов.
На первом этапе дегидрогеназы катализируют отщепление водорода от различных субстратов. Если субстратами служат а-гидрокси-кислоты малат, изоцитрат, 3-гидроксибутират, водород переносится на NAD+. Образовавшийся NADH в дыхательной цепи, в свою очередь, окисляется NADH-дегидрогеназой (комплекс I).
Если субстратом служат такие соединения, как сукцинат или глицерол-3-фосфат, акцептором водорода служат FAD-зависимые дегидрогеназы. От NADH и FADH2 электроны и протоны передаются на убихинон и далее через цепь цитохромов к молекулярному кислороду.
До сих пор точно неизвестно, каким образом расположены все переносчики электронов дыхательной цепи. Однако установлено, что в расположении дыхательных комплексов существует определённая асимметрия: некоторые из белков-переносчиков находятся ближе к той стороне внутренней мембраны, которая обращена к матриксу, а другие - к противоположной; некоторые белки пронизывают мембрану насквозь
Комплекс I (НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии.
Комплекс II (Сукцинатдегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината.
Комплекс III (Цитохром bc1 комплекс) переносит электроны с убихинола на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии.Убихинол передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинола и перекачиваются комплексом.
Комплекс IV (Цитохром c оксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов А и А3, которые, помимо гема, содержат ионы меди.
Ингибиторы I комплекса — барбитураты, ротенон, пиерицидин
Ингибитор II комплекса — малонат.
Ингибитор III комплекса — антимицин А, миксотиазол, стигматтелин
Ингибиторы IV комплекса — сероводород, цианиды, угарный газ, оксид азота.
2(25) При анаэробных условиях пировиноградная кислота превращается в молочную кислоту или в этиловый спирт, или в пропионовую кислоту. Этот анаэробный процесс называют еще брожением. В данном случае речь идет о молочнокислом, спиртовом и пропионовом брожении (соответственно). Молочная кислота образуется из пирувата при метаболизме ряда микроорганизмов, а также в клетках мышц многоклеточных организмов. Суммарная реакция превращения глюкозы в лактат имеет следующий вид:
Цикл Кори — совокупность биохимических ферментативных процессов транспорта лактата из мышц в печень, и дальнейшего синтеза глюкозы из лактата, катализируемое ферментами глюконеогенеза.
Биологическое значение:
При интенсивной мышечной работе, а также в условиях отсутствия или недостаточного числа митохондрий глюкоза вступает на путь анаэробного гликолиза с образованием лактата. Лактат не может далее окисляться, он накапливается .С током крови лактат поступает в печень. Печень является основным местом скопления ферментов глюконеогенеза , и лактат идет на синтез глюкозы. Реакция превращения лактата в пируват катализируется лактатдегидрогеназой, далее пируват подвергается окислительному декарбоксилированию или может подвергаться брожению. последовательность называют циклом Кори. обеспечивает утилизацию лактата; 2 предотвращает накопление лактата и лактоацидоз
3(44) .катаболизм ЖК и его этапы.β-Окисление - специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно отделяется по 2 атома углерода в виде ацетил-КоА. Метаболический путь - β-окисление - окисления жирной кислоты происходят у β-углеродного атома только в аэробных условиях.. Реакции β-окисления служат одним из основных источников энергии для синтеза АТФ при окислительном фосфорилировании.
Перед тем, как вступить в различные реакции, жирные кислоты должны быть активированы
RCOOH + HSKoA + АТФ → RCO КоА + АМФ + PPi. фермент ацил-КоАсин-тетаза
Ацил-КоАсинтетазы находятся как в цитозоле, так и в матриксе митохондрий. Эти ферменты отличаются по специфичности к жирным кислотам с различной длиной углеводородной цепи.
Транспорт жирных кислот с длинной углеводородной цепью в митохондриях
β-Окисление жирных кислот, происходит в матриксе митохондрий. Жирные кислоты с длинной углеводородной цепью переносятся через плотную внутреннюю мембрану митохондрий с помощью карнитина. В наружной мембране митохондрий находится фермент карнитинацилтрансфераза 1, катализирующий реакцию с образованием ацилкарнитина. он проходит через межмембранное пространство к наружной стороне внутренней мембраны и транспортируется с помощью карнитинацилкарнитинтранс-локазы на внутреннюю поверхность внутренней мембраны митохондрий, где фермент карнитинацилтрансфераза II катализирует перенос ацила на внутримитохондриальныйКоА . Свободный карнитин возвращается на цитозольную сторону внутренней мембраны митохондрий.
β-Окисление жирных кислот - специфический путь катаболизма жирных кислот, протекающий в матриксе митохондрий заканчивающийся образованием ацетил-КоА. Водород из реакций β-окисления поступает в ЦПЭ, а ацетил-КоА окисляется в цитратном цикле, также поставляющем водород для ЦПЭ.
Регуляция скорости β-окисления его скорость регулируется соотношениями АТФ/АДФ и NADH/NAD Скорость β-окисления в тканях зависит от количества жирных кислот, поступающих в митохондрии. Концентрация свободных жирных кислот в крови повышается при активации липолиза в жировой ткани при голодании под действием глюкагона и при физической работе под действием адреналина. Превращение пирувата, образующегося из глюкозы, в ацетил-КоА замедляется глюкозо-6-фосфат кот, препятствует использованию глюкозы в процессе гликолиза. Скорость завис от активности карнитинацилтрансферазы I

Билет № 15
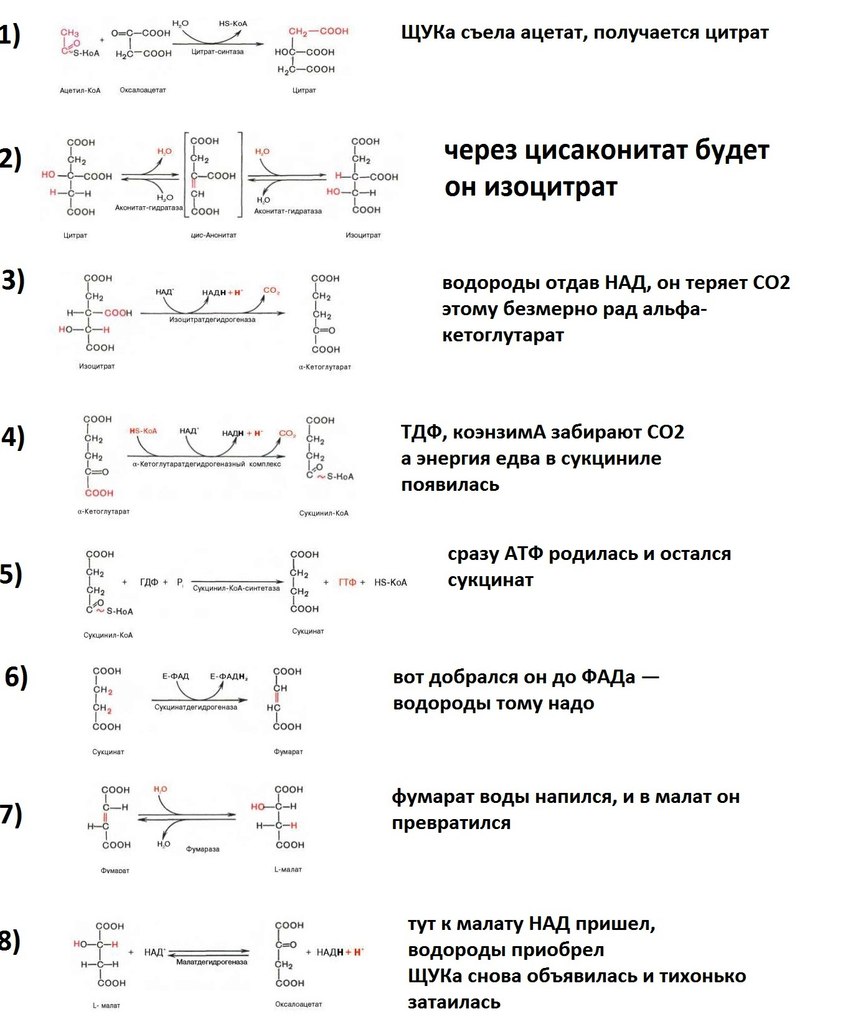
1(13) Ключевые реакции цикла лимонной кислоты
Образование цитрата. В реакции образования цитрата углеродный атом метильной труппы ацетил-КоА связывается с карбонильной группой оксалоацетата (одновременно расщепляется тиоэфирная связь и освобождается коэнзим A . Реакция сопровождается потерей большого количества энергии в виде теплоты. Катализирует реакцию цитрат синтаза, фермент, локализованный в матриксе митохондрий.
Окислительное декарбоксилирование изоцитрата. Эту реакцию катализирует изоцитратдегидрогеназа. Существуют 2 формы изоцитратдегидрогеназы: одна содержит в качестве коферментaNAD+, вторая - NADP+. NAD-зависимый фермент локализован в митохондриях и участвует в ЦТК; NADP-зависимый фермент, присутствующий и в митохондриях, и В) цитоплазме, играет иную метаболическую роль, В результате действия этого фермента на изоцитрат образуется α-кетоглутарат. Реакция, катализируемая NAD-зависимой изоцитратдегидрогеназой, - самая медленная реакция цитратного цикла. АДФ - аллостерический активатор фермента.
Окислительное декарбоксилирование α-кетоглутарата
α-кетоглутарат подвергается окислительному декарбоксилированию с образованием в качестве конечных продуктов сук-цинил-КоА, СО2 и NADH + Н+. В результате этой реакции образуется сукцинил-КоА. Реакцию катализирует α-кетоглутаратдегидрогеназный комплекс, который по структуре и функциям сходен с пируватдегидрогеназным комплексом (ПДК). Подобно ПДК, он состоит из 3 ферментов: α-кетоглутаратдекарбоксилазы, дигидролипоилтранссукцинилазы и дигидролипоилдегидрогеназы. Кроме того, в этот ферментный комплекс входят 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, NAD+ и FAD. она не имеет сложного механизма регуляции, , в этом комплексе отсутствуют регуляторные субъединицы..
Регуляция общего пути катаболизма. 1 - ПДК активируется пируватом, NAD+, КоА; ингибируется NADH и ацетил-КоА; 2 - цитратсинтаза (реакция ускоряется при повышении концентрации оксалоацетата и замедляется при повышении концентрации цитрата, NADH, АТФ и сукцинил-КоА); 3 - изоцитратдегидрогеназа аллостерически активируется АДФ, ионами кальция, ингибируется NADH; 4 - α-кетоглутаратдегидрогеназный комплекс ингибируется NADH, АТФ и сукцинил-КоА, а активируется ионами кальция.
2(23)Глюконеогенез - процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Процесс протекает в основном в печени и менее интенсивно в корковом веществе почек, а также в слизистой оболочке кишечника.
Большинство реакций глюконеогенеза протекает за счёт обратимых реакций гликолиза (реакции 9, 8, 7, 6, 5, 4, 2) и катализируется теми же ферментами. Однако 3 реакции гликолиза термодинамически необратимы.
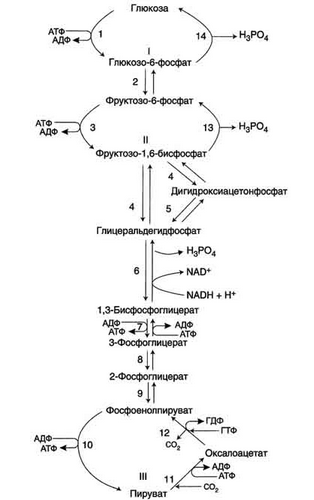
1. Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата.Пируват-карбоксилаза,катализирующая данную реакциюкоферментом которого является биотин. затрата АТФ. Оксалоацетат в митохондриальном матриксе восстанавливается с образованием манатапри участии NADH. В цитозоле малат вновь превращается в оксалоацетат в ходе реакции окисления с участием кофермента NAD+. катализируют малатдегидрогеназа
2. Гидролиз фруктозо-1,6-бисфосфатаи глюкоза-6-фосфата. Отщепление фосфатной группы из фруктозо-1,6-бисфосфата и глюкозо-6-фосфата - также необратимые реакции глюконеогенеза. В ходе гликолиза эти реакции катализируют специфические киназы с затратой АТФ. Ферменты фруктозо-1,6-бисфосфатаза и глюкозо-6-фосфатаза катализируют отщепление фосфатной группы от фруктозо-1,6-бисфосфата и глюкозо-6-фосфата. После чего свободная глюкоза выходит из клетки в кровь
В ходе этого процесса расходуются 6 моль АТФ на синтез 1 моль глюкозы из 2 моль пирувата. Суммарный результат глюконеогенеза из пирувата выражается следующим уравнением:
2 Пируват + 4 АТФ + 2 ГТФ + 2 (NADH + Н+)+ 4 Н20 → Глюкоза + 4 АДФ + 2 ГДФ + 6 H3PO4+ 2 NAD+
3(58) Холестерол - стероид, характерный для животных организмов. основное место синтеза - печень-более 50% х., в тонком кишечнике - 15- 20%, остальной х. синтезируется в коже, коре надпочечников, половых железах. В сутки в организме синтезируется около 1 г х.; с пищей поступает 300-500 мг. функций: входит в состав всех мембран клеток и влияет на их св-ва, исходный субстрат в синтезе жёлчных кислот и стероидных гормонов. Предшественники в метаболическом пути синтеза х. превращаются также в убихинон - компонент дыхательной цепи и долихол, участвующий в синтезе гликопротеинов. за счёт своей гидроксильной группы может образовывать эфиры с жирными кислотами. Этерифицированный х.преобладает в крови. Х. и его эфиры - гидрофобные молекулы, поэтому они транспортируются кровью только в составе разных типов ЛП. Нарушения обмена х. приводят к одному из наиболее распространённых заболеваний - атеросклерозу. Накопление х. в организме приводит к развитию желчнокаменной болезни.
Пути поступления х.: с пищей извне и процесс синтеза собственного х. в печени из ацитилКоА. холестерол поступает в клетки из крови в основном в составе лпнп
Пути использования и выведения х.:вывед с фекалиями, синт Д3, выдел с кожнми покровами, синт стероидн гормонов, синтез и вывед желчных к-т.
Определение содержания общего х. в сыворотке крови: свободный х. образуется при гидролизе эфиров холестерина ферментом холестролэстеразой. Х. окисляют кислородом воздуха с ферментом холестеролоксидазой с образованием перекиси водорода. образуется окрашивание продукта блягодаря окислению перекисью водорода хромогенных субстратов. В ФЭКе измеряют оптическую плотность проб.
Клиническое значение. повышение уровня х. в крови — один из основных факторов риска атеросклероза. Развитие ГЛП может быть обусловлено генетическими аномалиями и факторами среды, а также такими заболеваниями, как сахарный диабет, патология печени, почек, гормональными нарушениями. липидограмма позволяет как диагностировать нарушения липидного обмена, так и оценить риск развития атеросклероза и ишемической болезни сердца.
Норма ХС в крови: Содержание холестерина в крови человека может варьировать от 3,6 ммоль/л до 7,8 ммоль/л.
Оптимальный уровень: менее 5 ммоль/л
Слегка высокий уровень холестерина: между 5 и 6,4 ммоль/л
Умеренно высокий уровень холестерина: между 6,5 и 7,8 ммоль/л
Очень высокий уровень холестерина: выше 7,8 ммоль/л
