Биологические мембраны
 Скачать 1.56 Mb. Скачать 1.56 Mb.
|
особенности строенияи локализации белков в мембранах 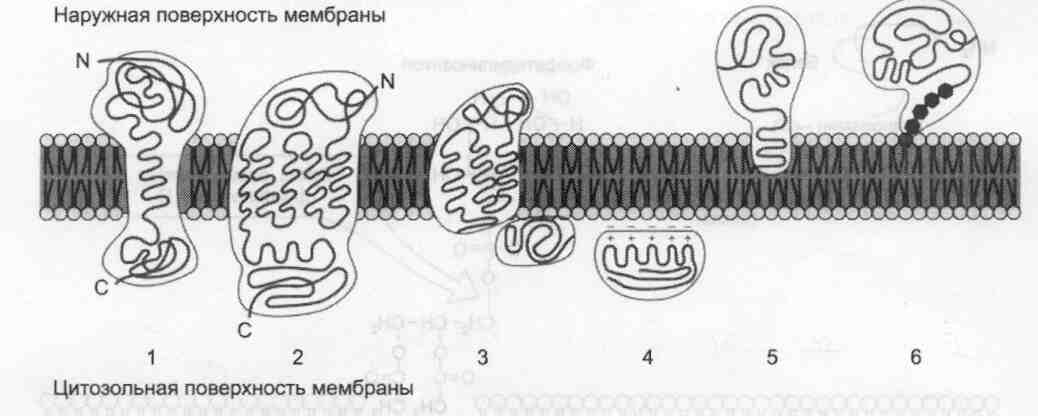 Мембранные белки, контактирующие с гидрофобной частью липидного бислоя, должны быть амфифильными. Те участки белка, которые взаимодействуют с углеводородными цепями жирных кислот, содержат преимущественно неполярные аминокислоты. Участки белка, находящиеся в области полярных «головок», обогащены гидрофильными аминокислотными остатками. Локализация белков в мембранах. Трансмембранные белки, например: 1 — гликофорин А; 2 — рецептор адреналина. Поверхностные белки: 3 — белки, связанные с интегральными белками, например, фермент сукцинатдегидрогеназа; 4 — белки, присоединенные к полярным «головкам» липидного слоя, например, протеинкинаэа С; 5 — белки, -заякоренные» в мембране с помощью короткого гидрофобного концевого домена, например, цитохрои b5;6 — «заякоренные» белки, ковалентно соединённые с пипидом мембраны (например, фермент щелочная фосфатаза). Белки мембран различаются по своему положению в мембране. Они могут глубоко проникать в липидный бислой или даже пронизывать его — интегральные белки, либо разными способами прикрепляться к мембране — поверхностные белки. Поверхностные белки Поверхностные белки часто прикрепляются к мембране, взаимодействуя с интегральными белками или поверхностными участками липидного слоя. Белки, образующие комплексы с интегральными белками мембраны Ряд пищеварительных ферментов, участвующих в гидролизе крахмала и белков, прикрепляется к интегральным белкам мембран микроворсинок кишечника. Примерами таких комплексов могут быть сахараза-изомальтаза и мальтаза-гликоамилаза. Белки, связанные с полярными «головками» липидов мембран Полярные или заряженные домены белковой молекулы могут взаимодействовать с полярными «головками» липидов, образуя ионные и водородные связи. Кроме того, множество растворимых в цитозоле белков при определённых условиях могут связываться с поверхностью мембраны на непродолжительное время. Иногда связывание белка — необходимое условие проявления ферментативной активности. К таким белкам, например, относят протеинкиназу С, факторы свёртывания крови. Закрепление с помощью мембранного «якоря» «Якорем» может быть неполярный домен белка, построенный из аминокислот с гидро- фобными радикалами. Примером такого белка может служить цитохром b5 мембраны ЭР. Этот белок участвует в окислительно-восстановительных реакциях, как переносчик электронов. Роль мембранного «якоря» может выполнять также ковалентно связанный с белком остаток жирной кислоты (миристиновой — С14 или пальмитиновой — С16). Белки, связанные с жирными кислотами, локализованы в основном на внутренней поверхности плазматической мембраны. Миристиновая кислота присоединяется к N-концевому глицину с образованием амидной связи. Пальмитиновая кислота образует тиоэфирную связь с цистеином или слож-ноэфирную с остатками серина и треонина. Небольшая группа белков может взаимодействовать с наружной поверхностью клетки с помощью ковалентно присоединённого к С-концу белка фосфатидилинозитолгликана. Этот «якорь» — часто единственное связующее звено между белком и мембраной, поэтому при действии фосфолипазы С этот белок отделяется от мембраны. Трансмембранные (интегральные) белки Некоторые из трансмембранных белков пронизывают мембрану один раз (гликофорин), другие имеют несколько участков (доменов), последовательно пересекающих бислой. Трансмембранные домены, пронизывающие бислой, имеют конформацию α -спирали. Полярные остатки аминокислот обращены внутрь глобулы, а неполярные контактируют с мембранными липидами. Такие белки называют «вывернутыми» по сравнению с растворимыми в воде белками, в которых большинство гидрофобных остатков аминокислот спрятано внутрь, а гидрофильные располагаются на поверхности. Радикалы заряженных аминокислот в составе этих доменов лишены заряда и протониро-ваны (-СООН) или депротонированы (-NH2). Гликозилированные белки Поверхностные белки или домены интегральных белков, расположенные на наружной поверхности всех мембран, почти всегда гликози-лированы. Олигосахаридные Остатки могут быть присоединены через амидную группу аспараги-на или гидроксильные группы серина и треонина. Олигосахаридные остатки защищают белок от протеолиза, участвуют в узнавании лигандов или адгезии. Латеральная диффузия белков Некоторые мембранные белки перемещаются вдоль бислоя (латеральная диффузия) или поворачиваются вокруг оси, перпендикулярно его поверхности. Латеральная диффузия интегральных белков в мембране ограничена, это связано с их большими размерами, взаимодействием с другими мембранными белками, элементами цитоскелета или внеклеточного матрикса. Белки мембран не совершают перемещений с одной стороны мембраны на другую («флип-флоп» перескоки), подобно фосфолипидам. |
