Диплом жұмысы. дип раб. Дипломная работа Химический эксперимент по неорганической химии в системе проблемного обучения
 Скачать 199.49 Kb. Скачать 199.49 Kb.
|
|
Тема «Металлы» Этот опыт проводится на уроке № 21 (см. тематическое планирование 9 класс) по теме «Соединения алюминия». Цель опыта: изучить химические свойства солей алюминия Форма проведения опыта: фронтальная (демонстрационный эксперимент). Реактивы и оборудование: Na, 10 % раствор сульфата (хлорида) алюминия, фенолфталеин; пробирки, кристаллизатор. Ход опыта: В кристаллизатор с раствором хлорида алюминия и несколькими каплями фенолфталеина поместить небольшой кусочек натрия. Наблюдения: выделение пузырьков газа, розово-малиновое окрашивание раствора и осадка белого цвета. Учитель: натрий – это более активный металл, чем алюминий. Следовательно, натрий должен вытеснять алюминий из растворов его солей по уравнению: 3Na + AlCl3 → Al + 3NaCl Проблема: Согласно этому уравнению реакции мы не должны наблюдать выделение газа и осадка белого цвета. Кроме того, ни полученное по нашей схеме вещество NaCl, ни исходное вещество AlCl3 не имеет щелочной реакции среды (можно для сравнения предложить раствор хлорида натрия и раствор хлорида алюминия с фенолфталеином). То есть, активный металл натрий не вытесняет менее активный алюминий из растворов его солей? Учащиеся: натрий активно реагирует с водой растворяющей хлорид алюминия по уравнению: 2Na + 2 H2O → 2 NaOH + H2↑. Таким образом, мы объясняем выделение газа (водорода). Учитель: как объяснить выделение осадка? Обратимся к таблице растворимости (растворимость исходных и продуктов). Учащиеся: все исходные вещества и предполагаемые продукты реакции растворимы в воде. Учитель: какие ионы имеются в предложенном растворе? Учащиеся: ионы Na+, OH–, Al3+, Cl–. Учитель: запишите возможные уравнения реакций взаимодействия между этими ионами: Учащиеся: Na+ + OH → NaOH; Na+ + Cl– → NaСl; Al3++ 3Cl– → AlСl3; Al3++ 3OH– → Al(OH)3↓ . Таким образом, все вещества находятся в одной пробирке, следовательно, вступать во взаимодействие могут не только исходные вещества, но и продукты их взаимодействия. Учитель: запишем оба уравнения и суммируем их: 2Na + 2 H2O → 2 NaOH + H2↑ 3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl Суммарно: Na + AlCl3 + H2O → Al(OH)3↓ + NaCl + H2↑ Расставим коэффициенты методом электронного баланса: Na0 + AlCl3 + H+2O → Al(OH)3↓ + Na+Cl + H20 ↑ Na0 е– → Na+ 2 2 H+ + 2е– → H20 1 2Na0 + AlCl3 + H+2O → Al(OH)3↓ + 2Na+Cl + H20 ↑ Занятие № 5. Тема: Металлы Приведённые ниже опыты проводятся в 9 классе при изучении темы «Металлы» на уроке № 23 «Генетические ряды Fe2+ и Fe3+» (см. тематическое планирование 9 класс). Цель работы: изучить свойства солей железа (III), как окислителей Форма работы: фронтальная (демонстрационный эксперимент). Реактивы и оборудование: кристаллический хлорид аммония и хлорид железа (Ш), колба Вюрца, известковая вода, лучинка, склянки Дрекселя, спиртовка, индикаторная бумага. Опыт 1. Взаимодействие хлорида железа (III) с хлоридом аммония Хлорид Fe (III) проявляет окислительные свойства по отношению к различным восстановителям. В беседе предшествующей проведению опыта, перед учащимися ставим вопрос: возможно ли химическое взаимодействие между двумя кристаллическими солями хлоридом железа трехвалентного и хлоридом аммония? В поиске ответа на данный вопрос ученики обращаются к таблице растворимости, так как, им известно, что соли взаимодействуют между собой при условии, что они хорошо растворимы, а в результате реакции обмена получается новая нерастворимая соль. В процессе беседы учитель поясняет, что таблицу растворимости в данном случае, при использовании кристаллических вещест, применять нельзя. Таким образом, предварительное обсуждение приводит учащихся к выводу о невозможности химического взаимодействия между указанными веществами. Далее проводим эксперимент. Он представляет интерес не только для выяснения окислительных свойств хлорида железа (III), но и как способ получения азота в лабораторных условиях. Ход опыта: В соответствии с стехиометрическими коэффициентами в уравнении реакции: 6FeCl3 + 2NH4Cl = 6FeCl2 + 8HCl + N2, учитель готовит смесь кристаллических солей хлорида железа (III) и хлорида аммония. Эту смесь помещают в колбу Вюрца, которую соединяют с двумя склянками Дрекселя, заполненными водой (рис. 1). Промывные склянки необходимы для того, чтобы поглотить выделяющийся в ходе реакции хлороводород. Соблюдая технику безопасности, проводят нагревание. Образовавшийся азот можно собрать в 2-3 пробирки над водой. 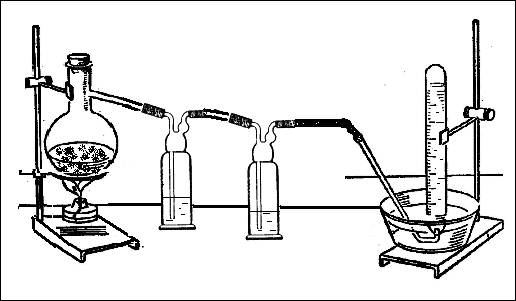 Рис. 1. Взаимодействие хлорида железа (III) с хлоридом аммония Далее проверяем отсутствие примеси хлороводорода, поднеся влажную индикаторную бумагу к отверстию пробирки с азотом. Она не изменяет цвет. Проводим опыт подтверждающий, что собранный газ действительно азот. а) В первую пробирку с азотом опускаем горящую лучинку она гаснет, не оставляя даже раскаленного уголька. б) Во вторую – наливаем известковую воду, в отличие от углекислого газа, известковая вода от азота не мутнеет. Доказав учащимся, что получен азот, отвергаем их мнение о невозможности взаимодействия хлорида железа (III) с хлоридом аммония. Создается проблемная ситуация. Далее ученики должны выдвинуть свои предположения о роли каждого вещества в данной химической реакции. Анализ состава исходных веществ и результатов опыта приводит к выводу, что хлорид железа (III) выступает в роли окислителя, а соль аммония, имея в своем составе атомы азота в низшей степени окисления (– 3), проявляет восстановительные свойства. Подтверждаем этот вывод и напоминаем учащимся другие примеры проявления данными веществами указанных свойств. Затем предлагаем учащимся самостоятельную работу по составлению уравнения окислительно-восстановительной реакции между хлоридом железа (III) и хлоридом аммония. При составлении уравнения реакции учащиеся должны учесть, что один из продуктов реакции хлороводород. 6FeCl3 + 2NH4Cl = 6FeCl2 + 8HCl + N2 Fe3+ + e- ® Fe2+ | 6 2N3- - 6e- ® N20 | 1 Опыт 2. Взаимодействие роданида железа (III) с фосфорной кислотой Этот опыт очень эффектен и может быть использован в процессе эвристической беседы не только при изучении темы «Металлы», но и при рассмотрении качеств реакции на фосфат-ионы. В аналитической химии известна реакция взаимодействия растворимых солей железа (III) с фосфат-ионами, сопровождающаяся образованием желтовато-белого осадка фосфата железа трехвалентного. Этот опыт рекомендуем провести на уроке, как пример качественной реакции на фосфат-ионы и с целью подготовки учащихся к обсуждению проблемного эксперимента. Учитель: будет ли роданид железа (III) взаимодействовать с фосфорной кислотой? Ученики: такая реакция невозможна, поскольку эта соль железа – малодиссоциированное соединение, и ионы железа (III), необходимые для образования осадка фосфата железа (III), в растворе отсутствуют. Реактивы и оборудование: раствор роданида железа (Ш), раствор фосфорной кислоты, пробирки. Ход опыта: Для проведения опыта получен роданид железа (III) путем взаимодействия растворимой соли железа (III) с роданидом калия или аммония. Этому процессу соответствует краткое ионное уравнение реакции. Fe3+ + 3SCN- = Fe(SCN)3 К винно-красному раствору роданида железа (III) приливаем фосфорную кислоту. Протекает эффектная реакция, сопровождающаяся обесцвечиванием реакционной смеси с одновременным образованием желтовато-белого осадка фосфата железа (III). Результаты опыта вызывают проблемную ситуацию. Учитель: роданид железа (III), как и любое малодиссоциирующее соединение, очень плохо, но подвергается диссоциации. Ученики: Fe(SCN)3 <=> Fe3+ + 3SCN- Учитель: Диссоциация процесс обратимый, следовательно, его равновесие можно сместить, добавив в раствор вещество, способное связывать ионы в соединение с меньшей степенью диссоциации. В данном случае происходит разрушение комплексного соединения роданида железа (III) вследствие образования осадка фосфата железа (III). Fe(SCN)3 + PO43- = FePO4 + 3SCN- Занятие № 6. Тема: «Гидролиз солей» Предложенные ниже опыты рекомендуется проводить при изучении темы «Строение вещества и их свойства» у учащихся 11 классов, обучающихся по учебнику О. С. Габриеляна «Химия-11» на уроке по теме «Гидролиз неорганических веществ» (см. тематическое планирование 10 класс) Цель работы: получить представления о гидролизе неорганических веществ, используя проблемный эксперимент. Форма работы: Работа выполняется в группах (4–5 человек) или в парах учащихся. Оборудование и реактивы: растворы веществ: HCl, HNO3, H2SO4, NaOH, KOH, Ba(OH)2, NaCl, K2SO4, Na2CO3, CuSO4, CuCl2, Pb(NO3)2, FeCl3, Na2S, K2SO3, CH3COONa, KBr, NaNO3, лакмус, фенолфталеин. Ход опыта: В подписанные пробирки с предложенными веществами прилить соответствующие индикаторы. Учащиеся знакомы со свойствами кислот и щелочей изменять окраску индикаторов. Поэтому они быстро проводят соответствующие реакции с кислотами и щелочами и объясняют изменение окраски лакмуса и фенолфталеина взаимодействием индикатора с ионами H+ и OH–. При диссоциации средних солей образуются катионы металлов и анионы кислотных остатков, которые с индикаторами не взаимодействуют. Проблема возникает тогда, когда цвет индикатора изменяется в растворах карбоната натрия и сульфата меди (II). Причем цвет лакмуса в растворе Na2CO3 становится синим, а в растворе CuSO4 – красным. Учитель: составим таблицу «Окраска лакмуса в растворах солей»
Учащиеся: Для объяснения наблюдаемых явлений учащиеся выдвигают ряд гипотез, одна из которых – посторонние примеси в растворах солей Na2CO3 и CuSO4. Учитель: Для проверки этой гипотезы учитель предлагает для анализа растворы других солей: CuCl2, Pb(NO3)2, FeCl3, Na2S, K2SO3, CH3COONa, KBr, NaNO3. Учащиеся: продолжают таблицу «Окраска лакмуса в растворах солей»
|
