Биохимия. ЭКЗАМЕНАЦИОННЫЕ ВОПРОСЫ ПО БИОЛОГИЧЕСКОЙ ХИМИИ. Экзаменационные вопросы по биологической химии для студентов лечебного, педиатрического и медикопрофилактического факультетов
 Скачать 6.22 Mb. Скачать 6.22 Mb.
|
|
Тканевая коллагеназаприсутствует у человека в различных органах и тканях. В норме она синтезируется клетками соединительной ткани, прежде всего, фибробластами и макрофагами. Тканевая коллагеназа - металлозависимый фермент, который содержит Zn2+ в активном центре. В настоящее время известно 4 изоформы этого фермента. Активность коллагеназы зависит от соотношения в межклеточном матриксе её активаторов и ингибиторов. Среди активаторов особую роль играют плазмин, калликреин и катепсин В (см. раздел 14). Тканевая коллагеназа обладает высокой специфичностью, она перерезает тройную спираль коллагена в определённом месте, примерно на 1/4 расстояния от С-конца, между остатками глицина и лейцина (или изолейцина). Образующиеся фрагменты коллагена растворимы в воде, при температуре тела они спонтанно денатурируются и становятся доступными для действия других протеолитических ферментов. Нарушение катаболизма коллагена ведёт к фиброзу органов и тканей (в основном печени и лёгких). А усиление распада коллагена происходит при аутоиммунных заболеваниях (ревматоидном артрите и системной красной волчанке) в результате избыточного синтеза коллагеназы при иммунном ответе. Бактериальная коллагеназасинтезируется некоторыми микроорганизмами. Например,Clostridium histolyticum(возбудитель газовой гангрены) выделяет коллагеназу, расщепляющую пептидную цепь коллагена более чем в 200 местах. Этот фермент гидролизует следующую связь -X-Гли-Про-У- между звеньями X и Гли. Таким образом разрушаются соединительнотканные барьеры в организме человека, что обеспечивает проникновение (или инвазию) этого микроорганизма и способствует возникновению и развитию газовой гангрены. Сам возбудитель не содержит коллагена и поэтому не подвержен действию коллагеназы. Заболевания, связанные с нарушением синтеза и созревания коллагена
160. Важнейшие белки миофибрилл: миозин, актин, актомиозин, тропомиозин, тропонин, актинин. Молекулярная структура миофибрилл. В настоящее время белки мышечной ткани делят на три основные группы: саркоплазматические, миофибриллярные и белки стромы. На долю первых приходится около 35%, вторых – 45% и третьих – 20% от всего количества мышечного белка. Эти группы белков резко отличаются друг от друга порастворимости в воде и солевых средах с различной ионной силой. К группе миофибриллярных белковотносятся миозин, актин и актомиозин – белки, растворимые в солевых средах с высокой ионной силой, и так называемые регуляторные белки: тропомиозин, тропонин, α- и β-актинин, образующие в мышце с актомиозином единый комплекс. Перечисленные миофибриллярные белки тесно связаны с сократительной функцией мышц. Миозин составляет 50–55% от сухой массы миофибрилл. Представление о миозине как о главном белке миофибрилл сложилось в результате работ А.Я. Данилевского, О. Фюрта, Э. Вебера и ряда других исследователей. Однако всеобщее внимание к миозину было привлечено лишь после опубликования работ В.А. Энгельгардта и М.Н. Любимовой (1939– 1942). В этих работах впервые было показано, что миозин обладает АТФазной активностью, т.е. способностью катализировать расщепление АТФ на АДФ и Н3РО4. Химическая энергия АТФ, освобождающаяся в ходе данной ферментативной реакции, превращается в механическую энергию сокращающейся мышцы. Молекулярная масса миозина скелетных мышц около 500000 (для миозина кролика 470000). Молекула миозина имеет сильно вытянутую форму, длину 150 нм. Она может быть расщеплена без разрыва ковалентных связей на субъединицы: две тяжелые полипептидные цепи с мол. массой 205000–210000 и несколько коротких легких цепей, мол. масса которых около 20000. Тяжелые цепи образуют длинную закрученную α-спираль («хвост» молекулы), конец каждой тяжелой цепи совместно с легкими цепями создает глобулу («головка» молекулы), способную соединяться с актином. Эти «головки» выдаются из основного стержня молекулы. Легкие цепи, находящиеся в «головке» миозиновой молекулы и принимающие участие в проявлении АТФазнойактивности миозина, гетерогенны по своему составу. Количество легких цепей в молекуле миозина у различных видов животных и в разных типах мышц неодинаково. Кратковременная обработка трипсином расщепляет молекулу миозина на два фрагмента. Из хвостового участка (С-концевой участокмолекулы) образуется легкий меромиозин (ЛММ) - фрагмент длиной 90 нм, а из остальной части, включающей «головки»,- тяжелый меромиозин (ТММ). ЛММ, подобно миозину, образует нити, однако он не обладает АТФазной активностью и не связывает актин. ТММ катализирует гидролиз АТФ и связывает актин. ТММ можно расщепить далее путем более длительной обработки трипсином илипапаином, в результате чего получается один S2-фрагмент длиной 40 нм с мол. массой 62000 и два S1-фрагмента с мол. массой 110000, представляющие собой «головки» миозина. Толстые нити (толстые миофиламенты) в саркомере надо понимать как образование, полученное путем соединения большого числа определенным образом ориентированных в пространстве молекул миозина Актин, составляющий 20% от сухой массы миофибрилл, был открыт Ф. Штраубом в 1942 г. Известны две формы актина: глобулярныйактин (G-актин) и фибриллярный актин (F-актин). Молекула G-актина с мол. массой 42000 состоит из одной полипептидной цепочки (глобула), в образовании которой принимают участие 374 аминокислотных остатка. При повышении ионной силы до физиологического уровня G-актин полиме-ризуется в F-актин (фибриллярная форма). На электронных микрофотографиях волокна F-актина выглядят как две нити бус, закрученных одна вокруг другой. Актомиозинобразуется при соединении миозина с F-актином. Актомиозин, как естественный, так и искусственный, т.е. полученный путем соединения in vitro высокоочищенных препаратов миозина и F-актина, обладает АТФазной активностью, которая отличается от таковой миозина, АТФазная активность миозина значительно возрастает в присутствии стехиометрических количеств F-актина.Фермент актомиозин активируется ионами Mg2+и ингибируется этилендиаминтетраацетатом (ЭДТА) и высокой концентрацией АТФ, тогда как миозиновая АТФаза ингибируется ионами Mg2+, активируется ЭДТА и не ингибируется высокой концентрацией АТФ. Оптимальные значения рН для обоих ферментов также различны. Как отмечалось, кроме рассмотренных основных белков, в миофибриллах содержатся также тропомиозин, тропонин и некоторые другие ре-гуляторные белки. Тропомиозин был открыт К. Бейли в 1946 г. Молекула тропомиозина состоит из двух α-спиралей и имеет вид стержня длиной 40 нм; его мол. масса 65000. На долю тропомиозина приходится около 4–7% всех белков миофибрилл. Тропонин – глобулярный белок, открытый С. Эбаси в 1963 г.; его мол. масса 80000. В скелетных мышцах взрослых животных и человека тропонин (Тн) составляет лишь около 2% от всех миофибриллярных белков. В его состав входят три субъединицы (Тн-I, Тн-С, Тн-Т). Тн-I (ингибирующий) может ингибировать АТФазную активность, ТН-С (кальцийсвязывающий) обладает значительным сродством к ионамкальция, Тн-Т (тропомиозин-связывающий) обеспечивает связь с тропомиозином. Тропонин, соединяясь с тропомиозином, образует комплекс, названный нативным тропомиози-ном. Этот комплекс прикрепляется к актиновым филаментам и придает актомиозинускелетных мышц позвоночных чувствительность к ионам Са2+ Установлено, что тропонин (его субъединицы Тн-Т и Тн-I) способен фосфорилироваться при участии цАМФ-зависимых протеинкиназ. Вопрос о том, имеет ли отношение фосфорилирование тропонина in vitro к регуляции мышечного сокращения, остается пока открытым. Белкистромы в поперечно-полосатой мускулатуре представлены в основном коллагеном и эластином. Известно, что строма скелетных мышц, остающаяся после исчерпывающей экстракции мышечной кашицы солевыми растворами с высокой ионной силой, состоит в значительной мере из соединительнотканных элементов стенок сосудов и нервов, а также сарколеммы и некоторых других структур. Миофибриллы - цилиндрические нити толщиной 1 - 2 мкм, идущие вдоль от одного конца мышечного волокна до другого. Изолированная миофибрилла способна сокращаться в присутствии АТФ , именно она и есть сократимый элемент мышечной клетки . ократимые единицы миофибрил легко различимы в световом микроскопе, именно они обусловливают полосатость скелетных мышц . Каждая из таких единиц - саркомеров - имеет длину около 2,5 мкм. Границы саркомеров в соседних миофибриллах совпадают, поэтому вся мышечная клетка приобретает регулярную исчерченность. Каждый саркомер состоит из множества параллельных белковых филаментов (нитей). Существуют филаменты двух типов - толстые(длиной около 1,6 мкм м толщиной 15 нм), которые тянутся от одного края А-диска до другого, и тонкие (длиной около 1 мкм и толщиной 8 нм), которые идут от Z-линии через I-диск и заходят в А-диск в промежутки между толстыми филаментами. На участке А-диска, содержащем перекрывающиеся тонкие и толстые филаменты, толстые филаменты расположены в виде регулярной гексагональной системы, причем каждый толстый филамент окружен тонкими, тоже расположенными регулярно. При помощи электронного микроскопа удалось увидеть на толстых филаментах множество боковых отростков, образующих поперечные мостики между толстыми филаментами и расположенными на расстоянии 13 нм от них тонкими филаментами. В настоящее время известно, что при сокращении мышцы толстые и тонкие нити перемещаются относительно друг друга именно с помощью этих поперечных мостиков, которые работают циклично. Взаимодействующие белки толстых и тонких филаментов были выделены и получили названия соответственно миозин и актин . Кроме них, в миофибриллах имеется еще целый ряд вспомогательных белков. Предполагается, что белок альфа-актинин обеспечивает надлежащую упаковку филаментов в саркомере , а десмин связывает между собой соседние саркомеры. 161. Биохимические механизмы мышечного сокращения и расслабления. Роль градиента одновалентных ионов и ионов кальция в регуляции мышечного сокращения и расслабления. В настоящее время принято считать, что биохимический цикл мышечного сокращения состоит из 5 стадий: 1) миозиновая «головка» может гидролизовать АТФ до АДФ и Н3РО4 (Pi), но не обеспечивает освобождения продуктов гидролиза. Поэтому данный процесс носит скорее стехиометрический, чем каталитический, характер; 2) содержащая АДФ и Н3РО4 миозиновая «головка» может свободно вращаться под большим углом и (при достижении нужного положения) связываться с F-актином, образуя с осью фибриллы угол около 90°; 3) это взаимодействие обеспечивает высвобождение АДФ и Н3РО4 из актин-миозинового комплекса. Актомиозиновая связь имеет наименьшую энергию при величине угла 45°, поэтому изменяется угол миозина с осью фибриллы с 90° на 45° (примерно) и происходит продвижение актина(на 10–15 нм) в направлении центра саркомера; 4) новая молекула АТФ связывается с комплексом миозин–F-актин; 5) комплекс миозин–АТФ обладает низким сродством к актину, и поэтому происходит отделение миозиновой (АТФ) «головки» от F-актина. Последняя стадия и есть собственно расслабление, которое отчетливо зависит от связывания АТФ с актин-миозиновым комплексом Затем цикл возобновляется. Регуляция сокращения и расслабления мышц. Сокращение любых мышц происходит по общему механизму, описанному ранее. Мышечные волокна разных органов могут обладать различными молекулярными механизмами регуляции сокращения и расслабления, однако всегда ключевая регулятор-ная роль принадлежит ионам Са2+. Установлено, что миофибриллы обладают способностью взаимодействовать с АТФ и сокращаться в его присутствии лишь при наличии в среде определенных концентраций ионов кальция . Наибольшая сократительная активность наблюдается при концентрации ионов Са2+ около 10–6–10–5 М. При понижении концентрации до 10–7 М или ниже мышечные волокна теряют способность к укорочению и развитию напряжения в присутствии АТФ.По современным представлениям, в покоящейся мышце (в миофибриллах и межфибриллярном пространстве) концентрация ионов Са2+ поддерживается ниже пороговой величины в результате связывания их структурами (трубочками и пузырьками) саркоплазматической сети и так называемой Т-системой при участии особого Са2+-связывающего белка, получившего название кальсеквестрина, входящего в состав этих структур. Связывание ионов Са2+ разветвленной сетью трубочек и цистерн сарко-плазматической сети не является простой адсорбцией. Это активный физиологический процесс, который осуществляется за счет энергии, освобождающейся при расщеплении АТФ Са2+-зависимой АТФазой саркоплазматической сети . При этом наблюдается весьма своеобразная картина: скорость выкачивания ионовСа2+ из межфибриллярного пространства стимулируется этими же ионами. В целом такой механизм получил название «кальциевая помпа» по аналогии с хорошо известным в физиологии натриевым насосом. Возможность пребывания живой мышцы в расслабленном состоянии при наличии в ней достаточно высокой концентрации АТФобъясняется снижением в результате действия кальциевой помпы концентрации ионов Са2+ в среде, окружающей миофибриллы, ниже того предела, при котором еще возможны проявление АТФазной активности и сократимость акто-миозиновых структур волокна. Быстрое сокращение мышечного волокна при его раздражении от нерва (или электрическим током) является результатом внезапного изменения проницаемости мембран и как следствие выхода из цистерн и трубочек саркоплазматической сети и Т-системы некоторого количества ионов Са2+ в саркоплазму. Как отмечалось, «чувствительность» актомиозиновой системы к ионам Са2+ (т.е. потеря актомиозином способности расщеплять АТФ и сокращаться в присутствии АТФ при снижении концентрации ионов Са2+ до 10–7 М) обусловлена присутствием в контрактильной системе (на нитях F-акти-на) белка тропонина, связанного с тропомиозином. В тропонин-тропомио-зиновом комплексе ионы Са2+связываются именно с тропонином. В молекуле тропонина при этом происходят конформационные изменения, которые, по-видимому, приводят к сдвигу всего тропонин-тропомиози-нового стержня и деблокировке активных центров актина, способных взаимодействовать с миозином с образованием сократительного комплекса и активной Mg2+-АТФазы. В продвижении актиновых нитей вдоль миозиновых, по данным Э. Хаксли, важную роль играют временно замыкающиеся между нитями поперечные мостики, которые являются «головками» миозиновых молекул. Итак, чем большее число мостиков прикреплено в данный момент к акти-новым нитям, тем больше сила мышечного сокращения. Наконец, если возбуждение прекращается, содержание ионов Са2+ в саркоплазме снижается (кальциевая помпа), то циклы прикрепление–освобождение прекращаются, т.е. «головки» миозиновых нитей перестают прикрепляться к актиновым нитям. В присутствии АТФ мышца расслабляется и ее длина достигает исходной. Если прекращается поступление АТФ (аноксия, отравлениедыхательными ядами или смерть), то мышца переходит в состояние окоченения. Почти все поперечные мостики толстых (миозиновых) нитей присоединены при этом к тонким актиновым нитям, следствием чего и является полная неподвижность мышцы. 162. Саркоплазматические белки: миоглобин, его строение и функции. Экстрактивные вещества мышц. Белки, входящие в состав саркоплазмы, относятся к протеинам, растворимым в солевых средах с низкой ионной силой. Принятое ранее подразделение саркоплазматических белков на миоген, глобулин X, миоальбумин и белки-пигменты в значительной мере утратило смысл, поскольку существование глобулина X и миогена как индивидуальных белков в настоящее время отрицается. Установлено, что глобулин X представляет собой смесь различных белковых веществ со свойствами глобулинов. Термин «миоген» также является собирательным понятием. В частности, в состав белков группы миогена входит ряд протеинов, наделенных ферментативной активностью: например, ферменты гликолиза. К числу саркоплазматических белков относятся также дыхательныйпигмент миоглобин и разнообразные белки-ферменты, локализованные главным образом в митохондриях и катализирующие процессы тканевого дыхания, окислительного фосфорилирования, а также многие стороны азотистого и липидного обмена. Недавно была открыта группа саркоплазматических белков – пар-вальбумины, которые способны связывать ионы Са2+. Их физиологическая роль остается еще неясной. Миоглобин. Состоит из одной полипептидной цепи, содержащей 153 аминокислотных остатка (мол. м. 17800), к-рая уложена в плотную глобулу размером 4,5 х 2,5 нм. В специальной полости миоглобина ("кармане") помещается гем, который связан с остальной частью молекулы (глобином), как в гемоглобине. Около 75% полипептидной цепи находится в конформации α-спирали (все α-спирали правозакрученные). Между областями спирализации находятся 5 неспирализованных участков; такие же участки находятся на концах цепи. Внутренняя область молекулы состоит . из неполярных остатков лейцина, валина, метионина, фенилаланина и не содержит боковых полярных цепей глутаминовой и аспарагиновой к-т, глута-мина, аспарагина, лизина и аргинина. На наружной стороне молекулы расположены как полярные, так и неполярные аминокислотные остатки. Атом железа тема может находиться в 4 состояниях: в ферросостоянии (дезоксимиоглобин, Fe2 +), в феррисостоянии (метмиоглобин, Fe3 + , 6-й лиганд Н2О) и в низкоспиновых ферро- и феррисостояниях (соответственно Fe2+ и Fe3+ ). Связывание лигандов сопровождается конформационными изменениями белка, и, наоборот, конформационные изменения вблизи гема изменяют его электронное состояние и реакционную способность. Функция миоглобина запасать О2 в мышцах при его избытке и освобождать при недостатке основана на способности иона Fe2+ обратимо связывать молекулу О2 с образованием оксимиоглобина. Высвобождение из оксимиоглобина молекулы О2, необходимого работающей мышце, происходит в момент сокращения последней, когда в результате сжатия капилляров парциальное давление О2 резко падает. Белок выполняет роль водорастворимого носителя гема, предохраняет Fe2+ от окисления при его взаимодействии с О2 и регулирует величину сродства к О2. Небелковые азотистые экстрактивные вещества. В скелетных мышцах содержится ряд важных азотистых экстрактивных веществ: адениновые нуклеотиды (АТФ, АДФ и АМФ), нуклеотиды неаденинового ряда, креатинфосфат, креатин, креатинин, карнозин, ансерин, свободные аминокислоты и др. Концентрация адениновых нуклеотидов в скелетной мускулатуре кролика (в микромолях на 1 г сырой массы ткани) составляет: АТФ – 4,43, АДФ – 0,81,АМФ – 0,93. Количество нуклеотидов неаденинового ряда (ГТФ, УТФ, ЦТФ и др.) в мышечной ткани по сравнению с концентрациейадениновых нуклеотидов очень мало. На долю креатина и креатинфосфата приходится до 60% небелкового азота мышц. Креатинфосфат и креатин относятся к тем азотистым экстрактивным веществам мышц, которые участвуют в химических процессах, связанных с мышечным сокращением. К азотистым веществам мышечной ткани принадлежат имидазолсо-держащие дипептиды карнозин и ансерин. Карнозин был открыт В.С. Гулевичем в 1900 г.; метилированное производное карнозина ансерин был обнаружен в мышечной ткани несколько позже. 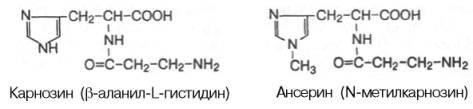 Карнозин и ансерин – специфические азотистые вещества скелетной мускулатуры позвоночных. Они увеличивают амплитуду мышечного сокращения, предварительно сниженную утомлением. Работами акад. С.Е. Северина показано, что имидазолсодержащие дипептиды не влияют непосредственно на сократительный аппарат, но увеличивают эффективность работы ионных насосов мышечной клетки. Среди свободных аминокислот в мышцах наиболее высока концентрация глутаминовой кислоты (до 1,2 г/кг) и ее амида глутамина(0,8–1,0 г/кг). В состав различных клеточных мембран мышечной ткани входит ряд фосфоглицеридов: фосфатидилхолин, фосфатидилэтанол-амин, фосфатидилсерин и др. Кроме того, фосфоглицериды принимают участие в обменных процессах, в частности, в качестве субстратов тканевого дыхания. Другие азотсодержащие вещества: мочевина, мочевая кислота, аденин, гуанин,ксантин и гипоксантин – встречаются в мышечной ткани в небольшом количестве и, как правило, являются либо промежуточными, либо конечными продуктами азотистого обмена. Безазотистые экстрактивные вещества. Одним из основных представителей безазотистых органических веществ мышечной ткани является гликоген. Его концентрацияколеблется от 0,3 до 2% и выше. На долю других представителей углеводов приходятся десятые и сотые доли процента. В мышцах находят лишь следы свободной глюкозы и очень мало гексозофосфатов. В процессе метаболизма глюкозы, а также аминокислот вмышечной ткани образуются молочная, пиро-виноградная кислоты и много других карбоновых кислот. В том или ином количестве вмышечной ткани обнаруживаются также триглицериды и холестерин. Состав неорганических солей в мышцах разнообразен. Из катионов больше всего калия и натрия. Калий сосредоточен главным образом внутри мышечных волокон, а натрий – преимущественно в межклеточном веществе. Значительно меньше в мышцах магния, кальция ижелеза. В мышечной ткани содержится ряд микроэлементов: кобальт, алюминий, никель, бор, цинк и др. 163. Особенности энергетического обмена в мышцах. Креатинфосфат. Принято считать, что процессом, непосредственно связанным с работающим механизмом поперечно-полосатого мышечного волокна, является распад АТФ с образованием АДФ и неорганического фосфата. Возникает вопрос: каким образом мышечная клетка может обеспечить свой сократительный аппарат достаточным количеством энергии в форме АТФ, т.е. каким образом в процессе мышечной деятельности происходит непрерывный ресинтез этого соединения? Прежде всего ресинтез АТФ обеспечивается трансфосфорилированием АДФ с креатинфосфатом. Данная реакция катализируетсяферментом креатинкиназой: Креатинкиназный путь ресинтеза АТФ является чрезвычайно быстрым и максимально эффективным (за счет каждой молекулыкреатинфосфата образуется молекула АТФ). Именно поэтому долгое время не удавалось установить уменьшение концентрации АТФ и соответственно повышение концентрации АДФ даже при достаточно продолжительном тетанусе. Применив специфический ингибиторкреатинкиназы (1-фтор-2,4-динитро-фенол), а также с помощью агентов, препятствующих окислительному фосфорилированию АДФ вАТФ, Т. Кейн и соавт. (1962) смогли продемонстрировать прямой распад АТФ с одновременным приростом неорганического фосфата иАДФ при одиночном сокращении изолированной мышцы лягушки. Некоторое количество АТФ может ресинтезироваться в ходе аденилаткиназной (миокиназной) реакции: Запасы креатинфосфата в мышце невелики, а доступность энергии креатинфосфата имеет ценность для работающей мышцы только в том случае, если расход его постоянно возмещается синтезом АТФ в процессе метаболизма. Для любой ткани, в том числе мышечной, известны два фундаментальных биохимических процесса, в ходе которых регенерируются богатые энергией фосфорные соединения. Один из этих процессов – гликолиз, другой – окислительное фосфорилирование. Наиболее важным и эффективным из них является последний. При достаточном снабжении кислородом мышца, несмотря на анаэробный механизм сокращения, в конечном итоге работает за счет энергии, образующейся при окислении (в цикле Кребса) как продуктов распада углеводов, так и ряда других субстратовтканевого дыхания, в частности жирных кислот, а также ацетата и ацетоацетата. В последнее время появились данные, доказывающие, что креатинфос-фат в мышечной ткани (в частности, в сердечной мышце) способен выполнять не только роль как бы депо легкомобилизуемых макроэргических фосфатных групп, но также роль транспортной формы макроэргических фосфатных связей, образующихся в процессе тканевого дыхания и связанного с ним окислительного фосфорилирования. Предложена схема переноса энергии из митохондрий в цитоплазму клетки миокарда. АТФ, синтезированный в матриксе митохондрий, переносится через внутреннюю мембрану с участием специфической АТФ–АДФ-транслоказы на активный центр митохондриального изофермента креатинкиназы, который расположен на внешней стороне внутреннеймембраны; в межмембранном пространстве (в присутствии ионов Mg2+) при наличии в среде креатина образуется равновесный тройной фермент-субстратный комплекс креатин–креатинкиназа–АТФ–Mg2+, который затем распадается с образованиемкреатинфосфата и АДФ–Mg2+. Креатинфосфат диффундирует в цитоплазму, где используется в миофибриллярной креатинкиназнойреакции для рефосфорилирования АДФ, образовавшегося при сокращении. Высказываются предположения, что не только в сердечной мышце, но и в скелетной мускулатуре имеется подобный путь транспорта энергии из митохондрий в миофибриллы. При работе умеренной интенсивности мышца может покрывать свои энергетические затраты за счет аэробного метаболизма. Однако при больших нагрузках, когда возможность снабжения кислородом отстает от потребности в нем, мышца вынуждена использовать гликолитический путь снабжения энергией. При интенсивной мышечной работе скорость расщепления гликогена или глюкозы с образованием молочной кислоты увеличивается в сотни раз. Соответственно содержание молочной кислоты в мышечной ткани может повышаться до 1,0–1,2 г/кг и более. С током крови значительное количество молочной кислоты поступает в печень, где ресинтезируется в глюкозу и гликоген (глюконеогенез) за счет энергии окислительных процессов . Перечисленные механизмы ресин-тезаАТФ при мышечной деятельности включаются в строго определенной последовательности. Наиболее экстренным является креатинкиназный механизм, и лишь примерно через 20 с максимально интенсивной работы начинается усиление гликолиза, интенсивность которого достигает максимума через 40–80 с. При более длительной, а следовательно, и менее интенсивной работе все большее значение приобретает аэробный путь ресинтеза АТФ. Содержание АТФ и креатинфосфата в сердечной мышце ниже, чем в скелетной мускулатуре, а расход АТФ велик. В связи с этим ресинтез АТФ в миокарде должен происходить намного интенсивнее, чем в скелетной мускулатуре. Для сердечной мышцы теплокровных животных и человека основным путем образования богатых энергией фосфорных соединений является путь окислительного фосфорилирования, связанный с поглощением кислорода. Регенерация АТФ в процессе анаэробного расщепленияуглеводов (гликолиз) в сердце человека практического значения не имеет. Именно поэтому сердечная мышца очень чувствительна к недостатку кислорода. Характерной особенностью обмена веществ в сердечной мышце по сравнению со скелетной является также то, что аэробное окисление веществ неуглеводной природы при работе сердечной мышцы имеет большее значение, чем при сокращении скелетной мышцы. Только 30–35% кислорода, поглощаемого сердцем в норме, расходуется на окисление углеводов и продуктов их превращения. Главным субстратом дыхания в сердечной мышце являются жирные кислоты. Окисление неуглеводных веществобеспечивает около 65–70% потребности миокарда в энергии. Из свободных жирных кислот в сердечной мышце особенно легко подвергается окислению олеиновая кислота. 164. Биохимические изменения при мышечных дистрофиях и денервации мышц. Креатинурия. Общими для большинства заболеваний мышц (прогрессирующие мышечные дистрофии, атрофия мышц в результате их денервации, тенотомия, полимиозит, некоторые авитаминозы и т.д.) являются резкое снижение в мышцах содержания миофибриллярных белков, возрастание концентрации белков стромы и некоторых саркоплазматических белков, в том числе миоальбумина. Наряду с изменениями фракционного состава мышечных белков при поражениях мышц наблюдается снижение уровня АТФ и креатинфосфата. Например, через 12 дней после денервации содержание АТФ в денервированной икроножной мышце кролика снижается более чем в 2 раза. Отмечаются также снижение АТФазной активности контрактиль-ных белков (миозина), уменьшение количества имидазолсодержащих дипептидов. При прогрессирующих мышечных дистрофиях и других заболеваниях, связанных с распадом мышечной ткани, часто отмечаются сдвиги в фосфолипидном составе мышц: значительно снижается уровень фосфатидилхолина и фосфатидилэтаноламина, концентрациясфингомиелина и лизо-фосфатидилхолина повышается. До сих пор истинные механизмы изменения фосфолипидного составамышечной ткани при патологии не выяснены, неизвестна также роль этих сдвигов в патогенезе мышечных дистрофий. Для многих форм патологии мышечной ткани характерны нарушение метаболизма креатина и его усиленное выделение с мочой(креатинурия). Несмотря на многочисленные исследования и обилие фактического материала, вопрос о причинах креатинурии при заболеваниях мышц не может считаться окончательно решенным. Принято считать, что креатинурия у больных миопатией является результатом нарушения в скелетной мускулатуре процессов фиксации (удержания) креатина и его фосфорилирования. Если нарушен процесс синтеза креатинфосфата, то не образуется и креатинина; содержание последнего в моче резко снижается. В результате креатинурии и нарушения синтеза креатинина резко повышается креатиновый показатель (креатин/креатинин) мочи. При патологии мышечной ткани можно наблюдать определенную закономерность в изменении активности ферментов в мышцах: уменьшается активность ферментов, локализованных в саркоплазме; незначительно изменяется активность ферментов, связанных смитохондриями; заметно возрастает активность лизосомальных ферментов. Наконец, показано, что при многих заболеваниях мышечной системы наступают сдвиги в системе цАМФ: снижается содержание цАМФ в мышечной ткани, повышается активностьфосфодиэстеразы и нарушается способность аденилатциклазы активироваться под влиянием адреналина и фторида натрия. 165. Химический состав нервной ткани. Миелиновые мембраны: особенности состава и структуры. 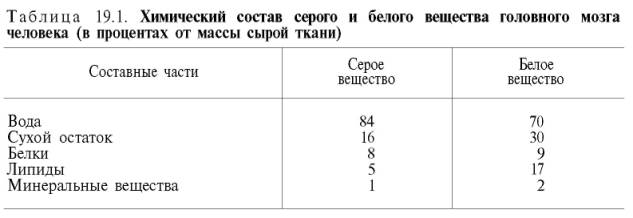 На долю белков приходится примерно 40% от сухой массы головного мозга. Мозговая ткань является трудным объектом для изучения белкового состава вследствие большого содержания липидов и наличия белково-ли-пидных комплексов. А.Я. Данилевский впервые разделил белки мозговой ткани на растворимые в воде и солевых растворах белки и нерастворимые белки. Обширные исследования в этой области были проведены также А.В. Палладиным и сотр., которые разделили белки нервной ткани на 4 фракции: извлекаемые водой, 4,5% раствором КСl, 0,1% раствором NaOH и нерастворимый остаток. Установлено, что серое веществобогаче белками, растворимыми в воде, чем белое вещество,– соответственно 30 и 19%. Белое вещество, напротив, содержит гораздо больше (22%) нерастворимого белкового остатка, чем серое вещество (5%). В дальнейшем было выделено 5–10 фракций растворимых белков мозга, различающихся по своей электрофоретической подвижности. В настоящее время, сочетая методы экстракции буферными растворами, хроматографии на колонках с ДЭАЭ-целлюлозой и диск-электрофореза в полиакриламидном геле, удалось выделить из ткани мозга около 100 различных растворимых белковых фракций. В нервной ткани содержатся как простые, так и сложные белки. Простые белки – это альбумины (нейроальбумины), глобулины(нейроглобулины), катионные белки (гистоны и др.) и опорные белки (нейросклеропротеины). Альбумины и глобулины по своим физико-химическим свойствам несколько отличаются от аналогичных белков сыворотки крови, поэтому их называют нейроальбуминамии нейроглобулинами. Количество нейрогло-булинов в головном мозге относительно велико – в среднем 5% по отношению ко всем растворимым белкам. Нейроальбумины являются основным белковым компонентомфосфопротеинов нервной ткани, на их долю приходится основная масса растворимых белков (89–90%). В свободном состоянии нейроальбумины встречаются редко. В частности, они легко соединяются с липидами, нуклеиновыми кислотами, углеводами и другими небелковыми компонентами. Белки, которые в процессе электрофоретического разделения при рН 10,5–12,0 движутся к катоду, получили название катионных. Главнейшими представителями этой группы белков в нервной ткани являются гистоны, которые делятся на пять основных фракций в зависимости от содержания в их полипептидных цепях остатков лизина, аргинина и глицина. |
