Информ.материал_протозоозы. Эпидемиология и профилактика протозоозов (амебиаз, лямблиоз, малярия, трипаносомоз, лейшманиоз и др.).
 Скачать 3.57 Mb. Скачать 3.57 Mb.
|
|
Неглерия (Naegleria fowleri). N. fowleri вызывает неглериоз - протозойное заболевание, проявляющееся поражением кожи, легких, глаз и центральной нервной системы. Этиология. Неглерия - свободноживущая амеба, жизненный цикл которой включает 3 морфологические формы: амебоидный трофозоит, жгутиковую стадию и цисту. Размеры трофозоитов - 15-40 мкм. Энергичная пульсация сократительной вакуоли отличает неглерию от клеток хозяина. Ядро (5 мкм) имеет эндосому. Псевдоподии прозрачные и широкие. Как и у всех амеб, цитоплазма подразделяется на экто- и эндоплазму, но неглерии имеют пластинчатый комплекс Гольджи, выраженный эндоплазматический ретикулум и сократительную вакуоль. Цисты округлые, с гладкой двойной стенкой, размером 10-20 мкм. Биология развития. N. fowleri - свободноживущая амеба, которая обитает в пресноводных водоемах (сточные воды, бассейны, термальные источники и др.). При повышении температуры до 35 оС неглерии начинают активно размножаться, и численность их значительно возрастает. Часть амеб при резких колебаниях температуры и изменении рН среды формирует 2 жгутика и активно плавает в толще воды в течение суток, затем вновь переходит в амебоидную форму. При неблагоприятных условиях амебы легко инцистируются. В отличие от акантамеб цисты неглерий менее устойчивы к высыханию. Эпидемиология. Чаще всего неглериями заражаются (рис. 2.6) молодые люди и дети, главным образом при купании в открытых водоемах, бассейнах и горячих ваннах. По-видимому, это обусловлено наличием у неглерии жгутиковых стадий развития, плавающих в толще воды, что облегчает контакт человека с амебами. Цисты неглерий могут проникать также в носовую полость при вдыхании содержащих их аэрозолей. Неглерии распространены повсеместно, но чаще встречаются в районах с тропическим и субтропическим климатом. До 1985 г. в литературе были приведены сведения о 128 случаях неглериоза ЦНС в мире, из которых 50 зарегистрированы в США. Патогенез и клинические проявления. Заражение человека амебами происходит, по-видимому, при попадании их в ротовую и носовую полости с загрязненной водой. Из носоглотки через обонятельный эпителий амебы проникают в богато васкуляризованное субарахноидальное пространство, откуда распространяются во все отделы мозга. В тканях мозга они локализуются вокруг кровеносных сосудов и интенсивно размножаются. Вследствие этого как в сером, так и в белом веществе мозга возникают кровоизлияния и некроз. Развивается первичный амебный менингоэнцефалит. Инкубационный период длится 2-3 дня, реже - 7-15 дней. Болезнь начинается внезапно. Сначала во многих случаях возникают нарушения вкусовых или обонятельных ощущений. Появляются головные боли, лихорадка, тошнота, рвота, судороги. На слизистой оболочке глотки нередко образуются язвы. Наблюдаются симптомы менингита и энцефалита. Развивается отек легких. Вскоре наступает кома. В большинстве случаев в пределах 1 нед после появления первых симптомов больные погибают вследствие отека легких и остановки дыхания. N. fowleri, так же как акантамебы, могут вызывать поражения кожи, легких и глаз. 2.1.2.1. Отряд Kinetoplastida К данной группе относятся трипаносомы и лейшмании. Эти паразиты передаются кровососущими паразитами-переносчиками, которые одновременно являются промежуточными хозяевами. В организме позвоночных животных паразиты присутствуют в крови и тканевых жидкостях, а также внутри клеток. Размножение всегда происходит путем бинарного деления. Единственный жгутик отходит от кинетосомы, расположенной рядом с более крупным дисковидным или изогнутым образованием - кинетопластом, однако при исследовании в световом микроскопе эти два образования дифференцировать невозможно. Кинетопласт, который связан с крупной митохондрией, проходящей через большую часть клетки организма, содержит ДНК, которая генетически отличается от ядерной ДНК. 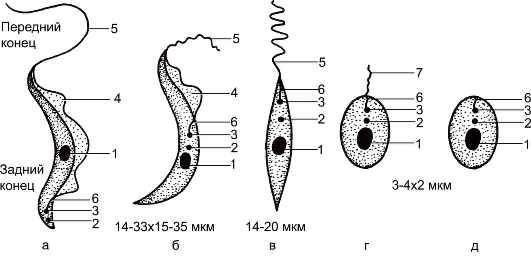 Рис. 7. Морфологические формы лейшманий и трипаносом. а - трипомастигота; б - эпимастигота; в - промастигота; г - сферомастигота (микромастигота); д - амастигота: 1 - ядро; 2 - кинетопласт; 3 - кинетосома; 4 - ундулирующая мембрана; 5 - жгутик; 6 - ризопласт; 7 - рудиментарный жгутик. В переносчике жгутик может функционировать как орган прикрепления. Эти паразиты меняют форму тела в процессе смены фаз жизненного цикла (рис. 7). Амастигота, или амастиготная (безжгутиковая) стадия, соответствующая прежней лейшманиальной стадии, имеет округлую или удлиненную форму; лишена наружного жгутика у Leishmania, Trypanosoma cruzi. Сферомастигота (микромастигота), или сферомастиготная стадия, имеет округлую форму с рудиментарным свободным жгутиком (у лейшманий). Промастигота, или промастиготная (переднежгутиковая) стадия, соответствующая прежней лептомонадной стадии, имеет удлиненную форму; кинетопласт лежит впереди ядра, жгутик начинается там же и выходит наружу в переднем конце тела (у Leishmania, Trypanosoma cruzi). Эпимастигота, или эпимастиготная (бокожгутиковая) стадия, соответствующая бывшей критидиалъной стадии, характеризуется удлиненной формой; кинетопласт лежит рядом с ядром, жгутик начинается там же и выходит наружу сбоку, после чего проходит по поверхности тела или вдоль короткой ундулирующей мембраны (у трипаносом). Трипомастигота, или трипомастиготная стадия, соответствующая трипаносомной стадии, отличается удлиненной формой; кинетопласт лежит позади ядра, жгутик начинается там же и выходит наружу сбоку, после чего проходит по поверхности тела или вдоль длинной ундулирующей мембраны. Хотя эта форма сходна с эпимастиготной, ее как важную стадию, свойственную роду Trypanosoma, желательно обозначить специальным термином, который определяет ее структуру, но не связан с родовым названием. Наряду с полиморфизмом трипаносоматид (трипаносомы и лейшмании) в процессе их жизненных циклов выявлен также полиморфизм на уровне их геномов. Кариотипы трипаносоматид очень изменчивы. Они сильно различаются даже между разными изолятами одного вида. Кариотип трипаносом не поддается анализу в световом микроскопе, но при применении электрофореза в геле хромосомы могут быть разделены на 4 основных класса: большая ДНК, остающаяся вблизи щели геля; около 5 длинных хромосом; 5-7 хромосом промежуточного размера и от 0 до 100 сателлитных и теломерных мини-хромосом. Вероятно, эволюция кариотипа происходила в направлении увеличения разнообразия антигенной вариации. Одна особь трипаносомы несет до 1000 поверхностных вариантов генов. Такой полиморфизм является одним из важнейших способов уклонения паразитов от защитных механизмов своих хозяев благодаря изменчивости их поверхностных антигенов. Так, в каждой новой генерации часть трипаносом несет поверхностный антиген, отличающийся от предыдущих. Эта смена антигенов происходит в результате транспозиции и дупликации генов, кодирующих антигенные детерминанты. В результате меняется расположение гена по отношению к промотору. Изменение поверхностных генов паразита в сторону сближения с антигенами хозяина обеспечивает так называемую молекулярную мимикрию, или связывание антигенов хозяина. Локализация паразитов в клетках иммунной системы направленно инактивирует лизосомные ферменты макрофага, что обеспечивает их жизнедеятельность и условия для размножения. Род Trypanosoma (трипаносомы). Размеры трипаносом больше, чем лейшманий. Трипаносомы имеют узкую продолговатую форму (ширина 1,5-3 мкм, длина 15-30 мкм), жгутик и ундулирующую мембрану. В процессе жизненного цикла изменяются морфологически. Трипаносомозы - группа трансмиссивных тропических болезней, вызываемых простейшими рода Trypanosoma. Для человека патогенны Т. gambiense и Т. rhodesiense, которые вызывают африканский трипаносомоз (сонная болезнь), и Т. cruzi - возбудитель американского трипаносомоза (болезнь Шагаса). Трипаносомы проходят сложный цикл развития со сменой хозяев, в процессе которого они находятся в морфологически разных стадиях. Трипаносомы размножаются продольным делением, питаются растворенными веществами. Жизненный цикл трипаносом осуществляется со сменой двух хозяев, одним из которых являются позвоночные животные и человек, другим - кровососущие членистоногие, служащие переносчиками возбудителя. Различают африканский и американский трипаносомозы. Трипаносома гамбийская (Trypanosoma gambiense). T. gambiense вызывает африканский трипаносомоз (сонная болезнь) - облигатно-трансмиссивную инвазию, характеризующуюся лихорадкой, высыпаниями на коже, увеличением лимфатических узлов, появлением местных отеков и поражением центральной нервной системы, приводящим к летаргии, кахексии и летальному исходу. Африканский трипаносомоз распространен в зоне саванн. Его нозоареал ограничен ареалом переносчика - мухи цеце. Эта болезнь эндемична в 36 странах тропической Африки. Ежегодно регистрируют до 40 тыс. новых случаев. Известны два типа африканского трипаносомоза - гамбийский, или западноафриканский, и родезийский, или восточноафриканский. Первый вызывает T. gambiense, второй - T. rhodesiense. Оба возбудителя африканского трипаносомоза относятся к секции Salivaria, т. е. передаются через слюну. Гамбийский тип африканского трипаносомоза - это облигатно-трансмиссивное заболевание, фактически антропоноз, хотя в передаче его возбудителя некоторое участие принимают и сельскохозяйственные животные. 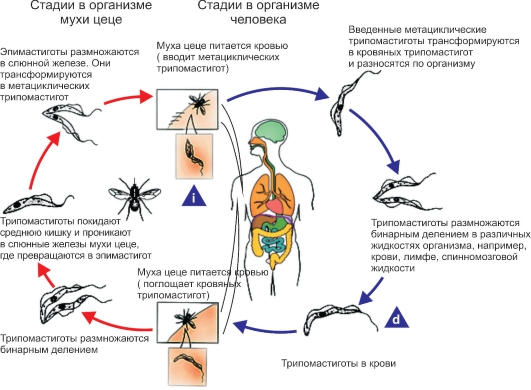 Рис. 2.8. Жизненный цикл Trypanosoma gambiense и Trypanosoma rhodesiense. i - инфекционная стадия; d - диагностическая стадия. Впервые клинику африканского трипаносомоза описал в 1734 г. английский врач Atkins, наблюдавший эту болезнь у жителей побережья Гвинейского залива (Западная Африка). В 1902 г. P. Ford и J. Dutton нашли в крови человека Т. gambiense. D. Bruce и D. Nabarro установили, что муха Glossina palpalis (цеце) является переносчиком возбудителя болезни. Этиология. Возбудитель - Trypanosoma gambiense. В крови позвоночных хозяев развиваются полиморфные стадии трипаносом - трипомастиготы и эпимастиготы. (рис. 2.8). Среди них обнаруживаются тонкие трипомастиготные формы длиной 14-39 мкм (в среднем 27 мкм) с хорошо выраженной ундулирующей мембраной и длинной свободной частью жгутика. Их задний конец заострен, кинетопласт находится на расстоянии около 4 мкм от заднего конца тела. Биология развития. Основным хозяином является человек, дополнительным - свиньи. Переносчиками служат кровососущие мухи рода Glossina, преимущественно G. palpalis. Отличительным признаком мухи цеце является сильно хитинизированный выступающий хоботок, способный прокалывать кожу даже таких животных, как носорог и слон, поэтому любая одежда человека не защитит от мухи цеце. Вторая особенность мухи - великолепная растяжимость стенок кишки, что позволяет ей поглощать количество крови, превышающее массу голодной мухи в десятки раз. Эти особенности обеспечивают надежность передачи возбудителя от донора реципиенту. Мухи цеце нападают в светлое время суток преимущественно в открытой природе, некоторые антропофильные виды могут залетать в поселки. Кровь пьют и самцы, и самки. Инвазионной стадией для переносчика является трипомастиготная форма. Грипаносомы попадают в организм переносчика при питании кровью инвазированного позвоночного животного или человека. Около 90 % трипаносом, поглощенных мухой цеце, погибают. Остальные размножаются в просвете ее средней и задней кишок. В первые дни после заражения разнообразные формы трипаносом находятся внутри комка поглощенной крови, окруженного перитрофической мембраной. Они мало отличаются от тех, которые присутствуют в крови человека, но несколько более короткие и имеют слабовыраженную ундулирующую мембрану. Затем трипаносомы выходят в просвет кишечника насекомого. При попадании в желудок мухи цеце после кровососания трипаносомы к 3-4-му дню изменяются и трансформируются в эпимастиготные формы, становятся более узкими и вытянутыми и интенсивно делятся. Проникнуть в слюнные железы трипаносомы могут и через гемоцель. В слюнных железах трипаносомы претерпевают ряд морфологических изменений, многократно делятся и превращаются в инвазионную для человека и позвоночных стадию - трипомастиготу. Развитие трипаносом в переносчике продолжается в среднем 15-35 дней в зависимости от температуры среды. Эффективное заражение мух происходит при температуре от 24 до 37оС. После заражения муха цеце способна передавать трипаносомы на протяжении всей жизни. Цикл развития в позвоночном хозяине. Способ заражения африканским трипаносомозом позволяет отнести его возбудителя к секции Salivaria, а заболевание - к «слюнным» (саливарным) трипаносомозам. После проникновения в кожу трипаносомы несколько дней сохраняются в подкожной клетчатке (рис. 2.9), а затем проникают в кровяное русло и лимфу, где происходит их простое бинарное деление (рис. 2.10). Иногда их обнаруживают в сосудистом сплетении мозга в стадии амастиготы, при этом выделяются разные формы трипаносом: тонкие и длинные, короткие, широкие и промежуточные трипомастиготные формы. Инкубационный период сонной болезни длится от нескольких дней до нескольких недель. 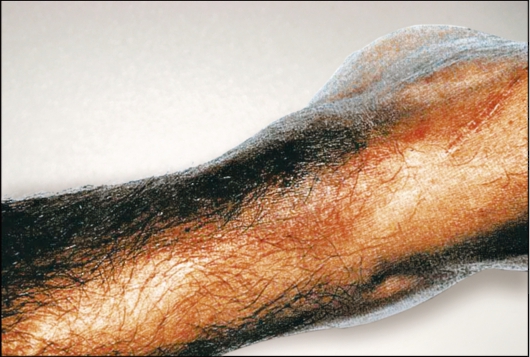 Рис. 9. Грипаносомный шанкр - самое раннее клиническое проявление. В шанкре содержится большое количество лимфы с активно делящимися трипаносомами. Шанкр чаще наблюдается при родезийской инфекции, чем при гамбийской.  Рис. 10. Trypanosoma gambiense в крови человека (препарат крови, окрашенный по Романовскому-Гимзе). Эпидемиология. Гамбийский тип трипаносомоза является преимущественно антропонозом. Основным источником инвазии служит человек, дополнительным - свинья. Переносчиками служат кровососущие мухи рода Glossina, преимущественно G. palpalis. Эти виды тенелюбивы, активны в светлое время суток. Они обитают в зарослях растительности по берегам рек и ручьев в ряде районов Западной и Центральной Африки. Мухи цеце живородящие. Самка откладывает единственную личинку прямо на поверхность почвы, в расщелины, под корни деревьев. Личинка сразу зарывается в почву и через 5 ч превращается в куколку. Вылет имаго происходит через 3-4 нед после окукливания. Достаточно одного укуса зараженной мухи, чтобы человек заболел сонной болезнью, поскольку минимальная инвазирующая доза трипаносом составляет 300-400 паразитов, а муха со слюной за один укус выделяет их около 400 тыс. Больной становится источником инвазии примерно с 10-го дня после заражения и остается им на протяжении всего периода болезни, даже в период ремиссии и отсутствия клинических проявлений. Теоретически возможен механический занос трипаносом в кровь человека кровососущими членистоногими при повторных кровососаниях после питания на больном человеке, так как на хоботке мух, слепней, комаров, клопов и других членистоногих возбудители сохраняют жизнеспособность в течение нескольких часов. Заражение может происходить также при гемотрансфузиях или при недостаточной стерилизации шприцев во время инъекций. Гамбийский тип трипаносомоза встречается в виде очагов в Западной и Центральной Африке между 15о с. ш. и 18о ю. ш. Летальность от трипаносомоза в Конго в середине прошлого века составляла около 24 %, а в Габоне - 27,7 %, поэтому трипаносомоз для стран тропической Африки представляет серьезную экономическую и социальную проблему. Заболеваемость носит сезонный характер. Пик приходится на сухой сезон года, когда мухи цеце концентрируются около оставшихся непересохшими водоемов, интенсивно используемых населением для хозяйственных нужд. Патогенез и клинические проявления. В течении болезни выделяют 2 стадии: гемолимфатическую и менингоэнцефалитическую, или терминальную (сонную болезнь в узком смысле слова). Гемолимфатическая стадия наступает через 1-3 нед после инвазирования и связана с распространением трипаносом по организму (по лимфатической и кровеносной системе) из места их первичного внедрения. Заболевание характеризуется длительным течением. В течение 2-3 нед первичное местное поражение спонтанно исчезает, на его месте остается пигментированный рубец. Грипаносомный шанкр возникает главным образом у некоренных жителей Африки. Одновременно с появлением первичного аффекта на коже туловища и конечностей могут возникнуть так называемые трипаниды, имеющие вид розовых или фиолетовых пятен различной формы диаметром 5-7 см. У африканцев на фоне темной кожи трипаниды заметны слабее, чем у европейцев. На лице, кистях, стопах и в месте эритематозных высыпаний заметны отеки, отмечается болезненность кожи при ее сжатии. В период развития шанкра или через несколько дней после его исчезновения паразиты появляются в крови и наблюдается лихорадка неправильного типа с подъемом температуры до 38,5оС (редко до 41 оС). К симптомам гемолимфатической стадии болезни относятся также слабость, потеря массы тела, тахикардия, боли в суставах, гепатоспленомегалия. Нарастают слабость и апатия, являющиеся ранними симптомами поражения ЦНС. Менингоэнцефалитическая стадия. Спустя несколько месяцев или лет у подавляющего большинства пациентов болезнь переходит во вторую стадию, которая характеризуется поражением ЦНС. Грипаносомы преодолевают гематоэнцефалический барьер и проникают в ЦНС. Наиболее характерным признаком второй стадии болезни является нарастающая сонливость, которая появляется преимущественно в дневное время, тогда как ночной сон часто бывает прерывистым и беспокойным. Сонливость настолько сильна, что больной может заснуть даже во время приема пищи. Постепенно нарастают и прогрессируют нейропсихические нарушения. При ходьбе больной волочит ноги, выражение его лица угрюмое, нижняя губа отвисает, изо рта течет слюна. Позднее появляются судороги, сменяющиеся параличами. Диагностика. Предварительный диагноз сонной болезни можно поставить и на основании клинических симптомов, однако неопровержимым подтверждением диагноза сонной болезни служит обнаружение Т. gambiense при лабораторных паразитологических исследованиях. Для выявления трипаносом проводят исследование пунктатов шанкра, увеличенных лимфатических узлов (до развития в них фиброзных изменений), крови, спинномозговой жидкости. Из полученного субстрата готовят нативные препараты и препараты, окрашенные по Романовскому-Гимзе. Профилактика и меры борьбы. Комплекс мероприятий по оздоровлению очагов сонной болезни включает выявление и лечение больных, общественную и индивидуальную профилактику населения, борьбу с переносчиками, серологические обследования, прежде всего людей, относящихся к группе риска (охотники, лесорубы, строители дорог и др.). Обследования следует проводить не реже 2 раз в год (перед и после сезона наибольшей опасности заражения). Иммунитет. Заболевание сонной болезнью не приводит к выработке стойкого иммунитета. Гечение болезни характеризуется периодическими обострениями, что обусловлено изменением морфологии, антигенных осо- бенностей и численности трипаносом в крови. Численность паразитов в крови хозяина претерпевает периодические колебания от чрезвычайно высокой до очень низкой. Во время высокой паразитемии в крови преобладают тонкие и длинные, а при низком ее уровне - короткие и толстые формы трипомастигот. Колебания численности паразитов в крови хозяина обусловлены защитными реакциями их организма и своеобразным свойством изменять свою антигенную структуру под влиянием этих реакций. Антигенная изменчивость при сонной болезни, особенно гамбийского типа, - механизм уклонения от воздействия защитных систем хозяина. Антигенная вариабельность обеспечивает возможность хронически рецидивирующего процесса при трипаносомозах. Увеличение численности паразитов в крови стимулирует развитие специфических антител (IgM-ответ хозяина), которые приводят к уничтожению большинства паразитирующей популяции. Те паразиты, которые сохранились (менее чем 1 %), претерпевают антигенную трансформацию, что делает их неуязвимыми для циркулирующих антител, однако по мере увеличения численности нового антигенного варианта возрастает концентрация соответствующих новых специфических антител. Каждый такой повторяющийся цикл занимает несколько дней, заканчиваясь появлением новых антигенных вариантов, резистентных к предшествовавшим вариантам антител. С каждым изменением поверхностных антигенов иммунный механизм позвоночного хозяина активируется, постепенно снижая способность иммунной системы к ответу. Число антигенов, продуцируемых трипаносомой, неизвестно, но было показано, что одна клетка способна продуцировать до 22 различных специфических для трипаносом антигенов. Материальным субстратом указанных вариаций служат поверхностные антигены гликопротеина (VSG), расположенные на оболочке паразита. По оценке, многочисленные варианты транскрибируются более чем в 1000 генов, что теоретически возможно для T.b. gambiense. Из этих вариантов только один является генетически доминантным в определенные моменты времени. Экспрессия каждого гена сопровождается перестройкой генов. Антигенная вариабельность этих паразитов делает получение эффективных вакцин, обеспечивающих длительную защиту, достаточно бесперспективным для контроля данного заболевания. |
