Лабораторные фх. Лабник по ф и к химии. Физическая и коллоидная химия сборник лабораторных работ СанктПетербург 2008 удк 541 076 (075. 83) Физическая и коллоидная химия. Сборник лабораторных работ
 Скачать 4.14 Mb. Скачать 4.14 Mb.
|
Лабораторная работа №11. Определение чисел переноса ионовЦель работы: определить числа переноса катиона и аниона заданного раствора электролита. Сущность метода. Метод определения чисел переноса по Гитторфу основан на измерении концентрации электролита в приэлектродных пространствах до и после электролиза с пересчетом на изменение количества вещества (Δn) катиона и аниона. Схема лабораторной установки показана на рис. ____. При электролиза серной кислоты происходит разложение воды. На катоде – восстановление водорода Оборудование и реактивы. Источник постоянного тока; реостат; амперметр; штатив с лапами – 2 шт.; графитовые электроды – 2 шт.; свинцовые электроды – 2 шт.; стакан химический объемом 100 мл – 2 шт.; стакан химический объемом 500 мл – 1 шт.; стакан химический объемом 50 мл – 1 шт.; бюретка с краном объемом 25 мл – 2 шт.; бюретка с шариком объемом 25 мл – 1 шт.; мерная пипетка (Мора) объемом 20 мл – 1 шт.; мерная пипетка объемом 50 мл – 1 шт.; мостик электролитический с краном – 1 шт.; колба коническая объемом 250 мл – 2 шт.; мерный цилиндр объемом 50 мл – 1 шт. наждачная бумага; серная кислота – 1 н. раствор; серная кислота – 0,02 н. раствор; груша; гидроксид натрия – 0,02 н. раствор; фенолфталеин. Выполнение работы1. В химические стаканы объемом 50 мл мерной пипеткой отобрать по 50 мл 0,02 н. раствора серной кислоты. 2. В стаканы поместить электролитический ключ. 3. Открыть кран ключа и при помощи груши заполнить его 0,02 н. раствором серной кислоты, после чего закрыть кран ключа. 4. Свинцовые электроды зачистить наждачной бумагой и поместить их в химические стаканы объемом 50 мл с 0,02 н. раствором серной кислоты. 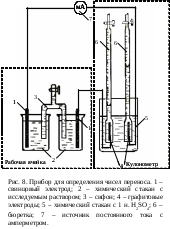 5. В химический стакан объемом 500 мл налить около 450 мл 1 н. раствора серной кислоты. 6. В химический стакан объемом 500 мл с серной кислотой опустить две бюретки с краном и графитовые электроды так, как показано на рис. 8. При помощи груши заполнить бюретки 1 н. раствором серной кислоты до середины бюретки и отметить уровень жидкости в каждой бюретке. Краны бюреток закрыть. 7. Оформить установку в соответствии с рис. 8. 8. Включить ток при максимальном сопротивлении реостата. 9. Установить значение силы тока 7 - 10 А. 10. Вести электролиз в течение часа. 11. Выключить ток. 12. Открыть кран электролитического мостика. 13. При помощи мерного цилиндра измерить объем жидкости в катодном и анодном пространстве (стакан объемом 50 мл № 1). 14. Из катодного пространства мерной пипеткой объемом 20 мл в две конические колбы объемом 250 мл отобрать 2 пробы. 15. К пробам добавить по 4 капли фенолфталеина. 16. Оттитровать пробы 0,02 н. раствором гидроксида натрия. 17. Из анодного пространства мерной пипеткой объемом 20 мл в две конические колбы объемом 250 мл отобрать 2 пробы. 18. К пробам добавить по 4 капли фенолфталеина. 19. Оттитровать пробы 0,02 н. раствором гидроксида натрия. Содержание протокола лабораторной работыЭлектролит _______________. Исходная концентрация электролита C0 = ______ н. Температура Т = ________°С. Атмосферное давление Ратм = _________ мм рт. ст. Объем 1 н. раствора серной кислоты в бюретках до начала электролиза V1 = ________ мл; V2 = ________ мл; Сила тока __________ А Продолжительность электролиза _____ мин. Уровень 1 н. раствора серной кислоты в бюретках по окончании электролиза V*1 = ________ мл; V*2 = ________ мл; h1 = ________ мм; h2 = ________ мм Концентрация титранта (гидроксида натрия) CT = ________ н. Объем раствора в катодном пространстве VK = __________ мл Объем пробы, взятой для анализа Va,K = ______ мл Объем титранта Средний объем титранта Объем раствора в анодном пространстве VА = __________ мл Объем пробы, взятой для анализа Va,A = ______ мл Объем титранта Средний объем титранта Обработка результатов экспериментаВычислить равновесную концентрацию электролита в катодном пространстве: Вычислить равновесную концентрацию электролита в анодном пространстве: Вычислить убыль вещества в катодном пространстве: Вычислить прибыль вещества в анодном пространстве: Вычислить объем выделившегося кислорода: Рассчитать давление газа в бюретке: где Вычислить количество эквивалентов газа, которое соответствует количеству электричества, прошедшего через раствор, т.к. 1 фарадей электричества переносит 1 эквивалент вещества: где n – согласно закону эквивалентов – количество вещества, разложившееся под действием заданного количества электричества Давление газа следует перевести в Па (760 мм рт.ст. = 1,013·105Па), объем газа – в м3 (1 мл = 10−6 м3). Рассчитать число переноса сульфат-иона: Проверить правильность определения чисел переноса: Содержание отчета по лабораторной работе1. Название работы. 2. Цель работы. 3. Ход эксперимента. 4. Экспериментальные данные (см. протокол к лабораторной работе). 5. Обработка экспериментальных данных. 6. Вывод. |
