Лабораторные фх. Лабник по ф и к химии. Физическая и коллоидная химия сборник лабораторных работ СанктПетербург 2008 удк 541 076 (075. 83) Физическая и коллоидная химия. Сборник лабораторных работ
 Скачать 4.14 Mb. Скачать 4.14 Mb.
|
Лабораторная работа № 1. Определение интегральной теплоты растворения соли и теплоты гидратообразованияЦель работы: определение теплового эффекта процессов растворения соли и гидратообразования. Сущность работы: при растворении солей часто наблюдается экзо- или эндотермический эффект. Для определения теплового эффекта процесса гидратообразования необходимо знать теплоемкость системы и изменение температуры системы вызванное процессами растворения безводной соли и ее кристаллогидрата Оборудование и реактивы.Стеклянный стакан объемом 500 мл – 1 шт. Фарфоровый или стеклянный внешний стакан объемом 750 мл – 1 шт. Стеклянная палочка для перемешивания – 1 шт. Кристаллизатор – 1 шт. Штатив с лапками – 1 шт. Термометр Бекмана – 1 шт. Мерный цилиндр объемом 100 мл (для определения объема ртутного баллона термометра Бекмана) – 1 шт. Мерный цилиндр объемом 500 мл – 1 шт. Секундомер – 1 шт. Весы лабораторные – 1 шт. Безводная соль (сульфат меди, никеля или магния). Кристаллогидрат этой соли. Выполнение работы1. Собрать калориметрическую установку. 2. Получить у преподавателя наименование соли, с которой будет выполняться эксперимент. 3. Решить задачу. Масса безводной соли 5 г. Какую массу будет иметь эквимолярное количество кристаллогидрата этой соли (можно проверить правильность решения у преподавателя)? 4. Отобрать навески безводной соли и кристаллогидрата. 5. Взвесить на технических весах стеклянный внутренний стакан и стеклянную палочку для перемешивания mст. 6. Определить объем ртутного баллона термометра. Для этого опустить нос термометра в мерный цилиндр объемом 100 мл, куда предварительно налито 50 мл воды и по разности уровней воды определить объем ртути, VHg. 7. Во внутренний стакан калориметрической установки поместить 300 мл (300 г) дистиллированной воды V и опустить в воду термометр Бекмана. 8. Пустить секундомер и через каждые 30 секунд записывать показания температуры (см. табл.) по термометру Бекмана в течение 5 минут (10 показаний) при постоянном перемешивании (начальный период). 9. Не прекращая отсчета времени и измерения температуры высыпать навеску безводной соли во внутренний стакан калориметра и размешать до полного растворения (главный период). По-прежнему через каждые 30 секунд записывать показания термометра Бекмана до установления постоянной температуры в калориметрической установке. 10. Получить еще 10 показаний при постоянной температуре как в п. 8 (конечный период). 11. Повторить п.п. 7 – 10 с кристаллогидратом данной соли. Содержание протокола лабораторной работыНазвание исследуемой соли и ее формула_________. Формула кристаллогидрата__________. Масса безводной соли Масса кристаллогидрата (с решением задачи п. 3) Масса стеклянного внутреннего стакана + масса стеклянной палочки mст = …, г. Объем дистиллированной воды во внутреннем стакане Объем ртутного баллона термометра Бекмана VHg, мл. Масса раствора безводной соли Масса раствора кристаллогидрата Измерения температуры с кристаллогидратом:
Обработка результатов экспериментаПри оформлении работы все расчеты производятся для каждого опыта отдельно, после чего берется среднее арифметическое значение для конечных результатов расчета. 1. Построить график зависимости Т = f(τ), отражая показания температуры по начальному и конечному периодам. 2. Соединить последнюю точку начального периода с начальной точкой конечного периода. 3. Полученную линию разделить пополам. 4. Через точку середины провести перпендикуляр к оси абсцисс. 5. Продлить температурные зависимости начального и конечного периодов до пересечения с перпендикуляром – получим значение изменения температуры Т. 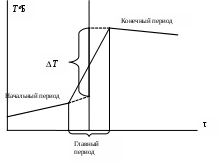 6. Рассчитать теплоемкость калориметрической установки по уравнению: Сcal = Cр-рmp-p + СHgVHg + Cстmст, Дж/К, где Cр-р – удельная теплоемкость раствора, 4,18 Дж/гК; mp-p – масса раствора во внутреннем стакане, г; СHg – объемная теплоемкость ртути и стекла, 1,92 Дж/см3К, VHg – объем баллона термометра, содержащего ртуть, мл; Cст – удельная теплоемкость стекла, 0,79 дж/гК; mст – общая масса стеклянных частей калориметрической установки, г. 7. Вычислить интегральную теплоту растворения безводной соли и кристаллогидрата по уравнению: где nсоли – количество вещества соли (безводной или кристаллогидрата), моль. 9. Вычислить тепловой эффект процесса гидратации по уравнению: Содержание отчета по лабораторной работе1. Название работы. 2. Цель работы. 3. Ход эксперимента. 4. Экспериментальные данные (см. протокол к лабораторной работе). 5. Обработка экспериментальных данных. 6. Вывод. | ||||||||||||||||||
