Лабораторные фх. Лабник по ф и к химии. Физическая и коллоидная химия сборник лабораторных работ СанктПетербург 2008 удк 541 076 (075. 83) Физическая и коллоидная химия. Сборник лабораторных работ
 Скачать 4.14 Mb. Скачать 4.14 Mb.
|
Лабораторная работа № 19. Исследование молекулярной адсорбции растворенного вещества из растворов на активированном углеЦель работы: Построить изотерму адсорбции, проверить применимость к ней уравнений Фрейндлиха и Ленгмюра, оценить удельную поверхность активированного угля. Сущность работы: для границы раздела «твердое тело – раствор ПАВ» возможно прямое экспериментальное определение удельной адсорбции, например, статическим методом. В статическом методе определяют концентрацию исходного раствора, перемешиванию навески адсорбента в каждом раствора в течение определенного времени, необходимого для установления адсорбционного равновесия, фильтрованию и определению равновесной концентрации растворенного вещества в фильтратах. Оборудование и реактивы. Перемешивающее устройство; бюретка объемом 25 мл – 1 шт.; мерная пипетка объемом 50 мл – 1 шт.; мерная пипетка объемом 5 мл – 1 шт.; колбы круглые объемом 250 мл – 4 шт.; колбы конические объемом 250 мл – 6 шт; стакан химический объемом 150 мл – 1 шт.; стакан химический объемом 50 мл – 1 шт.; стакан химический объемом 250 – 300 мл – 1 шт.; воронка химическая - 4 шт.; фильтр беззольный «белая лента» – 4 шт.; гидроксид натрия – 0,1 н.. раствор; фенолфталеин; Карбоновые кислоты (муравьиная, уксусная) – растворы (концентрация раствора кислоты указана на емкости с реактивом). Выполнение работы1. Получить у преподавателя раствор кислоты. 2. Отобрать пробу кислоты в химический стакан объемом 150 мл 3. Приготовить 4 раствора путем последовательного разведения в 2 раза: в круглые колбы №№ 2, 3, 4 отобрать мерной пипеткой по 50 мл дистиллированной воды; в колбу № 1 и 2 мерной пипеткой объемом 50 мл поместить по 50 мл исходного раствора кислоты; из колбы №2 50 мл раствора перенести в колбу №3 и перемешать; из колбы №3 50 мл раствора перенести в колбу №4; из колбы №4 отобрать 50 мл раствора и выбросить. 4. В каждую колбу с приготовленными растворами высыпать по навеске 3 г активированного угля. 5. Колбы поставить на перемешивающее устройство на 15 минут. 6. Осторожно слить растворы через бумажный в конические колбы под теми же номерами., стараясь, чтобы основная масса угля осталась в круглой колбе. 7. Определить концентрацию кислоты в исходном С0 и равновесных С* растворах по следующей методике. В 2 конические колбы отобрать по 5 мл пробы; добавить немного дистиллированной воды (до толщины слоя жидкости около 5 мм); прилить 2-3 капли индикатора – фенолфталеина; отобрать раствор щелочи в химический стакан объемом 50 мл; из стакана раствор щелочи налить в бюретку, выпустить воздух из носика бюретки, для чего поднять носик бюретки, подставить стакан со щелочью и нажать на шарик; довести объем щелочи в бюретке до отметки «0»; титровать одну из колб с пробой кислоты раствором гидроксидом натрия до перехода окраски фенолфталеина от бесцветной к малиновой, сохраняющейся при перемешивании в течение 30 с; довести объем щелочи в бюретке до отметки «0»; провести титрование пробы во второй конической колбе. Содержание протокола лабораторной работыМасса навески угля g = …………….г Концентрация раствора щелочи С(NaOH) = …………….экв/л Слабый электролит (название и химическая формула) Ориентировочная концентрация слабого электролита (указана на емкости с кислотой) Результаты анализа проб:
Обработка результатов эксперимента1. Заполнить таблицу
С0, i рассчитывают по результатам титрования с учетом разведения пробы (С0,2 = С0/2, С0,3 = С0/4 и т. д.). С* вычисляют по результатам титрования: С = С0,i С*. Удельную адсорбцию растворенного вещества Г вычисляют по уравнению: где V – объем кислоты, взятый на адсорбцию, л; ms – навеска адсорбента (активированного угля), кг. 2. Построить изотерму удельной адсорбции кислоты в координатах Г = f(C). 3. Построить изотерму адсорбции Фрейндлиха lgГ = lga + (1/n)lgC (линейная зависимость lgГ = f(C)) и вычислить коэффициенты уравнения Фрейндлиха. 4. Построить зависимость в координатах С/Г = f(C) и 1/Г = f(1/C) (изотерма адсорбции по Ленгмюру 5. Определить константы уравнения Ленгмюра Г∞ и K по графику С/m = f(C): 6. Оценить удельную поверхность активированного угля по уравнению: г 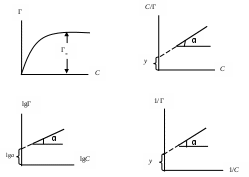 де NA – число Авогадро; SM – площадь поперечного сечения молекулы адсорбата, равная для карбоновых кислот 20,51020 м2. Содержание отчета по лабораторной работе1. Название работы. 2. Цель работы. 3. Ход эксперимента. 4. Экспериментальные данные (см. протокол к лабораторной работе). 5. Обработка экспериментальных данных. 6. Вывод. | ||||||||||||||||||||||||||||||||||||||||||||||||||||
