Лабораторные фх. Лабник по ф и к химии. Физическая и коллоидная химия сборник лабораторных работ СанктПетербург 2008 удк 541 076 (075. 83) Физическая и коллоидная химия. Сборник лабораторных работ
 Скачать 4.14 Mb. Скачать 4.14 Mb.
|
Лабораторная работа № 20. Исследование обменной адсорбции ионовЦель работы: определить характеристики ионообменной смолы: полную обменную емкость (ПОЕ) и обменную емкость до проскока (ДОЕ) динамическим методом. Сущность работы: Получить выходную кривую сорбента. Через колонку (бюретку) заполненную слоем ионита высотой не менее 10 см медленно пропускают раствор соли металла известной концентрации. На выходе из колонки раствор собирают порциями в мерные цилиндры, точно определяя объем каждой порции и содержание поглощаемых ионов. По данным эксперимента строят график в координатах: объем раствора, прошедшего через ионит – концентрация иона. По графику определяют ПОЕ и ДОЕ. Оборудование и реактивы. Колонка с катионитом; мерный цилиндр объемом 10 мл – 2 шт.; пипетка Мора объемом 10 мл – 1 шт.; колбы конические объемом 250 мл – 2 шт.; бюретка для титрования объемом 25 мл – 1 шт.; стакан химический объемом 100 мл – 2 шт.; стакан химический объемом 50 мл – 2 шт.; Трилон Б – 0,05 М раствор; мурексид; хлорид аммония – 1 н. раствор; гидроксид аммония – разбавленный 1:1; сульфаты меди, никеля, кобальта – 0,05 н. растворы. Выполнение работы1. Получить от преподавателя раствор соли металла для исследования. 2. Отобрать пробу раствора соли металла в маркированный химический стакан объемом 100 мл. 3. Провести анализ исходного раствора соли металла. Анализ содержания меди (2+): отобрать мерной пипеткой в конические колбы аликвоту объемом 10 мл; прилить дистиллированную воду до объема 20-30 мл; добавить по каплям при перемешивании аммиак до получения прозрачного синего раствора, добавить немного сухого индикатора «мурексид»; отобрать раствор трилона Б в химический стакан объемом 50 мл; из стакана раствор трилона Б налить в бюретку, выпустить воздух из носика бюретки, для чего поднять носик бюретки, подставить стакан с трилоном Б и нажать на шарик; довести объем трилона Б в бюретке до отметки «0»; титровать одну из колб с пробой раствором трилона Б до перехода окраски до перехода окраски индикатора в эквивалентной точке от желтой (хаки) к сиренево-фиолетовой; довести объем щелочи в бюретке до отметки «0»; провести титрование пробы во второй конической колбе. Анализ содержания кобальта и никеля: отобрать мерной пипеткой в конические колбы аликвоту объемом 10 мл; прилить дистиллированную воду до объема 20-30 мл; с помощью мерного цилиндра добавить 5 мл раствора хлорида аммония; добавить немного сухого индикатора «мурексид» отобрать раствор трилона Б в химический стакан объемом 50 мл; из стакана раствор трилона Б налить в бюретку, выпустить воздух из носика бюретки, для чего поднять носик бюретки, подставить стакан с трилоном Б и нажать на шарик; довести объем трилона Б в бюретке до отметки «0»; титровать одну из колб с пробой раствором трилона Б до перехода окраски до перехода окраски индикатора в эквивалентной точке от желтой к фиолетовой; довести объем щелочи в бюретке до отметки «0»; провести титрование пробы во второй конической колбе. Желтую окраску раствора поддерживают аммиаком: если в процессе титрования раствор краснеет, то добавить несколько капель аммиака. 4. Налить в колонку раствор соли металла. Осторожно открыть кран так, чтобы раствор проходил через ионит со скоростью 3 – 4 мл в минуту (примерно 1 капля в секунду). 5. Фильтрат собирать в мерный цилиндр порциями по 10 мл. 6. Каждую порцию анализировать на содержание в ней иона металла. 7. Пропускать раствор соли металла через колонку продолжать до тех пор, пока концентрация металла на выходе из колонки не станет равной исходной. ИЛИ! Объем трилона Б на титрование порции из колонки не станет равным объему трилона Б при титровании исходной соли металла. Содержание протокола лабораторной работыНаименование соли металла и ее химическая формула Ориентировочная концентрация соли металла (указана на емкости с реактивом) Концентрация раствора трилона Б СТ = ________ Таблица экспериментальных данных
Обработка результатов эксперимента1. Заполнить таблицу:
2. Построить график выходной кривой ионообменной адсорбции 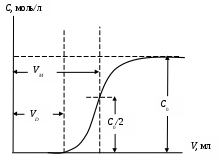 Рис. 16. Обработка выходной кривой ионообменной адсорбции. 3. Вычислить полную обменную емкость ионита по уравнению: где С0 – исходная концентрация иона металла в растворе, моль/л; VМ – объем раствора, соответствующий половине исходной концентрации и определяемый графически по выходной кривой, мл; m – масса сухого ионита, г. 4. Вычислить динамическую обменную емкость до проскока по уравнению: Содержание отчета по лабораторной работе1. Название работы. 2. Цель работы. 3. Ход эксперимента. 4. Экспериментальные данные (см. протокол к лабораторной работе). 5. Обработка экспериментальных данных. 6. Вывод. | ||||||||||||||||||||||||||||||||||||||||||||||||||||
