Posibnyk_chimiya_ingener-конвертирован. Харьковский национальный автомобильно дорожный университет
 Скачать 4.12 Mb. Скачать 4.12 Mb.
|
§15. Валентность и степень окисленияПрочитайте слова и словосочетания, переведитеих. валентность возбуждённое состояние неспаренные электроны степень окисления поглощать энергию  Прочитайте текст и ответьте на вопросы сначала устно,потом письменно.Понять физический смысл валентности и структурных формул помогает учение о строении атома и химической связи. Атомы элементов при образовании соединений могут отдавать или присоединять электроны и  образовывать общие электронные пары. Электроны, которые наиболее слабо связываются с ядром – это электроны внешних незавершённых уровней.  Валентность определяет число химических связей, которыми данный атом связывается с другими атомами. Число связей равно числу его неспаренных электронов. Поэтому валентность определяет число неспаренных электронов в атоме. При этом не учитывается полярность связей, валентность не имеет знака. Валентность не может быть отрицательной и не может равняться нулю. В настоящее время для характеристики состояния атома в соединении используют понятие «степень окисления». Степень окисления может иметь отрицательное, положительное и нулевое значения. Для определения степени окисления каждого элемента в соединении следует запомнить правила: Степень окисления простых веществ равна нулю. Гидроген имеет степень окисления +1, кроме гидридов металлов, в которых степень окисления гидрогена –1. Все металлы в соединениях имеют только положительную степень окисления. Степень окисления оксигена в большинстве соединений –2. В пероксидах степень окисления –1, в флуор оксиде F2O она равна +2. Флуор имеет только отрицательную степень окисления –1. Алгебраическая сумма степеней окисления атомов в молекуле равна нулю.  Напишите ответы навопросы. Вспомните, что такое валентность? Чем определяется валентность? Что такое степень окисления?  Определите степень окисления хрома всоединениях: Cr2O3; Cr(OH)2; K2Cr2O7; Cr2(SO4)3; CrO3; Cr(OH)3; H2CrO4 Определите степень окисления галогенов F, Cl, Br,I: HCl; SiF4; NaClO4; F2; Cl2; HClO3; Br2O7; F2O; I2O5 Укажите причину инертности неонаNe: малый заряд ядра; большое количество электронов на внешнем уровне; завершённость внешнего электронного слоя; близость электронов до ядра атома.  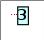  Установите соответствие между символом элемента и максимальным количеством связей, которые он может образовывать за счёт перекрывания неспаренныхэлектронов: Установите соответствие между символом элемента и максимальным количеством связей, которые он может образовывать за счёт перекрывания неспаренныхэлектронов: 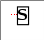 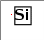 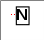 ☻Задание для любознательных: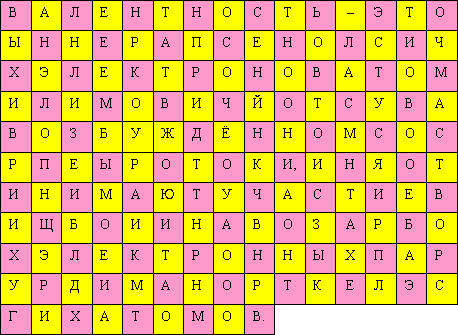 Отгадайте зашифрованное предложение. Guess cryptic sentence. Devinez phrase sibylline. Отгадайте зашифрованное предложение. Guess cryptic sentence. Devinez phrase sibylline. Какие классификации химических элементов вы знаете? В каком году Д.И. Менделеев открыл периодический закон и создал периодическую систему элементов? Сформулируйте периодический закон. В каком году Э. Резерфорд предложил ядерную модель атома, почему она носит такое название? Сформулируйте постулаты Н. Бора. В чём заключается физический смысл порядкового номера элемента в периодической системе согласно Г. Мозли? Сформулируйте современную протонно-нейтронную теорию строения атома. Что такое изотопы? Что образует электрон, когда вращается вокруг ядра? Как можно описать состояние электрона? Какие квантовые числа вы знаете? Сформулируйте принцип найменьшей энергии. Сформулируйте принцип Паули. Сформулируйте правило Хунда. Чему равно число электронов на последнем уровне у элементов главных подгрупп? Чему равно число энергетических уровней у атомов? Какие процессы лежат в основе химических реакций? Какие электронные слои называются завершёнными? Что такое энергия ионизации? Что называется энергией сродства к электрону? Как изменяется радиус атома в периоде и группе? Как изменяются металлические свойства в периоде и группе? В чём заключается значение периодического закона Д.И. Менделеева? В результате чего образуется химическая связь в каждом соединении? Какие электроны называются валентными? В чём причина образования химической связи? Как называется тип химической связи, которая образуется при помощи общих пар электронов? Назовите характеристики ковалентного типа связи. Что такое кристаллическая решётка? Какие физические свойства характерны для соединений с ковалентным типом связи? Какой тип связи образуется за счёт электростатического взаимодействия ионов? Какие физические свойства характерны для соединений с ионным типом связи? Что называется металлическим типом связи? Какой тип связи возникает между молекулами? Чем определяется валентность атома? Что такое степень окисления? 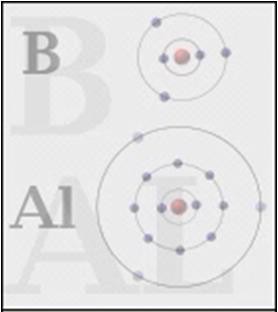   |
