История урологии
 Скачать 6.12 Mb. Скачать 6.12 Mb.
|
|
Рис. 11.4. Трансэзофагальная сонограмма во время операции. Почечный опухолевый тромб (1) в правом предсердии (2)
(рис. 11.3). В процессе операции УЗИ с использованием внутрипищевод-ного (трансэзофагального) датчика позволяет контролировать положение и смещение опухолевого почечного тромба в полой вене и правом предсердии (рис. 11.4). При ультразвуковой доплерографии можно обнаружить атипичную васкуляризацию, опухолевый тромбоз почечных и нижней полой вен, нарушения структуры паренхимы. С помощью сонографии выявляют увеличенные лимфатические узлы и метастазы в печени. Экскреторная урография позволяет установить характерные призна- ки опухолевого поражения и оценить функцию контрлатеральной почки. Она мало информативна при начальных стадиях заболевания и небольших размерах опухоли. При опухолях более 3-4 см на экскреторных урограммах можно увидеть дефект наполнения лоханки и/или чашечек вплоть до их ампутации, сегментарное расширение чашечно-лоханочного комплекса. деформацию или укорочение чашечек с оттеснением их в сторону, медиальную девиацию мочеточника (рис. 11.5). КТ является методом выбора в диагностике и стадировании почечно-кле-точного рака. Она позволяет не только выявить факт наличия новообразования, но и оценить его размеры, локализацию, отношение к чашечно-лоханочной системе, окружающим органам и тканям, а также наличие регионарных и отдаленных метастазов. На КТ рак почки визуализируется как объемное образование с гомогенной или неоднородной внутренней структурой, с плотностью ниже или выше нормальной почечной паренхимы (рис. 11.6). Оно может распространяться на паранефральную клетчатку и почечный синус, деформировать и вовлекать в опухолевый процесс ча-шечно-лоханочную систему. С помощью КТ можно определить инвазию опухоли в почечную, полую вены и правое предсердие (рис. 11.7). При контрастировании
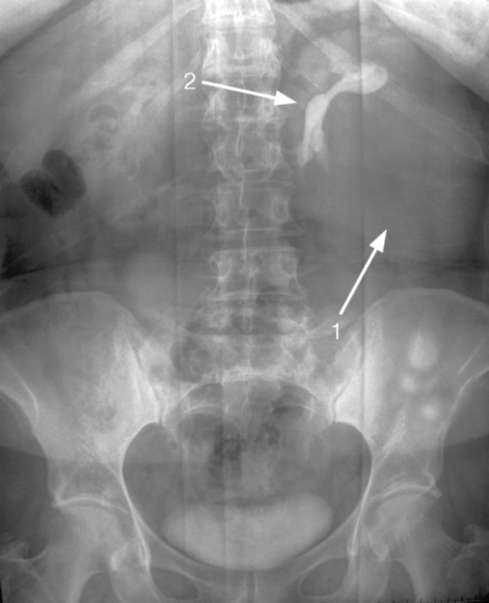 Рис. 11.5. Экскреторная урограмма. Опухоль левой почки (1), деформация опухолью чашечно-лоханочной системы (2) 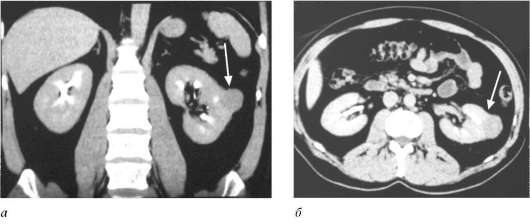 Рис. 11.6. Мультиспиральная КТ: а - фронтальная проекция; б - аксиальная проекция на уровне почечных ворот. Опухоль левой почки (стрелки) рак почки чаще характеризуется меньшим усилением плотности, чем нормальная паренхима, и более четко отграничен от здоровой почечной ткани. Чувствительность КТ в диагностике новообразований почки приближается к 100 %. МРТ позволяет установить диагноз и является методом выбора при выявлении размеров и границ опухолевого тромба в почечной и нижней полой венах (рис. 11.8). Этот метод незаменим для пациентов с аллергией на йодсодержащие 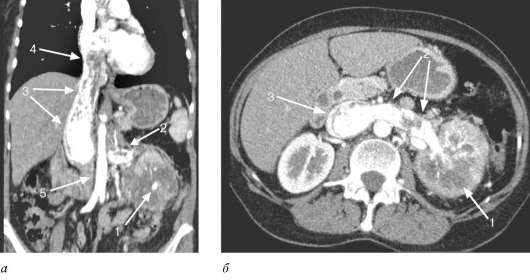 Рис. 11.7. Мультиспиральная КТ: а - фронтальная проекция; б - аксиальная проекция на уровне ворот почки. Рак левой почки с опухолевым тромбом, распространяющимся по почечной и полой вене до правого предсердия: 1 - опухоль почки; 2 - опухолевый тромб в почечной вене; 3 - опухолевый тромб в нижней полой вене; 4 - дистальная часть опухолевого тромба в правом предсердии; 5 - аорта 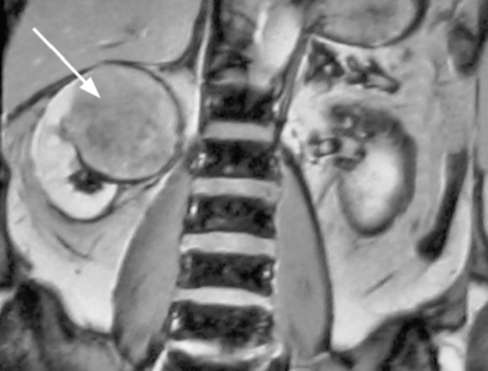 Рис. 11.8. МРТ. Опухоль правой почки (стрелка) рентгеноконтрастные препараты и для больных с опухолью почки и хронической почечной недостаточностью. Аортография (рис. 11.9), селективная почечная артериография(рис. 11.10) и венокаваграфия (рис. 11.11) уступают в информативности вышеуказанным методам и в основном используются для уточнения стадии заболевания, дифференциальной диагностики с за-брюшинными неорганными опухолями и новообразованиями надпочечника, выявления объема и границ опухолевого тромбоза и выяснения состояния ангиоархитектоники поч- ки при ее планируемой резекции (рис. 62, см. цв. вклейку). Характерными признаками опухоли почки являются: расширение почечной артерии с пораженной стороны; наличие участков гиперваскуляризации; изменение сосудистого рисунка; наличие беспорядочных, различной величины и формы скоплений рентгеноконтрастного вещества в опухолевой ткани («симптом озер и лужиц»); дефекты наполнения в просвете вен при опухолевой инвазии.
Радионуклидные методы исследования используются для выявления очаговых поражений почки, обусловленных опухолью, оценки раздельного функционального состояния почек и обнаружения метастатического поражения костной ткани. При обследовании пациента с опухолью почки необходимо провести исследования, направленные на выявление возможного метастазирования. 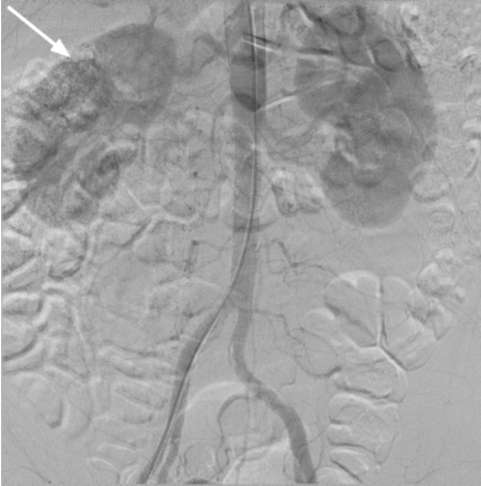 Рис. 11.9. Аортограмма. Опухоль правой почки (стрелка) 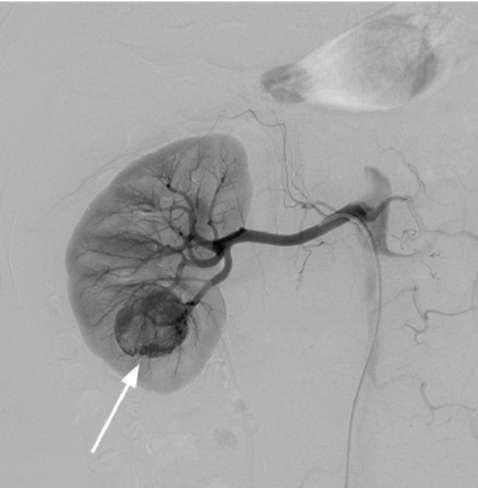 Рис. 11.10. Селективная ангиограмма. Опухоль нижнего сегмента почки (стрелка) 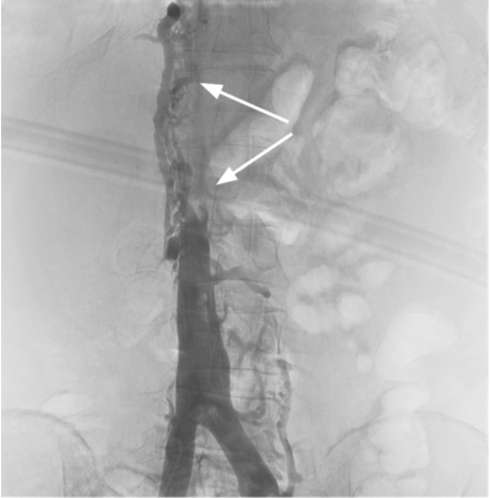 Рис. 11.11. Венокаваграмма. Опухолевый почечный тромб в нижней полой вене (стрелки) Метастатическое поражение лимфатических узлов, головного мозга, позвоночника, легких (рис. 11.12), печени диагностируется при помощи лучевых методов и МРТ. Костные метастазы позволяют выявить рентгенография и остеосцинтиграфия. Цистоскопия, выполненная при макрогематурии, позволяет обнаружить выделение крови из устья мочеточника и тем самым определить сторону поражения, а также исключить ее источник в мочевом пузыре (рис. 13, см. цв. вклейку). Дифференциальная диагностика. Опухоль почки дифференцируют с ее солитарной кистой, поликистозом, гидронефрозом, нефроптозом, карбункулом, абцессом, эхинококкозом почки, забрюшинными неорганными опухолями и новообразованиями надпочечника. При УЗИ киста определяется как гипоэхогенное образование с четкими ровными контурами и феноменом дорсального усиления. Такой же характерный вид киста почки имеет при КТ. Выполняя различные вмешательства по поводу кисты почки (пункция, иссечение), необходимо проводить цитологическое исследование ее содержимого на наличие атипичных клеток. Для поликистоза характерно двустороннее поражение и разной степени выраженности хроническая почечная недостаточность. При пальпации обнаруживаются бугристые, плотные смещаемые почки. Отличить их от двусторонних опухолей почек позволяют УЗИ, экскреторная урография и КТ.
Абсцесс (карбункул) или туберкулез почки при УЗИ могут быть приняты за опухоль, однако они имеют соответствующую клиническую картину. Правильный диагноз позволяют установить КТ, МРТ и артериография почки. 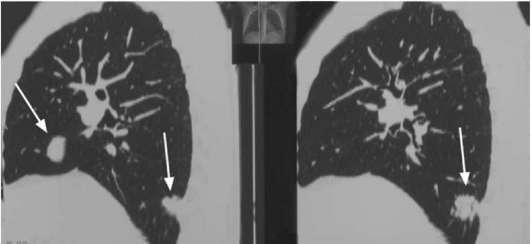 Рис. 11.12. КТ легких. Метастазы рака почки (стрелки) Почка бывает увеличена и может пальпироваться при гидронефрозе. Забрю-шинные неорганные опухоли и опухоли надпочечника могут тесно предлежать к почке и симулировать ее новообразование. Правильный диагноз устанавливается на основании результатов УЗИ, экскреторной урографии и КТ и селективной артериографии почки. Соответствующий анамнез, эозинофилия, эхинококкурия, кольцевидное обызвествление в проекции почки, положительные специфические реакции лежат в основе дифференциальной диагностики опухолей и эхинококкоза почки. Лечение рака почки оперативное. Консервативная терапия является вспомогательным методом, малоэффективна и применяется в основном при метастатическом или рецидивном раке почки. Она включает иммунотерапию (интерферон-альфа, интерлейкин-2), химиотерапию (винбластин, флуороурацил) и гормонотерапию. Определенные перспективы связаны с достижениями молекулярной генетики почечно-клеточного рака, которые позволили разработать таргетные препараты. Эти лекарственные средства подразделяются на три группы: 1) тирозинкиназные (мультикиназные) ингибиторы - сорафениб и суни-тиниб; 2) ингибиторы mTOR - темсиролимус и эверолимус; 3) моноклональ-ные антитела - бевацизумаб. В настоящее время производится их дальнейшее изучение, что позволяет надеяться на скорое появление новых лекарственных средств для лечения больных раком почки. Низкая эффективность химиотерапии при почечно-клеточном раке обусловлена феноменом мультилекарственной резистентности, связанной с геном р170. Этот протеин, изменяя внутриклеточную структуру карциномы, снижает поступление противоопухолевых препаратов в клетку и усиливает их выведение из нее. К наиболее часто назначаемым цитотоксическим препаратам относятся винбластин (эффективен у 6-9 % больных) и 5-флуороурацил (эффективен у 5-8 % больных).
Лучевая терапия из-за радиорезистентности рака почки также не получила широкого распространения. Ее используют с паллиативной целью, для снижения болевого синдрома у больных с метастазами в костях. В качестве паллиативного метода лечения у ряда больных раком почки выполняют эмболизацию почечной артерии. К ней прибегают при угрожающих кровотечениях у пациентов с неоперабельными большими опухолями почки и метастазами в регионарные лимфатические узлы. Оперативное лечение включает: ■ радикальную нефрэктомию; ■ резекцию почки; ■ малоинвазивные чрескожные методы деструкции опухоли (радиоаблация, криоаблация, микроволновая и лазерная аблация, аблация HIFU). Удаление опухоли оперативным путем является единственным радикальным методом лечения рака почки. Оно заключается в выполнении радикальной нефрэк-томии или резекции почки с опухолью в пределах здоровых тканей. В связи с этим показания к оперативному лечению рака почки максимально расширены. Абсолютными противопоказаниями являются только поздние стадии заболевания с множественными метастазами и кахексией или тяжелая сопутствующая патология, не позволяющая выполнить под наркозом расширенное оперативное вмешательство. Операция должна выполняться с учетом основных онкологических требований: абластичности и радикальности. Абластичность осуществляется предварительным (до начала манипуляций на почке) лигированием почечных сосудов, что достигается использованием адекватного доступа. При операциях на почке применяют следующие оперативные доступы: ■ транслюмбальный; ■ трансторакальный (тораколюмбальный, торакофренолюмбальный, тора-коабдоминальный); ■ трансперитонеальный (срединная, параректальная, косая и поперечная лапаротомия); ■ эндовидеохирургический (лапароскопический), в том числе с использованием роботассистированной техники.
Внебрюшинный люмботомический доступ сейчас используется редко, в основном при небольших по размеру опухолях, позволяющих соблюсти принципы абластичности. Широкое распространение в настоящее время получили трансторакальные и лапаротомные доступы, которые позволяют первоначально раздельно перевязать и пересечь артерию и вены, выделить и удалить почку единым блоком с жировой капсулой и фасциями, выполнить расширенную лимфаденэктомию, осуществить ревизию окружающих органов и при необходимости удалить опухолевые тромбы из полой вены, резецировать ее стенку, кишку или поджелудочную железу и выполнить спленэктомию. Соблюдение этих правил позволяет свести к минимуму вероятность интраоперационного метастазирования и местного рецидива опухоли. Органосохраняющие операции при раке почки выполняются по абсолютным, относительным или избирательным показаниям. Абсолютные показания - рак единственной или единственной функционирующей почки, двусторонний рак почек, рак почки при наличии хронической почечной недостаточности в результате неонкологических заболеваний противоположной или обеих почек. Относительные показания - почечно-клеточный рак при наличии хронического заболевания противоположной почки. Избирательные показания - рак почки при здоровой противоположной почке. Различают следующие органосохраняющие операции: ■ резекция почки (плоскостная, фронтальная, клиновидная) - удаление опухоли с прилежащим участком здоровой ткани шириной не менее 1 см (рис. 68, см. цв. вклейку); ■ энуклеация опухолевого узла - он вылущивается из паренхимы вместе с капсулой; ■ энуклеорезекция - удаление опухоли с прилежащим участком здоровой ткани шириной менее 1 см. Широкое распространение за последнее десятилетие получили эндовидео-хирургические (лапароскопические) операции на почке, которые все чаще выполняются с помощью роботизированной техники. Показаниями к такого рода операциям при раке почки являются размеры опухоли не более 5-7 см
при отсутствии инфильтрации сосудистой ножки и предшествующих операций на почке. Преимущества данного подхода заключаются в лучшей визуализации операционного поля, меньшей кровопотере и травматичности операции, быстрой реабилитации больных и хорошем косметическом эффекте. Этапы операции такие же, как при открытом доступе: первоначально выполняется раздельное лигирование и пересечение артерии и вены, почка выделяется единым блоком вместе с жировой капсулой и фасциями, помещается в специальный синтетический контейнер (мешочек) и удаляется через небольшой умбили-кальный разрез (рис. 69, см. цв. вклейку). Эндовидеохирургический метод используют и при резекции почки (рис. 68, см. цв. вклейку). Деструкцию опухолевой ткани можно осуществить с помощью минимально инвазивных высокотехнологичных методов лечения. Они выполняются при локализованном раке почки и включают радиочастотную, крио-, микроволновую и лазерную аблацию, а также аблацию высокоинтенсивной сфокусированной ультразвуковой волной (HIFU). Прогноз определяется клинико-морфологическим вариантом опухоли, степенью ее дифференцировки, наличием регионарных и отдаленных метастазов. Выживаемость после радикального оперативного лечения варьирует в широких пределах и зависит от стадии опухоли. При начальных локализованных формах заболевания пятилетняя выживаемость, по данным различных авторов, составляет от 60 до 90 %. Контрольные обследования больных почечно-клеточным раком после оперативного лечения необходимо проводить 1 раз в 4 месяца на протяжении первых трех лет, каждые 6 месяцев в течение пяти лет, а затем 1 раз в год. 11.2. ЭМБРИОНАЛЬНАЯ НЕФРОБЛАСТОМА (ОПУХОЛЬ ВИЛЬМСА) Эмбриональная нефробластома была подробно изучена и описана М. Wilms в 1899 году. Он выдвинул теорию, что эта опухоль развивается из недифференцированной мезодермы, с тех пор она носит его имя.
Эпидемиология. Опухоль Вильмса (нефробластома) является одним из самых частых злокачественных новообразований детского возраста и составляет в их структуре примерно 20-25 %. Она встречается с частотой 1 на 100 000 детей. Опухоль Вильмса выявляют у детей разного возраста, однако пик заболевания приходится на интервал от 2 до 5 лет. Среди мальчиков и девочек частота выявления нефробластомы приблизительно одинакова. С одинаковой частотой опухолевым процессом поражается как левая, так и правая почка. В 4-5 % случаев опухоль Вильмса является двусторонней. У взрослых опухоль Вильмса встречается очень редко и составляет 0,9 % от всех опухолей почки. Этиология и патогенез. Опухоль Вильмса является врожденным дизэмбрио-генетическим злокачественным новообразованием. Развитие медицинской генетики позволило картировать два гена WT1 (11р13) и WT2 (11р15), которые ассоциированы с данной опухолью. Опухоль Вильмса нередко сочетается с другими различными аномалиями. Опухоль представляет собой округлое образование с мягко-эластичной или плотной консистенцией, с бугристой поверхностью. Разрастаясь, она вызывает сдавливание почечной паренхимы и деформацию чашечно-лоханочного комплекса. Микроскопически - это эмбриональная опухоль, состоящая из различных сочетаний клеток трех типов: эпителиального, стромального и бластемно-го (незрелые клетки паренхимы почки). Метастазирование опухоли Вильмса происходит чаще гематогенным путем и в 80 % случаев в легкие. Описаны отдаленные метастазы в печень, головной мозг, кости и противоположную почку. Симптоматика и клиническое течение. Обычно опухоль Вильмса выявляется случайно родителями или врачом при профилактическом осмотре ребенка, который не предъявляет никаких жалоб и хорошо себя чувствует. Патогномо-ничных симптомов, характерных только для нефробластомы, нет. Клиника зависит от стадии опухолевого процесса и возраста ребенка. На ранних стадиях заболевания клинические проявления опухоли скудные и чаще всего выражаются в слабости, недомогании, похудании, снижении аппетита, периодическом субфебрилитете, желудочно-кишечных расстройствах. В 25 % случаев у детей с пухолью Вильмса наблюдается артериальная гипертензия. Гематурия обнаруживается примерно у 10-12 % больных.
На поздних стадиях развития опухоли Вильмса наиболее специфическим признаком является пальпируемое через переднюю брюшную стенку плотно-эластическое, гладкое, объемное образование. Боли не характерны для опухоли Вильмса, но иногда имеют место у детей с большой опухолью. Причиной болей служат либо давление на окружающие органы, либо прорастание опухолью диафрагмы, печени или забрюшинной клетчатки. Клиника острого живота может наблюдаться у ребенка при разрыве капсулы опухоли. В таких случаях она является интраоперационной находкой. Диагностика. При подозрении на опухоль Вильмса ребенку необходимо провести комплексное обследование, включающее физикальный осмотр, лабораторные и специальные методы обследования. Пальпацию опухоли проводят осторожно, а у детей младшего возраста для получения более полной информации это исследование выполняют под наркозом. В анализах выявляются гипохромная анемия, умеренный лейкоцитоз и увеличение СОЭ. В сыворотке крови определяют уровень тканевого полипептид-специфического антигена, который является маркером опухолевой активности. У детей с нефробластомой концентрация этого белка достоверно выше, чем у здоровых и пациентов с доброкачественными опухолями почки. Характерны гематурия, протеинурия, а в случае присоединения мочевой инфекции - лей-коцитурия и бактериурия. УЗИ позволяет выявить объемное тканевое образование, деформирующее контуры и чашечно-лоханочную систему почки, увеличенные забрюшинные лимфатические узлы и метастазы в печени. С помощью экскреторной урографии устанавливают характерные признаки заболевания (деформацию и нарушение структуры чашечно-лоханочной системы опухолью, дефект наполнения лоханки и/или чашечек) и оценивают функцию здоровой почки. КТ и МРТ позволяют не только выявить новообразование, но и определить его размеры, локализацию, отношение к чашечно-лоханочной системе, окружающим органам и тканям, а также состояние регионарных лимфатических узлов. Опухоль Вильмса визуализируется как объемное образование с гомогенной или неоднородной внутренней структурой, которое может распространяться на паранефральную клетчатку и почечный синус, деформировать чашечно-лоханочную систему.
Сцинтиграфия почек позволяет увидеть дефект накопления радионуклидно-го препарата, соответствующий опухоли, или отсутствие изображения органа, а также оценить раздельную функцию почек. Костные метастазы диагностируются с помощью рентгенографии и сцинтиграфии костей скелета. Дифференциальную диагностику опухоли Вильмса проводят с солитарной кистой почки, гидронефрозом, поликистозом, нейробластомой, ангиолипоми-омой и другими заболеваниями почки, встречающимися у детей. Установить правильный диагноз позволяют лучевые методы диагностики и МРТ. Для дифференциальной диагностики с нейробластомой определяются уровни метаболитов катехоламинов (дофамина, гомованилиновой и ванилинмин-дальной кислот) в суточной моче и сыворотке крови ребенка. Лечение опухоли Вильмса комбинированное и заключается в проведении оперативного вмешательства, химио- и лучевой терапии. Основным является хирургическое лечение. При односторонней опухоли операция выбора - трансперитонеальная радикальная нефрэктомия, при двустороннем процессе - резекция обеих почек с опухолью в пределах здоровых тканей. Химиотерапия служит важным компонентом комбинированного лечения больных с опухолью Вильмса и используется на всех стадиях болезни. На I и II стадиях заболевания проводится неоадъювантная химиотерапия с использованием винкристина, дактиномицина, доксорубицина. После контрольного обследования выполняется оперативное лечение. На III и IV стадиях болезни этапы лечения следующие: неоадъювантная полихимиотерапия, уретеронефрэктомия, дистанционное облучение ложа удаленной почки и лимфатических коллекторов на стороне поражения, послеоперационная полихимиотерапия. V стадия требует выполнения следующего плана лечебных мероприятий: неоадъювантная полихимиотерапия (продолжается до тех пор, пока опухоль уменьшается), оперативное лечение (одноили двусторонняя резекция почки с опухолью), лучевая терапия, послеоперационная полихимиотерапия согласно гистологическому строению опухоли.
Прогноз с гистологически благоприятной опухолью хороший. Пятилетняя выживаемость у детей с опухолью Вильмса после проведенного комплексного лечения при I стадии - не менее 90-95 %, при II - около 90-95 %, при III- более 70 % и при IV стадии заболевания- не менее 60 %. |
