Курс лекций по нормальной физиологии. Ю. И. Савченков. Красноярск Издво , 2012, 470 с
 Скачать 8.6 Mb. Скачать 8.6 Mb.
|
ЛЕКЦИЯ 24. РЕГУЛЯЦИЯ ДЫХАНИЯ24. 1. Структурно-функциональная характеристика дыхательного центра. Роль гуморальных факторов в регуляциИ интенсивности дыхания. Рефлекторная саморегуляция вдоха и выдоха.Основная функция дыхательной системы заключается в обеспечении газообмена О2 и СО2 между окружающей средой и организмом в соответствии с его метаболическими потребностями. В целом эту функцию регулирует сеть многочисленных нейронов ЦНС, которые связаны с дыхательным центром продолговатого мозга. Дыхательный центр. Под дыхательным центром в узком (анатомическом) смысле понимают совокупность нейронов специфических (дыхательных) ядер продолговатого мозга, способных генерировать дыхательный ритм. В физиологическом понимании в состав дыхательного центра входят все нервные образования, расположенные на разных этажах нервной системы, которые принимают участие в регуляции дыхания и в приспособлении его параметров к запросам организма в разных условиях. Анализируя результаты перерезок, электрического раздражения и коагуляции различных участков продолговатого мозга, Миславский (1885) пришел к заключению, что дыхательный центр (ДЦ) находится в ретикулярной формации продолговатого мозга по обеим сторонам шва на уровне корней подъязычного нерва. Клеточные структуры центра простираются от нижнего угла почти до основания писчего пера. С боков они ограничены веревчатыми телами, а снизу оливами и пирамидами. Миславский доказал, что дыхательный центр имеет инспираторную и экспираторную части (центр вдоха и центр выдоха). В настоящее время показано, что инспираторные нейроны преобладают каудальном отделе tractus solitarius, экспираторные - в вентральном ядре (nucleus ambiguus). В нормальных (физиологических) условиях дыхательный центр получает афферентные сигналы от периферических и центральных хеморецепторов, сигнализирующих соответственно о парциальном давлении О2 в крови и концентрации Н+ во внеклеточной жидкости мозга. В период бодрствования деятельность дыхательного центра регулируется дополнительными сигналами, исходящими из различных структур ЦНС. У человека это, например, структуры, обеспечивающие речь. Речь (пение) может в значительной степени отклонить от нормального уровень газов крови, даже снизить реакцию дыхательного центра на гипоксию или гиперкапнию. Афферентные сигналы от хеморецепторов тесно взаимодействуют с другими афферентными стимулами дыхательного центра, но, в конечном счете, химический, или гуморальный, контроль дыхания всегда доминирует над нейрогенным. Например, человек произвольно не может бесконечно долго задерживать дыхание из-за нарастающих во время остановки дыхания гипоксии и гиперкапнии. Дыхательный центр выполняет две основные функции в системе дыхания: моторную, или двигательную, которая проявляется в виде сокращения дыхательных мышц, и гомеостатическую, связанную с изменением характера дыхания при сдвигах содержания О2 и СО2 во внутренней среде организма. Двигательная функция дыхательного центра заключается в генерации дыхательного ритма и его паттерна. Под генерацией дыхательного ритма понимают генерацию дыхательным центром вдоха и его прекращение (переход в экспирацию). Под паттерном дыхания следует понимать длительность вдоха и выдоха, величину дыхательного объема, минутного объема дыхания. Моторная функция дыхательного центра адаптирует дыхание к метаболическим потребностям организма, приспосабливает дыхание в поведенческих реакциях (поза, бег и др.), а также осуществляет интеграцию дыхания с другими функциями ЦНС. Эта функция осуществляется, прежде всего, за счет деятельности бульбарного дыхательного центра. Гомеостатическая функция дыхательного центра поддерживает нормальные величины дыхательных газов (O2, CO2) и рН в крови и внеклеточной жидкости мозга, регулирует дыхание при изменении температуры тела, адаптирует дыхательную функцию к условиям измененной газовой среды, например при пониженном и повышенном барометрическом давлении. Эта функция осуществляется дыхательными нейронами гипоталамуса и коры головного мозга. Локализация и функциональные свойства дыхательных нейронов. Нейроны дыхательного центра локализованы в дорсомедиальной и вентролатеральной областях продолговатого мозга и образуют так называемые дорсальную и вентральную дыхательную группу. Дыхательные нейроны, активность которых вызывает инспирацию или экспирацию, называются соответственно инспираторными и экспираторными нейронами. Инспираторные и экспираторные нейроны иннервируют дыхательные мышцы. В дорсальной и вентральной дыхательной группах продолговатого мозга обнаружены следующие основные типы дыхательных нейронов: 1) ранние инспираторные, которые разряжаются с максимальной частотой в начале фазы вдоха; 2) поздние инспираторные, максимальная частота разрядов которых приходится на конец инспирации; 3) полные инспираторные с постоянной или с постепенно нарастающей активностью в течение фазы вдоха; 4) постинспираторные, которые имеют максимальный разряд в начале фазы выдоха; 5) экспираторные с постоянной или постепенно нарастающей активностью, которую они проявляют во вторую часть фазы выдоха; 6) преинспираторные, которые имеют максимальный пик активности непосредственно перед началом вдоха. Тип нейронов определяется по проявлению его активности относительно фазы вдоха и выдоха. На рис. 44 схематично изображены паттерны электрической активности дыхательных нейронов. Нейроны дыхательного центра в зависимости от проекции их аксонов подразделяют на три группы: 1) нейроны, иннервирующие мышцы верхних дыхательных путей и регулирующие поток воздуха в дыхательных путях; 2) нейроны, которые синаптически связаны с дыхательными мотонейронами спинного мозга и управляют таким образом мышцами вдоха и выдоха; Р 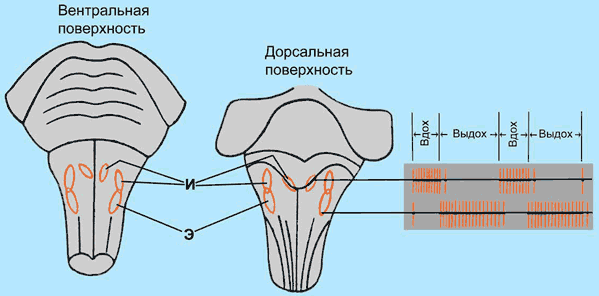 ис. 44. Локализация инспиратолрных (И) и экспираторных (Э) центров в продолговатом мозге. Изображены разряды нейронов этих центров в различные фазы дыхательного цикла. ис. 44. Локализация инспиратолрных (И) и экспираторных (Э) центров в продолговатом мозге. Изображены разряды нейронов этих центров в различные фазы дыхательного цикла.3) проприобульбарные нейроны, которые связаны с другими нейронами дыхательного центра и участвуют только в генерации дыхательного ритма. Другие области локализации дыхательных нейронов. В мосту находятся два ядра дыхательных нейронов, которые называют пневмотаксическим центром. В первом ядре находятся преимущественно инспираторные, экспираторные, а также фазавопереходные нейроны, а во втором — инспираторные нейроны. У наркотизированных животных разрушение этих ядер вызывает уменьшение частоты и увеличение амплитуды дыхательных движений. Предполагают, что дыхательные нейроны моста участвуют в механизме смены фаз дыхания и регулируют величину дыхательного объема. В сочетании с двусторонней перерезкой блуждающих нервов разрушение указанных ядер вызывает остановку дыхания на вдохе, или инспираторный апнейзис. Инспираторный апнейзис прерывается редкими, кратковременными и быстрыми выдохами. После выхода животных из наркоза апнейзис исчезает и восстанавливается ритмичное дыхание. Диафрагмальные мотонейроны образуют диафрагмальный нерв. Нейроны расположены узким столбом в медиальной части вентральных рогов от СIII до CV. Подавляющее количество волокон диафрагмального нерва является аксонами α-мотонейронов, а меньшая часть представлена афферентными волокнами мышечных и сухожильных веретен, локализованных в диафрагме, а также рецепторов плевры, брюшины и свободных нервных окончаний самой диафрагмы. Мотонейроны сегментов спинного мозга, иннервирующие дыхательные мышцы. На уровне CI—СII вблизи латерального края промежуточной зоны серого вещества находятся инспираторные нейроны, которые участвуют в регуляции активности межреберных и диафрагмальных мотонейронов. Мотонейроны, иннервирующие межреберные мышцы, локализованы в сером веществе передних рогов на уровне от TIV до ТX. Причем одни нейроны регулируют преимущественно дыхательную, а другие — преимущественно познотоническую активность межреберных мышц. Мотонейроны, иннервирующие мышцы брюшной стенки, локализованы в пределах вентральных рогов спинного мозга на уровне TIV—LIII. Генерация дыхательного ритма. Спонтанная активность нейронов дыхательного центра начинает появляться к концу периода внутриутробного развития. В настоящее время доказано, что возбуждение дыхательного центра у плода появляется благодаря пейсмекерным свойствам сети дыхательных нейронов продолговатого мозга. Иными словами, первоначально дыхательные нейроны способны самовозбуждаться. Этот же механизм поддерживает вентиляцию легких у новорожденных в первые дни после рождения. С момента рождения по мере формирования синаптических связей дыхательного центра с различными отделами ЦНС, пейсмекерный механизм дыхательной активности быстро теряет свое физиологическое значение. У взрослых ритм активности в нейронах дыхательного центра возникает и изменяется только под влиянием различных синаптических воздействий на дыхательные нейроны. Генерация дыхательного ритма происходит в сети нейронов продолговатого мозга. Доказано, что сеть основных типов дыхательных нейронов продолговатого мозга способна генерировать дыхательный ритм in vitro в срезах продолговатого мозга толщиной всего 500 мкм, помещенных в искусственную питательную среду. Инспираторная активность дыхательного центра начинается с мощного стартового разряда ранних инспираторных нейронов, который появляется спонтанно за 100—200 мс до разряда в диафрагмальном нерве. В этот момент ранние инспираторные нейроны полностью освобождаются от сильного торможения со стороны постинспираторных нейронов. Полное растормаживание ранних инспираторных нейронов происходит в момент, когда активируются преинспираторные нейроны дыхательного центра, которые окончательно блокируют разряд экспираторных нейронов. Стартовый разряд ранних инспираторных нейронов начинает активировать полные инспираторные нейроны, которые способны возбуждать друг друга. Полные инспираторные нейроны, благодаря этому свойству, поддерживают и увеличивают частоту генерации потенциалов действия в течение фазы вдоха. Именно этот тип дыхательных нейронов создает нарастающую активность в диафрагмальном и межреберных нервах, вызывая увеличение силы сокращения диафрагмы и наружных межреберных мышц. Ранние инспираторные нейроны в силу особых физиологических свойств их мембраны прекращают генерировать потенциалы действия к середине фазы вдоха. Это моносинаптически растормаживает поздние инспираторные нейроны, поэтому их активность появляется в конце вдоха. Прекращение активности всех типов инспираторных нейронов дыхательного центра растормаживает постинспираторные нейроны. Причем процесс растормаживания постинспираторных нейронов начинается гораздо раньше, а именно в период убывания разрядов ранних инспираторных нейронов. Выключается инспирация и начинается фаза пассивной контролируемой экспирации. Постинспираторные нейроны регулируют степень расслабления диафрагмы в первую половину фазы выдоха. В эту фазу заторможены все другие типы нейронов дыхательного центра. Вторая половина фазы выдоха, или фаза активной экспирации, полностью зависит от механизма ритмогенеза инспираторной и постинспираторной активности. Например, при быстрых дыхательных движениях постинспираторная фаза может непосредственно переходить в фазу следующей инспирации. Взаимодействие между нейронами ДЦ в настоящее время представляется следующим образом. Вследствие рефлекторных импульсом с хеморецепторов возникает возбуждение инспираторных нейронов и реципрокное торможение экспираторных. Одновременно импульсы от инспираторных нейронов поступают к центру пневмотаксиса, а от него к экспираторным нейронам, вызывая их возбуждение и акт выдоха. Одновременно центр выдоха возбуждается импульсацией с рецепторов растяжения легких. Активация экспираторных нейронов реципрокно тормозит инспираторный центр, но через центр пневмотаксиса наступает новое его возбуждение, подкрепляемое импульсацией от рецепторов спадения легких. Активность дыхательных мышц в течение трех фаз нейронной активности дыхательного центра изменяется. В инспирацию мышечные волокна диафрагмы и наружных межреберных мышц постепенно увеличивают силу сокращения. В этот же период активируются мышцы гортани, которые расширяют голосовую щель, что снижает сопротивление воздушному потоку на вдохе. Работа инспираторных мышц во время вдоха создает достаточный запас энергии, которая высвобождается в постинспираторную фазу, или в фазу пассивной контролируемой экспирации. В постинспираторную фазу дыхания объем выдыхаемого из легких воздуха контролируется медленным расслаблением диафрагмы и одновременным сокращением мышц гортани. Сужение голосовой щели в постинспираторную фазу увеличивает сопротивление воздушному потоку на выдохе. Это является очень важным физиологическим механизмом, который препятствует спадению воздухоносных путей легких при резком увеличении скорости воздушного потока на выдохе, например при форсированном дыхании или защитных рефлексах кашля и чихания. Во вторую фазу выдоха, или фазу активной экспирации, экспираторный поток воздуха усиливается за счет сокращения внутренних межреберных мышц и мышц брюшной стенки. В эту фазу отсутствует электрическая активность диафрагмы и наружных межреберных мышц. Координация деятельности правой и левой половин дыхательного центра является еще одной функцией дыхательных нейронов. Дыхательный центр имеет дорсальную и вентральную группу нейронов, как в правой, так и в левой половине продолговатого мозга и таким образом состоит из двух симметричных половин. Эта функция выполняется за счет синаптического взаимодействия различных типов дыхательных нейронов. Дыхательные нейроны взаимосвязаны как в пределах одной половины дыхательного центра, так и с нейронами противоположной стороны. При этом наибольшее значение в синхронизации деятельности правой и левой половин дыхательного центра имеют проприобульбарные дыхательные нейроны и экспираторные нейроны комплекса Бетцингера. Рефлекторная регуляция дыхания. Рефлекторная регуляция дыхания осуществляется благодаря тому, что нейроны дыхательного центра имеют связи с многочисленными механорецепторами дыхательных путей и альвеол легких и рецепторов сосудистых рефлексогенных зон. В легких человека находятся следующие типы механорецепторов: 1) ирритантные, или быстроадаптирующиеся, рецепторы слизистой оболочки дыхательных путей; 2) рецепторы растяжения гладких мышц дыхательных путей; 3) J-рецепторы. Рефлексы со слизистой оболочки полости носа. Раздражение ирритантных рецепторов слизистой оболочки полости носа, например табачным дымом, инертными частицами пыли, газообразными веществами, водой вызывает сужение бронхов, голосовой щели, брадикардию, снижение сердечного выброса, сужение просвета сосудов кожи и мышц. Защитный рефлекс проявляется у новорожденных при кратковременном погружении в воду. У них возникает остановка дыхания, препятствующая проникновению воды в верхние дыхательные пути. Рефлексы с глотки. Механическое раздражение рецепторов слизистой оболочки задней части полости носа вызывает сильнейшее сокращение диафрагмы, наружных межреберных мышц, а следовательно, вдох, который открывает дыхательный путь через носовые ходы (аспирационный рефлекс). Этот рефлекс выражен у новорожденных. Рефлексы с гортани и трахеи. Многочисленные нервные окончания расположены между эпителиальными клетками слизистой оболочки гортани и главных бронхов. Эти рецепторы раздражаются вдыхаемыми частицами, раздражающими газами, бронхиальным секретом, инородными телами. Все это вызывает кашлевой рефлекс, проявляющийся в резком выдохе на фоне сужения гортани и сокращение гладких мышц бронхов, которое сохраняется долгое время после рефлекса. Кашлевой рефлекс является основным легочным рефлексом блуждающего нерва. Рефлексы с рецепторов бронхиол. Многочисленные миелинизированные рецепторы находятся в эпителии внутрилегочных бронхов и бронхиол. Раздражение этих рецепторов вызывает гиперпноэ, бронхоконстрикцию, сокращение гортани, гиперсекрецию слизи, но никогда не сопровождается кашлем. Рецепторы наиболее чувствительны к трем типам раздражителей: 1) табачному дыму, многочисленным инертным и раздражающим химическим веществам; 2) повреждению и механическому растяжению дыхательных путей при глубоком дыхании, а также пневмотораксе, ателектазах, действии бронхоконстрикторов; 3) легочной эмболии, легочной капиллярной гипертензии и к легочным анафилактическим феноменам. Рефлексы с J-рецепторов. В альвеолярных перегородках в контакте с капиллярами находятся особые J-рецепторы. Эти рецепторы особенно чувствительны к интерстициальному отеку, легочной венозной гипертензии, микроэмболии, раздражающим газам и ингаляционным наркотическим веществам, фенилдигуаниду (при внутривенном введении этого вещества). Стимуляция J-рецепторов вызывает вначале апноэ, затем поверхностное тахипноэ, гипотензию и брадикардию. Рефлекс Геринга — Брейера. Раздувание легких у наркотизированного животного рефлекторно тормозит вдох и вызывает выдох. Перерезка блуждающих нервов устраняет рефлекс. Нервные окончания, расположенные в бронхиальных мышцах, играют роль рецепторов растяжения легких. Их относят к медленно адаптирующимся рецепторам растяжения легких, которые иннервируются миелинизированными волокнами блуждающего нерва. Рефлекс Геринга — Брейера контролирует глубину и частоту дыхания. У человека он имеет физиологическое значение при дыхательных объемах свыше 1 л (например, при физической нагрузке). У бодрствующего взрослого человека кратковременная двусторонняя блокада блуждающих нервов с помощью местной анестезии не влияет ни на глубину, ни на частоту дыхания. У новорожденных рефлекс Геринга — Брейера четко проявляется только в первые 3—4 дня после рождения. Проприоцептивный контроль дыхания. Рецепторы суставов грудной клетки посылают импульсы в кору больших полушарий и являются единственным источником информации о движениях грудной клетки и дыхательных объемах. Межреберные мышцы, в меньшей степени диафрагма, содержат большое количество мышечных веретен. Активность этих рецепторов проявляется при пассивном растяжении мышц, изометрическом сокращении и изолированном сокращении интрафузальных мышечных волокон. Рецепторы посылают сигналы в соответствующие сегменты спинного мозга. Недостаточное укорочение инспираторных или экспираторных мышц усиливает импульсацию от мышечных веретен, которые через γ-мотонейроны повышают активность α-мотонейронов и дозируют таким образом мышечное усилие. Хеморефлексы дыхания. РO2 и РСО2 в артериальной крови человека и животных поддерживается на достаточно стабильном уровне, несмотря на значительные изменения потребления О2 и выделение СО2. Гипоксия и понижение рН крови (ацидоз) вызывают усиление вентиляции (гипервентиляция), а гипероксия и повышение рН крови (алкалоз) — понижение вентиляции (гиповентиляция) или апноэ. Контроль за нормальным содержанием во внутренней среде организма О2, СО2 и рН осуществляется периферическими и центральными хеморецепторами. Адекватным раздражителем для периферических хеморецепторов является уменьшение РO2 артериальной крови, в меньшей степени увеличение РСО2 и рН, а для центральных хеморецепторов — увеличение концентрации Н+ во внеклеточной жидкости мозга. Артериальные (периферические) хеморецепторы. Периферические хеморецепторы находятся в каротидных и аортальных тельцах. Сигналы от артериальных хеморецепторов по синокаротидным и аортальным нервам первоначально поступают к нейронам ядра одиночного пучка продолговатого мозга, а затем переключаются на нейроны дыхательного центра. Ответ периферических хеморецепторов на понижение РаО2 (парциального давления кислорода в артериальной крови) является очень быстрым, но нелинейным. При РаО2 в пределах 80—60 мм рт.ст. наблюдается слабое усиление вентиляции, а при РаO2 ниже 50 мм рт.ст.) возникает выраженная гипервентиляция. Недостаток О2 в артериальной крови является основным раздражителем периферических хеморецепторов. Импульсная активность в афферентных волокнах синокаротидного нерва прекращается при РаО2 выше 400 мм рт.ст. (53,2 кПа). При нормоксии частота разрядов синокаротидного нерва составляет 10% от их максимальной реакции, которая наблюдается при РаО2 около 50 мм рт.ст. и ниже. Гипоксическая реакция дыхания практически отсутствует у коренных жителей высокогорья и исчезает примерно через 5 лет у жителей равнин после начала их адаптации к высокогорью (3500 м и выше). Центральные хеморецепторы. Окончательно не установлено местоположение центральных хеморецепторов. Исследователи считают, что такие хеморецепторы находятся в ростральных отделах продолговатого мозга вблизи его вентральной поверхности, а также в различных зонах дорсального дыхательного ядра. Наличие центральных хеморецепторов доказывается достаточно просто: после перерезки синокаротидных и аортальных нервов у подопытных животных исчезает чувствительность дыхательного центра к гипоксии, но полностью сохраняется реакция дыхания на гиперкапнию и ацидоз. Перерезка ствола мозга непосредственно выше продолговатого мозга не влияет на характер этой реакции. Адекватным раздражителем для центральных хеморецепторов является изменение концентрации Н* во внеклеточной жидкости мозга. Функцию регулятора пороговых сдвигов рН в области центральных хеморецепторов выполняют структуры гематоэнцефалического барьера, который отделяет кровь от внеклеточной жидкости мозга. Через этот барьер осуществляется транспорт О2, СО2 и Н+ между кровью и внеклеточной жидкостью мозга. Транспорт СО2 и Н+ из внутренней среды мозга в плазму крови через структуры гематоэнцефалического барьера регулируется с участием фермента карбоангидразы. Реакция дыхания на СО2. Гиперкапния и ацидоз стимулируют, а гипокапния и алкалоз тормозят центральные хеморецепторы. При снижении рСО2 в артериальной крови стимуляция дыхания резко уменьшается. Это нетрудно обнаружить, если произвести усиленную гипервентиляцию легких в течение нескольких секунд. После этого некоторое время не хочется дышать. Когда в условиях общего наркоза анестезиологи превышают нормальный уровень вентиляции легких, часто наблюдается примерно минутная остановка дыхания. Таким образом, увеличение рСО2 в артериальной крови вызывает усиление вентиляции легких. Это обусловлено, главным образом, реакцией центральных хемоцепторов на повышенную концентрацию ионов Н+ во внеклеточной жидкости мозга. Определенную, но меньшую роль в повышении вентиляции играет импульсация от периферических рецепторов, реагирующих как на повышение рСО2, так и понижение рН артериальной крови. Координация дыхания с другими функциями организма. В отличие от других физиологических функций организма дыхание находится под контролем и автономной (вегетативной), и соматической нервной системы, поэтому у человека и животных дыхание нередко называют вегето-соматической функцией. Существует тесное взаимодействие регуляции дыхания гуморальной и рефлекторной природы и процессами сознательной деятельности мозга. Однако во время сна или в состояниях, связанных с отсутствием сознания у человека, сохраняется внешнее дыхание и обеспечивается нормальное поддержание газового гомеостаза внутренней среды. С другой стороны, человек имеет возможность по собственному желанию изменять глубину и частоту дыхания или задерживать его, например во время пребывания под водой. Произвольное управление дыханием основано на корковом представительстве проприоцептивного анализатора дыхательных мышц и на наличии коркового контроля дыхательных мышц. Электрическое раздражение коры больших полушарий у человека и животных показало, что возбуждение одних корковых зон вызывает увеличение, а раздражение других — уменьшение легочной вентиляции. Наиболее сильное угнетение дыхания возникает при электрической стимуляции лимбической системы переднего мозга. При участии центров терморегуляции гипоталамуса возникает гиперпноэ при гипертермических состояниях. Дыхание опосредованно, через газы крови (СО2), влияет на кровообращение во многих органах. Важнейшим гуморальным, или метаболическим, регулятором локального мозгового кровотока являются Н+ артериальной крови и межклеточной жидкости. В головном мозге повышение концентрации Н+ расширяет сосуды, а понижение концентрации Н+ в артериальной крови или межклеточной жидкости, напротив, повышает тонус гладких мышц сосудистой стенки. Возникающие при этом изменения мозгового кровотока способствуют изменению градиента рН по обе стороны гематоэнцефалического барьера и создают благоприятные условия либо для вымывания из сосудов мозга крови с низким значением рН, либо для понижения рН крови в результате замедления кровотока. Корковая регуляция дыхания. Деятельность всей совокупности нейронов, образующих ДЦ, необходима для сохранения нормального дыхания. Однако в процессах регуляции дыхания принимают участие также вышележащие отделы ЦНС, которые обеспечивают тонкие приспособительные изменения дыхания при различных видах деятельности. Важная роль в регуляции дыхания принадлежит большим полушариям головного мозга и их коре, благодаря которой осуществляется приспособление дыхательных движений при разговоре, пении, спорте и трудовой деятельности. Способность коры головного мозга влиять на процессы внешнего дыхания видна из того, что можно произвольно менять частоту и ритм дыхания, и, кроме того, можно выработать условно-рефлекторные изменения дыхания (например, предстартовые изменения дыхания у спортсменов и т.п.). Дыхание в значительной мере происходит осознанно, т.е. кора мозга в определенных пределах может подчинять себе деятельность дыхательных центров, расположенных в стволе мозга. Например, можно осознанно гипервентилировать легкие настолько сильно, что произойдет значительное снижение рСО2, а рН артериальной крови при этом повысится на 0,2 единицы. Дыхательные центры ствола мозга связаны с моторной областью коры больших полушарий. Эта связь обеспечивает согласование дыхания с ритмикой движений (речью, пением). Предполагают, что моторные области коры могут непосредственно действовать на спинальные мотонейроны дыхательных мышц. На характер дыхания могут оказывать влияние другие отделы мозга. Лимбическая система и гипоталамус влияют на дыхание при аффективных состояниях (ярость, испуг). |
