Лабораторная работа Основные классы неорганических соединений
 Скачать 2.63 Mb. Скачать 2.63 Mb.
|
|
Лабораторная работа 32 Получение фенолоформальдегидных смол Цель работы: изучить способы получение полимеров. Задание: реакцией поликонденсации получить новолачную и резольную фенолоформальдегидные смолы. Выполнить требования к результатам опытов, оформить отчет, решить задачу. Теоретическое введение Фенолоформальдегидные смолы получают реакцией поликонденсации фенола С6Н5ОН и формальдегида СН2О. В зависимости от соотношения компонентов и условий процесса поликонденсации образуются новолачные или резольные смолы. Новолачные смолы образуются при небольшом избытке фенола с катализатором – соляной кислотой. Реакция идет по следующей схеме: 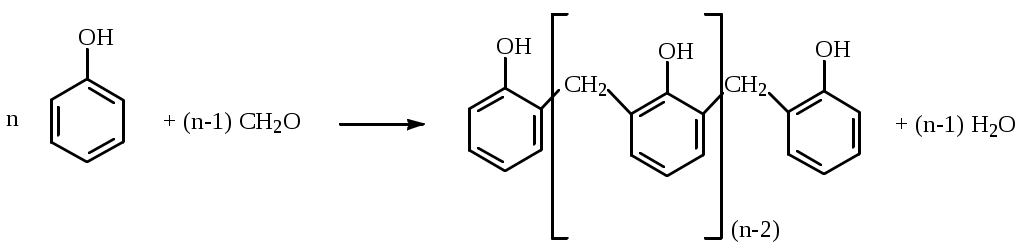 Новолачная смола имеет линейное строение и при нагревании размягчается, при охлаждении затвердевает, т.е. является термопластичным полимером. Новолачная смола имеет линейное строение и при нагревании размягчается, при охлаждении затвердевает, т.е. является термопластичным полимером.Резольные смолы получают при небольшом избытке формальдегида со щелочным катализатором. Эта смола имеет трехмерное сетчатое строение и не размягчается при нагревании, т.е. является термореактивным полимером. Выполнение работы Опыт 1. Получение новолачной смолы Поместить в пробирку 2 г кристаллического фенола, добавить туда же 3−4 мл 40 %-го раствора формалина. Смесь взболтать до полного растворения и добавить 2−3 капли концентрированной соляной кислоты. Пробирку погрузить в водяную баню (90 °С) и время от времени перемешивать содержимое пробирки стеклянной палочкой. Когда начнется бурная реакция (через 5−10 мин), вынуть пробирку из водяной бани и погрузить в холодную воду до прекращения реакции. Затем пробирку снова поместить в водяную баню (90 °С) и держать там до разделения смеси на два слоя. После этого дать пробирке остыть и осторожно слить верхний водный слой, а смоляной продукт несколько раз промыть водой, а затем разделить его на две пробирки. В одну пробирку добавить спирт и слегка подогреть на водяной бане. Другую часть смолы нагреть на пламени спиртовки. Требования к результатам опыта 1. Составить схему реакции поликонденсации фенола с формальдегидом. Какое вещество является вторым продуктом в данной реакции? 2. Сделать вывод о растворимости смолы в спирте. 3. Отметить поведение смолы при нагревании. Опыт 2. Получение резольной смолы В круглодонную колбу на 50 мл поместить 2,5 г фенола и 3,6 мл формалина. Смесь взболтать до полного растворения и добавить 0,5 мл 25 %-го раствора аммиака. Колбу с содержимым соединить с обратным холодильником, нагревать на водяной бане при 90 °С в течение 15−20 мин до отчетливого расслоения смеси (верхний – водяной слой, нижний – смоляной). Слить содержимое в фарфоровую чашку (в вытяжном шкафу!) и дать отстояться. Слить верхний водный слой. Половину полученной смолы (резита) перенести стеклянной палочкой в чистую пробирку и нагреть на пламени. Плавится ли смола? Охладить пробирку, проверить полученную смолу на растворимость в спирте. Требования к результатам опыта 1. Объяснить затвердевание смолы при нагревании. 2. Сделать вывод о термических свойствах резольной смолы. 3. Отметить растворимость смолы в спирте. Примеры решения задач Пример 32.1. Чему равна степень полимеризации изобутилена при получении полиизобутилена с молекулярной массой 56280? Решение. Полиизобутилен (полимер) получается реакцией полимеризации изобутилена (мономера), реакция представлена следующей схемой:      СН3 СН3   n CH2=C–CH3 −СH2–C– n CH2=C–CH3 −СH2–C–CH3 CH3 n изобутилен полиизобутилен Степень полимеризации nпоказывает, какое число молекул мономера вступает в реакцию полимеризации. Молекулярная масса изобутилена С4Н8 равна 56, средняя молекулярная масса полимера 56280. Следовательно, степень полимеризации Пример 32.2. Составить уравнение реакции сополимеризации бутена-1 (  CH2=CH–CH2–CH3) и стирола CH2=CH, CH2=CH–CH2–CH3) и стирола CH2=CH,C6H5 если число молекул бутена-1 и стирола, входящих в состав макромолекул, находятся в соотношении 2:1. Решение. Сополимеризация – это реакция полимеризации, в которой участвуют молекулы разных мономеров. В данном случае одним мономером является бутилен, другим стирол. Уравнение реакции сополимеризации имеет вид: n  (CH2=CH–CH2–CH3 + CH2=CH + CH2=CH–CH2–CH3) ® (CH2=CH–CH2–CH3 + CH2=CH + CH2=CH–CH2–CH3) ®C6H5 ®  (–CH2–CH–CH2–CH–CH2–CH–) n (–CH2–CH–CH2–CH–CH2–CH–) n  C2H5 C6H5 C2H5 Пример 32.3. Составить схему реакции поликонденсации ацетальдегида с фенолятом натрия, считая, что на 2 моль фенолята натрия приходится 1 моль ацетальдегида. Решение. Поликонденсация – это реакция синтеза полимера из низкомолекулярных соединений, содержащих две или несколько функциональных групп, сопровождающаяся выделением за счет этих групп таких низкомолекулярных веществ, как вода, аммиак, галогеноводород. Данная реакция поликонденсации может быть представлена следующей схемой:  Задачи и упражнения для самостоятельного решения 32.1. Для получения синтетического волокна «нитрон» в качестве мономера используют акрилонитрил CH2=CH–CN. Составить уравнение полимеризации этого мономера. 32.2. Написать уравнение реакции полимеризации формальдегида и определить степень полимеризации в реакции получения полиформальдегида со средней молекулярной массой 45000. (Ответ: 1500). 32.3. Написать уравнение реакции получения политетрафторэтилена (фторпласта-4) и определить среднюю молекулярную массу полимера, если степень полимеризации равна 1200. (Ответ: 120000). 32.4. Составить уравнение реакции сополимеризации пропилена и изобутилена. Вычислить степень полимеризации, если полимер имеет молекулярную массу 160000. (Ответ: 1600). 32.5. Как можно получить винилхлорид, имея карбид кальция, хлорид натрия, серную кислоту и воду? Написать уравнения соответствующих реакций. Составить схему полимеризации винилхлорида. 32.6. Муравьиный альдегид вступает в реакцию поликонденсации с мочевиной CO(NH2)2 и образует синтетическую карбамидную смолу. Написать уравнение реакции поликонденсации, считая, что на 2 моль мочевины необходим 1 моль формальдегида. 32.7. Как из карбида кальция и воды, применив реакцию Кучерова, получить уксусный альдегид, а затем винилуксусную кислоту? Написать уравнения соответствующих реакций. Привести схему полимеризации винилацетата. 32.8. Привести схему сополимеризации акрилонитрила CH2=CH−СN и винилацетата СН2=СН−СН2−СООН. 32.9. Привести схему получения полимера при реакции сополимеризации стирола и акрилонитрила. 32.10. Составить схему поликонденсации адипиновой кислоты C4H8(COOH)2 и гексаметилендиамина (NH2)2(CH2)6. 32.11. Написать структурную формулу метакриловой кислоты. Какое соединение получается при взаимодействии ее с метанолом? Написать уравнение реакции. Составить схему полимеризации образующегося продукта. 32.12. Как можно получить винилхлорид, имея карбид кальция, хлорид натрия, серную кислоту и воду? Написать уравнения соответствующих реакций. Составить схему полимеризации винилхлорида. 32.13. Полимером какого непредельного диенового углеводорода является натуральный каучук? Написать структурную формулу этого углеводорода и реакцию его полимеризации. 32.14. Составить схему сополимеризации бутадиена и стирола. 32.15. Для получения синтетического волокна «энант» в качестве мономера используют аминоэнантовую кислоту NH2–(CH2)6–COOH. Составить схему поликонденсации аминоэнантовой кислоты. 32.16. Составить схему сополимеризации изопрена и изобутилена. 32.17. Написать уравнение реакции поликонденсации карбамида CO(NH2)2 с уксусным альдегидом, исходя из того, что с каждыми 3 моль карбамида вступают в реакцию 2 моль альдегида. 32.18. При взаимодействии этилакриловой кислоты CH2=C(C2H5)–COOH с пропиловым спиртом C3H7OH образуется пропилэтилакрилат. Написать реакцию его получения и полимеризации. Какая масса полимера получится в результате реакции, если степень полимеризации равна 32? (Ответ: 4992). 32.19. Написать уравнение реакции получения метилового эфира метакриловой кислоты и реакцию полимеризации его в полиметилметакрилат. Определить среднюю молекулярную массу полимера, если степень полимеризации равна 150. (Ответ: 13200). 32.20. Волокно «лавсан» является продуктом поликонденсации терефталевой кислоты C6H4(COOH)2 и этиленгликоля. Соотношение между числом молекул терефталевой кислоты и этиленгликоля 2:1. Изобразить строение структурного звена этого полимера. Лабораторная работа 33 Качественный анализ металлов Цель работы: изучить качественные реакции на катионы металлов. Задание: перевести исследуемые металлы в растворимое состояние и доказать наличие катионов определенных металлов с помощью специфическх качественных реакций. Выполнить требования к результатам работы, оформить отчет, решить задачу. Качественный анализ – это совокупность химических, физико-химических и физических методов, применяемых для обнаружения компонентов, входящих в состав анализируемого вещества или смеси веществ. Методы качественного анализа в водных растворах сводятся к проведению химических реакций между ионами анализируемого вещества и прибавленных к ним реагентов (реактивов). Обычно проводят характерные реакции, которые могут быть замечены по какому-либо внешнему эффекту, например по образованию осадков, выделению газа, изменению окраски раствора или осадка и т.д. Реагенты, применяемые в качественном анализе, делятся на групповые и специфические. Специфическими реагентами называются такие реагенты, которые дают в определенных условиях характерную реакцию только с одним каким-либо ионом. Например, реактивом на ион Fe3+ является раствор гексацианоферрата (II) калия (желтая кровяная соль), который образует с катионом Fe3+ темно-синий осадок берлинской лазури: 4FeCl3 + 3K4[Fe(CN)6] = Fe4[Fe(CN)6]3↓ + 12KCl. Также для обнаружения ионов Fe3+ используется роданид аммония (NH4SCN) или калия (KSCN), который образует с катионом Fe3+ роданид железа Fe(SCN)3 кроваво-красного цвета. Групповыми реагентами называются такие реактивы, которые дают аналогичные реакции с несколькими ионами. Ионы, одинаково относящиеся к групповому реагенту, называются ионами одной аналитической группы. Существуют различные аналитические классификации катионов по группам. Для идентификации с помощью образования малорастворимых соединений наиболее распространенными являются кислотно-основная и сероводородная. Кислотно-основная классификация основана на использовании в качестве групповых реагентов водных растворов кислот и щелочей. По этой классификации групповым реагентом на катионы Ca2+, Sr2+, Ba2+, Pb2+ является раствор серной кислоты H2SO4, реже – растворимые сульфаты Na2SO4, K2SO4, (NH4)2SO4. Названные катионы образуют с групповым реагентом нерастворимые сульфаты МSO4 белого цвета. Сероводородная классификация базируется на использовании групповых реагентов: растворов HCl; H2S; (NH4)2S и (NH4)2CO3. Для ионов Ag+, Pb2+, Hg2+ групповым осадителем служит HCl (образуются нерастворимые хлориды белого цвета); для ионов Ca2+, Sr2+, Ba2+ – (NH4)2CO3 (получаются нерастворимые карбонаты МСО3 белого цвета); для ионов Al3+, Cr3+, Fe3+, Fe2+, Mn2+, Co2+, Ni2+, Zn2+, Pb2+, Cd2+ и др. – (NH4)2S. При действии группового реагента на ионы Fe2+, Co2+, Ni2+, Pb2+, Сu2+ образуются нерастворимые сульфиды черного цвета, сульфид цинка ZnS белого цвета, CdS − желтый. Сульфиды алюминия, хрома (III), железа (III) подвергаются гидролизу, поэтому в водном растворе не образуются. Вместо сульфидов выделяются продукты их гидролиза − гидроксиды этих металлов и сероводород. Выполнение работы Студент получает у преподавателя металл в виде стружки или гранул. Металл необходимо разделить на 5 частей. Работа по анализу сводится к тому, что металл под действием какого-нибудь растворителя (HCl, HNO3, NH4Cl) окисляется и переводится в раствор в виде катиона металла. Затем с помощью характерных реакций доказывается наличие данного металла в полученном растворе. Растворение металла во всех случаях вести при слабом нагревании, в течение 3−5 минут примерно в 1 мл растворителя. С концентрированными кислотами соблюдать особую осторожность и работать только в вытяжном шкафу. Опыт 1. Обнаружение магния В пробирку поместить кусочек металла и добавить 2−3 мл концентрированного раствора хлорида аммония. Интенсивное выделение водорода дает основание предположить, что это магний (алюминий очень медленно взаимодействует с раствором NH4Cl). Взаимодействие магния с раствором хлорида аммония объясняется частичным гидролизом NH4Cl с образованием слабокислой среды. Чтобы доказать наличие ионов Mg+2, часть полученного раствора перелить в другую пробирку, разбавить примерно 1 мл воды, добавить 1 мл разбавленной соляной кислоты и 1−2 мл раствора Na2HPO4, затем по каплям, при постоянном встряхивании пробирки, добавить разбавленный раствор NH4OH до появления запаха аммиака. При наличии ионов Mg+2 должен образоваться белый кристаллический осадок MgNH4PO4: Mg + H2O + 2NH4Cl = MgCl2 + H2 + 2NH4OH; MgCl2 + Na2HPO4 + NH4OH = MgNH4PO4↓ + 2NaCl + H2O. Если магний не обнаружен, к одному кусочку металла (в пробирке) прилить концентрированного раствора NaOH и осторожно нагреть до начала реакции. Обильное выделение водорода возможно в случае алюминия, цинк реагирует со щелочью гораздо спокойнее, олово и свинец растворяются в щелочи очень медленно. Опыт 2. Обнаружение алюминия В пробирку поместить кусочек металла и добавить 2−3 разбавленной соляной кислоты. Нанести каплю полученного раствора на кусочек фильтровальной бумаги, после чего бумагу выдержать 1−2 минуты над горлом склянки с концентрированным раствором аммиака (в этом момент образуется гидроксид алюминия). Далее получившееся пятно обработать каплей спиртового раствора ализарина и снова выдержать в парах аммиака. Затем бумагу подсушить над пламенем спиртовки. Аммиак при этом улетучивается, и фиолетовая окраска заменяется бледно-желтой, на фоне которой отчетливо видно розово-красное пятно. Его появление объясняется тем, что ализарин образует с гидроксидом алюминия трудно растворимое соединение красноватого цвета. Опыт 3. Обнаружение цинка В пробирку поместить два кусочка металла и добавить 2−3 мл разбавленной азотной кислоты. Смочить кусочек фильтровальной бумаги полученным раствором Zn(NO3)2, а затем 2−3 каплями разбавленного раствора Co(NO3)2 и прокалить бумагу в тигле (прокаливание вести в вытяжном шкафу). При наличии катиона Zn2+ пепел окрашивается в зеленый цвет за счет образования цинката кобальта CoZnO2 – «Зелень Ринмана»: Zn(NO3)2 + Co(NO3)2 → CoZnO2 + 4NO2 + O2. Если магний, алюминий и цинк не обнаружены, провести характерные реакции на остальные металлы – свинец, медь, олово и кадмий. Опыт 4. Обнаружение свинца и меди В пробирку поместить два кусочка металла и растворить их в 2−3 мл разбавленной азотной кислоты. В случае свинца получается бесцветный раствор нитрата свинца Pb(NO3)2. Чтобы проверить наличие ионов Pb2+, нужно отлить часть полученного раствора в другую пробирку, туда же добавить раствор сульфата натрия. В присутствии ионов Pb2+ должен получиться белый осадок PbSO4. Медь при растворении в разбавленной азотной кислоте дает голубой раствор нитрата меди Cu(NO3)2. Наличие ионов Cu2+ в растворе проверяется действием разбавленного раствора NH4OH. При осторожном добавлении NH4OH сначала можно наблюдать образование голубого осадка гидроксида меди, затем темно-синий раствор аммиаката меди: Сu(NO3)2 + 2NH4OH = Cu(OH)2↓ + 2NH4NO3; Сu(OH)2↓ + 4NH4OH = [Cu(NH3)4](ОН)2 + 4H2O. Опыт 5. Обнаружение олова В пробирку поместить 1−2 кусочка металла и растворить осторожно, в вытяжном шкафу, в 1−2 мл концентрированной азотной кислоты. Для устранения ядовитого газа (бурого диоксида азота) в пробирку сразу же налить воды. При наличии олова образуется белый осадок β-оловянной кислоты, не растворяющейся после разбавления раствора водой: Sn + 4HNO3 + (n+2)H2O = SnO2·nH2O↑ + 4NO2 + 2H2O. Опыт 6. Обнаружение кадмия В пробирку поместить кусочек металла, осторожно, в вытяжном шкафу, растворить в 1−2 мл концентрированной соляной кислоты. Для проведения характерной реакции на ионы Cd2+ часть полученного раствора отлить в другую пробирку, добавить туда же по каплям при постоянном встряхивании пробирки разбавленный раствор NaOH до появления легкого помутнения, затем прилить раствор сульфида натрия. Щелочь добавляется для нейтрализации избытка соляной кислоты. В присутствии ионов Cd2+, в зависимости от количества добавленной щелочи, образуется желтый или оранжевый осадок CdS (не спутать с белым или желтоватым осадком свободной серы, которая может осаждаться в кислой среде). Требования к результатам опытов 1. Написать уравнение реакции взаимодействия каждого металла с растворителем, под действием которого металл окисляется и переводится в раствор в виде катиона. 2. Составить уравнение реакции, доказывающей наличие катионов данного металла в полученном растворе. 3. Описать последовательный ход анализа. 4. Сделать вывод, какой металл был выдан преподавателем. Примеры решения задач |
