О
жирная кислота ацил-КоА
Известны ацил-КоА-синтетазы, которые катализируют активирование жирных кислот с длиной цепью, а другие – с более короткой цепью (4-12 углеродных атомов).
В переносе КоА-производных жирных кислот через мембраны митохондрий участвуют молекулы карнитина, имеющего биполярную группирову. Во внутренней мембране митохондрий имеется ацилтрансфераза, катализирующая перенос ацильных остатков с КоА на карнитин по следующей схеме:
СН2–N+(СН3)3 СН2–N+(СН3)3
| /
R–C
S–КоА + НО-С-Н ¾® R–С–О–СН + НS–КоА
|| | || \
O СН2–СОО- O СН2–СОО‾
ацил-КоА карнитин сложный эфир карнитина
и жирной кислоты
В соединении с карнитином жирная кислота проникает через мембраны митохондрий во внутренний митохондриальный матрикс, где осуществляется замещение остатка карнитина снова на кофермент А. Определённая часть жирных кислот (до 30%) могут проходить через мембраны митохондрий в свободном виде и их соединение с коферментом А уже происходит в митохондриальном матриксе.
Активированные жирные кислоты, соединённые с коферментом А, в митохондриальном матриксе подвергаются действию фермента ацил-КоА-дегидрогеназы (1.3.99.3), имеющего в качестве простетической группы ФАД. В ходе реакции окисления от остатка жирной кислоты отщепляются электроны и протоны с образованием a,b-ненасыщенного производного жирной кислоты, присоединённой к коферменту А:
R–СН2–СН2–С
S–КоА + ФАД ¾® R–СН=СН–С
S–КоА + ФАД×Н2
|| ||
О О
ацил-КоА ненасыщенное ацил-
КоА-производное
От образовавшегося b-оксиацил-КоА-производного жирной кислоты отщепляется водород. Эту реакцию катализирует фермент 3-оксоацил-КоА-дегидрогеназа (1.1.1.35), имеющий в активном центре кофермент НАД:
R–CН–CН2–С
S–КоА + НАД+ ¾® R–С–СН2–С
S–КоА + НАД×Н + Н+
│ ║ ║ ║
ОН О О О
b-оксиацил-КоА β-оксоацил-КоА
Под действием 3-оксоацил-КоА-дегидрогеназы атомы водорода отщепляются от b-углеродного атома, в результате чего оксипроизводное жирной кислоты превращается в кетопроизводное – b-оксоацилкофермент А. На последнем этапе b-окисления b-оксоацил-КоА-поизводное жирной кислоты взаимодействует со свободной молекулой кофермента А, образуя два продукта – ацетил-КоА и ацил-КоА, который имеет углеродную цепь на два углеродных атома короче исходной жирной кислоты. Синтез этих продуктов катализирует фермент ацил-КоА-тиолаза (2.3.1.9):
R–C–CН2–С
S–КоА + НS–КоА ¾® R–С
S–КоА + CН3–С
S–КоА
║ ║ ║ ║
О О О О
β-оксоацил-КоА ацил-КоА ацетил-КоА
В связи с тем, что конечный этап окисления КоА-производного жирной кислоты с образованием b-оксоацил-КоА происходит у b-углеродного атома, весь цикл представленных здесь реакций получил название b-окисления жирных кислот. Остаток жирной кислоты, укороченный на два углеродных атома, вновь вступает в реакции b-окисления и от него отщепляется молекула ацетил-КоА. Затем цикл реакций b-окисления повторяется снова и снова до тех пор, пока вся цепочка жирной кислоты, имеющая чётное число углеродных атомов, не будет расщеплена полностью на молекулы ацетил-КоА.
Если же b-окислению подвергается жирная кислота с нечётным числом углеродных атомов, то в результате каждого цикла реакций b-окисления будут отщепляться двууглеродные фрагменты ацетил-КоА, однако на последнем этапе b-окисления в результате отщепления ацетил-КоА остаётся конечный фрагмент молекулы жирной кислоты в виде пропионил-КоА. В матриксе митохондрий имеется набор ацил-КоА-тиолаз, специфичных к цепям жирных кислот разной длины.
Как указывалось ранее, в организмах встречаются жирные кислоты, имеющие боковые радикалы, как правило, в виде метильной группы. При этом такие ответвления обычно находятся у чётных углеродных атомов жирной кислоты. В опытах выяснено, что жирные кислоты с боковыми метильными радикалами у чётных углеродных атомов подвергаются b-окислению, но в результате тиолазной реакции от остатка жирной кислоты отщепляется не ацетил-КоА, а молекула пропионил-КоА:
СН3
|
R–С–СН–С
S–КоА + НS–КоА ¾® R–С
S–КоА + СН3–СН2–С
S–КоА
|| || || ||
О О О О
b-оксоацил-КоА ацил-КоА пропионил-КоА
Если же боковые радикалы присоединены к нечётным углеродным атомам, то b-окисление жирной кислоты блокируется на стадии образования b-оксиацил-КоА-производного, так как возникающий на этой стадии b-окисления продукт не может окисляться ферментом b-оксоацил-КоА-дегидрогеназой:
СН3
|
R–С–СН2–С
S–КоА + НАД+ ¾® реакция не идёт
| ||
ОН О
Впервые отрицательные последствия блокирования b-окисления жирных кислот наблюдали в сельскохозяйственной отрасли. В ряде развитых стран до 1966 г. в больших количествах применяли синтетические ферменты с беспорядочно расположенными метильными радикалами в их жирнокислотных цепях. В результате процесс их b-окисления при биодеградации почвенными микроорганизмами блокировался в точках, где метильные радикалы были присоединены к нечётным углеродным атомам. Последнее приводило к накоплению пенистых образований в почве, наносивших значительный ущерб урожайности сельскохозяйственных культур. После этого было принято решение производить детергенты только на основе жирных кислот с неразветвленными углеродными цепями.
У некоторых микроорганизмов при блокировании процесса b-окисления жирных кислот в качестве обходного пути используется механизм a-окисления, или процесс окисления начинается с противоположного по отношению к карбоксильной группе конца. В этом случае вначале гидроксилированию подвергается первичный углеродный атом с образованием оксипроизводного жирной кислоты, которое затем окисляется в альдегид, а последний – в карбоновую кислоту, способную далее вступать в реакции a-окисления. Окисление жирной кислоты с противоположного от карбоксильной группы конца получил название w-окисления.
У растений и микроорганизмов большая часть жирных кислот в составе липидов являются представителями ненасыщенного ряда. Но они так же, как и насыщенные кислоты, подвергаются b-окислению, образуя в качестве конечного продукта ацетил-КоА. Если в процессе окисления после очередного отщепления ацетил-КоА двойная связь ненасыщенной кислоты оказывается в a,b-положении, то в этом случае нормально происходят последующие реакции b-окисления. Однако, если двойная связь оказывается смещённой в b, g-положение, то для нормального осуществления реакций b-окисления требуется перемещение двойной связи в a,b-положение. Такую реакцию осуществляют специфические изомеразы ненасыщенных жирных кислот.
Основной продукт b-окисления жирных кислот ацетил-КоА может далее участвовать в двух видах превращений – окисляться в дыхательных реакциях до СО2 и Н2О или использоваться на синтез углеводов.
Значительная часть молекул ацетил-КоА, образующихся в ходе b-окисления жирных кислот, вступает в реакции цикла Кребса, которые локализованы во внутреннем матриксе митохондрий. Окисление одной молекулы ацетил-КоА в реакциях цикла Кребса даёт три молекулы восстановленных динуклеотидов НАД×Н, одну молекулу ФАД×Н2 и одну молекулу АТФ за счёт субстратного фосфорилирования при фосфоролизе сукцинил-КоА. Как мы уже знаем, восстановленные динуклеотиды НАД×Н и ФАД×Н2 внутри митохондрий окисляются в системе окислительного фосфорилирования, обеспечивая синтеез АТФ. При окислении одной молекулы НАД×Н возможно образование 3 молекул АТФ, а при окислении одной молекулы ФАД×Н2 – двух молекул АТФ. Всего за счёт окисления одной молекулы ацетил-КоА возможен синтез (3АТФ х 3НАД×Н) + (2АТФ х ФАД×Н2) + АТФ = 12 молекул АТФ.
В ходе реакций b-окисления жирных кислот также синтезируются восстановленные динуклеотиды ФАД×Н2 и НАД×Н, которые, поступая в систему окислительного фосфорилирования, используются для синтеза АТФ. В каждом цикле β-окисления насыщенной жирной кислоты образуется по одной молекуле НАД·Н и ФАД·Н2, что может обеспечить синтез 5 молекул АТФ. Однако при оценке общего выхода АТФ при β-окислении каждой молекулы жирной кислоты следует учитывать, что одна молекула АТФ затрачивается на активирование жирной кислоты путём её перевода в ацил-КоА-производное.
Попытаемся сравнить энергетический эффект окисления жирных кислот и углеводов. В качестве примера для расчёта энергетического эффекта окисления жирных кислот возьмём стеариновую кислоту, а углеводов – глюкозу. Стеариновая кислота имеет углеродную цепь, включающую 18 атомов углерода . В ходе её распада 8 раз повторяется цикл реакций b-окисления и образуется 9 молекул ацетил-КоА . Как было показано ранее, в каждом цикле b-окисления накапливаются восстановленные динуклеотиды, при окислении которых в системе окислительного фосфорилированя могут синтезироваться 5 молекул АТФ, а за 8 циклов реакций b-окисления – могут синтезироваться соответственно 40 молекул АТФ.
При окислении в дыхательных реакциях 1 молекулы ацетил-КоА возможно образование 12 молекул АТФ, а в результате окисления 9 молекул ацетил-КоА могут синтезироваться 108 молекул АТФ. Таким образом, в результате окисления одной молекулы стеариновой кислоты через механизм b-окисления и дыхательных реакций возможно образование в системе окислительного фосфорилирования 40 + 108 = 148 молекул АТФ. Однако, если учесть, что одна молекула АТФ затрачивается на активирование жирной кислоты, то окончательный выход АТФ при окислении одной молекулы стеариновой кислоты составляет 147 молекул АТФ (или 147 молей АТФ в расчёте на 1 моль стеариновой кислоты).
Если произвести расчёт выхода АТФ при окислении 1 г стеариновой кислоты (284 г/моль), то получим следующий результат: 147 : 284 = 0,52 моля АТФ в расчёте на 1 г стеариновой кислоты. В главе «Обмен углеводов» (стр. 400) было показано, что при окислении 1 моля глюкозы (180 г/моль) синтезируется 38 молей АТФ (или 38 : 180 = 0,21 моль АТФ в расчёте на 1 г глюкозы). Из этих показателей видно, что энергетический эффект окисления одной единицы массы стеариновой кислоты более чем в 2 раза превышает эффективность окисления глюкозы.
В качестве примера нами определён энергетический эффект окисления насыщенной жирной кислоты – стеариновой. Однако ненасыщенные жирные кислоты также дают высокий выход АТФ при их окислении в митохондриях. У них только на одном из этапов окисления, когда в реакцию вступает ненасыщенное производное, не происходит образования ФАД×Н2, которое в системе окислительного фосфорилирования обеспе-чивает синтез двух молекул АТФ. Поэтому в ходе окисления каждого моля ненасыщенной жирной кислоты с одной двойной связью выход АТФ уменьшается на 2 моля, с двумя двойными связями – на 4 моля, с тремя двойными связями – на 6 молей. Следовательно, в процессе окисления в митохондриях 1 моля линоленовой кислоты, имеющей 3 двойные связи, выход АТФ по сравнению со стеариновой кислотой будет составлять не 147 молей, а 141. 147 молей, а 141. И в расчёте на 1 г окисляемой линоленовой кислоты выход АТФ составит 0,51 моля, то есть значительно больше, чем для глюкозы и других углеводов.
Как было показано ранее, определённая часть жирных кислот, образующихся при распаде жиров, у растений подвергается a-окислению в цитоплазме и при каждом обороте a-окисления происходит отщепление от жирной кислоты одной молекулы СО2 и синтез одной молекулы восстановленного динуклеотида НАД×Н. Следовательно, если даже предположить, что происходит полное окисление жирной кислоты, то может осуществиться синтез такого числа молекул НАД×Н, которое на один меньше числа углеродных атомов в молекуле жирной кислоты.
Например, для молекулы стеариновой кислоты оно будет равно 17. Если сделать пересчёт синтезированных молекул НАД×Н в эквиваленты АТФ, принятые для системы окислительного фосфорилирования, то мы получим выход АТФ значительно меньший, чем при окислении жирных кислот по механизму b-окисления и последующего окисления ацетилкофермента А в цикле Кребса. Однако, надо иметь в виду, что большая часть восстановленных динуклеотидов НАД×Н, образуемых в цитоплазме по механизму a-окисления, не окисляется в системе окислительного фосфорилирования митохондрий, а используется в восстановительных реакциях, происходящих в цитоплазме.
Распад фосфолипидов. В клетках листьев большая часть фосфолипидов находится в связанном состоянии, так как они участвуют в построении клеточных мембран. Переход их в свободное состояние может происходить при перестройке и обновлении структур клеточных мембран. В несвязанном (свободном) состоянии много фосфолипидов откладывается в семенах, где они используются в качестве запасных веществ. При прорастании семян наблюдается высокая активность гидролитических ферментов, катализирующих распад запасных веществ, в том числе и запасных фосфолипидов, главным образом фосфатидилэтаноламинов и фосфатидилхолинов.
Р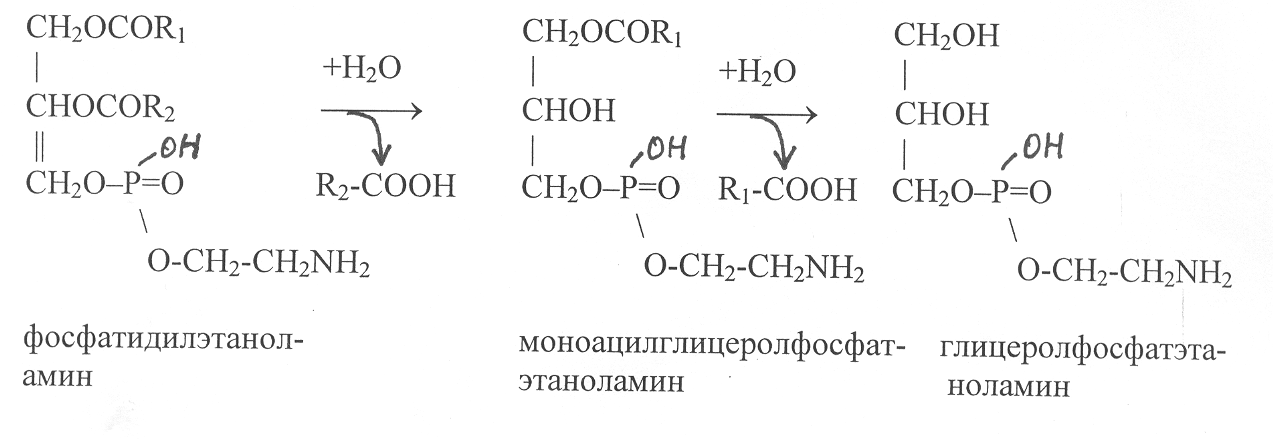
аспад фосфолипидов начинается с действия фосфолипаз, катализирующих гидролиз сложноэфирных связей глицерина и жирных кислот. Вначале происходит отщепление остатка жирной кислоты, связанного со вторым углеродным атомом, а затем связанного с первым углеродным атомом. В результате действия этих ферментов образуются свободные жирные кислоты и соединения азотистого основания с глицеролфосфатом:
На следующем этапе под действием специфической фосфатазы гидролизу подвергается сложноэфирная связь между остатком глицерина и фосфатом азотистого основания:
СН2ОН СН2ОН
| фосфатаза |
CНОН ОН + Н2О ¾¾® СНОН + (Р)–О–СН2–СН2NH2
| ∕ | этаноламинфосфат
СН2О–Р=О СН2ОН
\ глицерин
О-СН2-СН2NH2
глицеролфосфатэтаноламин
Гидролиз образовавшегося этаноламинфосфата также катализирует специфическая фосфатаза:
фосфатаза
(Р)–О–СН2–СН2NH2 + Н2О ¾¾® НО–СН2–СН2NH2 + Н3РО4
этаноламинфосфат этаноламин
Под действием указанных ферментов осуществляется превращение фосфолипидов в свободный глицерин, жирные кислоты, азотистые основания и неорганический фосфат, которые далее могут включаться в различные биохимические реакции или окисляться в процессе дыхания.
9.4. Превращение жирных кислот в углеводы.
У растений процесс распада жиров интенсивно происходит при прорастании семян, в которых они служат основным запасным веществом. При этом часть запасного жира в прорастающих семенах расходуется как энергетический материал для инициации сопряжённого синтеза органических веществ, необходимых для жизнедеятельности развивающихся проростков, а другая часть является источником органических метаболитов для построения молекул структурных и функционально активных компонентов их клеток. Важнейший путь использования жиров в качестве биохимических метаболитов – это превращение их в углеводы, которое осуществляется через реакции глиоксилатного цикла, называемого также циклом глиоксиловой кислоты.
Ферменты, катализирующие реакции глиоксилатного цикла, лакализованы в специализированных внутриклеточных структурах – глиоксисомах, которые функционально связаны с митохондриями. Участие глиоксисом в превращении жирных кислот в углеводы наиболее хорошо изучено при прорастании семян масличных растений. Глиоксисомы формируются в начале прорастания этих семян и деградируют после полного расщепления жира. Кроме ферментов глиоксилатного цикла в глиоксисомах также содержатся ферменты, катализирующие b-окисление жирных кислот. Продукт b-окисления жирных кислот – ацетил-КоА – далее включается в реакции глиоксилатного цикла.
Первые три реакции этого цикла такие же как и в цикле Кребса. Вначале ацетил-КоА реагирует с енольной формой щевелевоуксусной кислоты, образуя лимонную кислоту. Затем последовательно происходит превращение лимонной кислоты в цис-аконитовую и изолимонную кислоты:
(1-3)
СН-СООН СН2-СООН СН2-СООН СН2-СООН
|| + СН3-СS-КоА+Н2О ® | ® | Н₂О |
С(ОН)-СООН || ↓ С(ОН)-СООН ↓ C-CООН ® СН-СООН
O –НS-КоА | –Н₂О || |
СН2-СООН CН-СООН СН(ОН)-СООН
Щавелево- ацетил-КоА лимонная цис-акони- изолимонная
уксусная кислота товая кислота
кислота кислота
|
На следующем этапе превращений изолимонная кислота расщепляется ферментом изоцитратлиазой (4.1.3.1) на два продукта – янтарную и глиоксиловую кислоты:
CН2-СООН CН2-СООН Н
| | \
СН-СООН ¾® СН2-СООН + С-СООН
| янтарная кислота //
СН(ОН)-СООН О
изолимонная кислота глиоксиловая
кислота
Изоцитратлиаза - аллостерический фермент, активность которого подавляется избыточной концентрацией фосфоенолпировиногадной кис-лоты, образующейся в цитоплазме из продуктов превращения янтарной кислоты. Последняя для дальнейших реакций поступает в митохондрию. А глиоксиловая кислота в глиоксисоме вступает во взаимодействие с новой молекулой ацетил-КоА, образуя яблочную кислоту. Эту реакцию катализирует фермент малатсинтаза (4.1.3.2):
Н СН2-СООН
\ |
С-СООН + СН3-СS-КоА + Н2О ¾® СН(ОН)-СООН + НS-КоА
// ||
О О
глиокси- ацетил-КоА яблочная кислота
ловая кислота
В последней реакции глиоксилатного цикла яблочная кислота окисляется ферментом малатдегидрогеназой в щавелевоуксусную кислоту:
СН2-СООН СН2-СООН
| + НАД+ ¾® | + НАД×Н + Н+
СН(ОН)-СООН CО-СООН
яблочная кислота щавелевоук-
сусная кислота
После этого щавелевоуксусная кислота изомеризуется в свою енольную форму и может снова вступать в первую реакцию цикла. Как видно из представленных выше реакций, в глиоксилатный цикл, кроме регенерирующегося субстрата – енольной формы щавелевоуксусной кислоты, включаются две молекулы ацетил-КоА, а продуктами цикла являются янтарная кислота и НАД×Н. Поэтому суммарное уравнение глиоксилатного цикла можно записать в следующем виде:
СН2-СООН
2СН3-СS-КоА + НАД+ + Н2О ¾® | + НАД×Н + Н+ + 2НS-КоА
|| СН2-СООН
O
ацетил-КоА янтарная кислота
Янтарная кислота, поступающая из глиоксисомы в митохондрию, включается там в реакции цикла Кребса и превращается в щавелевоуксусную кислоту, которая далее из митохондрии транспортируется в цитоплазму, где c участием соответствующих ферментов используется для синтеза углеводов.
СН2-СООН СН2
| + ГТФ ¾® || + ГДФ + СО2
СО-СООН СО(Р)
щавелевоук- |
сусная кислота CООН
фосфоенол-
пировиноградная кислота
Под действием фермента фосфоенолпируваткарбоксикиназы (4.1.1.32) щавелевоуксусная кислота с участием ГТФ подвергается декарбоксилированию, превращаясь в фосфоенолпировиноградную кислоту:
Образовавшаяся здесь фосфоенолпировиноградная кислота далее включается в уже известный нам цикл реакций обращения гликолиза (стр 375-377), конечным продуктом которого является фруктозо-6-фосфат. А из фруктозо-6-фосфата могут синтезироваться различные углеводы. Но если фруктозо-6-фосфат вступает в дыхательные реакции, дающие кетокислоты, то возможно его использование и на синтез аминокислот. Общая схема превращения жиров в углеводы показана на рисунке 39.
У бактерий реакции глиоксилатного цикла пространственно не отделены от цикла Кребса, поэтому глиоксилатный путь превращений ацетил-КоА можно рассматривать как видоизменённый цикл трикар-боновых кислот. У человека и животных глиоксилатный цикл отсутствует, в связи с чем у данных организмов отложенный в жировых тканях жир не может так легко использоваться для превращения в углеводы, как у бактерий или растений.
Весь процесс биосинтеза углеводов из продуктов распада жира получил название глюконеогенеза. Такое название он имеет вследствие того, что в ходе обращения реакций гликолиза из продукта распада ных кислот фосфоенолпировиноградной кислоты осуществляется синтез важнейшего представителя сахаров–глюкозы, из которой уже довольно легко могут синтезироваться другие углеводы.
9.5. Синтез и превращения других липидов
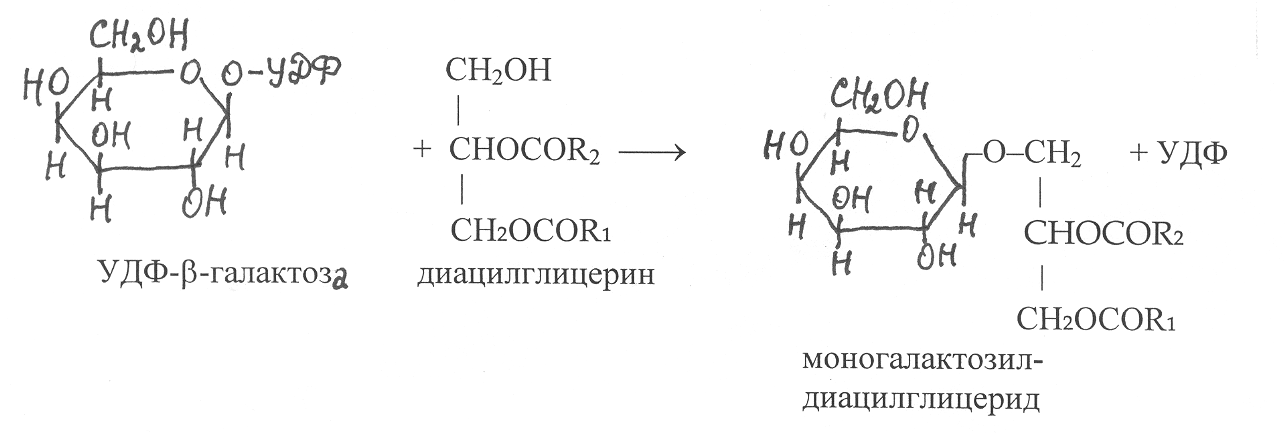
Синтезируемые в хлоропластах растений галактолипиды образуются в ходе реакций переноса остатков галактозы от УДФ-галактозы на диацилглицерины. Если осуществляется перенос одного остатка галактозы в виде b-пиранозы на диацилглицерин, синтезируются молекулы b-галактозилдиацилглицеридов:
П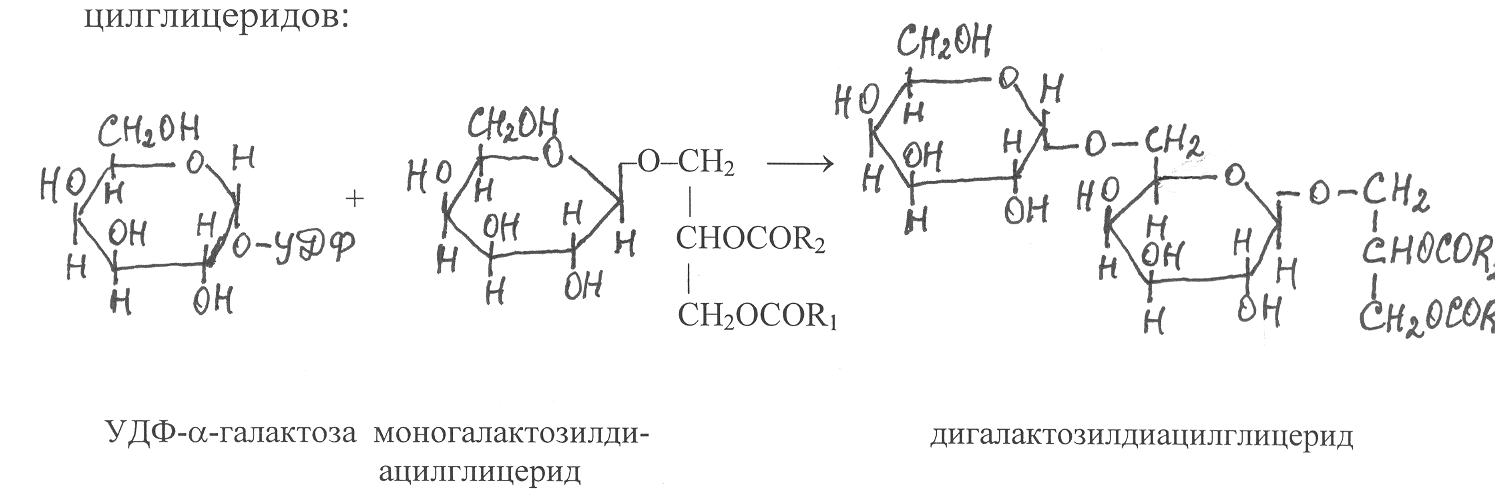
ри переносе на моногалактозилдиацилгицерид ещё одного остатка галактозы в виде a-пиранозы осуществляется синтез дигалактозил-диацилглицеридов:
Следует отметить, что в процессе синтеза диацилглицеринов, входящих в состав гликолипидов, к первому углеродному атому глицерина присоединяется остаток насыщенной жирной кислоты (имеющей радикал R1), а ко второму углеродному атому преимущественно остаток линоленовой кислоты (имеющей радикал R2).
При перестройке и обновлении структуры хлоропластных мембран образуются свободные формы гликолипидов, которые могут подвергаться превращениям в результате действия соответствующих гидролаз. Отщеп-
л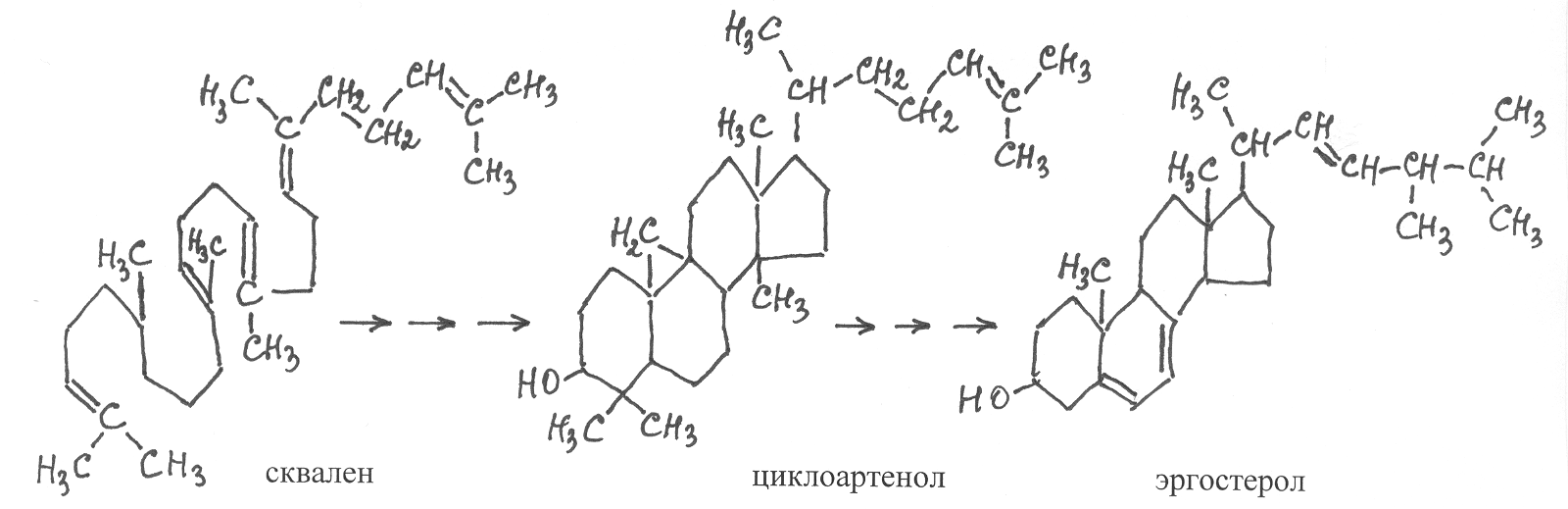
ение остатков моносахаридов катализируют специфические гликозидазы, а остатков жирных кислот – гидролазы сложных эфиров. Механизмы этих реакций в растительных клетках пока ещё недостаточно изучены.
Исходным соединением для синтеза стеролов служит продукт обмена углеводов и жирных кислот ацетилкофермент А, который, включаясь в обмен терпеноидных соединений, образует сквален (стр…). А уже из сквалена через ряд промежуточных стадий синтезируются стеролы. Важнейшим промежуточным продуктом в этих реакциях у растений является циклоартенол, который служит важнейшим биохимическим предшественником при образовании стеролов из сквалена.
В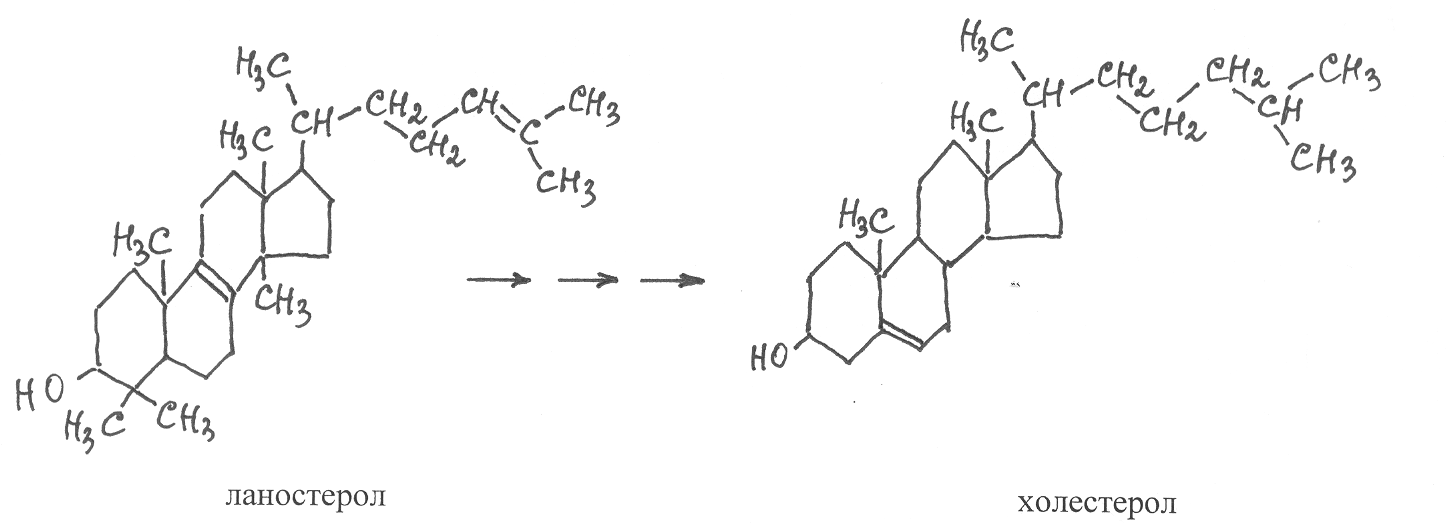
организмах животных стероидные липиды синтезируются из сквалена, однако непосредственным биохимическим предшественником для их образования служит ланостерол, который через ряд промежуточных стадий превращается в холестерол. А уже путём превращений холестерола образуются другие стероидные вещества животного организма.
Распад стероидных липидов представляет собой сложный многоступенчатый процесс, который пока ещё слабо изучен. Однако известно, что конечным продуктом распада стеролов, как и при распаде других липидов, является ацетилкофермент А. Ещё меньше сведений имеется по обмену липидов воска. В ряде опытов было показано, что главные липидные компоненты воска высокомолекулярные одноатомные спирты образуются из пальмитиновой кислоты.
|
 Скачать 4.12 Mb.
Скачать 4.12 Mb.




