Cl2 СН3—СН2—СН2—СН=О CH3—CH2—CH—CH=O + HCl Cl масляный альдегид -хлормасляный альдегид Подвижность атомов водорода в -положении к карбонильной группе связана с вызываемыми ею электронными смещениями: Н  + - + - RCCH=O Н Наличие у карбонильного углерода частичного положительного заряда (+), возникающего вследствие смещения -электронов двойной связи к кислороду, вызывает электронное смещения в -связях Н—С при -углеродном атоме. Увеличивается поляризация этих связей и способность -водородных атомов отрываться в виде протона. Реакции на двойную связь для непредельных альдегидов и кетонов Подобно этиленовым углеводородам непредельные альдегиды и кетоны дают характерные реакции на этиленовую двойную связь. Например, они обесцвечивают раствор брома; с непредельным альдегидом - акролеином реакция протекает по схеме: Br2 СН2=СН—СН СН2—СН—СН II II ,-дибромпро- акролеин О Br Br O пионовый альдегид Присоединение галогенводородов к непредельным альдегидам, в которых карбоновая группа непосредственно связана с этиленовой группировкой, протекает так, что галоген присоединяется к углероду в -положение к карбонильной группе. Так, бромистый водород присоединяется к акролеину по схеме: НBr СН2=СН—СН СН2—СН2—СН II II -бромпропионовый акролеин О Br O альдегид В этом случае влияние карбонильной группы приводит к тому, что НBr присоединяется по месту двойной связи не в соответствии с правилом Марковникова. Аналогично протекает реакция присоединения воды. Это объясняется смещением -электронов этиленовой двойной связи, вызываемым электронным сдвигом в карбонильной группе: 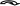  + - + - СН=СН—СН=О Естественно, что анион галогена (в данном случае Br-) присоединяется к атому углерода этиленовой группы, несущему частичный положительный заряд (+). Для соединений с карбонильной группой, особенно для альдегидов, характерны межмолекулярные реакции, при которых происходит взаимодействие (уплотнение) нескольких или многих молекул с образованием продуктов, обладающих большим молекулярным весом. Полимеризация альдегидов Альдегиды, особенно их низшие представители, очень склонны к полимеризации. Реакция идет с разрывом двойных связей альдегидных групп, причем атомы карбонильного кислорода одной молекулы альдегида соединяются с атомами карбонильного углерода другой молекулы. Так, например, формальдегид полимеризуется по схеме: nCH2=O (—CH2—O—)n формальдегид полимер формальдегида ....—СН2—О—СН2—О—СН2—О—.... Число молекул, участвующих в образовании полимерной цепи (число n), зависит от условий полимеризации и природы альдегида. Формальдегид образует полимеры – полиформальдегиды с различной степенью полимеризации (с различной величиной n), обладающие разнообразными свойствами. Склонность к полимеризации с образованием линейных полимеров проявляется также у уксусного альдегида, но не характерна для других альдегидов. Альдегиды полимеризуются и с образование не очень сложных циклических полимеров. Так, из уксусного альдегида под влиянием минеральных кислот образуется жидкий циклический тример (полимер, образованный тремя молекулами мономера), называемый паральдегидом: 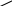    О О О О СН3—СН СН—СН2 СН3—НС СН—СН3 + II     О О О О О О О О |
 Скачать 180 Kb.
Скачать 180 Kb.
 + -
+ -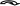
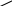

 О О
О О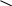 О О О О
О О О О