МГ ответы. Медицинская генетика 104. Наследственные заболевания человека, определение, классификация, методы лабораторной диагностики. Наследственные болезни
 Скачать 1.51 Mb. Скачать 1.51 Mb.
|
|
106. Врождённые пороки развития. Классификация. Мониторинг ВПР, его задачи и организация. Классификация и этиология врожденных пороков Наиболее объективные критерии классификации - локализация и этиология пороков. Врожденные пороки развития подразделяют на изолированные(в одном органе, например, стеноз привратника), системные(в пределах одной системы органов, например, хондродисплазии), множественные(в органах двух систем и более). Синдромом множественных врожденных пороков развитияназывают такие сочетания пороков, при которых очевидна их этиологическая и патогенетическая связь, а также клинически очерчена морфологическая картина. Множественные аномалии, которые являются каскадом одного первичного нарушения, называют последовательностью(не причинная, а патогенетическая связь). Если множественные аномалии в определенных сочетаниях появились неслучайно у нескольких больных, то говорят об ассоциациях. Этиологияврожденных пороков развития может быть наследственной, экзогенной многофакторной. Мониторинг ВПР. В настоящее время в большинстве стран, в том числе и в России, в структуре детской заболеваемости и смертности все большее значение приобретают врожденные пороки развития (ВПР), которые встречаются у 5% новорожденных, а их вклад в структуру младенческой смертности достигает 20%. Столь высокий уровень ВПР обусловливает необходимость разработки и проведения мероприятий по их профилактике. Среди программ профилактической направленности немаловажное место занимает мониторинг врожденных пороков развития, представляющий собой систему определения и контроля популяционных частот ВПР. Главными задачами, которые решаются при проведении мониторинга, являются: - определение частот ВПР и проведение эпидемиологических исследований; - изучение динамики частот врожденных пороков развития; - изучение этиологии врожденных пороков развития; - выявление и контроль новых тератогенных факторов среды; - оценка влияний на популяционные показатели частот ВПР массовых программ первичной и вторичной профилактики. В России регулярный мониторинг ВПР проводится с 1999 года. Основная задача первого уровня мониторинга заключается в определении популяционных частот ВПР. Для выполнения этой задачи в первую очередь усилия были направлены на то, чтобы региональные регистры работали по единой схеме. Это необходимо как в целях создания единой базы данных, так и в целях сравнительного анализа распространенности пороков развития по регионам. В этой связи были разработаны единые принципы организации и функционирования системы мониторинга в России. Основные принципы организации системы мониторинга в России: 1. Популяционный метод сбора материала. 2. Учет всех выявляемых пороков развития с обязательной регистрацией 21 формы пороков. 3. Множественные источники регистрации: роддома, детские поликлиники, больницы, презектуры. 4. Учет ВПР как среди живорожденных, так и среди мертворожденных, а также плодов с ВПР, выявленных в процессе УЗ скрининга. 107. Клинико-генеалогический метод, его применение в консультировании больных с наследственной патологией. Клинико-генеалогический метод дает возможность: - выявлять наследственный характер признака; - определять тип наследования; - определять зиготность членов родословной; - определять особенности взаимодействия генов; - устанавливать сцепленное наследование и проводить картирование хромосом; - определять пенетрантность гена; - изучать закономерности мутирования отдельных генов; - устанавливать носительство мутантного гена тем или иным членом семьи; - определять вероятность генетически обусловленных событий и рассчитывать риск наследования патологического гена (признака) при медико-генетическом консультировании. Клинико-генеалогический метод часто осложняется невозможностью сбора достаточного количества информации из-за малодетности семей, либо из-за прерывания связей между поколениями, отсутствия связей между родственниками, либо по морально-этическим причинам. Клинико-генеалогический метод лежит в основе медико-генетического консультирования и включает 3 этапа: 1 этап – клиническое обследование; 2 этап – составление родословной; 3 этап – генетический анализ родословной. Первый этап – клиническое обследование. При составлении родословной сбор сведений о семье начинается с человека, которого называют пробанд (обычно это больной с изучаемым заболеванием или признаком). В сведениях о пробанде указывается анамнез заболевания, включающий начальные признаки и возраст их манифестации, последующее течение болезни; если пробанд – ребенок – сведения о раннем психомоторном и последующим умственном и физическом развитии. Чем больше поколений удается проследить и чем более полно охватить членов родословной при сборе сведений, тем больше вероятность получения достоверных сведений о характере наследования изучаемого признака. Сбор генетической информации проводится путем опроса, анкетирования, личного собеседования. Опрос начинается обычно с родственников по материнской линии. В родословную вносят сведения о выкидышах, абортах, мертворожденных, бесплодных браках, внебрачных детях и др. При сборе генетической информации о проявлении изучаемого признака ведется краткая запись данных о каждом члене рода с указанием его родства по отношению к пробанду. Обычно указывается фамилия (для женщин девичья фамилия), имя, отчество, дата рождения и смерти. Полученные данные записываются в медико-генетическую карту. При сборе информации необходимо внимательно анализировать сообщения об инфекциях и травмах, следует учитывать гетерогенность и варьирующую экспрессивность наследственных заболеваний. Необходимо выяснять акушерский анамнез, учитывать наличие и характер профессиональных вредностей, возраст, национальность, место жительства семьи, профессию, наличие хронических заболеваний в семье, причину смерти умерших и др. На основании изученных данных составляется анамнез (греч. – anamnesis – воспоминание). Второй этап – составление родословной. После сбора сведений составляется графическое изображение родословной, для этого используется система символов, предложенная в 1931 году Г. Юстом. (Рис. 1). При составлении графического изображения родословной важно соблюдать следующие правила: Составление родословной начинают с пробанда. Братья и сестры (сибсы) располагаются в порядке рождения слева направо, начиная со старшего. Все члены родословной располагаются строго по поколениям, в один ряд. Поколения обозначаются римскими цифрами слева от родословной сверху вниз. Арабскими цифрами нумеруется потомство одного поколения (одного ряда) слева направо. Благодаря такой нумерации каждый член семьи имеет свой шифр (например: I-1, I-2, II-2, II-4 и др.) Указывается возраст членов семьи (родословной), в связи с тем, что некоторые болезни проявляются в разные периоды жизни. Отмечаются лично обследованные члены родословной. Графическое изображение родословной может быть вертикально-горизонтальным или расположенным по кругу (в случае многочисленных данных). Схема родословной сопровождается описанием обозначений под рисунком (легендой). Третий этап – генетический анализ родословной. Этот этап требует хороших знаний критериев установленных типов наследования. Задача генетического анализа – установление наследственного характера заболевания и типа наследования, выявление гетерозиготных носителей мутационного гена, установление генотипа пробанда и, как заключение, прогнозирование потомства. Анализ родословной рекомендуется проводить в следующей последовательности: 1. Установление, является ли данный признак (заболевание) наследственным. Если признак встречается несколько раз в разных поколениях (имеет семейный характер), то можно предполагать, что признак имеет наследственную природу. 2. Определение типа наследования признака. Для этого учитывают: во всех ли поколениях и как часто среди членов родословной встречается признак; одинакова ли частота признака у обоих полов и если нет, то у какого пола встречается чаще; детям какого пола передается признак от больного отца и от больной матери; есть ли семьи, в которых от больных родителей рождаются здоровые дети, или, наоборот, от здоровых родителей рождаются больные дети; какая часть потомства имеет наследуемый признак в семьях, где болен один из родителей. Наряду с заболеваниями, обусловленными ядерными генами у человека все более изученными становятся заболевания митохондриальные и болезни геномного импритинга. Под генетическим импритингом понимают эпигенетический процесс, приводящий к стойким функциональным различиям экспрессии гомологичных генов, полученных от одного из родителей. Так, например, в настоящее время хорошо известно влияние ряда отцовских и материнских генов на вес плода, степень развития плаценты и другие особенности внутриутробного развития. Наличие генов, подверженных импритингу, четко установлено для хромосом 7,11,15. Предполагают, что такие гены присутствуют и в хромосомах 2, 3, 6, 14 и 20. В настоящее время идентифицировано не менее 30 импритированных генов, часто группирующихся в кластеры, по некоторым данным, таких генов в геноме человека насчитывается не менее 100. 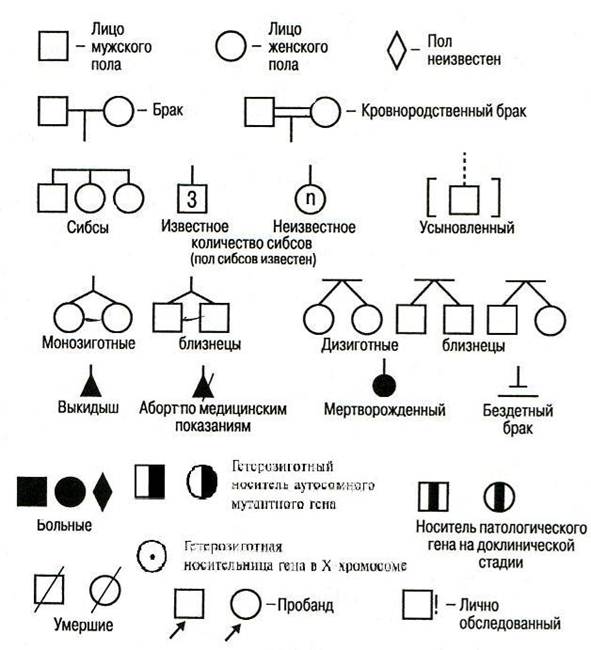 Рис. 1– Символы, используемые при составлении родословных Большой класс составляют болезни экспансии тринуклеотидных повторов, и наследственные болезни обмена. У человека установлены следующие типы наследования, подчиняющиеся менделеевским закономерностям наследования: аутосомно-рецессивное наследование (АР), аутосомно-доминантное наследование (АД). Болезни с нетрадиционными типами наследования: доминантное, сцепленное с Х хромосомой наследование (ХД), рецессивное, сцепленное с Х хромосомой наследование (ХР), сцепленное с Y хромосомой наследование (YН) и цитоплазматическое наследование (ЦН). В зависимости от типа наследования родословные выглядят по-разному. 108. Цитогенетические методы, их цель и сущность, использование в клинической практике. Цитогенетический метод С помощью данного метода можно изучать наследственный материал клетки: совокупность хромосом в целом (кариотипирование) или наличие и количество Х-хромосом (определение полового хроматина — число глыбок полового хроматина или телец Барра). Исследование проводится с помощью светового микроскопа (изготовление и изучение микропрепаратов). Кариотипирование На рис. 56 представлена последовательность действий для получения кариотипа человека.  Половой хроматин В клетках мужчин (кариотип 46, XY) Х-хромосома всегда выполняет активную функцию, а у женщин (46, XX) одна Х-хромосома является активной, а другая Х-хромосома находится в неактивном, спирализованном состоянии. Она выявляется в виде компактной темной глыбки в интерфазном ядре соматических клеток нормальных женщин и называется тельцем Барра или половым Х-хроматином. Инактивация одной из двух Х-хромосом происходит в эмбриогенезе, причем закономерности в инактивации отцовской или материнской хромосомы нет (гипотеза Лайон). При любом числе Х-хромосом в активном состоянии будет только одна, следовательно, половой Х-хроматин в норме выявляется только у женщин и отсутствует у мужчин. Зная число глыбок полового хроматина, можно определить число Х-хромосом по формуле п + 1, где п — число глыбок, а 1 — активная Х-хромосома; и наоборот, зная число Х-хромосом, можно определить число телец Барра по формуле п -1, где п — число Х-хромосом, а 1 — активная Х-хромосома (табл. 12). У мужчин в норме выявляется Y-половой хроматин (он представляет длинное плечо Y-хромосомы), который обнаруживается с помощью люминисцентной микроскопии и выглядит в виде яркого пятна диаметром 0,3-1 мкм. Изменение числа глыбок полового хроматина происходит при геномных мутациях (изменение числа X- и Y-хромосом). Определение полового хроматина используется как экспресс-метод при пренатальном и постнатальном определении пола и диагностике хромосомных болезней (см. табл. 12).  Пренатальная диагностика Пренатальная диагностика проводится до 22 недели беременности и является одним из методов первичной профилактики наследственных болезней. Методы делятся на три группы: просеивающие, неинвазивные, инвазивные (с последующей лабораторной диагностикой). Для каждого метода есть свои показания и противопоказания, разрешающие возможности, осложнения после проведения процедур. Выбор метода строго индивидуализирован в соответствии с конкретной ситуацией в семье и состоянием здоровья беременной женщины. Просеивающие методы позволяют выявить женщин, имеющих повышенный риск рождения ребенка с наследственной патологией (возраст матери — 35 лет и старше, повторные спонтанные прерывания беременности и др.). К этим методам относятся: определение концентрации альфа-фетопротеина (АФП) в сыворотке крови беременной (выявляют врожденные дефекты нервной трубки); уровня хорионического гонадотропина (повышен при синдроме Дауна) и несвязанного эстриола (уменьшен при синдроме Дауна); ультразвуковое обследование (УЗИ). Неинвазивные методы: обследование плода без оперативного вмешательства с помощью ультразвукового обследования (УЗИ). Проводится с 6 до 23 недели с целью выявления врожденных пороков развития (редукция конечностей, отставание в росте, анэнцефалия и др.). Инвазивные методы: хорион- и плацентобиопсия (получение небольших кусочков ворсин хориона и кусочков плаценты с 7 по 16 неделю беременности трансабдоминально или трансцервикально под контролем УЗИ), получение амниотической жидкости и клеток плода на 15-18 неделе беременности (рис. 57), биопсия кожи плода, кордоцентез (взятие крови из пуповины под контролем УЗИ с 18-22 недели беременности). Полученный материал подвергается цитогенетическому, биохимическому, молекулярно-генетическому исследованию. Результаты используются в пренатальной диагностике хромосомных и генных болезней, определении пола, выявлении пороков развития. 109.Массовый и селективный биохимический скрининг наследственных болезней обмена. Неонатальный скрининг в Российской Федерации: ٠фенилкетонурия ٠врожденный гипотиреоз ٠адреногенитальный синдром ٠галактоземия ٠муковисцидоз Массовое обследование новорожденных на НБО – начальный этап системы диагностических, лечебных и профилактических мероприятий направленных на борьбу с тестируемым заболеванием. Для массовых программ решающую роль играет чувствительность, а для селективных программ - специфичность. Общие характеристики скринингового подхода к диагностике наследственных болезней: 1) массовый и безотборочный характер обследования, 2) профилактическая направленность, 3) двухэтапность (по меньшей мере) диагностики Массовому просеиванию подлежат НБ, которые отвечают следующим критериям: Без своевременного профилактического лечения болезнь существенно снижает жизнеспособность, приводит к инвалидности. Больной нуждается в социальной помощи. Имеются биохимические или молекулярно- генетические методы для точной диагностики заболевания на доклинической стадии. Для выявляемой болезни необходимо иметь эффективные методы профилактического лечения. Частота выявляемой болезни должна быть в пределах 1: 10 000 и выше. Лабораторные методы массового скрининга: 1) Микробиологический метод Гатри, 2) Хроматография на бумаге или другом носителем (селикагель и др.), 3) Флуорометрический метод (более чувствительный), основанный на образовании флуоресцирующего комплекса фенилаланина с лейцил-аланином. В России на основе этого метода используются аппараты типа Флюороскан, Дельфия, “Victor” «Авто-Дельфия». 4) Тандемная масс-спектрометрия(MS/MS) 5) Газовая хроматография с тандемной масс- спектрометрией(GC/MS) Селективный скрининг - предусматривает обследование определенных детских коллективов с отклонениями в состоянии здоровья для выявления наследственной патологии. Например, обследование всех детей с отклонениями в нервно-психическом развитии для диагностики наследственных дефектов обмена веществ. Чаще всего для этих целей используются качественные или полуколичественные методы, в качестве материала используется моча или кровь. Качественные и полуколичественные тесты для диагностики наследственной патологии (методы селективного биохимического скрининга) довольно разнообразны, однако, к сожалению, они не находят широкого распространения. 1) Простые качественные экспресс-тесты (капельные и цветные реакции мочи) для ориентировочной диагностики наследственных болезней. С их помощью можно выявить ряд веществ (метаболитов), которые, как правило, характерны для целой группы заболеваний. Чаще всего речь идет об избыточном выделении продуктов блокированной ферментативной реакции или разнообразных промежуточных продуктов обмена (побочные продукты). Количественные пробы, как правило, просты в выполнении, чувствительны и отличаются дешевизной. Положительные реакции, полученные с помощью подобных простых тестов, являются важным этапом, позволяющим заподозрить наследственное заболевание обмена веществ. В качестве материала для проведения качественных проб в подавляющем большинстве случаев используется моча. |
