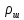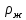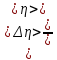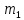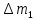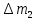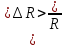Физика молекулярная. Методические указания к лабораторным работам для студентов инженерных специальностей
 Скачать 0.62 Mb. Скачать 0.62 Mb.
|
Описание экспериментальной установки и метода измеренийСтеклянный цилиндр с жидкостью, вязкость которой нужно определить, с двумя метками 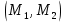 , расположенными друг от друга на расстоянии , расположенными друг от друга на расстоянии 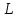 (рис. 12), закрывают пробкой с просверленным по ее оси каналом. (рис. 12), закрывают пробкой с просверленным по ее оси каналом.При повороте ручки 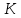 заслонка, закрывающая отверстие канала снизу, поворачивается, и шарик, помещенный в канал, падает вдоль оси цилиндра. На дно цилиндра опущена сетка Сс держателем, при помощи которой извлекаются шарики, упавшие на дно. заслонка, закрывающая отверстие канала снизу, поворачивается, и шарик, помещенный в канал, падает вдоль оси цилиндра. На дно цилиндра опущена сетка Сс держателем, при помощи которой извлекаются шарики, упавшие на дно.  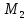 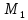 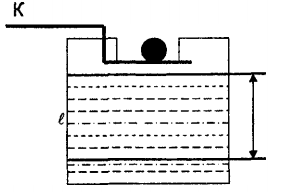 Рис. 12. Схема проведения опыта Секундомер служит для измерения времени падения шарика. Масштабная линейка служит для измерения пути, пройденного шариком 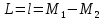 (точность ее 1 мм). (точность ее 1 мм).Микрометр служит для измерения диаметра шарика. Порядок выполнения работыС помощью микрометра определяют диаметр шарика. Помещают шарик в отверстие пробки при закрытой заслонке. Масштабной линейкой измеряют с точностью до 1 мм расстояние между верхними границами меток M1,М2. Производят не менее 5 измерений. Поворотом рукоятки 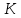 выпускают шарик. В момент прохождения шарика через верхнюю метку M1 пускают секундомер и останавливают его в момент, когда шарик пройдет через нижнюю метку М2. выпускают шарик. В момент прохождения шарика через верхнюю метку M1 пускают секундомер и останавливают его в момент, когда шарик пройдет через нижнюю метку М2.С помощью термометра определяют температуру жидкости. Результаты измерений заносят в табл. 6. Вычисление погрешности производят по формуле: 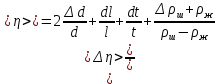 Окончательный результат измерения записывают в следующем виде: 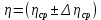 Таблица 6 - Значения коэффициента внутреннего трения жидкости
Вопросы для самопроверкиПочему скорость течения вязкой жидкости различна в разных сечениях потока? Что такое градиент скорости? Объясните причины вязкости жидкости. Дайте определение единицы градиента скорости и коэффициента динамической вязкости в системе СИ. ЛАБОРАТОРНАЯ РАБОТА 7ОПРЕДЕЛЕНИЕ УНИВЕРСАЛЬНОЙ, ГАЗОВОЙ ПОСТОЯННОЙЦель работы — экспериментальное определение универсальной газовой постоянной. Следует научиться давать определение физического смысла универсальной газовой постоянной, уметь писать уравнение Майера. Оборудование: стеклянная колба с емкостью 500 см3, насос Комовского. манометр, цилиндрические стеклянные трубки. Теоретическое введениеСостояние идеального газа определяется уравнением Клапейрона- Менделеева: 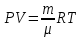 (1) (1)где 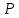 - давление газа; - давление газа; 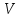 - объем газа; - объем газа; 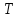 - абсолютная температура; m- масса газа; - абсолютная температура; m- масса газа; 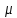 - молекулярный вес газа; - молекулярный вес газа; 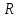 - универсальная газовая постоянная, числовое значение которой для всех газов одинаково. - универсальная газовая постоянная, числовое значение которой для всех газов одинаково.Величина 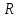 - универсальная газовая постоянная - имеет существенное значение во многих вопросах физики. Выясним физический смысл универсальной газовой постоянной. - универсальная газовая постоянная - имеет существенное значение во многих вопросах физики. Выясним физический смысл универсальной газовой постоянной.Предположим, что грамм-молекула данного газа, занимающая объем 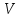 , при температуре , при температуре 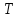 и давлении и давлении 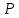 заключена в цилиндр с поршнем (рис. 13). заключена в цилиндр с поршнем (рис. 13).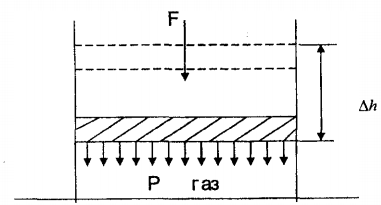 Рис. 13. Схема сжатия газа внутри цилиндра Внешняя сила, удерживающая поршень, 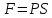 , где , где 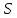 - площадь поршня. При нагревании газа, при постоянном давлении - площадь поршня. При нагревании газа, при постоянном давлении 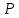 на один градус газ расширяется, и поршень будет поднят на высоту Δh; газ совершит при этом работу (рис. 13): на один градус газ расширяется, и поршень будет поднят на высоту Δh; газ совершит при этом работу (рис. 13):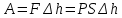 (2) (2)но 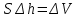 , где , где 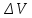 - увеличение объема газа, откуда: - увеличение объема газа, откуда: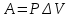 (3) (3)Теперь найдем увеличение объема газа, воспользовались уравнением Клапейрона - Менделеева для одного моля газа т.е, (  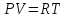 , ,При температуре 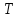 и давлении и давлении 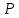 объем одного моля газа равен: объем одного моля газа равен: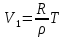 При изменении температуры на 1 °С газ занимает объем: 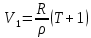 , ,Приращение объема при изменении температуры, на 1 °С равно: 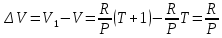 , (4) , (4)Подставляя (4) в (3), имеем 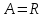 . .Отсюда следует физический смысл универсальной газовой постоянной: «она равна работе расширения одного моля газа при нагреве на температуру на 1 °С при постоянном давлении.» Используя уравнение Клапейрона-Менделеева, можно найти расчетную формулу для определения численного значения универсальной газовой постоянной. Считая объем и температуру газа постоянными, напишем уравнение (1) для двух состояний: 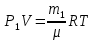 (5) (5)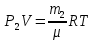 (6) (6)Вычитая из (5) выражение (6), имеем: 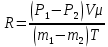 (7) (7)Здесь 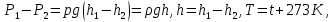 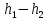 – показания манометра. Окончательно имеем: – показания манометра. Окончательно имеем: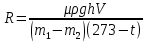 (8) (8)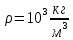 - плотность воды в манометре, - плотность воды в манометре, 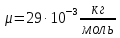 , , 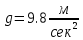 Описание установки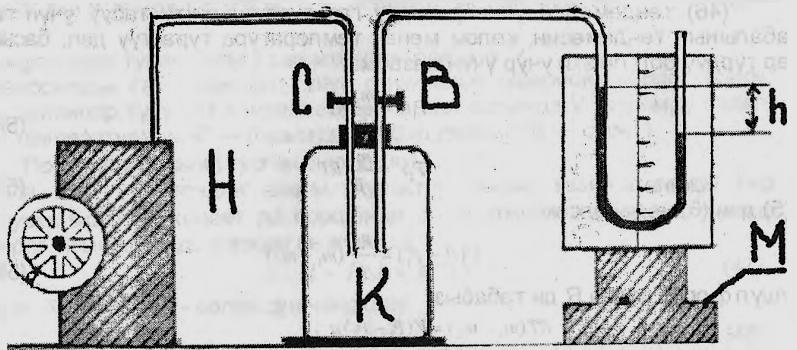 Рис. 14. Схема проведения опыта Прибор для определения Rпредставляет собой стеклянную колбу с емкостью 500 см3, имеющую два отвода с зажимами. Один отвод колбы соединяют с водяным манометром, а другой - с насосом Комовского. Порядок выполнения работы1. Определить взваливанием на аналитических весах .массу колбы с открытыми кранами и содержащегося в ней воздуха. 2. Измерить комнатную температуру t. 3. Соединить колбу с манометром и насосом и откачивать до некоторого давления. Записывать показания манометра 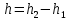 ( 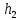 - верхний уровень и - верхний уровень и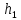 - нижний уровень манометра) - нижний уровень манометра)4. Закрыть отводы при помощи зажимов на аналитических весах, определить массу колбы и содержащегося в ней после откачки воздуха 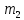 , при этом показание манометра не превышает , при этом показание манометра не превышает 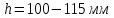 . .5. Вычислить R по формуле (10). 6. Все результаты измерения занести в табл. 7. 7. Вычисление погрешности произвести по формуле 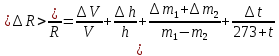 Вопросы для самопроверкиКакой физический смысл имеет величина R? Что такое грамм-молекула вещества? Таблица 7 - Расчетные значения универсальной газовой постоянной
СПИСОК ЛИТЕРАТУРЫДетлаф А.А., Яворский Б.Т. Курс физики. - М, Высшая школа 1989 - С. 114-120. Трофимова Т.И. Курс физики. - М.: Высшая школа, 1990. - С. 81-85. Савельев И.В. Курс общей физики. Т. 1. - М.: Высшая школа. 1987 Физический практикум /Под ред. В.И. Ивероновой. - М, Высшая МОЛЕКУЛЯРНАЯ ФИЗИКА МЕТОДИЧЕСКИЕ УКАЗАНИЯ к лабораторным работам для студентов инженерных специальностей Составители: АсанбайИсманбаевичИсманбаев МурзалыЗарлыковичБайтемиров Бердибекова Космира Нурпашовна Редактор: А.Б. Аманкулова Подписано в печать 06.03.2017. Формат 60x84 1/16. Объем 2,7 уч.-изд. л. Печать офсетная. Бумага офсетная. Тираж 100 экз. Заказ ___________________________________________ Учебно-издательский центр «Авангард» ИНИТ КГУСТА 720020, Бишкек, ул. Малдыбаева, 34, б Кыргызский государственный университет строительства, транспорта и архитектуры |