Метотрексат methotrexate 0,0025 по 1 т через 12 часов 1 раз неделю при ра
 Скачать 7.74 Mb. Скачать 7.74 Mb.
|
|
Дифференциальная диагностика гемолитических анемий в зависимости от локализации гемолиза
Критерии гемолиза (принято считать достаточным наличие 4 признаков из нижеперечисленных): 1. Высокий ретикулоцитоз в периферической крови (более 5 %). 2. Выраженный нормобластоз в миелограмме. 3. Увеличение свободного (неконъюгированного) билирубина в крови. 4. Увеличение железа в сыворотке крови (кроме болезни Маркиафавы-Микели). 5. Увеличение активности ЛДГ (лактатдегидрогеназы). 6. Сокращение продолжительности жизни эритроцитов - с помощью радиоактивного хрома, технеция, индия (наиболее информативный метод, в отличие от вышеперечисленных косвенных, но не распространен широко). Существуют отличия в лабораторных данных при ситуациях с преимущественным внутриклеточным или внутрисосудистым гемолизом. При внутриклеточном гемолизе обязательна сидеремия, желтуха с уробилинурией и вовлечение в процесс гепатобилиарного комплекса. При внутрисосудистом — уровень регенерации может быть не очень высоким, уровень железа — нормальным, а в моче появляется гемосидерин и свободный билирубин. Наследственные гемолитические анемии - обусловлены генетическими дефектами эритроцитов, которые становятся функционально неполноценными и легко разрушаются. 1) связанные с нарушением мембраны эритроцитов (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, стоматоцитоз, акантоцитоз); 2) связанные с нарушением активности ферментов в эритроцитах (глюкозо-6-фосфатдегидрогеназа (Г-6-ФД), пируваткиназа, глутатион-редуктаза); 3) связанные с нарушением структуры или синтеза цепей глобина (талассемия, серповидно-клеточная анемия). Приобретенные гемолитические анемии - следствие воздействия на нормальные эритроциты различных факторов, приводящих их к разрушению (образование антител, гемолитических ядов, механические воздействия). 1) связанные с воздействием антител (изоиммунные - изоантитела или изоантигены попадают в организм больного извне (гемолитическая болезнь новорожденных, трансфузии несовместимой крови по системе АВ0, Rh; гетероиммунные - обусловленные появлением антител против гаптена, сорбировавшегося на эритроцитах. Гаптеном может быть лекарство (пенициллин, цепорин, сульфаниламиды) или вирус; трансиммунные - наблюдаются у новорожденных, матери которых страдают аутоиммунной гемолитической анемией; аутоиммунные - обусловлены образованием антител к собственным антигенам эритроцитов); 2) связанные с изменением структуры мембраны эритроцитов вследствие соматической мутации (болезнь Маркиафавы-Микели – пароксизмальная ночная гемоглобинурия); 3) связанные с механическим повреждением мембраны эритроцита (протезы клапанов сердца, маршевая гемоглобинурия, внутрисосудистый гемолиз при ДВС-синдромах); 4) обусловленные химическими повреждениями эритроцитов (гемолитические яды, свинец, тяжелые металлы, органические кислоты, укусы змей); 5) обусловленные недостатком витамина Е; гипофосфатемия; 6) связанные с воздействием паразитов (малярия). Аутоиммунные гемолитические анемии (АИГА) — анемии, обусловленные образованием аутоантител, направленных против поверхностных антигенов аутологичных эритроцитов. Распространенность аутоиммунных гемолитических анемий 1:500 000 населения. Этиология. Различают: - идиопатические: аутоиммунные гемолитические анемии, возникающие без известной причины; - симптоматические: аутоиммунные гемолитические анемии развиваются на фоне других заболеваний, чаще всего аутоиммунных — СКВ, аутоиммунного гепатита, аутоиммунного тиреоидита, хронического лимфолейкоза, СПИДа и др. В зависимости от вида антител к эритроцитам аутоиммунные гемолитические анемии делятся на: 1) АИГА с неполными тепловыми агглютининами; 2) АИГА с тепловыми гемолизинами; 3) АИГА с полными холодовыми агглютининами; 4) АИГА с двухфазными холодовыми гемолизинами. Тепловые антитела активно связываются при 37 °С, а холодовые - при понижении температуры. Клиника АИГА складывается из общих симптомов анемии (бледность, слабость, одышка, признаки дистрофии миокарда), синдрома гемолитической желтухи (желтушность, увеличение печени, темный цвет мочи и кала) и признаков внутрисосудистого гемолиза (черная моча, гемоглобинурия, тромботические осложнения). Зачастую больные предъявляют много астеновегетативных жалоб при маловыраженных объективных изменениях. В некоторых случаях заболевание развивается остро с клиники гемолитического криза (резкая слабость, боли в пояснице и в области сердца, одышка, лихорадка, быстро развивается желтуха), в других случаях течение хроническое с периодами обострений и ремиссий. Различия в клинической картине между формами АИГА обусловлены тем, что механизм гибели эритроцитов зависит прежде всего от характера антител. Полные холодовые агглютинины вызывают агглютинацию эритроцитов при понижении температуры в сосудах, наиболее отдаленных от сердца (характерен синдром Рейно, непереносимость холода). Неполные антитела нарушают функцию ферментов эритроцитов, изменяют проницаемость мембраны для ионов натрия - возможен микросфероцитоз. При гемолизиновых формах уничтожение эритроцитов осуществляется комплементом непосредственно в сосудах (признаки внутрисосудистого гемолиза - черная моча, гемоглобинурия, тромботические осложнения). Лечение. 1. Глюкокортикоиды при гемолитическом кризе - преднизолон 1-2 мг/кг/сут, средняя доза 60 мг/сут. По мере улучшения состояния дозу постепенно снижают и препарат отменяют. 2. Спленэктомия (показания к операции см. ниже) при отсутствии эффекта от глюкокортикоидов. Положительный эффект в 66 % случаев. 3. Иммунодепрессанты (при неэффективности глюкокортикоидов и спленэктомии, системном заболевании): азатиоприн 100—150 мг в сутки, циклофосфан 400 мг через день, винкристин 2 мг 1 раз в неделю, циклоспорин А 5 мг/кг/сут. или другие цитостатики. 4. Переливание эритроцитарной массы — при быстром падении гемоглобина до 30—40 г/л с признаками гипоксии мозга и миокарда. Переливаются отмытые эритроциты, подобранные с помощью непрямой пробы Кумбса. 5. Плазмаферез. Дифференциально-диагностические различия между аутоиммунной гемолитической анемией и наследственной (врожденной) микросфероцитарной анемией
Наследственный микросфероцитоз (болезнь Минковского-Шоффара) - анемия, связанная с генетическим дефектом мембраны эритроцитов, что обусловливает их микросфероцитарную форму и гемолиз. Тип наследования - аутосомно-доминантный. Патогенез. Нарушение структурного белка (спектрина) ведет к изменению клеточной мембраны, изменению формы эритроцитов. При данном заболевании наблюдается повышение проницаемости эритроцита для натрия, что приводит к проникновению избытка натрия и воды в клетку. Эритроциты приобретают сферическую форму, что нарушает их способность деформироваться в узких участках кровотока, например, при переходе из межсинусных пространств селезенки в синусы. Здесь эритроциты повреждаются и разрушаются макрофагами селезенки. Отсюда, тип гемолиза при наследственном микросфероцитозе - внутриклеточный. В крови нарастает анемия и билирубинемия. Длительно существующий гемолиз ведет к стимуляции эритропоэза, у больных нарушается костеобразование: «башенный череп», «готическое небо», монголоидный тип лица. Клиника 1. Первые клинические симптомы анемии чаще проявляются в детском возрасте. 2. Желтуха, увеличение селезенки, боли в левом подреберье, иногда увеличение печени, склонность к образованию камней в желчном пузыре (желчная колика), изредка симметричные язвы голеней. 3. Деформации скелета («башенный череп», «готическое небо», деформация челюстей с неправильным расположением зубов, полидактилия), микрофтальмия. 4. Периодически возникают гемолитические кризы (часто провоцируются инфекцией): боли в области печени, селезенки и их увеличение, озноб, потемнение мочи, повышение температуры тела до 39-40 ºС, рвота, усиление желтухи и анемии, лейкоцитоз со сдвигом влево, в крови появляются нормоциты или нормобласты. 5. Иногда могут возникать апластические кризы, вызванные инфицированием парвовирусом (PV) — быстро нарастает арегенераторная анемия, иногда ведущая к летальному исходу. Если же происходит выживание, возникает пожизненный иммунитет, обеспечиваемый противовирусным IgG. Лечение 1. Наиболее эффективный метод - спленэктомия (при наличии конкрементов в ЖВП - их удаление), приводящая к клиническому выздоровлению. Показания к спленэктомии (рекомендуется проводить в возрасте 7-8 лет и старше): — выраженная анемия с частыми гемолитическими кризами, гиперспленизмом и спленомегалией (может быть показанием к операции в любом возрасте); — вторичная желчнокаменная болезнь (при ее наличии одновременно проводится холецистоэктомия); — упорная желтуха. 2. Переливание эритроцитарной массы производится только по жизненным показаниям - при крайне тяжелой степени анемии, в период тяжелых гемолитических кризов, а также при выраженной анемии и отказе от спленэктомии. Фолиевая кислота курсами. 3. При апластическом кризе Ig человека для в/в введения в дозе 1-2 г/сут в течение 5 дней. 4. Дезагреганты и антикоагулянты для профилактики тромбозов (Флебодиа). Прогноз благоприятный при адекватном лечении. Факторы, ухудшающие прогноз: возраст старше 60 лет; шок, тромбоэмболии; геморрагический синдром (синдром Эванса-Фишера); резистентность к терапии. 38. Железодефицитные состояния: латентный дефицит и железодефицитная анемия. Эпидемиология, этиология, патогенез, клиника, диагностика, лечение и профилактика. Латентный дефицит железа хар-ся уменьшением количества железа в его депо и снижением уровня транспортного железа крови при еще нормальных показателях гемоглобина и эритроцитов. Железодефицитная анемия (ЖДА) — гипохромная микроцитарная анемия, обусловленная дефицитом железа в сыворотке крови и костном мозге, что сопровождается нарушением образования гемоглобина и эритроцитов, развитием трофических нарушений в органах и тканях. Наиболее распространенный вид анемии (80-95 % всех форм). Каждый 4-5-ый житель планеты страдает железодефицитом. Этиология. 1. Хронические постгеморрагические анемии (желудочно-кишечные, маточные, рецидивирующие почечные, легочные, носовые кровотечения). 2. Нарушение всасывания железа (хронические энтериты, амилоидоз кишечника и др. заб-ния, приводящие к развитию синдрома мальабсорбции, обширные резекции тонкого кишечника). 3. Повышение потребности в железе (беременность, период лактации, резкий рост организма в юношеском возрасте). 4. Перераспределение железа (острые и хронические инфекционные заболевания, злокачественные новообразования). Женщины болеют значительно чаще, чем мужчины. Обмен железа в организме. Железо участвует во всех биологических процессах организма. Общее количество его в организме составляет 4-4,5 г: 3 г содержится в эритроцитах, 1 г - в депо, 1 г расходуется на структуру тканей (350 мг) и ферментов (15-30 мг). Перечисленное количество составляет в основном клеточное железо, железо в депо (ферритин и гемосидерин) относится к железу запасов, а железо, находящееся в соединении с сывороточным белком или в плазме, относится к внеклеточному железу. Суточная потребность организма в железе для синтеза гемоглобина составляет в среднем 10-20 мг (10-12 мг для мужчин и 18-20 мг для женщин). Для синтеза гемопорфирина, железофлавоноидов, железосодержащих белков, обеспечения гуморального и клеточного иммунитета, энергетического потенциала и др. целей расходуется до 40 мг железа в сутки. Из пищи в желудочно-кишечный тракт всасывается в среднем 1,5-2 мг железа. В то же время, ежесуточно потери железа составляют в среднем 1-2 мг: у мужчин - 1 мг (соответствует 2 мл крови), у менструирующих женщин - до 2 мг в сутки. Потери крови при нормальных менструациях (3-4 дня) составляют 20-30 мл крови, что эквивалентно потере 10-15 мг железа. Нормальные роды сопровождаются потерей около 300 мл крови (т. е. 150 мг железа, которое быстро извлекается из депо, но очень медленно восстанавливается). Следует иметь в виду и тот факт, что девочки, дочери матерей с железодефицитом, и сами имеют дефицит железа с рождения (жизнь женщин сопряжена с риском получения дефицита железа). Клиника складывается из анемического, сидеропенического (тканевого дефицита железа) и метаболического синдромов (см. таблицу). Симптомы железодефицитной анемии 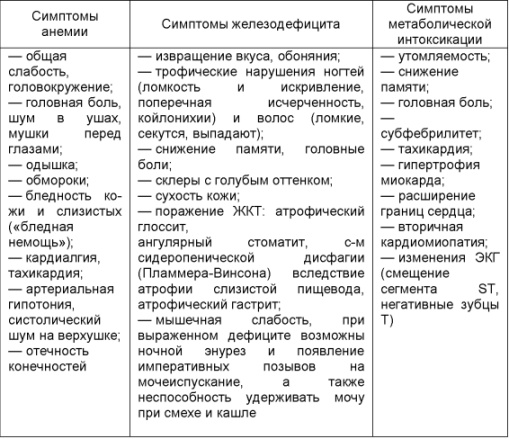 Лабораторные данные. 1. В крови - гипохромная, гипорегенераторная микроцитарная анемия, анизоцитоз, пойкилоцитоз, преобладание микроцитов, возможно ускорение СОЭ. 2. Снижение содержания ферритина (N 15-150 мкг/л) и снижение уровня железа сыворотки крови (в норме 13-30 мкмоль/л). Для получения достоверных результатов в течение 5 дней перед исследованием не принимать препараты, содержащие железо. 3. Железосвязывающая способность сыворотки (общая и латентная) может быть повышена. В норме ОЖСС 30-85 мкмоль/л, латентная ЖСС выше 47 мкмоль/л. Лечение. Существует 5 правил: 1. Не следует лечить только диетой (так как в суточном рационе пищи железа недостаточно для восстановления потери и всасываемость железа из пищевых продуктов ограничена). Без препаратов железа вылечить ЖДА невозможно, даже при употреблении пищи, богатой железом! Следует ограничить прием молочных продуктов за 2 часа до приема препаратов железа. 2. Не следует лечить переливанием эритромассы. Трансфузии делают только при уровне гемоглобина ниже 50 г/л (угроза гипоксической комы) либо перед экстренной операцией. 3. Не следует начинать лечение с парентерального введения железа. Парентеральная ферротерапия показана только при тяжелой непереносимости всех препаратов железа или появлении выраженной диспепсии после приема препаратов. В/в введение препаратов железа может сопровождаться тяжелыми аллергическими реакциями, саркомами мягких тканей, флебитов, абсцессов в местах в/м введения железосодержащих препаратов. 4. Основная патогенетическая терапия состоит в пероральном приеме железосодержащих препаратов. При выборе суточной дозировки следует ориентироваться на общее содержание в нем железа и на количество двухвалентного железа, содержащегося в выбранном препарате железа (какие, см. ниже). Суточная доза элементарного (двухвалентного) железа 100-300 мг. |
