зайко. Н. Н. Зайко Патологическая физиология Введение Предмет и задачи патологической физиологии Патологическая физиология есть наука, изучающая жизнедеятельность больного организма. Программа
 Скачать 7.32 Mb. Скачать 7.32 Mb.
|
|
Глава 20. Патологическая физиология внешнего дыхания Внешнее дыхание – это совокупность процессов, совершающихся в легких и обеспечивающих нормальное содержание в крови кислорода и углекислоты. В легких происходят три основных процесса – вентиляция альвеол,диффузия молекулярного кислорода и углекислого газа через альвеолокапиллярную мембрану и перфузия(протекание соответствующего количества крови через легочные капиллярные сосуды), строгая взаимосвязь которых и обеспечивает нормальный газовый состав крови. Какое бы заболевание ни развивалось в дыхательной системе, оно может привести к нарушению одного из этих процессов, снижению эффективности дыхания и развитию его недостаточности. Недостаточность дыхания Недостаточность дыхания – патологический процесс, развивающийся вследствие нарушения внешнего дыхания, при котором не обеспечивается поддержание адекватного потребностям организма газового состава артериальной крови в состоянии покоя или при физической нагрузке. Из этого следует, что недостаточность дыхания может уже в состоянии покоя привести к гипоксии и газовому ацидозу или ограничивает возможности организма по выполнению физической работы. Основные механизмы развития недостаточности дыхания заключаются в нарушении процессов вентиляции, перфузии, диффузии, а также их количественного соотношения. Нарушения альвеолярной вентиляции Альвеолярная вентиляция заключается в регулярном обновлении альвеолярных газов в соответствии с потребностями организма. Каждую минуту в альвеолярное пространство у человека в состоянии покоя входит 4,5 – 5 л воздуха, благодаря чему и обновляется газовый состав альвеол. В осуществлении этого процесса принимают участие центральная нервная система (дыхательный центр головного мозга и мононейроны спинного мозга), периферические нервы (двигательные и чувствительные), верхние дыхательные пути, грудная клетка и легкие. Расстройство функции одного из перечисленных звеньев может привести к нарушению альвеолярной вентиляции. Нарушение функции дыхательного центра. Вентиляция альвеол регулируется нейронами дыхательного центра, расположенного в продолговатом мозге и мосту. Благодаря работе дыхательного центра устанавливается определенный ритм, глубина и частота дыхания, что обеспечивает нормальный газообмен в соответствии с потребностями организма. Функция дыхательного центра может быть нарушена вследствие прямого действия на центральную нервную систему различных патогенных факторов или рефлекторно (влияния на хемо-, барорецепторы и т. д.). Недостаточность дыхания возникает при уменьшении глубины, частоты дыхания, различных видах периодического дыхания. Более подробно причины и механизмы нарушения деятельности дыхательного центра будут рассмотрены ниже. Нарушение функции мотонейронов спинного мозга. Функция мотонейронов спинного мозга, иннервирующих дыхательные мышцы, может быть нарушена при развитии опухоли в спинном мозге, при сирингомиелии, полиомиелите. Характер и степень нарушения внешнего дыхания при этом зависят от места повреждения спинного мозга (например, при поражении патологическим процессом верхней шейной части спинного мозга нарушается работа диафрагмы) и от количества пораженных мотонейронов. Нарушение функции нервно-мышечного аппарата.Нарушение вентиляции может возникать при поражении нервов, иннервирующих дыхательные мышцы (воспаление, авитаминоз, травма), при затруднении передачи мышцам нервного импульса (при миастении, ботулизме, столбняке), при нарушении функции самих дыхательных мышц (миозит, дистрофия). Из мышц, принимающих участие в акте дыхания, большое значение имеет диафрагма. Нарушение работы диафрагмы может привести к значительному расстройству дыхания, что бывает, в частности, при поражении n.frenicus. При поражении этого нерва возникают парадоксальные движения диафрагмы: вверх – при вдохе, вниз – при выдохе (диссоциированное дыхание). При клонических судорогах мышц диафрагмы появляется икота, во время которой воздух втягивается в легкие. Икота – рефлекторный акт, связанный обычно с раздражением афферентных окончаний в диафрагме или органах брюшной полости. Особенно упорной бывает икота при операциях на органах брюшной полости. Нарушение подвижности грудной клетки. Все патологические процессы, ограничивающие подвижность грудной клетки, ограничивают растяжение легких и, следовательно, влияют на альвеолярную вентиляцию. К ним относятся врожденная или приобретенная деформация ребер и позвоночного столба, окостенение реберных хрящей, плевральные шварты, асцит, метеоризм, большая тучность. Экскурсии грудной клетки могут ограничиваться также резкими болевыми ощущениями, возникающими во время дыхания, например при межреберной невралгии, воспалении плевры и т. д. Нарушение целости грудной клетки и плевральной полости. Целость плевральной полости обеспечивает создание постоянного транспульмонального давления (разность между давлением воздуха внутри альвеол и давлением в плевральной полости), которое поддерживает легкое в расправленном состоянии. Во время вдоха, когда объем грудной клетки увеличивается, транспульмональное давление возрастает до тех пор, пока. не преодолеет эластическую тягу легких, вследствие чего альвеолы расширяются. В том случае, когда нарушается целость плевральной полости и в нее попадает атмосферный воздух, транспульмональное давление снижается, а легкое спадается. Скопление воздуха в плевральной полости и повышение давления в ней называетсяпневмотораксом. Воздух может попасть в полость плевры при проникающем ранении грудной клетки, разрыве эмфизематозных альвеол на поверхности легкого, распаде легочной ткани (туберкулез, опухоль, абсцесс). При этом полость плевры может сообщаться с легкими и другими воздухоносными органами – пищеводом, желудком, кишкой. Иногда воздух вводят в плевральную полость с лечебной целью. Если при попадании воздуха в плевральную полость последняя не сообщается с атмосферным воздухом, возникающий пневмоторакс называют закрытым, если сообщается с атмосферным воздухом – открытым. Наконец, если особенности входного отверстия в полости плевры допускают попадание воздуха во время вдоха, но препятствуют его выходу при выдохе, пневмоторакс называют клапанным, или вентильным. Нарушение функции легких. Вентиляция альвеол может нарушаться при поражении легочной ткани и воздухоносных путей. В зависимости от механизмов, вызывающих нарушение вентиляции, различают два вида легочной недостаточности дыхания – обструктивную и рестриктивную. Обструктивная недостаточность внешнего дыхания возникает вследствие сужения воздухоносных путей (от лат. obstructio – препятствие) и повышения сопротивления движению воздуха. При этом препятствия движению воздуха могут возникать как в верхних дыхательных путях, так и в нижних. Причины сужения просвета верхних дыхательных путей или даже их полной закупорки могут быть следующие: 1. попадание инородных предметов в просвет верхних дыхательных путей; 2. утолщение стенок дыхательных путей, связанное с развитием воспалительного отека слизистой оболочки носа, гортани, трахеи или же с ростом опухоли в этих местах; 3. спазм мышц гортани – ларингоспазм; 4. сдавление стенок дыхательных путей извне. В качестве причин, вызывающих сдавление, можно назвать развитие опухолей в тканях, окружающих дыхательные пути, заглоточный абсцесс, увеличение соседних органов (например, щитовидной железы). При сужении просвета верхних дыхательных путей затрудняются и удлиняются во времени как вдох, так и выдох, значительно возрастает нагрузка на дыхательные мышцы. Постоянное компенсаторное напряжение системы регуляции внешнего дыхания в покое лимитирует возможности дальнейшего увеличения минутного объема дыхания при физической нагрузке. Нижние дыхательные пути (диаметром менее 2 мм) у здорового человека создают незначительное сопротивление дыханию. Однако именно они являются местом возникновения препятствия движению воздуха при большинстве заболеваний легких. Вызвано это тем, что сопротивление потоку воздушной струи возрастает пропорционально четвертой степени уменьшения просвета бронха, через который проходит воздух. Поэтому легко рассчитать, что если просвет бронха диаметром в 1 мм в силу каких-то причин уменьшился до 0,5 мм (т. е. в 2 раза), сопротивление току воздуха возрастет в 24 т. е. в 16 раз. К этому следует добавить еще и то, что при сужении бронхов соответственно растет и скорость движения в них воздуха, а это также сопровождается повышением сопротивления воздушному потоку (пропорционально квадрату увеличения скорости движения воздуха). Вот почему при сужении просвета нижних воздухоносных путей резко увеличиваемся работа дыхательных мышц, особенно во время выдоха, который теперь должен быть активным. Обструктивная недостаточность внешнего дыхания Обструкцию нижних дыхательных путей могут обусловить следующие причины: 1. попадание в просвет мелких бронхов и бронхиол различных жидкостей – рвотных масс, воды, гноя, транссудата; часто это может быть связано со скоплением в бронхах мокроты, возникающим вследствие трех взаимосвязанных расстройств – ухудшения свойств мокроты, нарушения мукоцилиарного транспорта и поражения кашлевого механизма; 2. утолщение слизистой оболочки нижних дыхательных путей вследствие ее отека и гиперемии (при воспалении, застойных явлениях в легких); 3. спазм непроизвольной мускулатуры бронхиол, возникающий при действии различных аллергенов, некоторых раздражающих веществ (например, сернистого газа), гистамина, холиномиметиков, бета-адреноблокаторов; 4. повышенная растяжимость легких вследствие утраты ими эластичности. Снижение эластических свойств легких наблюдается приэмфиземе – заболевании легочной паренхимы, которое сопровождается разрушением тонкой сети легочных капиллярных сосудов и альвеолярных перегородок, а также сужением просвета терминальных бронхиол. Важным фактором в происхождении эмфиземы является ферментативный распад волокнистых структур легочной ткани в результате избыточного действия протеолитических ферментов (эластазы, коллагеназы, трипсина), продуцируемых в основном нейтрофилами и альвеолярными макрофагами. Эти клетки в легких могут стимулироваться микробной флорой, табачным дымом, пылевыми частицами (углем, асбестом, цементом и т. п.). В развитии эмфиземы могут играть роль и наследственные факторы – дефицит в крови ?1-антитрипсина, дефекты в структуре коллагена, эластина, протеингликанов, атония гладкомышечных клеток, окружающих респираторную бронхиолу. Механизм возникновения обструктивных явлений при эмфиземе заключается в том, что просвет бронхиол, как уже упоминалось выше, обладающих мягкими и тонкими стенками, поддерживается транспульмональным давлением. Чем больше эластичность легкого, тем большее разрежение необходимо создать в плевральной полости во время вдоха (и тем самым повысить транспульмональное давление), чтобы преодолеть эластическую тягу легких и растянуть их. Если же легкие утрачивают свою эластичность, то они растягиваются гораздо легче, т. е. при гораздо меньшем транспульмональном давлении. В результате уменьшается сила, действующая на стенку бронхиол изнутри и расправляющая их – просвет бронхиол уменьшается вследствие спадения их стенок, Уменьшение просвета нижних дыхательных путей значительно повышает, сопротивление движению воздуха и мешает равномерному распределению его в альвеолах. Особенно сильно нарушается при этом акт выдоха. Объясняется это тем, что при эмфиземе во время вдоха транспульмональное давление, хотя и меньше нормального, но все-таки достаточное, чтобы расправить стенки бронхиол. Во время выдоха (который при эмфиземе становится активным, так как эластическая тяга легких ослабевает, а сопротивление движению воздуха увеличивается) давление в плевральной полости нарастает и соответственно по мере выдоха увеличивается сила, действующая на бронхиолы снаружи. Стенки бронхиол постепенно спадаются, и наступает такой момент, когда дальнейший выдох становится невозможным. Таким образом, при эмфиземе стенки бронхиол играют рольклапана, который во время выдоха закрывается, и воздух оказывается пойманным, как в ловушке. Вследствие этого альвеолы остаются постоянно раздутыми, в них увеличивается количество остаточного воздуха. Аналогичным образом раннее (преждевременное) экспираторное закрытие дыхательных путей может возникать и при других обструктивных процессах – бронхиальной астме, бронхитах и т. д. Результаты спирографии показывают, что при обструктивных процессах в легких нарушается механика дыхания (рис. 20.1). Падают абсолютные скоростные показатели, основанные на форсированном дыхании (максимальная легочная вентиляция, объем форсированного выдоха, индекс Тиффно1 и др.), увеличивается общая емкость легких, значительно возрастает остаточный объем. Все это наряду с гиповентиляцией альвеол (рис. 20.2) существенно ухудшает газообмен в легких. Рестриктивная недостаточность внешнего дыхания. Этот вид недостаточности связан с нарушением вентиляции альвеол вследствие ограничения растяжимости легких (от лат. restrictio – ограничение, уменьшение), уменьшения дыхательной поверхности. Уменьшение растяжимости легких ограничивает их способность расправляться. Чтобы компенсировать это и добиться необходимого изменения объема легких, во время вдоха следует создавать большее, чем обычно, транспульмональное давление. Это в свою очередь увеличивает работу, производимую дыхательными мышцами. Дыхание становится затрудненным, особенно при физической нагрузке. Рестриктивные процессы в легких приводят к гиповентиляции альвеол (см. рис. 20.2,Б), снижению общего объема легких и жизненной емкости легких (рис. 20.1, б), резервного объема вдоха. Растяжимость легких может ухудшаться по ряду причин: 1. Воспалительные процессы и застойные явления в легких. При этом переполненные кровью легочные капиллярные сосуды, а также отечная интерстициальная ткань сдавливают альвеолы и мешают им расправиться в полной мере. Кроме того, в этих условиях снижается растяжимость и самих капиллярных сосудов и интерстициальной ткани. 2. Фиброз легких. Этот процесс является исходом различных заболеваний легких. Фиброзу чаще всего предшествуют хронические воспалительные заболевания, токсическое поражение, длительное запыление легких (пневмокониоз), эмфизема, диффузные заболевания соединительной ткани, застой крови в легких при недостаточности кровообращения, действие ионизирующей радиации. Сущностью фиброза является избыточное разрастание соединительной ткани, преимущественно грубой волокнистой, на месте погибших паренхиматозных элементов, капиллярных сосудов и эластических волокон. 3. Нарушение сурфактантной системы легких. В норме, как известно, внутренняя поверхность альвеол покрыта сурфактантами – поверхностно-активными веществами, основную массу которых составляют липопротеиды. За счет высокой поверхностной активности сурфактантов поверхностное натяжение в легком близко к нулю, что предотвращает транссудацию жидкости в просвет альвеол из капилляров и предохраняет альвеолы от слипания. Растяжимость легких на две трети обеспечивается сурфактантами. К сурфактантной системе легких относятся пневмоциты I и II типов, которые принимают участие в синтезе фосфолипидов и белковой части сурфактантов, депонировании готового материала и его секреции, а также макрофаги, с помощью которых отработанный сурфактант удаляется с альвеолярной поверхности. Недостаток сурфактантов приводит к повышению поверхностного натяжения альвеол, в результате чего повышается сопротивление легких их растяжению, возникают ателектазы. К дефициту сурфактантов может привести нарушение их синтеза, повышенное удаление с поверхности альвеол или их разрушение. Например, дефицит сурфактантов является ведущим звеном патогенеза респираторного дистресс-синдрома новорожденных (болезнь гиалиновых мембран), что приводит к их асфиксии и гибели. При этом происходит частичное разрушение альвеол и накопление в их просвете бесструктурного вещества (гиалиновых мембран), в котором встречаются остатки эпителиальных клеток, форменных элементов крови. Кроме того, количество сурфактантов может снижаться при гипоксии, ацидозе, воспалении легких, нарушении кровообращения в них, аспирации рвотных масс и других жидкостей, при применении искусственного кровообращения. Сурфактант легко разрушается высокими концентрациями кислорода, и поэтому применение чистого кислорода при недостаточности дыхания может иногда сделать ее еще более тяжелой. 4. К нарушению расправления легких может привестиателектаз – патологический процесс, при котором прекращается вентиляция альвеол, и они спадаются вследствие рассасывания в них воздуха. Причиной ателектаза чаще всего бывает нарушение проходимости бронха со спадением легочной ткани дистальнее места закупорки (обтурационный ателектаз). Ателектаз может развиваться также в результате сдавливания легочной ткани извне экссудатом, опухолью и т. п. (компрессионный ателектаз). Наконец, в патогенезе ателектаза важное значение может иметь снижение содержания сурфактантов. Следует отметить, что при обструкции, которая возникает, например, при воспалительных процессах в дыхательных путях (обструктивные бронхиты) и которая местами приводит к обтурации бронхов, развитию множественных ателектазов препятствует коллатеральная вентиляция через межальвеолярные анастомозы, называемые порами Кона. Их роль в обеспечении газообмена невелика, но они имеют важное значение для поддержания стабильности просвета альвеол. 1 У здорового человека объем форсированного выдоха за первую секунду (ОФВ1) должен составлять не менее 70% от жизненной емкости его легких (ЖЕЛ). Индекс Тиффно (ОФВ1/ЖЕЛ х 100%) всегда ниже 70% у больных с обструктивной патологией легких. Нарушения легочного кровотока В норме величина общего кровотока в легких равна минутному объему крови сердца (МО) и составляет 4,5 – 5 л/мин. К нарушению перфузии легких могут привести следующие патологические процессы: 1. макро- и микроэмболии тромботическими массами, жиром, околоплодными водами, газом, вызывающие ишемию легкого; рефлекторные реакции в малом и большом круге кровообращения, бронхоспазм, выделение БАВ; 2. легочные васкулиты, в том числе аллергические, септические и др.; 3. легочная артериальная гипертензия, которая может быть следствием врожденных или приобретенных пороков сердца, левожелудочковой сердечной недостаточности, тромбоэмболии, гипоксии; 4. кардиогенный, анафилактический, гиповолемический шок и другие его виды. Первичное или вторичное поражение легочного кровотока не только вызывает дыхательную недостаточность вследствие вентиляционно-перфузионных расстройств (см. ниже), но и ведет к рестриктивному механизму нарушения дыхания из-за ишемии альвеолярной ткани, выделения БАВ, повышения проницаемости сосудов, интерстициального отека, уменьшения образования сурфактанта, ателектаза и т. п. [Зильбер А. П., 1989]. Нарушение общих и регионарных вентиляционно-перфузионных отношений в легких Для нормального течения газообмена в легких очень важно правильное соотношение вентиляции и кровотока. В покое у здорового человека эффективная альвеолярная вентиляция (АВ) равна 4 – 5 л, минутный объем крови – около 5 л, а соотношение альвеолярная вентиляция/ минутный объем крови (АВ/МО) составляет 0,8 – 1 (вентиляционно-перфузионный показатель). Именно такое соотношение и обеспечивает нормальный газовый состав крови, оттекающей от альвеол. В тех случаях, когда вентиляция начинает преобладать над кровотоком (АВ/МО › 1) из крови удаляется большее, чем обычно, количество углекислоты и развивается гипокапния. Если же вентиляция отстает от кровотока (АВ/МО ‹ 0,8), в альвеолярном воздухе будет увеличиваться парциальное давление СО2 и снижаться рO2, что приведет к развитиюгипоксемии и гиперкапнии. Для того чтобы газообмен в легких протекал нормально, оптимальное соотношение АВ/МО должно поддерживаться во всех альвеолах. Это означает, что во время дыхания вдыхаемый воздух и соответственно кровоток должны равномерно распределяться по всем легочным альвеолам. Однако полностью это условие не выполняется даже в норме; у здорового человека имеются отклонения в равномерности распределения как вентиляции, так и перфузии альвеол, находящихся в различных участках легких. Оказывается, что и вентиляция, и перфузия в нижних отделах легких преобладают над теми же показателями в верхних отделах. Кроме того, в верхних отделах вентиляция превышает кровоток, а в нижних кровоток преобладает над вентиляцией. При заболеваниях легких к физиологической неравномерности вентиляции и кровотока может присоединиться и патологическая. Например, при пневмонии, эмфиземе, ателектазе или пневмосклерозе в результате вовлечения в патологический процесс кровеносных сосудов кровоток в капиллярных сосудах части альвеол резко снижается, а в других участках легкого – усиливается. Наблюдающиеся при этом нарушения эластичности легких или прохождения воздуха в дыхательных путях могут быть выражены в различных участках легких в неодинаковой степени, что приведет к неравномерной вентиляции альвеол. Кроме того, значительные нарушения газообмена могут возникать и оттого, что в хорошо вентилируемых альвеолах кровоток может быть слабым (альвеолярное мертвое пространство)1, а альвеолы, хорошо снабжаемые кровью, могут плохо вентилироваться (альвеолярное шунтирование крови)2. В то же время общая альвеолярная вентиляция и общий кровоток в легких могут существенно не изменяться. На рис. 20.3 показано, как существенно могут изменяться вентиляционно-перфузионные отношения в подобных случаях. При этом видно, что высокое вентиляционно-перфузионное отношение приводит лишь к небольшому повышению оксигенированности крови, тогда как низкое вызывает ее значительное снижение, что в итоге приводит к уменьшению содержания кислорода в крови, оттекающей от данного участка легкого. Необходимо отметить, что в легких существует феномен гипоксической вазоконстрикции. Суть его заключается в том, что при снижении р02 в альвеолярном воздухе (а не в крови) наблюдается сокращение гладких мышц стенок артериол в гипоксической зоне. Точный механизм этой реакции неизвестен, но показано, что она происходит в изолированных легких и, следовательно, не зависит от центральной нервной системы. Есть предположение, что клетки околососудистых тканей в ответ на гипоксию выделяют некие сосудосуживающие вещества. Благодаря гипоксической вазоконстрикции уменьшается кровоснабжение плохо вентилируемых участков легких, появляющихся, например, в результате бронхиальной обструкции. Такое уменьшение улучшает общий газообмен, поскольку при этом выравнивается соотношение между альвеолярной вентиляцией и перфузией, уменьшается альвеолярное шунтирование крови. Во время внутриутробного периода сопротивление легочных сосудов у плода очень велико, главным образом благодаря гипоксической вазоконстрикции, и через легкие протекает лишь около 15% сердечного выброса. При рождении после первого вдоха в альвеолы поступает О2, сопротивление сосудов падает и легочный кровоток мгновенно возрастает. Нарушения диффузии газов в легких Проникновение кислорода из альвеолярного пространства в кровь и углекислоты из крови в альвеолярное пространство происходит, как известно, по законам диффузии. Установлено, что для того, чтобы молекулярный кислород соединился с гемоглобином, ему необходимо преодолеть тонкий слой жидкости на поверхности альвеолярных клеток, альвеолокапиллярную мембрану, представленную слоем альвеолярных и эндотелиальных клеток и находящимся между ними слоем волокнистых элементов и межуточного вещества соединительной ткани, слой плазмы крови и мембрану эритроцитов. Углекислота проходит тот же путь, но в обратном направлении. Диффузионная способность легких зависит, главным образом, от толщины указанных слоев, а также от степени их проницаемости для газов. Кроме того, для нормального течения диффузии имеет значение общая площадь мембран, через которые проходят O2 и СO2, и время контакта крови с альвеолярным воздухом. Изменение одного из этих факторов может привести к развитию недостаточности дыхания. Нарушение структуры альвеолокапиллярной мембраны. В легких могут развиваться патологические процессы, сопровождающиеся утолщением стенки альвеол и капиллярных сосудов, увеличением количества соединительной ткани между ними (рис. 20.4). При этом увеличивается путь для диффузии газов, понижается проницаемость мембран – развивается альвеолокапиллярный блок. К возникновению альвеолокапиллярного блока ведут многие диффузные поражения легких – саркоидоз, пневмокониоз различной этиологии, фиброз, склеродермия, пневмония (хроническая или острая), эмфизема, отек легкого. Следует отметить, что при таких заболеваниях, как пневмония или недостаточность сердца в стадии декомпенсации, путь прохождения газов удлиняется вследствие увеличения количества жидкости в просвете легочных артериол, а также в тканях легкого. 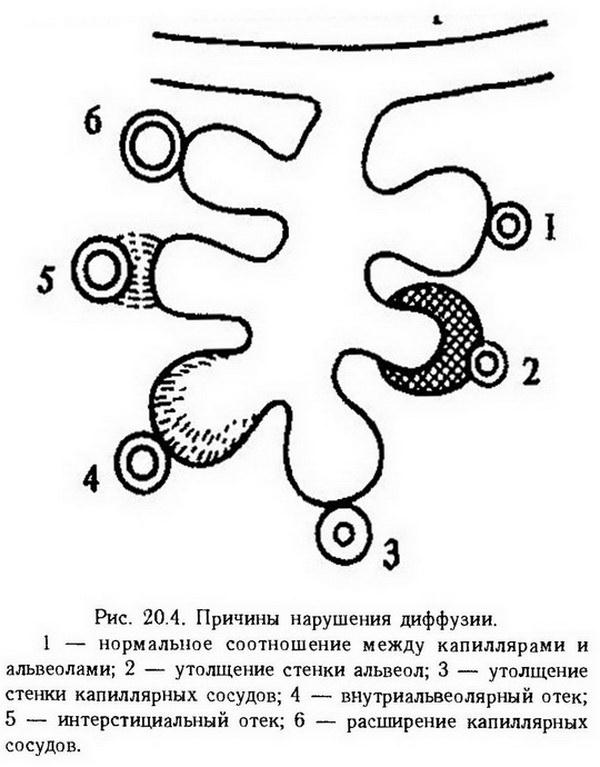 Уменьшение площади мембран, через которые осуществляется диффузия, может наблюдаться при резекции доли легкого, при деструкции обширных участков легкого (кавернозный туберкулез, абсцесс), при полном прекращении вентиляции легочных альвеол (ателектаз) или при уменьшении поверхности капиллярной сети (эмфизема, легочный васкулит). Уменьшение времени контакта крови с альвеолярным воздухом. Время прохождения крови по капиллярным сосудам легочных альвеол составляет 0,6 – 0,7 с, а для полной диффузии газов достаточно всего 0,2 с. Однако такое время диффузии характерно для нормальной альвеолокапиллярной мембраны. Если же она изменена (о чем было сказано выше), то при значительном ускорении кровотока (при физической нагрузке, анемии, горной болезни и др.) газы не успевают в достаточном количестве диффундировать через альвеолокапиллярную мембрану, и тогда меньшее количество гемоглобина связывается с кислородом. Следует отметить, что если в легких возникают процессы, затрудняющие диффузию, то они приводят к нарушению в первую очередь диффузии кислорода, поскольку углекислый газ диффундирует в 20 – 25 раз легче. Поэтому такие процессы часто сопровождаются гипоксемией без гиперкапнии. Влияние недостаточности внешнего дыхания на организм Недостаточность дыхания является одной из причин развития в организме гипоксии и ацидоза. Однако при многих заболеваниях системы внешнего дыхания, когда неизбежно нарушаются процессы вентиляции, диффузии и перфузии, в спокойном состоянии недостаточность дыхания может не возникать, так как при этом поддерживается нормальный газовый состав крови. Это связано, во-первых, с наличием в легких такого количества функциональных элементов (альвеол и капиллярных сосудов), которое во много раз превышает потребность организма в состоянии покоя в нормальном газообмене. Во-вторых, тонкая и совершенная система регуляции внешнего дыхания реагирует на малейшие колебания напряжения O2 и СO2 в крови и при необходимости увеличивает работу Дыхательных мышц, меняя глубину и частоту дыхания. Соответственно дыханию изменяется и деятельность системы кровообращения. Все это способствует поддержанию постоянства газового состава крови в покое при патологии органов дыхания. Однако поскольку в этих условиях компенсация достигается за счет мобилизации резервов дыхательной системы, признаки недостаточности дыхания обязательно появляются при физической нагрузке, так как при этом резервные приспособительные возможности внешнего дыхания у больного человека будут исчерпаны раньше, чем у здорового. По мере нарастания степени нарушения процессов вентиляции, диффузии или перфузии все больше увеличивается работа дыхательных мышц в покое и нагрузка на систему кровообращения. Увеличивается обмен веществ и потребность организма в кислороде. В итоге наступает такой момент, когда и в состоянии покоя поддержание нормального газового состава крови становится невозможным. Тогда ведущими звеньями в развитии дальнейших нарушений в организме становятся гипоксия, гиперкапния и газовый ацидоз. В том случае, когда недостаточность дыхания возникает остро или подостро и достигает такой степени, что в кровь перестает поступать кислород, а из крови не выводится углекислота, развивается асфиксия. Чаще всего асфиксия возникает при сдавлении дыхательных путей (удушение), закупорке их просвета (инородные тела, воспалительный отек), наличии жидкости в дыхательных путях и альвеолах (утопление, отек легкого, попадание рвотных масс), при двустороннем пневмотораксе. Кроме того, асфиксия может развиться при сильном угнетении дыхательного центра, нарушении проведения нервных импульсов к дыхательным мышцам, резком ограничении подвижности грудной клетки. В течении асфиксии выделяют три периода, которые можно наблюдать у животного в эксперименте, например при пережатии трахеи. Первый период асфиксии характеризуется быстрым увеличением глубины и частоты дыхания с преобладанием фазы вдоха над фазой выдоха. Развивается общее возбуждение, повышается тонус симпатической части вегетативной нервной системы (расширяются зрачки, появляется тахикардия, повышается артериальное давление), возможны судороги. Во втором периоде частота дыхания постепенно уменьшается при сохраняющейся максимальной амплитуде дыхательных движений, усиливается фаза выдоха. Преобладает тонус парасимпатической части вегетативной нервной системы (зрачки суживаются, снижается артериальное давление, отмечается брадикардия). В третьем периоде асфиксии наблюдается уменьшение амплитуды дыхания, его частоты и, наконец, остановка дыхания. Артериальное давление значительно снижается. После кратковременной остановки дыхания обычно появляется несколько редких судорожных дыхательных движений (гаспинг-дыхание), после которых наступает паралич дыхания. Явления, наблюдаемые при асфиксии, связаны вначале с накоплением в организме углекислоты. Действуя рефлекторно и через центральные хеморецепторы для Н -ионов, углекислота возбуждает дыхательный центр, доводя глубину и частоту дыхания до максимально возможных величин. Кроме того, дыхание рефлекторно стимулируется и снижением в крови напряжения молекулярного кислорода. По мере увеличения в крови содержания СO2 повышается и артериальное давление. Эксперименты с вдыханием газовых смесей, содержащих 10 – 20% СО2, показали, что это повышение связано, во-первых, с рефлекторным влиянием через хеморецепторы на сосудодвигательный центр; во-вторых, с усиленным выбросом адреналина в кровь; в-третьих, с увеличением минутного объема крови в результате повышения тонуса вен и увеличения притока крови при усилении дыхания. При дальнейшем увеличении концентрации СО2 в крови начинает проявляться его наркотическое действие, рН крови снижается до 6,8 – 6,5. Усиливается гипоксемия и соответственно гипоксия головного мозга. Это приводит в свою очередь к угнетению дыхания, снижению артериального давления. В итоге наступает паралич дыхания и остановка сердца. 1 В нормальных условиях анатомическое мертвое пространство составляет около 22% от дыхательного объема, а альвеолярное – около 16%. назад 2 Нормальные значения альвеолярного шунта не превышают 5 – 7% минутного объема крови сердца. При дыхательной недостаточности величина шунта может достигать 70 – 80% сердечного выброса [Зильбер А. П., 1989]. Нарушения регуляции внешнего дыхания В нормальных условиях правильная работа дыхательного центра приводит к тому, что у человека устанавливается определенная частота, глубина и ритм дыхания. Человек в покое дышит без каких-либо видимых усилий, чаще всего не замечая этого процесса. Такое состояние называется дыхательным комфортом, а наблюдающееся при этом дыхание – эупноэ. При патологии под влиянием рефлекторных, гуморальных или других воздействий на дыхательный центр может изменяться ритм дыхания, его глубина и частота, нередко сопровождающиеся одышкой. Эти изменения могут быть проявлением компенсаторных реакций организма, направленных на поддержание постоянства газового состава крови, или проявлением нарушений нормальной регуляции дыхания, ведущих к уменьшению альвеолярной вентиляции, к недостаточности дыхания. Брадипноэ – это редкое дыхание. Механизм развития редкого дыхания заключается в изменении характера нервной импульсации, идущей от различных рецепторов к дыхательному центру, или в первичном нарушении деятельности самих дыхательных нейронов. Рефлекторное уменьшение частоты дыхания может наблюдаться при повышенном артериальном давлении (рефлекс с барорецепторов дуги аорты и сонной пазухи), при гипероксии (вследствие выключения "гипоксического драйва" – периодического возбуждения хеморецепторов, чувствительных к понижению напряжения молекулярного кислорода в артериальной крови). Глубокое редкое дыхание может появиться при повышении сопротивления движению воздуха в верхних дыхательных путях – стенотическое дыхание. В этом случае вдох и выдох совершаются медленнее, чем обычно. В установлении такого типа дыхания определенную роль играют импульсы, поступающие в дыхательный центр от межреберных мышц, работающих с повышенной нагрузкой. Кроме того, имеет значение запаздывание в этом случае тормозящего рефлекса Геринга – Брейера. Выключением афферентного звена этого рефлекса объясняется очень редкое, но глубокое дыхание, наблюдающееся в эксперименте у животных после перерезки обоих блуждающих нервов (вагусное дыхание). Брадипноэ может развиваться в результате непосредственного воздействия патогенных факторов на дыхательный центр, снижающего возбудимость дыхательных нейронов. Полипноэ (или тахипноэ) – частое поверхностное дыхание. В основе развития полипноэ лежит рефлекторная перестройка работы дыхательного центра. У некоторых животных (например, у собак) частое поверхностное дыхание возникает при действии высокой температуры. У человека полипноэ может наблюдаться при лихорадке, при функциональных нарушениях центральной нервной системы (истерия), при поражении легких (ателектаз, пневмония, застойные явления). По-видимому, в отдельных случаях полипноэ возникает тогда, когда имеется, с одной стороны, большая, чем обычно, стимуляция центра вдоха, а с другой – чрезмерная активация во время вдоха факторов, тормозящих его. Например, при ателектазе центр вдоха возбуждается импульсами от рецепторов, раздражающихся чрезмерным спадением легочных альвеол. Но во время вдоха непораженные альвеолы растягиваются в большей, чем обычно, степени, что вызывает сильный поток импульсов со стороны тормозящих вдох рецепторов, которые и обрывают вдох раньше времени. Кроме того, к развитию полипноэ может привести боль, локализующаяся в областях тела, участвующих в дыхательном акте (грудная клетка, брюшная стенка, плевра). Боль приводит к ограничению глубины дыхания и увеличению его частоты (щадящее дыхание). Полипноэ снижает эффективность дыхания, так как при этом значительно уменьшается эффективный дыхательный объем и вентилируется в основном мертвое пространство. Гиперпноэ, или глубокое частое дыхание, в физиологических условиях возникает как реакция дыхательной системы, направленная на приведение вентиляции легких в соответствие с потребностями усилившегося обмена веществ, например, во время мышечной работы. При этом улучшается оксигенация крови и поддерживается кислотно-основное равновесие в организме выведением избыточного количества СО2. При патологических условиях гиперпноэ развивается вследствие интенсивной рефлекторной или гуморальной стимуляции дыхательного центра, например при снижении парциального давления молекулярного кислорода во вдыхаемом воздухе или при повышении в нем концентрации CO2, при анемии, ацидозе и т. д. Крайняя степень возбуждения дыхательного центра проявляется в виде дыхания Куссмауля, которое чаще всего наблюдается у больных в состоянии диабетической комы. Оно представляет собой глубокое шумное учащенное дыхание, при котором после глубокого вдоха следует усиленный выдох с активным участием экспираторных мышц. Апноэ дословно переводится как отсутствие дыхания, но обычно этим словом обозначают временную остановку дыхания. Апноэ может привести к нарушению газообмена в организме, тяжесть которого зависит от частоты возникновения и продолжительности апноэ, что в свою очередь определяется его причинами. Экспериментальные исследования показали, что временная остановка дыхания может быть связана с уменьшением рефлекторной или непосредственной стимуляции дыхательного центра. Например, апноэ возникает после пассивной гипервентиляции у животного или человека под наркозом вследствие уменьшения в артериальной крови напряжения СО2 и прекращается тотчас же, как только содержание СO2 нормализуется. Кашель и чиханье относятся к рефлекторным актам, возникающим в ответ на раздражение определенных рецепторных зон, главным образом верхних дыхательных путей, и сопровождающимся кратковременным изменением ритма и глубины дыхания. Кашель чаще всего возникает при раздражении нервных окончаний языкоглоточного и блуждающего нервов в слизистой оболочке глотки, гортани, трахеи (наиболее чувствительна область ее раздвоения) и бронхов. Кроме того, он может быть вызван раздражением чувствительных окончаний плевры. Кашель состоит из короткого вдоха, после которого немедленно смыкается голосовая щель и одновременно развивается экспираторное усилие дыхательных мышц. Вследствие этого резко повышается давление в дыхательных путях, легочных альвеолах и плевральной полости. Голосовая щель затем внезапно раскрывается, и воздух с большой силой и скоростью выходит из дыхательных путей, увлекая за собой частицы, расположенные на поверхности слизистой оболочки. Чиханье возникает в ответ на раздражение нервных окончаний тройничного нерва, находящихся в слизистой оболочке носа (особенно средней носовой раковины и перегородки). В отличие от кашля при чиханье форсированный выдох,. возникающий после открытия голосовой щели, происходит не через рот, а через нос. И кашель, и чиханье являются защитными реакциями, направленными на очищение дыхательных путей от слизи, мокроты, различных химических веществ и механических частиц. Возникая эпизодически, они не оказывают влияния на газообмен в легких. Однако длительные приступы кашля приводят к продолжительному повышению внутригрудного давления, что ухудшает вентиляцию альвеол и нарушает кровообращение, особенно в сосудах малого круга кровообращения. Периодическим дыханием называется такое нарушение ритма дыхания, при котором периоды дыхания чередуются с периодами апноэ. Существует два типа периодического дыхания – дыхание Чейна – Стокса и дыхание Биота. Дыхание Чейна – Стокса характеризуется нарастанием амплитуды дыхания до выраженного гиперпноэ, а затем уменьшением ее до апноэ, после которого опять наступает цикл дыхательных движений, заканчивающихся также апноэ (рис. 20.5).  Циклические изменения дыхания у человека могут сопровождаться помрачением сознания в период апноэ и нормализацией его в период увеличения вентиляции. Артериальное давление при этом также колеблется, как правило, повышаясь в фазе усиления дыхания и понижаясь в фазе его ослабления. Полагают, что в большинстве случаев дыхание Чейна – Стокса является признаком гипоксии головного мозга. Оно может возникать при недостаточности сердца, заболеваниях мозга и его оболочек, уремии. Некоторые лекарственные препараты (например, морфин) также могут вызывать дыхание Чейна – Стокса. Его можно наблюдать у здоровых людей на большой высоте (особенно во время сна), у недоношенных детей, что, по-видимому, связано с несовершенством нервных центров. Дыхание Чейна – Стокса у животных можно воспроизвести, вызывая недостаточное снабжение головного мозга кислородом (ингаляция газовых смесей с низким содержанием кислорода, нарушение кровоснабжения головного мозга) или путем перерезки мозгового ствола на различных уровнях. Патогенез дыхания Чейна – Стокса не вполне ясен. Некоторые исследователи объясняют его механизм следующим образом. Клетки коры большого мозга и подкорковых образований вследствие гипоксии угнетаются – дыхание останавливается, сознание исчезает, угнетается деятельность сосудодвигательного центра. Однако хеморецепторы при этом все еще способны реагировать на происходящие изменения содержания газов в крови. Резкое усиление импульсации с хеморецепторов наряду с прямым действием на центры высокой концентрации углекислоты и стимулами с барорецепторов вследствие снижения артериального давления оказывается достаточным, чтобы возбудить дыхательный центр – дыхание возобновляется. Восстановление дыхания ведет к оксигенации крови, уменьшающей гипоксию головного мозга и улучшающей функцию нейронов сосудодвигательного центра. Дыхание становится глубже, сознание проясняется, повышается артериальное давление, улучшается наполнение сердца. Увеличивающаяся вентиляция ведет к повышению напряжения кислорода и понижению напряжения углекислоты в артериальной крови. Это в свою очередь приводит к ослаблению рефлекторной и химической стимуляции дыхательного центра, деятельность которого начинает угасать, – наступает апноэ. Следует отметить, что опыты по воспроизведению периодического дыхания у животных путем перерезки мозгового ствола на различных уровнях позволяют некоторым исследователям утверждать, что дыхание Чейна – Стокса возникает вследствие инактивации тормозящей системы сетчатого образования или изменения ее равновесия с облегчающей системой. Нарушение тормозящей системы может быть вызвано не только перерезкой, но и введением фармакологических средств, гипоксией и др. Дыхание Биота отличается от дыхания Чейна – Стокса тем, что дыхательные движения, характеризующиеся постоянной амплитудой, внезапно прекращаются так же, как и внезапно начинаются (рис. 20.6).  Чаще всего дыхание Биота наблюдается при менингите, энцефалите и других заболеваниях, сопровождающихся повреждением центральной нервной системы, особенно продолговатого мозга. Терминальное дыхание. Апнейстическое дыханиехарактеризуется судорожным непрекращающимся усилием вдохнуть, изредка прерываемым выдохом. Апнейстическое дыхание в эксперименте наблюдается после перерезки у животного обоих блуждающих нервов и мозгового ствола между пневмотаксическим (в ростральной части моста) и апнейстическим центрами (в средней и каудальной части моста). Полагают, что апнейстический центр обладает способностью возбуждать инспираторные нейроны, которые периодически тормозятся импульсами с блуждающего нерва и пневмотаксического центра. Перерезка указанных структур приводит к постоянной инспираторной активности апнейстического центра. Гаспинг-дыхание (от англ. gasp – ловить воздух, задыхаться) – это единичные, редкие, убывающие по силе "вздохи", которые наблюдаются при агонии, например, в заключительной стадии асфиксии. Такое дыхание называется также терминальным или агональным. Обычно "вздохи" возникают после временной остановки дыхания (претерминальной паузы). Появление их, возможно, связано с возбуждением клеток, находящихся в каудальной части продолговатого мозга после выключения функции вышерасположенных отделов мозга. Одышка. При недостаточности дыхания и некоторых других патологических процессах у человека может возникнуть ощущение недостатка воздуха и связанная с ним потребность усилить дыхание. Это явление носит название одышки, илидиспноэ. Испытывая ощущение недостатка воздуха, человек не только непроизвольно, но и сознательно увеличивает активность дыхательных движений, стремясь избавиться от этого тягостного ощущения, наличие которого и является самым существенным отличием диспноэ от других видов нарушения регуляции дыхания (гиперпноэ, полипноэ и др.). Поэтому у человека в бессознательном состоянии одышки не бывает. У здорового человека одышка может возникнуть во время выполнения тяжелой мышечной работы, если эта работа сопряжена с большими усилиями, достигающими предела его физических возможностей. |
