иммунология. Новосибирская государственная медицинская академия кафедра патофизиологии
 Скачать 320.5 Kb. Скачать 320.5 Kb.
|
|
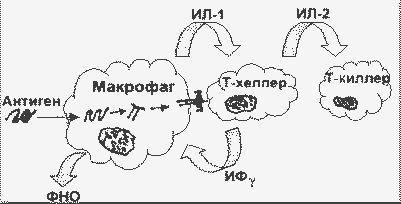
2. ИНДУКЦИЯ ИММУННОГО ОТВЕТА. Как и при других межклеточных взаимодействиях в кооперации А-клеток и Т-лимфоцитов участвует ряд медиаторов. Так, макрофаги вырабатывают интерлейкин-1 (IL-1), который выступает в роли дополнительного сигнала для клеток-индукторов и хелперов (рис.). С другой стороны, Т-лимфоциты вырабатывают интерферон, активирующий макрофаги. Таким образом, взаимосвязь между А-клетками и Т-лимфоцитами ни в коем случае нельзя рассматривать как "улицу с односторонним движением". Иммунный ответ на Т-зависимые антигены начинается с активации определенной субпопуляции Т-клеток, получивших название "индукторы". Характерным признаком индукторных Т-лимфоцитов является выработка и секреция IL-2, который выступает в роли дополнительной сигнала для лимфоцитов, стимулированных антигеном. IL-2 является универсальным стимулом для активации эффекторных Т-лимфоцитов независимо от их типа. Действие IL-2 направлено в основном на клетки-предшественники соответствующих эффекторных лимфоцитов (предшественник цитотоксической клетки, предшественник Т-хелпера), вызывая дифференцировку и пролиферацию антигенстимулированного клона. Считают, что хотя IL-2 не является Аг-специфическим сигналом, активация им лимфоцитов в основном антигенспецифична. Причина состоит в пространственном расположении участвующих в иммунном ответе клеток в периферических лимфоидных органах. АПК взаимодействуют с Т-индукторами и предшественниками цитотоксической Т-клетки и Т-хелпера через рецепторы, а также активирует их, продуцируя IL-1. Стимулированные Т-индукторы начинают продуцировать IL-2, активируя тем самым клетки, кооперирующие с ними через АПК. Покоящиеся, т.е. нестимулированные, Т-лимфоциты не несут рецептор для IL-2 и не могут быть им активированы. 3. ПРОДУКТИВНАЯ ФАЗА ИММУННОГО ОТВЕТА. Оптимальные иммунный ответ реализуется только при взаимодействии Т- и В-клеток. Этот факт был доказан на экспериментальных моделях. Если летально облученной мыши ввести клетки селезенки от интактного донора, то последующая иммунизация приводит к сильному иммунному ответу. Если донору ввести Т- и В-лимфоциты, то при последующей иммунизации наблюдается активное антителообразование. Так как антитела вырабатывают В-лимфоциты, то Т-клеткам отводится вспомогательная роль и их называют Т-хелперами. Экспериментально было доказано, что В- и Т- клетки реагируют на разные детерминанты антигена. Как правило, В-лимфоциты распознают детерминанты гаптена, а Т-клетки - носителя. Вторичная реакция на гаптен возможна только в том случае, если после контакта с антигеном образуются клетки памяти, специфичные как к гаптену, так и к носителю. При этом оказалось, что к носителю специфичны Т-лимфоциты, т.е. Т-хелперные клетки. Форма проявления влияния Т-хелперов на В-лимфоциты зависит, вероятно, от антигена. По аналогии с АПК В-клетки также могут осуществлять презентацию антигена в комплексе с белками класса II МНС. Таким образом, В-лимфоцит активируется путем рецепторного и медиаторного контакта с АПФ. Кроме того, на В-клетку действуют растворимые медиаторы Т-хелперов, называемые в данном случае хелперными факторами. Т-индуктор активирует В-клетку, выделяя IL-2. Таким образом, IL-1, IL-2, хелперный фактор способствуют превращению В-лимфоцита в плазматическую клетку. Фаза индуктивного периода иначе называется фазой наведения информации на В-клетку и заканчивается антителообразованием. В-лимфоциты реагируют по разному на три различных типа антигена: 1. Тимус-независимый антиген 1-го типа. Некоторые антигены, такие как бактериальные липополисахариды, при достаточно высокой концентрации способны к поликлональной активации значительной части популяции В-лимфоцитов, т.е. для такой активации антигенная специфичность поверхностных рецепторов клетки роли не играет. При низкой концентрации такого антигена не происходит активации В-лимфоцитов и антиген будет пассивно накапливаться на их мембранах. 2. Тимус-независимые антигены 2-го типа. Некоторые линейные антигены, медленно распадающиеся в организме и имеющие часто повторяющиеся, определенным образом организованные детерминанты, например, полисахарид пневмококка, полипептиды D-аминокислот, тоже способны непосредственно без участия Т-клеток стимулировать В-лимфоциты. Тимус-независимые антигены обоих типов вызывают преимущественно синтез Ig M и индуцируемый ими иммунный ответ практически не сопровождается формированием клеток памяти. 3. Тимус-зависимые антигены. Многие антигены относятся к тимус-зависимым. Эти антигены в отсутствии Т-лимфоцитов лишены иммуногенности. Т-хелперы распознают одну из детерминант антигена (носителя) для того, чтобы помощь В-клеткам прореагировать на другую детерминанту (гаптен) того же антигена. Кроме того, Т-хелперы стимулируют В-клетки дополнительным гуморальным сигналом. Синтез Ig M во время иммунного ответа быстро достигает пика и затем быстро снижается. Образование Ig G - более длительный процесс, и антитела данного изотипа образуются в больших количествах, особенно при вторичном иммунном ответе. Т-зависимые антигены, вовлекая в иммунную реакцию Т-хелперы и образуемые ими растворимые факторы, приводят к более эффективной продукции антител, чем Т-независимые, и, кроме того, вызывают переключение класса антител и образование клеток памяти. В Т-клеточном иммунном ответе принимают участие 2 типа Т-эффекторов: Т-хелперы, продуцирующие разнообразные растворимые факторы (лимфокины), и цитотоксические Т-лимфоциты, которые сами по себе способны уничтожать другие клетки. 6. МЕХАНИЗМЫ РАЗВИТИЯ АЛЛЕРГИЧЕСКИХ РЕАКЦИЙ. А. РЕАКЦИИ ТИПА 1 (АНАФИЛАКТИЧЕСКИЕ, АТОПИЧЕСКИЕ). Считается, что хорошая сенсибилизация по I типу развивается при введении в организм очень маленьких доз аллергена. По данным Н.Д.Беклемишева эта доза колеблется в пределах 1 – 10 мкг белка. Дозы более высокие дают слабую сенсибилизацию. Они активируют Тх – 1, и реакция развивается по пути образования IgG и других иммуноглобулинов. В этом случае антигены представляются Ia-позитивными макрофагами. На малые дозы антигена макрофаги не реагируют, и он представляется В-лимфацитами Ех – 2. В ответ Ех – 2 увеличивают секрецию IL-4, который стимулирует образование этих же клеток и экспрессию рецепторов для IL-1 на их поверхности, что повышает чувствительность Ех – 2 к стимуляции. Кроме того, IL-4 совместно с IL-5 и IL-13 переключают В-лимфоциты на синтез IgE. Циркулирующий IgE метаболизируется довольно быстро. Его период полужизни составляет всего 2,4 суток. Фиксированный на клетках IgE сохраняется намного дольше (около 28 сут.). Клетки, продуцирующие IgE, относятся к долгоживущим. Полагают, что они находятся преимущественно в лимфоидной ткани слизистых оболочек и лимфатических узлах, которые дренируют эти области (пейеровы бляшки, мезентериальные и бронхиальные лимфатические узлы). Реакции I типа обусловлены взаимодействием антигена со специфическими Ig E и Ig G, связанными с соответствующими Fc-рецепторами базофилов и тучных клеток. В результате этого связывания происходит распад фосфадитилинозитола с образованием инозитолтрифосфата (ИФ3) и диацилглицерола, а также увеличивается концентрация свободного Са++ в цитоплазме. ИФ3 обуславливает мобилизацию внутриклеточных запасов Са++, а диацилглицерол активирует протеинкиназу С. Ферментативный каскад приводит к образованию агентов (в частности, лизофосфатидной кислоты), которые стимулируют слияние плазматических мембран и могут вызвать дегрануляцию тучных клеток и базофилов; кроме того, по циклооксигеназному и липоксигеназному путям образуются метаболиты арахидоновой кислоты. В конечном итоге из гранул высвобождаются преобразованные медиаторы (гистамин, гепарин, хемотаксический фактор эозинофилов и нейтрофилов, фактор агрегации тромбоцитов) и вновь синтезированные (лейкотриены, простагландины, тромбоксан). В нормальных условиях перечисленные медиаторы способствуют развитию защитной острой воспалительной реакции. Однако в определенных условиях, например при атопиях, происходит интенсивное высвобождение этих анафилатоксинов, и тогда в первую очередь наступает сужение просвета бронхов и расширение кровеносных сосудов, что представляет опасность для жизни. В патогенезе атопических реакций имеет значение: 1. Наследственно обусловленная способность к гиперпродукции иммуноглобулинов класса Е. 2. Дефектная функция макрофагов, не приводящая к значительному разрушению антигенов. 3. Выделение макрофагами факторов, стимулирующих продукцию иммуноглобулинов класса Е. 4. Дефицит Т-супрессоров. 5. Недостаточность продукции иммуноглобулинов класса А (секреторных антител). Примером этого механизма атопий может быть перенесенные частые ОРВИ в детстве. При этом выработка антител типа А уменьшается и происходит бесконтрольная наработка антител типа Е, что увеличивает вероятность возникновения атопий. 6. Отсутствие конкурентного торможения продукции антител типа Е высокими концентрациями антител типа А. Б. РЕАКЦИИ ТИПА II (ГУМОРАЛЬНЫЕ ЦИТОТОКСИЧЕСКИЕ ИММУННЫЕ РЕАКЦИИ). В основе аллергической реакции II типа лежит образование антител к первичным или вторичным структурам клеточной поверхности. Антигеном могут быть компоненты клеточной мембраны или неклеточные структуры. Как правило, речь идет о довольно сложных антигенах, имеющих многочисленные детерминанты одинаковой или разной специфичности. Для того чтобы включился этот механизм, клетки тканей должны приобрести аутоаллергенные свойства. Большую роль в этом процессе играет действие на клетки различных химических веществ, чаще лекарств, попадающих в организм. Они могут изменять антигенную структуру клеточной мембраны за счет: а) конформационных изменений, присущих клетке антигенов; б) повреждение мембраны и появление новых антигенов; в) образование комплексных аллергенов с мембраной, в которых химическое вещество играет роль гаптена. Повреждение может быть вызвано тремя путями:
Для клиники имеют особое значение четыре группы антигенов: 1. Клетки крови. 2. Клетки тканей (особенно при органоспецифических аутоиммунных заболеваниях). 3. Антигены вторично фиксированные на клеточной мембране. 4. Антигены в виде неклеточных структурных белков (например, к миелину). Связывание антител с антигеном, экспонированным на поверхности клетки, может вызвать повреждение активированными макрофагами. Это происходит в результате снижения поверхностного заряда клетки, связывание фагоцитов с Fc-фрагментами антител или с присоединением к клетки С3 компонента комплемента. Антитела в этих реакциях представлены Ig G и I M. Непосредственное повреждение мембран вызывают компоненты С8 и С9, образующиеся в результате активации комплемента. Для лизиса одного эритроцита достаточно образование одного мембраноатакующего комплекса (МАК). Другие типы клеток, по-видимому, имеют механизмы репарации мембран, и для преодоления защитной реакции требуется образование нескольких мембраноатакующих комплексов. Оказалось, что существует еще один цитотоксический механизм: клетки-мишени, нагруженные небольшим количеством Ig G, могут "неспецифически" уничтожаться лимфоретикулярными клетками. Следует отметить, что этот механизм, получивший название "АНТИТЕЛОЗАВИСИМАЯ КЛЕТОЧНАЯ ЦИТОТОКСИЧНОСТЬ", лежит в основе функционирования как фагоцитирующих, так и нефагоцитирующих миелоидных клеток (лейкоциты), а также гранулярных лимфоцитов, несущих Fc-рецепторы (так называемые К-клетки). Последние почти наверняка идентичны нормальным киллерам. В. РЕАКЦИИ ТИПА III (ОБРАЗОВАНИЕ ИММУННЫХ КОМПЛЕКСОВ). Во многих случаях организм длительное время контактирует с избытком антигена. Это - персистентная инфекция, аутоиммунореактивность к компонентам собственного организма или повторяющийся контакт с внешним антигеном. В этих случаях взаимодействие между антигеном и антителом (Ig G) может привести к образованию нерастворимых иммунных комплексов, которые способны откладываться в определенных тканях и вызывать острые воспалительные реакции. Если такими комплексами связываются компоненты комплемента, то образуются продукты расщепления С3 и С5, представляющие собой анафилатоксины. Данные медиаторы приводят к высвобождению биологически активных веществ (БАВ) тучных клеток, которые повышают проницаемость сосудов и привлекают в зону воспаления полиморфноядерные лейкоциты, фагоцитирующие иммунные комплексы. Это в свою очередь приводит к выбросу содержимого лейкоцитарных гранул. Протеолитические ферменты, ферменты, образующие кинины, и катионные белки, высвобождающиеся из гранул, вызывают локальное повреждение тканей и стимулируют развитие воспаления. Дополнительное повреждение происходит в результате так называемого реактивного лизиса, когда активированные компоненты С5 - С7 случайно присоединяются к поверхности соседней клетки, а затем связывают компоненты С8 и С9. В некоторых случаях происходит и агрегация тромбоцитов с двумя важными последствиями: 1. Тромбоциты служат дополнительным источником вазоактивных аминов. 2. Тромбоциты формируют микротромб, что приводит к развитию локальной ишемии. Нерастворимые иммунные комплексы, поглощенные макрофагами, долго не перевариваются и служат причиной активации этих клеток. Эффект, вызываемый образованием иммунных комплексов зависит не только от абсолютного количества антигена и антител, определяющего интенсивность реакции, но и от их взаимного соотношения. Последнее обуславливает структуру комплексов и их распределение в организме. При избытке антител или небольшом избытке антигена комплексы быстро преципитируют и обычно локализуются в месте проникновения антигена в организм. По мере увеличения избытка антигена образуются растворимые комплексы. Циркулирующие иммунные комплексы (ЦИК) становятся патогенными только при определенных условиях:
а) освобождением вазоактивных аминов из тромбоцитов, базофилов и тучных клеток под влиянием анафилотоксина; б) действием выделяющихся из фагоцитов лизосомальных ферментов;
Судьба растворимых иммунных комплексов зависит прежде всего от активации комплемента по классическому пути. Фиксация компонентов комплемента подавляет преципитацию иммунных комплексов, поскольку ковалентное связывание С3b предотвращает взаимодействие Fc - Fc, необходимое для образования крупных нерастворимых агрегатов. Небольшие комплексы, связавшие С3b, прикрепляются к рецепторам комплемента, расположенным на эритроцитах, и переносятся к макрофагам печени, где в норме происходит их инактивация. При недостаточности компонентов комплемента комплексы накапливаются в плазме крови и могут откладываться в почках, сосудах и коже. Г. РЕАКЦИЯ ТИПА IY (ПАТОЛОГИЧЕСКИЕ ИММУННЫЕ РЕАКЦИИ, ОБУСЛОВЛЕННЫЕ КЛЕТКАМИ). Эта форма гиперчувствительности наблюдается при многих аллергических реакциях на бактерии, вирусы и грибы, а также при контактном дерматите, возникающем в результате сенсибилизации отдельными простыми химическими соединениями, и при отторжении трансплантированных тканей. Видимо, наиболее известный пример - это реакция Манту, развивающаяся при внутрикожном введении туберкулина человеку, у которого предшествующая микобактериальная инфекция индуцировала специфическую чувствительность. Гиперчувствительность замедленного типа - это зависимая от Т-клеток иммунная реакция, проявляющаяся в виде воспалительной реакции в месте попадания в организм антигена - обычно в коже. Максимальная интенсивность реакции достигается через 24-48 часов после инициации. По гистологическим данным эта реакция начинается околососудистой мононуклеарной инфильтрацией, которая постепенно усиливается и дополняется полиморфноядерной. Затем полиморфноядерные лейкоциты покидают место реакции, оставляя инфильтрат, состоящий преимущественно из лимфоцитов и клеток моноцитарно-макрофагального ряда. Реакции замедленного типа нельзя перенести от сенсибилизированного к несенсибилизированному организму с помощью сывороточных антител. Для этого необходим перенос лимфоидных клеток, а именно Т-лимфоцитов. У человека перенос достигается введением живых лейкоцитов, а также, что особенно интересно, низкомолекулярным материалом, экстрагированным из этих клеток (фактор переноса Лоуренса). Природа этого вещества до сих пор неизвестна.
Следует еще раз отметить, что гиперчувствительность и связанные с нею нарушения - это слишком интенсивное взаимодействие между антигеном и нормальными клеточными механизмами иммунитета. Примированные Т-клетки памяти распознают антиген в комплексе с продуктами МНС класса II на поверхности макрофага, что стимулирует их бласттрансформацию и пролиферацию. Активированные Т-клетки выделяют целый ряд растворимых факторов, которые представляют собой медиаторы клеточного иммунитета, в частности факторы привлекающие и активирующие макрофаги. Кроме того, под действием этих факторов происходит дифференцировка предшественников цитотоксических Т-лимфоцитов в киллерные клетки, что приводит к повреждению тканей. При аллергических реакциях замедленного типа повреждающее действие может развиваться несколькими путями. Основными являются следующие:
Осуществляемое Т-клетками разрушение ткани не зависит ни от антител, ни от системы комплемента. Рассмотрим три последовательные стадии литического цикла: 1) межклеточное взаимодействие; 2) события, приводящие к нанесению летального повреждения в мембране клетки-мишени, называемые иногда программированием лизиса; 3) разрыв мембраны и выход содержимого цитоплазмы. |