Общая микробиология
 Скачать 1.12 Mb. Скачать 1.12 Mb.
|
|
отдел Gracilicutes, семействоEnterobacteriaceae, родSalmonella, виды: S. typhimurium, S. enteritidis, S. choleraesius, S. heidelberg, S. anatum, S. Derby. Серологическая классификация: по наличию жгутикового и соматического антигена: Группа А- S. paratyphi A. ГруппаВ- S. sсhottmuelleri, S. Typhimurium, S. Derby, S. Heidelberg, S. abortus-eguina и тд Группа С (1,2)- S. Hirschfeldii, S. cholerae-suis, S. Typhisuis, S. Thomson, S. Duesseldorf и тд Группа D (1)- S. Typhi, S. Enteritidis, S. Dublin, S. Rostoc, S. Moscow и тд. Группа Е (1,3)- S. London, S. anatum, S. Harrisonburgитд. Дифференциация сальмонелл внутри серогрупп проводится по антигенной специфичности Н-антигенов, 1-ю фазу которых обозначают строчными буквами латинского алфавита (а, b, c, d, и т.д.), 2-ю фазу - обычно арабскими цифрами. Наиболее опасными источниками пищевых токсикоинфекций являются животные, страдающие вторичным сальмонеллезом и энтеритом крупного рогатого скота. Большую роль в эпидемиологии сальмонеллезов играют водоплавающие птицы и их яйца, а также куры, их яйца и другие птицепродукты. Сальмонеллы могут попасть в яйцо непосредственно во время его развития, но могут легко проникнуть и через неповрежденную скорлупу. Вспышки токсикоинфекций чаще всего связаны с употреблением мяса, инфицированного сальмонеллами, - до 70-75 %, в том числе до 30 % мяса скота вынужденного забоя. Вынужденному забою часто подвергают животных, находящихся в агональном состоянии. У ослабленных животных сальмонеллы легко проникают из кишечника в кровь, а через нее - в мышцы, обусловливая прижизненное инфицирование мяса. На долю яиц и птицепродуктов приходится более 10 %, на долю молока и молочных продуктов - около 10 %, и на долю рыбопродуктов - около 3-5 % всех вспышек сальмонеллезов. Современная эпидемиология сальмонеллезов характеризуется постоянным ростом заболеваемости людей и животных и увеличением числа серотипов сальмонелл, вызывающих эти заболевания. Одной из основных причин роста заболеваемости сальмонеллезом является инфицирование пищевых продуктов при их производстве в результате широкого распространения сальмонелл на объектах внешней среды и на обрабатывающих предприятиях, куда поступают животные, у которых сальмонеллез протекает в скрытой форме. Одной из главных причин широкой циркуляции сальмонелл среди животных является применение корма, содержащего переработанные побочные продукты животного происхождения и очень часто зараженного сальмонеллами. Симптомы сальмонеллеза Сальмонеллез может протекать с различной клинической картиной: в виде пищевой токсикоинфекции, сальмонеллезной диареи и генерализованной (тифозной) формы, - все зависит от величины заражающей дозы, степени вирулентности возбудителей и иммунного статуса организма. Массивное обсеменение сальмонеллами пищевого продукта обусловливает пищевую токсикоинфекцию, при которой основные симптомы связаны с поступлением возбудителя в кровь в большом количестве, его распадом и высвобождением эндотоксина. В основе сальмонеллезной диареи лежит колонизация сальмонеллами энтероцитов. После прикрепления к гликокаликсу тонкого кишечника сальмонеллы внедряются между ворсинками и, прикрепляясь к плазмолемме энтероцитов, колонизируют ее, повреждают микроворсинки, вызывают слущивание энтероцитов и умеренное воспаление слизистой оболочки. Освобождающийся энтеротоксин вызывает диарею, а цитотоксин - гибель клеток. Сальмонеллы размножаются на плазмолемме, но не в энтероцитах, а происходит их инвазия через эпителий в подлежащие ткани слизистой оболочки, они транспортируются через нее в макрофагах, поступают в лимфу и кровь, вызывая бактериемию и генерализацию инфекционного процесса. Постинфекционный иммунитет Постинфекционый иммунитет изучен недостаточно. Судя по тому, что сальмонеллезом болеют главным образом дети, постинфекционный иммунитет достаточно напряженный, но является, по-видимому, типоспецифическим. Лабораторная диагностика сальмонеллеза Материал - рвотные массы, промывные воды желудка, фекалии, остатки продуктов - возможных источников токсикоинфекции. Основной метод – бактериологический. Сальмонеллы хорошо растут на средах с желчью. Для дифференциальной диагностики используются дифференциально-диагностические среды - среда Эндо, висмут-сульфитагар, на котором колонии сальмонелл приобретают черный (некоторые - зеленоватый) цвет(S. arizonae и S. diarizonae ферментируют лактозу). Для посева крови использовать среду Рапопорт; Фаготипирование- использование для предварительной идентификации колоний 01-сальмонеллезного фага, к которому чувствительны до 98 % сальмонелл; Определение серовара с помощью реакции аглютинации ( с 2-мя монодиагностикумами - О и Н антигены). Надо иметь в виду, что в начале заболевания формируются антитела к О-антигену, а в конце - к Н-антигену. Выявление одного и того же серовара у больного и из продуктов позволяет сделать заключение об источнике заражения. Для быстрого обнаружения сальмонелл могут быть использованы поливалентные иммунофлуоресцентные сыворотки. Для выявления антител в сыворотке крови больных и переболевших используется РПГА с применением поливалентных эритроцитарных диагностикумов, содержащих полисахаридные антигены серогрупп А, В, С, D и Е. Лечение и профилактика: Используются (при генерализованных формах сальмонеллеза) антибактериальные препараты для Гр (-) микроорганизмов - производные пенициллина, фторхинолоны, нитрофурановые препараты, полимиксин. Также можно использовать сальмонелезные бактериофаги. Иногда вводят иммуноглобулины в молоко, так как сальмонеллезы часто встречаются у маленький детей. Напряженного иммунитета не формируется. Возможно бактерионосительство и повторные заболевания. Профилактика - комплекс ветеринарно-санитарных, медико-санитарных и противоэпидемических мероприятий. Не использовать в пищу недостаточно термически обработанные мясные продукты, рыбу, яйца, мыть овощи и фрукты. Специфической профилактики нет. 108. Шигеллы, таксономия, международная классификация, свойства. Характеристика токсинов. Эпидемиология. Патогенез острой и хронической дизентерии. Особенности современной дизентерии. Принципы и методы микробиологической диагностики. Специфические лечебно-профилактические препараты. Род Shigella включает 4 вида: S. dysenteriae — 12 сероваров, S.flexneri — 9 сероваров, S. boydii — 18 сероваров, S. sonnei — 1 серовар. Морфология. Шигеллы представлены неподвижными палочками. Спор и капсул не образуют. Культуральные свойства. Хорошо культивируются на простых питательных средах. На плотных средах образуют мелкие гладкие, блестящие, полупрозрачные колонии; на жидких — диффузное помутнение. Жидкой средой обогащения является селенитовый бульон. У S. sonnei отмечена при росте на плотных средах SR-диссоциация. Биохимическая активность: слабая; отсутствие газообразования при ферментации глюкозы, отсутствие продукции сероводорода, отсутствие ферментации лактозы. S.sonnei способен ферментировать лактозу медленно, в течение 72 ч. Является наиболее биохимически активным видом; по биохимической активности подразделяется на хемовары. S. dysenteriae не ферментирует маннит. Резистентность. В зависимости от температуры, влажности, PH, и вида возбудителей выживаемость шигелл во внешней среде колеблется от нескольких дней до нескольких месяцев. Наиболее неустойчив во внешней среде вид S. dysenteriae. Шигеллы переносят высушивание, низкие температуры, быстро погибают при нагревании. Благоприятная среда – пищевые продукты. S. sonnei в молоке способны не только длительно переживать, но и размножаться. У S. dysenteriae отмечен переход в некультивируемую форму. Антигенная структура. Соматический О-антиген, в зависимости от строения которого происходит их подразделение на серовары, aS. flexneri внутри сероваров подразделяется на подсеровары. S. sonnei обладает антигеном 1-й фазы, который является К-антигеном. Факторы патогенности. Способность вызывать инвазию с последующим межклеточным распространением и размножением в эпителии слизистой толстого кишечника. Функционирование крупной плазмиды инвазии, которая имеется у всех 4 видов шигелл. Плазмида инвазии детерминирует синтез белков, входящих в состав наружной мембраны, которые обеспечивают процесс инвазии слизистой. Продуцируют шига и шигаподобные белковые токсины. Эндотоксин защищает шигеллы от действия низких значений рН и желчи. Эпидемиология: Заболевания - шигеллезы, антропонозы с фекально-оральным механизмом передачи. Заболевание, вызываемое S. dysenteriae, имеет контактно-бытовой путь передачи. S. flexneri — водный, aS. sonnei — алиментарный. Патогенез и клиника: Инфекционные заболевания, характеризующиеся поражением толстого кишечника, с развитием колита и интоксикацией. Шигеллы взаимодействуют с эпителием слизистой толстой кишки. Прикрепляясь инвазинами к М-клеткам, шигеллы поглощаются макрофагами. Взаимодействие шигелл с макрофагами приводит к их гибели, следствием чего является выделение ИЛ-1, который инициирует воспаление в подслизистой. При гибели шигелл происходит выделение шига токсинов, действие которых приводит к появлению крови в испражнениях. Иммунитет. Секреторные IgA, предотвращающие адгезию, и цитотоксическая антителозависимая активность лимфоцитов. Микробиологическая диагностика. Бактериологический: материалом для исследования - испражнения. Для посева отбираются гнойно-кровяные образования из кала, которые при диагностике заболевания высеваются на лактозосодержащие дифференциальные питательные плотные среды. В случае выявления бактерионосителей посев испражнений проводится в селенитовый бульон с выделением возбудителя на плотных лактозосодержащихдифференциальных питательных средах. Среди выросших на этих средах отбирают лактозонегативные колонии, которые идентифицируют до вида и серовара, а выделенные культуры S. flexneri — до подсероваров, S. sonnei — до хемоваров. В качестве вспомогательного используют серологический метод с постановкой РНГА. Лечение и профилактика: Для лечения - бактериофаг орального применения, антибиотики после определения антибиотикограммы; в случае возникновения дисбактериоза — препараты пробиотиков для коррекции микрофлоры. Неспецифическая профилактика сводится к соблюдению санитарно-гигиенических правил приготовления, хранения и реализации пищевых продуктов, при водоснабжении, соблюдению правил личной гигиены и др. Многочисленная практика разработки и применения вакцинопрофилактики свидетельствует о неэффективности метода специфической профилактики шигеллезов. Особенностью современного течения дизентерии является относительно большой удельный вес легких и субклинических форм, длительное устойчивое бактерионосительство, большая резистентность к этиотропной терапии, а также редкость хронических форм. 109. Возбудители кишечного иерсиниоза и псевдотуберкулеза. Таксономия. Свойства. Культуральные особенности. Вызываемые заболевания. Эпидемиология. Принципы и методы лабораторной диагностики. Псевдотуберкулез — инфекционное за болевание, характеризующееся полиморфностью клинической картины, затяжным течением, аллергизацией организма. Возбудитель псевдотуберкулеза Y. Pseudotuberculosis относится к семейству Enterobacteriaceae, роду Yersinia Морфология. Палочка, с биполярным окрашиванием, размером 0,8-^2х0,4+0,6 мкм, подвижная, т. е. имеет жгутики, при температурах ниже 37 °С. Образует капсулу. Культуральные свойства. Хорошо растет на простых питательных средах. Оптимум размножения 22-28 °С. При температурах ниже 37 °С на плотных средах образует колонии в S-форме. При температуре 37 °С — колонии в R-форме. На жидких средах образует пленку. Физиология. Биохимически активен. Основные биохимические признаки, необходимые для идентифиации; — продукция уреазы, — ферментация рамнозы, — отсутствие ферментации сахарозы, — отсутствие продукции индола, —отрицательная реакция Фогеса—Проскауэра. Биохимически внутри рода однороден. Возбудитель устойчив во внешней среде: в воде при комнатной температуре выживает до 1,5 месяцев, при +4 °С — до полугода; в овощах (капуста, морковь, лук) и фруктах выживает несколько месяцев. Малоустойчив к нагреванию при 60°, при кипячении, к УФ-свету, к дезинфектантам. Антигенная структура. Обладает 0-антигеном, на основании строения которого подразделяет ся на 8 сероваров, а также Н-антигеном. Эпидемиология. Резервуаром возбудителя в природе являются многие виды млекопитающих (рогатый скот, кошки) и птиц, грызуны (мыши, крысы), выделяющие микроб с испражнениями, а также вода, почва, в которых происходит накапливание микроба. Человек заражается водным и алиментарным путями. Основными факторами передачи являются вода и овощи. Овощи заражаются Y.pseudotuberculosis в результате их загрязнения в хранилищах испражнениями инфицированных возбудителем мышей, а также непосредственно из почвы и воды. Заражение человека от больного или носителя не происходит. Естественная восприимчивость людей к возбудителю высокая. Болезнь распространена повсеместно, возникает в виде спорадических и эпидемических вспышек, имеет сезонность (февраль-март). В районе Дальнего Востока РФ заболевание протекает в виде эпидемических вспышек в генерализованной форме под названием Дальневосточная скарлатиноподобная лихорадка. Патогенез и клиника заболевания. Инкубционный период 3—10 дней. Заболевание протекает в виде локальной и генерализо ванной форм. Начало острое или подострое, сопровождается лихорадкой. Инвазировав слизистую кишечника трансцитозом через М-клетки, выделяя при этом цитотоксин, Y. pseudotuberculosis вследствие незавершенности фагоцитоза попадает в мезентериальные лимфатические узлы, вызывая мезентериальный лимфаденит. Следствием развития мезентериального лимфаденита являются боли в эпигастральной области, симптомы раздражения брюшины, которые имитируют симптомы острого аппендицита. В случае прорыва лимфатического барьера наступает бактериемия, в результате которой микроб разносится по организму, вызывая образование гранулем и микроабсцессов в макрофагальных элементах печени, селезенки, легких, суставов. При этом происходит аллергизация организма. На 1-6-й день по является розеолезная сыпь. Возможен летальный исход. Иммунитет. Непрочный, нестерильный. Антитела не обладают протективной активнотью. В организме происходит развитие ГЗТ. Микробиологическая диагностика. Применяют бактериологический и серологический методы исследования. Материалами для исследования при бактериологическом методе являются испражнения, кровь, желчь, сустав ная жидкость, бронхиальная жидкость. Мате риал помешают в фосфатный буфер и подвергают холодовому обогащению при температуре 4 “С в течение 21 дня, периодически делая высев на плотные среды (Эндо, Серова). Серологическое исследование проводят на 2-й неделе и 3-5-й неделе постановкой РИГА и ИФА. Профилактика и лечение. Специфическая профилактика не разработана. Лечение — этиотропная антибиотикотерапия. Неспецифическая профилактика включает: постоянный санитарный контроль за водоснабжением, технологическим режимом обработки и хранения пищевых продуктов, борьбу с грызунами. Кишечный иерсиниоз — инфекционное за болевание с поражением тонкого и толстого кишечника и развитием мезентериального лимфаденита. Этиология. Возбудителем кишечного иерсиниоза является Y. Enterocolitica, которая относится к отделу Gracilicutes, семейству Enterobacteriaceae, роду Yersinia. Морфология. Грамотрицательные палочки, размером 1,8-2,7х0,7-0,9 мкм, подвижные, капсулу не образуют. Физиология. Хорошо растут на обычных питательных средах. Оптимум роста 22-28 °С. Обладают выраженной биохимической активностью. Внутри вида по спектру биохимической активности — индолообразованию, утилизации эскулина, реакции Фогеса-Проскауэра — подразделяется на 5 хемоваров. Заболевание чаше вызывают биовары 2.3.4. Основные биохимические признаки, необходимые для идентификации; —расщепление мочевины, —ферментация сахарозы, —отсутствие ферментации рамнозы, —продукция орнитиндекарбоксилазы. Антигенная структура. Обладает О- и Н-антигенами. По строению О-антигена подразделяется более чем на 30 сероваров. Наиболее часто заболевание у человека вызывают серо- вары 03, 05, 09, 08. Патогенность. Помимо общих для энтеропатогенных иерсиний факторов патогенности, Y. enterocolitica обладает термостабильным энтеротоксином, гомологичным термостабильному энтеротоксину ЭТКП. Эпидемиология. Кишечный иерсиниоз вы является во всех странах, возникает в виде групповых, семейных, внутрибольничных вспышек. Резервуаром возбудителя в природе являются почва, вода, инфицированные через них растения. Инфицированные вода и растения способствуют распространению инфекции среди сельскохозяйственных животных. Резервуаром и источником инфекции могут быть крупный рогатый скот, свиньи, собаки, кошки, птицы. Основные пути пере дачи —водный и алиментарный, через воду, молоко, овощи. В отличие от Y. pseudotubeculosis, Y. enterocolitica может передаваться от человека к человеку, являясь даже причиной внутрибольничной инфекции. Патогенез и клиническая картина. Начальные этапы патогенеза аналогичны таковым при псевдотуберкулезе. Инвазировав трансцитоом через М-клетки слизистую подвздошной кишки, Y. entemcolitica внедряется в ее лимфоидные образования, из которых микроб попадает в мезентериальные лимфоузлы, вызывая в них развитие аденита. Действие цитотоксина и энтеротоксина вызывает воспалительный процесс в стенке кишечника и развитие диареи. При прорыве лимфатического барьера кишечника развивается бактериемия, следствием которой является развитие генерализованной формы инфекции, которая протекает с поражением селезенки, развитием полиаденита, полиартрита, менингита, с аллергизацией организма. У иммунодефицитных лиц может развиться сепсис. Инкубационный период составляет в среднем 3-7 суток. Начало острое: с лихорадкой, интоксикацией, болями в животе, расстройствами стула, появлением сыпи на коже. Различают гастроинтестинальную, абдоминальную, генерализованную и вторично-очаговую формы болезни. Болезнь может протекать хронически до 1,5-2 лет. Микробиологическая диагностика. Используют бактериологический и серологический методы исследования. Материалом для бактериологического метода исследования служат испражнения, ликвор, кровь, моча, иногда червеобразный отросток. Как и при диагностике псевдотуберкулеза, материал для исследования помещают в фосфатный буфер и подвергают холодовому обогащению. Серологическая диагностика проводится постановкой РИГА, с диагностическим титром 1:160. Важное диагностическое значение имеет наблюдение за нарастанием титра антител в динамике. Профилактика и лечение. Специфическая профилактика не разработана. Лечение — этиотропная антибиотикотерапия. Неспецифическая профилактика аналогична таковой при псевдотуберкулезе. 110. Возбудитель чумы, таксономия. Свойства. Культуральные особенности. Дифференциация возбудителей чумы, кишечного иерсиниоза и псевдотуберкулеза. Эпидемиология. Клинические формы чумы. Принципы и методы микробиологической диагностики. Препараты для специфического лечения и профилактики. Y.pestis вызывает чуму; отдел Gracilicutes, семейство Enterobacteriaceae, род Yersinia. Возбудитель – Yersiniapestis Морфология. Y. pestis, представляет собой неподвижную палочку овоидной формы, размером 1,5x0,7 мкм, с биполярным окрашиванием анилиновыми красителями. Образует нежную капсулу. Культуральные свойства. Факультативный анаэроб. Растет на простых питательных средах. Оптимальная температура роста 28 °С, но может расти в широком диапазоне температур от 2 до 40 °С. Для ускорения роста в питательные среды добавляют стимуляторы, сульфит натрия и гемолизированную кровь. При росте на плотных питательных средах через 8—12ч появляются колонии в виде «битого стекла». Через 18—20 ч инкубации вирулентные бактерии образуют колонии в R-форме, которые имеют форму «кружевных платочков»: со светлым центром и фестончатыми краями. Менее вирулентные бактерии образуют колонии в S-форме. На жидких средах бактерии растут в виде пленки, от которой спускаются нити, напоминающие пещерные сталактиты; на дне образуется хлопьевидный осадок. Биохимическая активность достаточно высокая. Синтезирует плазмокоагулазу, фибринолизин, гемолизин, лецитиназу, РНКазу. Основные Биохимические свойства, необходимые для идентификации: — не разжижает желатину, не расщепляет мочевину, — не ферментирует рамнозу и сахарозу, — ферментирует декстрин. По отношению к утилизации глицерина подразделяется на хемовары. Антигенная структура. Обладает комплексом антигенов, многие из которых относятся к факторам патогенности. Имеет термостабильные 0-антигены и термолабильные капсульные антигены. Протективной активностью обладает F1-антиген. Имеет антигены, общие с антигенами эритроцитов 0-группы крови человека. Резистентность. Микроб обладает психрофильностью. При понижении температуры увеличиваются сроки выживания бактерий. При температуре —22 °С бактерии сохраняют жизнеспособность 4 месяца, в замороженных трупах и блохах — до 1 года. При нагревании до50°Сгибнетвтечение10мин,до100°С-в течение 1 мин. Чувствителен к сулеме в концентрации 0,1 %, к 3-5% растворам лизола и фенола, ультрафиолетовому облучению. Патогенность. Y. pestis обладает многочисленными факторами патогенности, генетическая детерминация которых осуществляет ся как хромосомой, так и тремя плазмидами; pPst (6 мДа), pCad, (45 мДа), pFra (60 мДа). Синтез ферментов патогенности: фибринолизина и плазмокоагулазы, а также пестицина детерминирует pPst плазмида; синтез Р1-антигена — гликопротеидной природы, который продуцируется при температуре 37 °С и препятствует поглощению микроба фагоцитами, детерминируется pFra плазмидой; этой же плазмидой детерминируется синтезР2-фракции, «мышиного токсина», функция которого окончательно не ясна. Известно, что он обладает способностью блокировать адренергические рецепторы и ингибировать дыхательную активность митохондрий, понижая активность НАДФ-редуктазы. Синтез V- и W-антигенов (V-антиген является пептидом, а W-антиген — внеклеточным липопротеином), обеспечивающих способность бактерий сохраняться в фагоцитах, детерминирует pCad плазмида. К факторам патогенности, обеспечивающим антифагоцитарную активность микроба, относят также внеклеточную аденилатциклазу и цитохромоксидазу, а также пигмент, связывающий гемин и способность к синтезу эндогенных пуринов. Эпидемиология. Резервуаром возбудителя природной чумы являются дикие, синантропные и домашние животные (всего около 300видов). Основными носителями являются грызуны (сурки, суслики, полевки, песчанки, крысы, зайцы и др.). У грызунов, впадающих зимой в спячку, чума протекает в хронической латентной форме. Эти животные являются источником инфекции в межэпидемическийпериод. Вторичные очаги, связанные с деятельностью человека, обнаруживаются в географических зонах между 35° северной широты и 35°южной широты. В них источниками и хранителями возбудителя служат домовые виды крыс и мышей, от них заражаются некоторые виды домашних животных, в частности верблюды и, возможно, кошки. Специфическими переносчиками возбудителя в обоих типах очагов служат блохи. В инфицированной блохе возбудитель размножается в преджелудке, а при кровососаниичеловека попадает в ток его крови. Человек заражается в очаге трансмиссивно — через укусы инфицированных блох, контактным путем при контакте с инфицированными животными (разделка шкур и мяса зараженных животных) и алиментарным путем — при употреблении в пишу продуктов, обсемененных чумными микробами. От больных легочной формой чумы происходит аэрогенноезаражение. Восприимчивость людей к чуме очень высокая Патогенез и клиника заболевания. Зависят от пути заражения. При контактном пути, проникая через неповрежденную кожу, и трансмиссивном пути заражения возбудитель с током лимфы заносится в регионарные лимфатические узлы, где происходит его размножение. Вследствие незавершенности фагоцитоза в лимфатических узлах развивается серозно-геморрагическое воспаление, сразвитием бубона, т. е. увеличенного лимфатического узла, иногда достигающего размеров куриного яйца. Так возникает первичная бубонная форма. Утрата лимфатическим уз лом барьерной функции приводит к генерализации процесса. Возбудитель разносится гематогенно в отдаленные лимфатические узлы, где формируются вторичные бубоны,а также в органы, где развиваются септико- пиемические очаги. Гематогенный занос чумных микробов в легкие приводит к развитию вторично-легочной формы заболевания, которая характеризуется развитием пневмонии с обильным серозно-геморрагическим экссудатом, содержащим большое число микробов. При воздушно-капельном заражении возникает первично-легочная форма, а при контактном и алиментарном путях заражения развиваются соответственно кожная и, в редких случаях, кишечная формы заболевания. Инкубационный период — от нескольких часов до 2-6 дней, у привитых — до 10 дней. Заболевание начинается остро: температура тела повышается до 39 °С и выше, возникает озноб, наблюдаются явления интоксикации, которая проявляется резкой головной болью, разбитостью, мышечными болями, помрачением сознания. Больной возбужден. При бубонной форме на 1—2-й день болезни появляется лимфаденит (чумной бубон). Различают несколько клинических форм чумы: кожную, бубонную, первично- и вторично-септическую, первично- и вторично-легочную формы. Летальность до применения антибиотиков при диссеминированных формах чумы достигла 100 %, при локальных формах —до 70 %; при антибиотикотерапии достигает 10 %. Иммунитет. Различной длительности и напряженности. Отмечены случаи повторных заболеваний. Протективная активность обеспечивается главным образом клеточным иммунным ответом, реализуюшимся через иммунные макрофаги. Микробиологическая диагаостика. Используют бактериоскопический, бактериологический, биологический и серологический методы исследования, которые проводят в специальных лабораториях, работающих в соответствии с инструкциями о режиме работы противочумных учреждений. Материалами для исследования являются: пунктаты бубонов мокрота, отделяемое карбункулов и язв, кровь, моча, рвотные массы, трупный материал. Материал засевают на питательные среды (мясопептонный агар — МПА, бульон Хоттингера, элективные среды), и ставят биопробу на морских свинках и белых мышах. В качестве экспресс- диагностики используют РИФ, позволяющуюпоставить предварительный диагноз уже через 2 ч. Серологическое исследование проводится постановкой РИГА, ИФА, PH антител. Профилактика и лечение. Больные чумой подлежат строгой изоляции и обязательной госпитализации. Для лечения используют этиотропную антибиотикотерапию. Прогноз неблагоприятный, так как при генерализованных формах болезни летальность может достигать 100 %. Специфическая профилактика осуществляется живой вакциной из штамма EV. После вакцинации развивается иммунитет продолжительностью до 6 месяцев. Вакцина вводится однократно накожно или подкожно с помощью безыгольного инъектора; разработана таблетированная живая вакцина из штамма EV для перорального применения (А. А. Воробьев, Е. М. Земсков), а также аэрозольная вакцина (В. А. Лебединский и соавт.). Большое значение имеет не специфическая профилактика, которая включает: предупреждение заболевания людей и возникновения эпизоотий в природных очагах, предупреждение завоза чумы на территорию страны, которое осуществляется согласно специальным «Международным санитарным правилам»; предупреждение заражения лиц, работающих с заразным Y. pestis материалом, осуществляемое регламентом работы противочумных учреждений. Вся работа с заразным У. pestis материалом и в госпиталях для больных чумой должна проводиться в специальных защитных противочумных костюмах с соблюден ем строгого порядка их надевания и снятия. В случае появления больного чумой проводятся карантинные мероприятия. 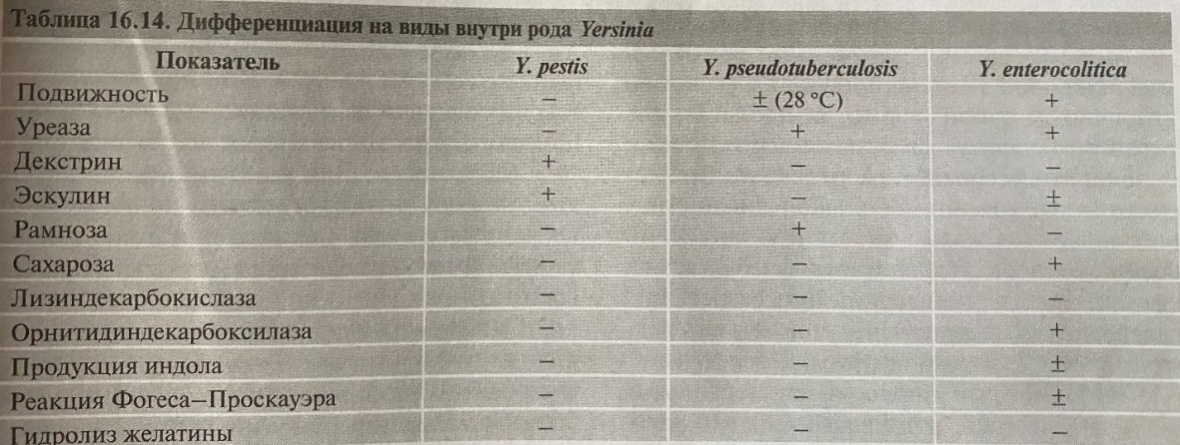 111. Возбудитель холеры, таксономия, свойства, особенности культивирования. Характеристика токсинов. Классификация вибрионов по Хейбергу и антигенной структуре. Дифференциация биоваров. Эпидемиология. Основной метод и экспресс- методы лабораторной диагностики. Специфические профилактические препараты. Возбудитель – Vibriocholerae, серогрупп О1 и О139, характеризуется токсическим поражением тонкого кишечника, нарушением водно-солевого баланса. Морфологические и культуральные свойства. Вибрион имеет один полярно расположенный жгутик. Под действием пени- циллина образуются L-формы. Грамотрицательны, спор не образуют. Факультативный анаэроб. Не требователен к питательным средам. Температурный оптимум 37C. На плотных средах вибрионы образуют мелкие круглые прозрачные S-колонии с ровными краями. На скошенном агаре образуется желтоватый налет. В непрозрачных R-колониях бактерии становятся устойчивыми к действию бактериофагов, антибиотиков и не агглютинируются О-сыворотками. Биохимические свойства. Активны: сбраживают до кислоты глюкозу, мальтозу, сахарозу, маннит, лактозу, крахмал. Все вибрионы делятся на шесть групп по отношению к трем сахарам (манноза, сахароза, арабиноза). Первую группу, к которой относятся истинные возбудители холеры, составляют вибрионы, разлагающие маннозу и сахарозу и не разлагающие арабинозу: разлагают белки до аммиака и индола. H2S не образуют. По Хейбергу, все вибрионы делятся на 6 групп по отношению к трем сахарам – манноза, сахароза, арабиноза. Первую группу, к которой относятся истинные возбудители холеры, составляют вибрионы, разлагающие маннозу и сахарозу и не разлагающие арабинозу. Остальные пять групп объединяют нехолерные вибрионы. Антигенная структура. Термостабильный О-антиген и термолабильный Н-антиген. Н-АГ являются общими для большой груп- пы вибрионов. Возбудители классической холеры и холеры Эль-Тор объединяются в серогруппу 01. Антигены серогруппы 01 включают в различных сочетаниях А-, В- и С-субъединицы. Сочетание субъединиц АВ называется сероваром Огава, сочетание АС — сероваром Инаба, сочетание ABC — Гикошима. R-формы колоний утрачивают О-АГ. Резистентность. Вибрионы плохо переносят высушивание. Долго сохраняются в водоемах, пищевых продуктах.. Биовар Эль- Тор более устойчив в окружающей среде, чем классический вибрион. Эпидемиология. Острая кишечная инфекция с фекально-оральным механизмом передачи. Путь передачи - водный, пищевой. Источник инфекции — больной человек или вибрионоситель. Факторы патогенности. Пили адгезии; фермент муциназа, разжижающий слизь и обеспечивающий доступ к эпителию. Эпителиальные клетки выделяют щелочной секрет, который в сочетании с желчью является прекрасной питательной средой для размножения вибрионов. Токсинообразование вибрионов, которые вырабатывают эндо- и экзотоксины. Экзотоксин (энтеротоксин) холероген — термолабильный белок, чувствителен к протеолитическим ферментам. Холероген содержит 2 субъединицы: А и В. А активизирует внутриклеточную аденилатциклазу, происходит повышение выхода жидкости в просвет кишечника. Диарея, рвота. Фермент нейраминидаза усиливает связывание холерного экзотоксина с эпителием слизистой кишечника. Эндотоксин запускает каскад арахидоновой кислоты, которая запускает синтез простагландинов (Е, F). Они вызывают сокращение гладкой мускулатуры тонкого кишечника и подавляют иммунный ответ, чем обусловлены диарея. Клинические проявления. Инкубационный период 2—3 дня. Боль в животе, рвота, диарея. Иммунитет. Гуморально-клеточный. При выздоровлении возникает напряженный непродолжительный иммунитет. Микробиологическая диагностика. Выделение и идентификация возбудителя. Материал для исследования - выделения от больных (кал, рвота), вода. Для экспресс-диагностики используют РИФ, ПЦР. Бактериоскопический метод в настоящее время не используется. Лечение: а)регидратация (восполнение потерь жидкости и электролитов введением изотонических, растворов, а также плазмозаменяющих жидкостей внутривенно;б) антибактериальная терапия (тетрациклины, фторхинолоны). Профилактика. Санит.-гиг. мероприятия. Экстренная профилактика антибиотиками широкого спектра действия, а также вакцинопрофилактика. Современная вакцина представляет собой комплексный препарат, состоящий из холероген-анатоксина и химического О-антигена, обоих биоваров и сероваров Огава и Инаба. Прививка обеспечивает выработку вибриоцидных антител и антитоксинов в высоких титрах. |
