Ответы по аналитике. Основные положения качественного анализа
 Скачать 0.71 Mb. Скачать 0.71 Mb.
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | |
| | 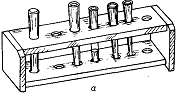 |
Штативы: а—для пробирок; б—с набором реактивов для полумикроанализа; в—физический
Шпатели предназначены для отбора сыпучих реактивов. Они невелики по размеру, могут быть изготовлены из фарфора, стекла, металла .
Фарфоровые чашки и тигли вместимостью 5—10 мл используют для нагревания, кипячения, выпаривания растворов, прокаливания сухих остатков .
Тигельные щипцы необходимы для работы с го рячими фарфоровыми чашками и тиглями.
Держатели для пробирок используют при нагре вании растворов в пробирках на газовых горелках.
Асбестовые сетки и фарфоровые треугольники нужны при нагревании растворов и прокаливании сухих остатков на газовых горелках.
Для нагревания растворов могут быть использованы водяные бани .
Газовые горелки,спиртовки, электроплитки требуются для выполнения операций, связанных с нагреванием.
Центрифуги предназначены для отделения осадка от раствора. Они могут быть ручными и электрическими.
Микроскопы необходимы при выполнении микрокристаллоскопических реакций.
Штативы, используемые в качественном анализе, разнообразны по своему назначению. Штативы для пробирок, ящики-штативыдля реактивов индивидуального и общего пользования, физические штативы с набором колец и лапок для работ, связанных с нагреванием .
Для мытья посуды используют ерши.
Кислотно – основной метод, индикаторы
Таблица значений рН перехода наиболее распространённых индикаторов
Приведены распространённые в лабораторной практике кислотно-основные индикаторы в порядке возрастания значений pH, вызывающих изменение окраски. Римские цифры в квадратных скобках отвечают номеру перехода окраски (для индикаторов с несколькими точками перехода).
| Индикатор и номер перехода | х[3] | Цвет более кислой формы | Интервал pH и номер перехода | Цвет более щелочной формы | ||
| Малахитовый зелёный | | | жёлтый | 0,1-2,0 [l] | | сине-зелёный |
| Метиловый фиолетовый | | | жёлтый | 0,13–0,5 [I] | | зелёный |
| Крезоловый красный [I] | | | красный | 0,2–1,8 [I] | | жёлтый |
| Метиловый фиолетовый [II] | | | зелёный | 1,0–1,5 [II] | | синий |
| Тимоловый синий [I] | к | | красный | 1,2–2,8 [I] | | жёлтый |
| Тропеолин 00 | o | | красный | 1,3–3,2 | | жёлтый |
| Метиловый фиолетовый [III] | | | синий | 2,0–3,0 [III] | | фиолетовый |
| (Ди)метиловый жёлтый | o | | красный | 3,0–4,0 | | жёлтый |
| Бромфеноловый синий | к | | жёлтый | 3,0–4,6 | | сине-фиолетовый |
| Конго красный | | | синий | 3,0–5,2 | к | красный |
| Метиловый оранжевый | o | | красный | 3,1–(4,0)4,4 | | (оранжево-)жёлтый |
| Бромкрезоловый зелёный | к | | жёлтый | 3,8–5,4 | | синий |
| Бромкрезоловый синий | | | жёлтый | 3,8–5,4 | | синий |
| Лакмоид | к | | красный | 4,0–6,4 | | синий |
| Метиловый красный | o | | красный | 4,2(4,4)–6,2(6,3) | | жёлтый |
| Хлорфеноловый красный | к | | жёлтый | 5,0–6,6 | | красный |
| Лакмус (азолитмин) | | | красный | 5,0–8,0 (4,5-8,3) | | синий |
| Бромкрезоловый пурпурный | к | | жёлтый | 5,2–6,8(6,7) | | фиолетовый |
| Бромтимоловый синий | к | | жёлтый | 6,0–7,6 | | синий |
| Нейтральный красный | o | | красный | 6,8–8,0 | | янтарно-жёлтый |
| Феноловый красный | о | | жёлтый | 6,8–(8,0)8,4 | | ярко-красный |
| Крезоловый красный [II] | к | | жёлтый | 7,0(7,2)–8,8 [II] | | тёмно-красный |
| α-Нафтолфталеин | к | | жёлто-розовый | 7,3–8,7 | | синий |
| Тимоловый синий [II] | к | | жёлтый | 8,0–9,6 [II] | | синий |
| Фенолфталеин[4] [I] | к | | бесцветный | 8,2–10,0 [I] | | малиново-красный |
| Тимолфталеин | к | | бесцветный | 9,3(9,4)–10,5(10,6) | | синий |
| Ализариновый жёлтый ЖЖ | к | | бледно-лимонно-жёлтый | 10,1–12,0 | | коричнево-жёлтый |
| Нильский голубой | | | синий | 10,1–11,1 | | красный |
| Диазофиолетовый | | | жёлтый | 10,1–12,0 | | фиолетовый |
| Малахитовый зелёный | | | сине-зелёный | 11,6-13,6 [ll] | | бесцветный |
| Индигокармин | | | синий | 11,6–14,0 | | жёлтый |
| Epsilon Blue | | | оранжевый | 11,6–13,0 | | тёмно-фиолетовый |
Кислотно - основное титрование, реакции нейтрализации, скачок титрования, построение кривых титрования, правила выбора индикатора при кислотно - основном титровании, требования, предъявляемые к индикаторам, методы амперометрического, кондуктометрического и потенциометрического титрования.
Частные реакции 4 аналит. группы
Реакции катионов хрома Cr3+
Реакция с гидроксидом аммония:
Cr3++3NH4OH→Cr(OH)3↓+3NH4Cl
Cr(OH)3+6NH4OH→[Cr(NH3)6](OH)3+6H2O
Раствор гидроксида аммония осаждает серо-зеленый осадок гидроксида хрома, который растворяется в избытке реактива с образованием комплексного соединения гидроксида гексаммина хрома.
Реакция с окислителями:
При действии окислителей, например, пероксида водорода, хлора, перманганата калия на катион хрома (3) образуются соли хромовой и дихромовой кислоты. Хроматы желтого цвета образуются в щелочной среде:
Cr3++2OH-→CrO2-+2H+
CrO2-+3H2O2+2OH-→2CrO42-+4H2O
Дихроматы, имеющие оранжевый цвет, образуются при воздействии окислителей в кислой среде:
10Cr3++6MnO4-+11H2O→5Cr2O72-+6Mn2++22H+
При большом избытке перманганата калия может образовываться бурый осадок дигидроксида оксида марганца (4):
KMnO4+3MnSO4+7H2O→5MnO(OH)2↓+2H2SO4+K2SO4
При окислении Cr3+ с персульфатом аммония в кислой среде образуется дихромат ион:
2Cr3++3S2O82-+7H2O→Cr2O72-+6SO42-+14H+
Реакция проходит хорошо в присутствии катализатора – нитрата серебра. При воздействии на образовавшийся дихромат-ион пероксидом водорода образуется пероксид хрома или надхромовая кислота:
Cr2O72-+4H2O2+2H+→2CrO5+5H2O
Cr2O72-+4H2O2+2H+→2H2CrO6+3H2O
Если к реакционной смеси добавить смесь изоамилового спирта с эфиром и взболтать, то верхний слой окрашивается в синий цвет вследствие перехода в спиртоэфирный слой пероксида хрома (надхромовой кислоты). Реакция очень чувствительна и специфична.
Реакции катионов цинка Zn2+
Реакция с гидроксидом аммония:
ZnCl2+2NH4OH→Zn(OH)2↓+2NH4Cl
Zn(OH)2+4NH4OH→[Zn(NH3)4](OH)2+4H2O
Раствор гидроксида аммония осаждает белый осадок гидроксида цинка, который растворяется в избытке реактива с образованием комплексного соединения гидроксида тетраминцинка.
Реакция с гексациано(2) ферратом калия (желтой кровяной солью):
3ZnSO4+2K4[Fe(CN)6]→ K2Zn3[Fe(CN)6]2↓+ 3K2SO4
При взаимодействии солей цинка с гексациано(2) ферратом калия образуется белый осадок гексациано(2) феррата калия и цинка. Реакция позволяет отличить катион алюминия от цинка.
Реакция с дитизоном (стр. 135)
При добавлении хлороформного раствора дитизона к водному раствору соли цинка образуется дитизонат цинка, окрашивающий в щелочной среде хлороформный и водный слои в красный цвет.
Реакция с нитратом кобальта:
Zn(NO3)2+Co(NO3)2→CoZnO2+4NO2↑+O2↑
После сжигания кусочка фильтровальной бумаги, смоченной раствором соли цинка и нитрата кобальта образуется зола, окрашенная в зеленый цвет цинкатом кобальта (зелень Ринмана).
Методы осаждения и комплексообразования, метод Фаянса
Методы осаждения основаны на использовании реакций, которые сопровождаются образованием осадков. По этому признаку данные методы сходны с гравиметрическим анализом. Но в отличие от гравиметрических методов образовавшиеся осадки, как правило, не подвергают исследованию. Их не фильтруют, не промывают, не взвешивают. Количество определяемого вещества находят так же, как и в других титриметрических методах. Точка эквивалентности совпадает в этих методах с момента прекращения дальнейшего образования осадка. Этот момен может быть установлен без применения индикаторов, но дл этого необходим значительный навык. В большинстве случае точку эквивалентности определяют с помощью индикаторов или же физико-химических методов (кондуктометрии, амперометрии). Для титриметрических определений используют только незначительное число реакций осаждения. Прежде всего это реакция между ионами Ag+ и С1-, Br -, I - и SCN -ионами, реакции между ионами ПНе2]2 + и С1 -, Вг - и I -ионами, а также между ионами Znr+ и K4[Fe(CN)6].
Широкому использованию в титриметрии реакций осажден» мешает обратимость процесса осаждения, незначительная скорост многих реакций осаждения, побочные явления при образовании осадка (соосаждение, коллоидообразование, адсорбция) и трудности в определении точки эквивалентности.
Процесс титрования может быть охарактеризован кривой титрования, построенной в координатах: концентрации ионов, образовавших осадок, рассчитанных с помощью правила произведения растворимости,-- объем титранта.
К наиболее известным методам осаждения относят аргентометрию, меркурометрию и тиоцианатометрию.
Аргентометрия основана на реакции образования малорастворимых солей серебра с галогенидами. В качестве титранта используют нитрат серебра:
AgN03+NaCl-АёСЦ+NaN03
Меркурометрия основана на образовании малорастворимых солей ртути (I) Hg2Cl2, Hg2I2 и т. д. В качестве титранта используют нитрат ртути (I):
Hg2 (N03)2 + 2NaCI-Hg2CI2i + 2NaN03
Тиоцианатометрия основана на образовании малорастворимой соли серебра AgNCS. В качестве титранта используют тиоцианат калия или аммония (KNCS или NH4NCS):
AgN03 + NH4NCS--AgNCS + NH4N03
Метод комплексообразования основан на том, что вещество, содержащееся в рабочем растворе, образует с анализируемым катионом прочное комплексное соединение, растворимое в воде. Хотя в ходе титрования осадок не образуется, концентрация определяемого иона по мере титрования уменьшается, так как все большее количество его связывается в комплекс. В этом отношении процесс комплексообразования аналогичен процессу осаждения. Осаждение происходит тем полнее, чем меньше растворимость осадка.
Метод комплексообразования основан на том, что вещество, содержащееся в рабочем растворе, образует с анализируемым катионом прочное комплексное соединение, растворимое в воде.
Распространен метод комплексообразования с карбамидом для разделения смесей индивидуальных органических веществ. Так, разработаны методики для разделения ди-н-бутиламина и диизобутиламина, н-нониламина и 3-метилгептана, октантиола-1 и этилгексантиола-1. Согласно последней методике, смесь обрабатывают не только карбамидом, но и тиокарбамидом. В результате получают чистые к-гептан и изооктан, содержащий только 5 % н-гептана. Предложена методика [260] выделения н-гептана из смеси его с толуолом. На примере фракций кислородсодержащих соединений, полученных при синтезе СО и Н2 и выкипающих в пределах 180 - 320 С, а также на примере фракции высших жирных спиртов, выкипающей в тех же пределах, показана возможность [261] разделения кислородсодержащих соединений по их строению методом образования комплексов с карбамидом / Гюнтером [33] осуществлено разделение н-парафинов и алкилированных моно - и бициклических углеводородов, основанное, во-первых, на том, что алкилированные бициклические ароматические углеводороды не образуют комплексов с карбамидом - это позволяет отделить их от алкилированных моноциклических ароматических углеводородов; а во-вторых, на различной способности образовывать комплекс к-парафинов и алкилированных моноциклических ароматических углеводородов. Комплексообразованием с карбамидом проведено также отделение к-октадецилбензола, к-октадецилциклогексана, н-октадецилнафталина, к-октадецилдекалина, к-тридекалина и других моно - и бициклических соединений от н-гептадекана и н-генейкозана.
Определено методом комплексообразования с мочевиной.
Применяют также метод комплексообразования, в частности, метод образования клатратов - ксилола с различными комплексными соединениями, которые содержат никель, замещенные пири-дины или изоцианаты. Обычно клатратообразование сочетают с кристаллизацией.
методом комплексообразования с карбамидом разделила твердые парафины, выделенные из нефти Каратонского и Мунайлинского месторождений ( Казахская ССР), на фракции. Она показала, что твердый парафин, выделенный из каратонской нефти ( температура плавления 52 - 57 С, молекулярный вес 420), на 2 / з состоит из структур разветвленного типа и только г / з составляют парафины нормального строения.
Метод Фаянса
Метод Фаянса-Ходакова основан на прямом титровании анионов (галогенидов, цианидов, тиоцианатов) стандартным раствором серебра нитрата в присутствии адсорбционных индикаторов.
Адсорбционные индикаторы представляют собой слабые органи-ческие кислоты, диссоциирующие на ионы:
HInd - H+ + Ind -
Анионы этих кислот вблизи точки эквивалентности адсорбируются по верхностью образующихся осадков, что приводит к изменению окраски осадка и позволяет фиксировать конечную точку титрования.
В качестве адсорбционных индикаторов в аналитической практике чаще всего используют флуоресцеин, дихлорфлуоресцеин, эозин и другие соединения
При титровании, например, хлорид-ионов ионами серебра образуется осадок серебра хлорида, склонный к образованию коллоидных растворов:
Ag+ + Сl - - AgCl
Осадки с ионной кристаллической решеткой адсорбируют на своей поверхности одноименные ионы, как правило, находящиеся в избытке. До конечной точки титрования на поверхности осадка AgCl адсорбируются находящиеся в избытке хлорид-ионы, и коллоидные частицы при обретают отрицательный заряд, то есть имеют следующее строение: [mАgСl] nCl-.
Эти заряженные частицы притягивают из раствора в качестве против ионов ионы K+ (вторичный адсорбционный слой):
{ [mАgСl] nCl- (n-x) K+}x-
Поскольку коллоидные частицы имеют отрицательный заряд, то адсорб ция анионов индикатора невозможна.
В конечной точке титрования коллоидные частицы теряют заряд, и вы падает осадок хлорида серебра. Первая избыточная капля раствора AgNО3 создает в растворе избыток ионов Ag+, которые адсорбируются поверхностью осадка AgCl и придают ей положительный заряд: [mАgСl] nAg+, то есть происходит изменение знака заряда частицы. В качестве противоионов теперь адсорбируются нитрат-ионы (вторичный адсорбционный слой - мицеллы): { [mАgСl] nАg+ (n-x) NO3-}x+
Нитрат-ионы NО3 - не образуют труднорастворимого соединения с ионами коллоидной частицы, поэтому легко замещаются окрашенными анионами индикатора, что приводит к изменению окраски поверхности осадка и указывает на конечную точку титрования.
Условия титрования по методу Фаянса-Ходакова:
1. Титрование следует выполнять при определенном значении рН, так как это существенно влияет на ионизацию индикатора. Титрование с флуоресцеином необходимо проводить в нейтральной или слабощелочной среде (рН = 7.10); в кислой среде ионизация флуоресцеина будет подавляться, при этом концентрация его анионов понизится на столько, что не сможет образовываться окрашенный адсорбционный слой. Дихлорфлуоресцеин - кислота более сильная, чем флуоресцеин, поэтому титрование можно проводить в слабокислой среде. Эозин более сильная кислота, поэтому его можно применять как индикатор в кислой среде при рН ? 2.
2. Титрование с адсорбционным индикатором следует проводить при большой поверхности осадка. Это достигается, когда осадок присутствует в виде коллоидных частиц. С этой целью к титруемому раствору прибавляют защитные коллоиды - декстрин, крахмал и др.
3. Необходимо, чтобы ионы индикатора адсорбировались осадком значительно слабее, чем определяемые ионы, иначе ионы индикатора будут адсорбироваться значительно раньше момента эквивалентности, что приведет к заниженным результатам анализа.
Метод Фаянса - Ходакова применим для определения Сl-, Br-, I-,CN - и NСS-ионов.
Частные реакции катионов 3 аналит. группы
Реакции катионов бария Ba2+
Реакция с солями хромовой кислоты:
BaCl2+K2CrO4→BaCrO4↓+2KCl
Образуется желтый кристаллический осадок хромата бария, растворимый в азотной и соляной кислотах:
BaCrO4+2HCl→BaCl2+H2CrO4
BaCrO4+2HNO3→Ba(NO3)2+ H2CrO4
В серной кислоте желтый осадок осадок хромата бария переходит в белый осадок сульфата бария:
BaCrO4+H2SO4→BaSO4↓+ H2CrO4
В уксусной кислоте и других слабых кислотах осадок хромата бария нерастворим.
При взаимодействии солей бария с солями дихромовой кислоты также образуется осадок хромата бария:
2BaCl2+K2Cr2O7+H2O→ 2BaCrO4↓+2KCl+2HCl
При проведении реакции выделяется соляная кислота, которая частично растворяет осадок хромата бария, поэтому при применении дихроматов осаждение хромата бария происходит не полностью.
Для полного осаждения хромата бария с помощью дихроматов используют добавку солей уксусной кислоты. Соли уксусной кислоты взаимодействует с соляной кислотой, в итоге образуется слабая уксусная кислота, в которой осадок хромата бария не растворяется:
CH3COONa+HCl→CH3COOH+NaCl
Ионы стронция и кальция осадка с дихроматами не образуют, так как образующиеся хроматы кальция и стронция растворяются полностью в выделяющейся соляной или уксусной кислоте.
Реакция с солями щавелевой кислоты:
BaCl2+(NH4)2C2O4→BaC2O4↓+NH4Cl
Образуется белый кристаллический осадок оксалата бария, растворимый в соляной и азотной кислотах, при нагревании – в концентрированной уксусной кислоте.
Реакция с карбонатами:
BaCl2+(NH4)2CO3→BaCO3↓+NH4Cl
Образуется белый аморфный осадок, при нагревании переходящий в кристаллический, растворимый в соляной, азотной и уксусной кислотах.
Реакция с моногидрофосфатом натрия:
BaCl2+Na2HPO4→BaHPO4↓+2NaCl
Образуется белый кристаллический осадок, растворимый в соляной, азотной и уксусной кислотах.
Реакция с гипсовой водой:
BaCl2+CaSO4→ BaSO4↓+CaCl2
Образуется белый осадок сульфата бария.
Капельная реакция с родизонатом натрия:
CO – CO – CO – Na CO – CO – CO
BaCl2+ │ ║ → │ ║ Ba ↓+ 2NaCl
CO – CO – CO – Na CO – CO – CO
При нанесении на фильтровальную бумажку капли нейтрального раствора соли бария и раствора родизоната натрия появляется красно-бурое окрашивание вследствие выделения осадка родизоната бария. При добавлении капли соляной кислоты красно-бурое окрашивание переходит в красное, так как родизонат бария переходит в гидрородизонат бария красного цвета.
CO – CO – CO CO – CO – CO -
2 │ ║ Ba+2HCl → │ ║ Ba ↓+ BaCl2
CO – CO – CO CO – CO – COH 2
В присутствии K2CrO4 родизонат бария не образуется . Реакция специфична для катионов бария.
Реакция окрашивания пламени. При внесении в пламя газовой горелки летучих солей бария(хлорид, нитрат) – пламя окрашивается в желто-зеленый цвет.
Реакции катионов стронция Sr2+
Дает осадки, аналогичные по свойствам катиону бария с солями щавелевой, угольной и хромовой кислот, с гидрофосфатами, щелочами, гипсовой водой. Но не дает осадка с дихроматами.
Капельная реакция с родизонатом натрия:
CO – CO – CO – Na CO – CO – CO
SrCl2+ │ ║ → │ ║ Sr ↓+ 2NaCl
CO – CO – CO – Na CO – CO – CO
При проведении этой реакции на фильтровальной бумаге образуется красно-бурое окрашивание осадка родизоната стронция, исчезающее при добавлении капли соляной кислоты (растворение осадка). Реакция катиона стронция с родизонатом натрия происходит в присутствии K2CrO4 вследствие слабой растворимости осадка SrCrO4. Это свойство используют при открытии ионов стронция в присутствии ионов бария. На фильтровальную бумагу наносят каплю раствора K2CrO4 и каплю исследуемого раствора. При этом бумага окрашивается в желтый цвет вследствие образования осадков SrCrO4 и ВаCrO4. Затем на пятно наносят каплю раствора родизоната натрия. В присутствии ионов стронция пятно окрашивается в буро-красный цвет, в отсутствии стронция окраска остается желтой, так как ВаCrO4 реакцию с родизонатом натрия не дает.
Реакция с родизонатом натрия позволяет открыть катионы бария и стронция при совместном присутствии. Если при проведении этой реакции на бумаге образовалось красно-бурое пятно, исчезающее при добавлении HCl, в растворе присутствует стронций. Если красно-бурое пятно краснеет при добавлении HCl, то в растворе присутсвует барий и возможно стронций. Для подтверждения присутствия стронция проводят реакцию с родизонатом натрия в присутствииK2CrO4. Окрашивание желтого пятна в красно-бурый цвет указывает на присутствие стронция.
Реакция окрашивания пламени. При внесении летучих солей стронция (хлорид, нитрат) в пламя газовой горелки пламя окрашивается в карминово-красный цвет.
Реакции катионов кальция Сa2+
Катион кальция образует в растворах осадки с гидрофосфатами, карбонатами, щелочами, хроматами, аналогичные по свойствам осадкам, образуемым катионами бария и стронция. Реакции с гипсовой водой, дихроматами, хроматами ион кальция не дает. С родизонатом натрия ион кальция образует фиолетовый осадок в щелочной среде, растворимый в HCl.
Реакция с оксалатами:
CaCl2+(NH4)2C2O4→CaC2O4↓+2NH4Cl
Образуется кристаллический белый осадок оксалата кальция, который растворим в минеральных кислотах и нерастворим в уксусной кислоте( в отличие от оксалатов бария и стронция).
Реакция с гексациано(2) ферратом калия K4[Fe(CN)6]:
CaCl2+ K4[Fe(CN)6]+2NH4OH→ Ca(NH4)2[Fe(CN)6]↓+ 2KCl+2KOH
В слабощелочной среде рН=9 образуется белый кристаллический осадок гексациано (2) феррата кальция-аммония, растворимый в минеральных кислотах, но не растворимый в уксусной кислоте. Реакцию проводят в присутствии буферной смеси NH4Cl+ NH4OH при нагревании. Проведению реакции мешает ион Ba2+.
Реакция окрашивания пламени. Пламя газовой горелки при внесении солей кальция окрашивается в кирпично-красный цвет.
Значение в медицине и фармации катионов 3-ей аналитической группы
В медицинской и фармацевтической практике применяют соли кальция и бария. Сульфат кальция или гипс применяют для наложения повязок, при изготовлении зубных порошков. Хлорид кальция, глюконат кальция, лактат кальция используют при аллергических заболеваниях, как кровоостанавливающее средство, при пониженной свертываемости крови. Карбонат кальция или мел способен снижать повышенную кислотность желудочного сока. Он входит в состав зубных порошков и паст. Соединения кальция играют важную роль в организме, входя в состав
костей, тканей, крови. Они регулируют деятельность системы свертывания крови, нервные и имунные процессы, работу сердца.
Из солей бария в медицине применяется сульфат бария как рентгеноконтрасное средство при рентгеноскопии желудка и кишечника.
