ОТВЕТЫ НА БИЛЕТЫ ПО БИОЛОГИЧЕСКОЙ ХИМИИ. Отдельное спасибо ребятам со второго потока лечебного факультета 2012 г
 Скачать 2.33 Mb. Скачать 2.33 Mb.
|
|
3. Зависимость скорости реакции от концентрации субстрата При увеличении концентрации субстрата скорость реакции сначала возрастает соответственно подключению к реакции новых молекул фермента, затем наблюдается эффект насыщения, когда все молекулы фермента взаимодействуют с молекулами субстрата. При дальнейшем увеличении концентрации субстрата между его молекулами возникает конкуренция за активный центр фермента и скорость реакции снижается. 4. Зависимость от концентрации фермента При увеличении количества молекул фермента скорость реакции возрастает непрерывно и прямо пропорционально количеству фермента, т.к. большее количество молекул фермента производит большее число молекул продукта. Основы количественного определения активности ферментов 1. Активность фермента выражается в скорости накопления продукта или скорости убыли субстрата в пересчете на количество материала, содержащего фермент.  В практике обычно используют: единицы количества вещества – моль (и его производные ммоль, мкмоль), грамм (кг, мг), единицы времени – минута, час, секунда, единицы массы или объема – грамм (кг, мг), литр (мл). Активно используются и другие производные – катал (моль/с), международная единица активности (МЕ, Unit) соответствует мкмоль/мин. Таким образом, активность фермента может выражаться, например, в ммоль/с×л, г/час×л, МЕ/л, кат/мл и т.д. Например, известно, что 1 г пепсина расщепляет 50 кг яичного белка за один час – таким образом, его активность составит 50 кг/час на 1 г фермента, если 1,6 мл слюны расщепляет 175 кг крахмала в час – активность амилазы слюны составит 109,4 кг крахмала в час на 1 мл слюны или 1,82 кг/мин×г или 30,3 г крахмала/ с×мл. 2. Создание стандартных условий, чтобы можно было сравнивать результаты, полученные в разных лабораториях – оптимальная рН и фиксированная температура, например, 25°С или 37°С, соблюдение времени инкубации субстрата с ферментом. 3. Необходимо наличие избытка субстрата, чтобы работали все имеющиеся в растворе молекулы фермента. 2) Синтез жирных кислот. Внутриклеточная локализация. Биосинтез три ацилглицеролов. Биосинтез жирных кислот идёт в цитоплазме, нужен ацетил-КоА из митохондрий, участвует малонил-КоА,происходит перенос ацетил-КоА в цитоплазму,участвует мультиферментный комплекс синтетаза жирных кислот, требуется биотин, нужен НАДФН2, требуется АПБ на всех этапах.Перенос ацетил-КоА из митохондрий в цитоплазму Ацетил-КоА не проникает через мембрану митохондрий в цитоплазму. Ацетил-КоА + ЩУК = цитрат + НSКоА Цитрат с помощью транслоказы переносится в цитоплазму. В цитоплазме: цитрат + НSКоА +АТФ = Ацетил-КоА +АДФ+Фн+ЩУК цитратлиаза НАДН+ НАД+ НАДФН+Н+ НАДФ+ ЩУК = малат = ПВК+ СО2 Малик-фермент Реакции синтеза жирных кислот СН3-CО-S-KoA + биотин-СО2 + АТФ = Ацетил-КоА-Карбоксилаза(Инсулинзависимая) НООС-СН2-CО-S-KoA + АДФ + Фн малонил-КоА Ацетил-КоА-карбоксилаза аллостерический фермент, активатором является цитрат, повышение содержания цитрата в митохондриях приводит к тому, что при помощи челночного механизма он поступает в цитоплазму. Далее действует мультиферментный комплекс – синтетаза жирных кислот, который представляет собой 6 ферментов, связанных с АПБ. СН3-CО-S-KoA + HS-АПБ = HS-КоА + СН3-CО-S-АПБ АПБ-ацетилтрансфераза ацетил-АПБ НООС-СН2-СО-S-КоА + НS-АПБ = HS-KoA + HOOC-CH2-CO-S-АПБ АПБ-малонилтрансфераза малонил-АПБ Далее происходит конденсация малонил-АПБ и ацетил-АПБ. СН3-CО-S-АПБ + НООС-СН2-CО-S-АПБ = ацетил-АПБ малонил-АПБ B-Кетоацетил-АПБсинтаза СН3-CО-СН2-CО-S-АПБ + НАДФН+Н+ = ацетоацетил-АПБ В-Кетоацил-АПБ-редуктаза СН3-CH(ОH)-СН2-CО-S-АПБ + НАДФ+ = β-оксибутирил-АПБ В-оксиацил-АПБ-дегидратаза СН3-CH=СН-CО-S-АПБ + НАДФН+Н+ = кротонил-АПБ еноилАПБ-редуктаза СН3-CH2-СН2-CО-S-АПБ +НАДФ+ бутирил-АПБ Далее цикл повторяется.Малонил-КоА переносится на SH-группу фосфопантетеина АПБ. Бутирил-АПБ + малонил-АПБ = кетокапронилАПБ + СО2 Пальмитиновая кислота – предшественник для других жирных кислот. Биосинтез ТАГ В почках, стенке кишечника, печени высока активность глицеролкиназы.В мышцах, жировой ткани активность глицеролкиназы низкая и образование глицерол-3-фосфата связано с гликолизом и гликогенолизом. Жиры, синтезированные в жировой ткани, там и откладываются, а из печени жиры транспортируются в составе липопротеинов 3. Больной жалуется на боли в правом подреберье. Слизистые и кожные покровы желтушны. Оцените состояние больного на основании дан ных анализа его крови: общий билирубин - 60 мкмоль/л, прямой билирубин - 45 мкмоль/л. Активность щелочной фосфатазы резко повышена. Механическая желтуха Билет 25 1)Нуклеопротеины и нуклеиновые кислоты. Структурная организация моле кул ДНК и РНК. Распад нуклеопротеинов в пищеварительном тракте. Нук леотидный пул клеток, пути его пополнения и расходования. Перевариивание нуклеопротеинов:
Расщепление НК 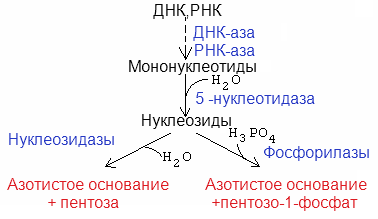 Нуклеотидный пул клеток, пути его пополнения и использования: 2)Витамины А, Е, К, влияние на обмен веществ, признаки витаминной не достаточности. Витамин К. К классу лиаз относится γ-глутаматкарбоксилаза, кофактором которой служит жирорастворимый витамин К (антигеморрагический). Пищевые источники витамина К крапива. Человек получает достаточное количество витамина К с пищей, а также за счет синтеза кишечной микрофлорой.Недостаточность витамина К может наступить из-за нарушения всасывания жиров в кишечнике, вместе с кото рыми всасывается витамин К. Недостаточность витамина К нарушается свертывание крови, возникает кровотечение. Для предупреждения и лечения геморрагии назначают витамин К. Различают витамин К1 (филлохинон) в растениях, витамин К2 (метахинон) в тканях животных,витамин К3 – Патология минерализации костей, наблюдается при генетическом дефекте γ-глутаматкарбоксилазы, применении антивитаминов К (дикумарин) в первые месяцы беременности. Витамин А (ретинол) – антиксерофтальмический витамин. Биологическая роль: Участвует в светоощущении (в синтезе зрительного пурпура родопсина, обеспечивающего нормальное зрение в условиях слабой освещенности).Участвует в окислительно-восстановительных процессах.Влияет на проницаемость клеточных мембран.Активирует синтез белка, нуклеиновых кислот.Влияет на барьерную функцию кожи, слизистых оболочек. Является антиоксидантом. Активирует включение сульфатов в гликаны, протеогликаны (компоненты соединительной ткани, хрящей, костей), обеспечивая трофику, нормальный рост и дефференцировку клеток развивающегося организма. Активирует ферменты, ответственные за дифференцировку клеток покровного эпителия (кожи, слизистых, роговицы) – предотвращает их ороговение и слущивание.Поддерживает деление клеток иммунно-компетентной системы, нормализует синтез иммунноглобулинов (IgA) и других факторов защиты организма от инфекций (интерферон, лизоцин). При отсутствии в пище витамина А в организме развивается ряд специфических симптомов авитаминоза: ослабление зрения, поражение эпителиальных тканей (слущивание и ороговение эпителия), в том числе роговицы глаза (сухость её и воспаление, вследствие закупорки слезного канала - ксерофтальмия), задержка роста. Витамин Е – токоферол. Биологическая роль:Токоферол регулирует интенсивность свободно-радикальных реакций в живых клетках, поскольку препятствует развитию цепных неуправляемых реакций пироксидного окисления ненасыщенных липидов в биологических мембранах. Это наиболее мощный природный антиоксидант, благодаря чему обеспечивается стабильность биологических мембран клеток организма.Токоферол повышает биологическую активность витамина А, защищая его ненасыщенную боковую цепь от пероксидного окисления.Регулирует окислительно-восстановительные процессы. Стимулирует синтез ГЕМа. 3)Оценить состояние больного по следующим данным анализа крови: ак тивность креатинфосфокиназы повышена, общая активность ЛДГ повышена, преимущественно за счет ЛДГ1. Коэффициент де Ритиса - 1,90. Инфаркт миокарда Билет 26 1)Биологическая роль печени. Роль печени в обмене углеводов, липидов, аминокислот и белков. Антитоксическая роль печени. Роль печени в углеводном обмене: Печень – депо гликогена. Печень обеспечивает постоянный уровень глюкозы в крови, регулируя соотношения между синтезом и распадом гликогена. В печени протекают:
Роль печени в липидном обмене: В печени осуществляется:
Роль печени в белковом обмене: В печени протекает:
альбуминов плазмы, 80 % a-глобулинов, 50 % b-глобулинов, ряда ферментов, аминокислот.
Антитоксическая роль печени: В печени происходит синтез мочевины (обезвреживание аммиака). Путем образования парных соединений с ФАФС или глюкуроновой кислотами обезвреживаются:
Образование парных соединений в печени протекает также с участием гликокола и таурина:
При участии моно- и диаминоокисидаз (МАО, ДАО) в печени происходит окислительный распад - адреналина и гистамина. Функции печени:
2)Биосинтез пуриновых и пиримидиновых нуклеотидов. Оротовая ацидурия. Пути синтеза пуринов:
При синтезе де ново конечный продукт ИМФ (затрачивается 6 АТФ) Реутилизация:
аденинфосфорибозилтрансфераза
Гипоксантин-гуанин-фосфорибозилтрансфераза
Гипоксантин-гуанин-фосфорибозилтрансфераза Синтез пиримидинов: 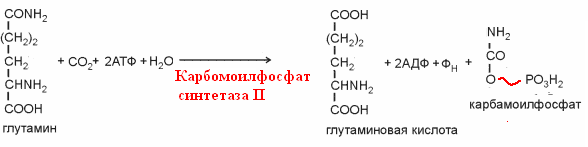 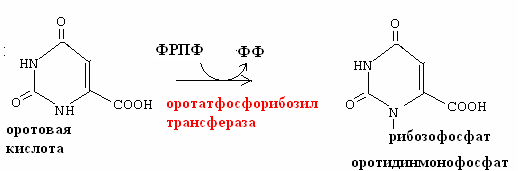 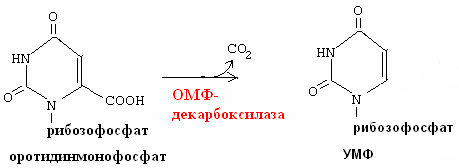 Оротовая ацидурия I типа связана с утратой функции двух ферментов: оротатфосфорибозилтрансферазы, ОМФ-декарбоксилазы. наследуется.С мочой выделяется много оротовой кислоты.Недостаток пиримидиновых нуклеотидов.Лечат уридином.В детстве приводит к: отставанию в развитии, мегалобластической анемии, «оранжевой» кристаллоурии, подверженности инфекциям. Оротовая ацидурия II типа связана с недостатком ОМФ-декарбоксилазы. С мочой выделяются оротидин и оротовая кислота. 3)Оценить состояние больного на основании данных сахарной нагрузки: глюкоза натощак - 5,5 ммоль/л, после нагрузки: через 60 мин - 15 ммоль/л, через 120 мин - 12,5 ммоль/л. В моче больного реакция на глюкозу положительная. скрытый диабет Билет 27 1)Распад гемоглобина. Образование билирубина и продуктов его обмена. Характеристика прямого и непрямого билирубина. Диагностическое значи ние их определения. Классификация желтух. Распад гемоглобина происходит в микросомальной фракции ретикулоэндотелиальных клеток печени, селезенки и костного мозга. В сутки образуется 250-350 мг билирубина. Непрямой (свободный, неконъюгированный) билирубин:
Токсичность непрямого билирубина:
Прямой (связанный, коньюгированный) билирубин:
В норме содержание общего билирубина в крови 1,7-20,5 мкмоль /л:
|
