ОТВЕТЫ НА БИЛЕТЫ ПО БИОЛОГИЧЕСКОЙ ХИМИИ. Отдельное спасибо ребятам со второго потока лечебного факультета 2012 г
 Скачать 2.33 Mb. Скачать 2.33 Mb.
|
|
Классификация желтух: Гемолитическая: Возникает при:
Усилен распад эритроцитов. Печеночная: Возникает при:
Клинические проявления:
Механическая: Возникает при:
Клинические проявления:
2)Глюкоза крови. Гипергликемия, гипогликемия, глюкозурия. Диагностическое значение определния глюкозы в крови и моче. Глюкоза - основной углевод крови. 3,3 – 5,5 ммоль/л – нормогликемия,уровень глюкозы менее 1,7 ммоль/л – смертелен. 90% углеводов крови составляет глюкоза,также содержатся пентозы, фруктоза, при патологии – галактоза. Концентрация глюкозы в крови определяется соотношением между интенсивностью поступления её в кровоток и выходом из крови. Уровни регуляции содержания глюкозы в крови. Регуляция содержания глюкозы в крови осуществляется на уровне: субстрата, регуляторных ферментов, взаимодействия циклов (эффект Пастера), ЦНС, гормонов. Гипергликемия Физиологическая 1)Алиментарная возникает после приёма пищи 2)Эмоциональная при стрессе Патологическая (Возникает при: 1) сахарном диабете2) избытке контринсулярных гормонов, 3) расстройствах мозгового кровообращения) Глюкозурия – появление глюкозы в моче.Наблюдается, если гипергликемия более 9,3 ммоль/л, то есть превышает почечный порог. Возникает при: нарушении углеводного обмена, повреждениях почек, острых инфекциях, сотрясении головного мозга. Гипогликемия- снижение содержания глюкозы крови. Симптомы гипогликемии сходны с симптомами гипоксии: головокружение, обморок, ступор, кома. Причины гипогликемии голодание, усиленная мышечная работа, введение инсулина, инсулинома, злокачественные опухоли из-за повышенной утилизации глюкозы, алкоголизм (угнетение глюконеогенеза), заболевания почек, нарушения функции печени, гипофизарная, надпочечниковая, тиреоидная недостаточность, беременность и лактация, гликогенозы. 3)Рассмотрите схему ферментативной реакции: пируват ----------- > лактат. Назовите класс фермента, катализирующего данную реакцию. С участием какого кофермента протекает реакция? Какой витамин входит в его состав. ЛДГ – оксидоредуктазы, РР – витамин, НАД – кофермент. Билет 28 1)Гликолиз. Биологическая роль, химизм процесса, биоэнергетика, регуляция. Эффект Пастера. -это анаэробный распад глюкозы до лактата. С6Н12О6 + 2АДФ +2Фн = 2 лактата + 2АТФ + 2Н20. -включает 11 реакций и 2 этапа. Значение гликолиза Благодаря гликолизу организм осуществляет ряд функций в условиях недостаточности кислорода. Когда на Земле не было кислорода, то гликолиз был основным источником энергии. Особенности гликолиза -Ферменты гликолиза локализуются в цитоплазме. -Наиболее интенсивен гликолиз в: эритроцитах, работающей мышце, эмбриональной ткани, опухоли. -3 необратимые реакции (киназные). Первый этап гликолиза Второй этап гликолиза В активном центре фермента глицеральдегидфосфатдегидрогеназы содержатся SН-группы цистеина. На первом этапе происходит отщепление водорода с альдегидной группы субстрата, а второй водород от SН-группы активного центра. Водород переходит на НАД, в результате получаем НАДН+Н+, образуется фермент-субстратный комплекс, который взаимодействует с фосфорной кислотой. Свободная энергия, освобождённая при окислении альдегидной группы, сохраняется в высокоэнергетической фосфатной группе. 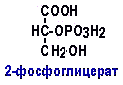 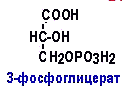 НАДН+Н , образующийся при окислении глицеральдегид-3фосфата,вновь окисляется в НАД, восстанавливая при этом ПВК до лактата. Эта реакция происходит в анаэробных условиях Баланс гликолиза АТФ образуется за счёт двух реакций субстратного фосфорилирования (ПК, фосфоглицераткиназной). Из глюкозы образуется 4АТФ. 2АТФ тратится в гликолизе на фосфорилирование (ГК, ФФК реакции). Гексокиназная реакция -1АТФ Фосфофруктокиназная реакция -1АТФ Фосфоглицераткиназная реакция 2АТФ Пируваткиназная реакция 2АТФ Итого: 4 – 2 = 2АТФ Регуляция гликолиза -Гексокиназа – аллостерический фермент, ингибируется глюкозо-6-фосфатом. Инсулин стимулирует синтез глюкокиназы, которая не ингибируется глюкозо-6-фосфатом. -Фосфофруктокиназа - аллостерический фермент. Положительный модулятор – АМФ, АДФ, Фн, цАМФ, ионы двухвалентных металлов. -Отрицательный модулятор – АТФ и цитрат. Когда величина значительна, то происходит угнетение ФФК. Эффект Пастера -торможение гликолиза кислородом. Причина этого: кислород окисляет НАДН+Н и он не восстанавливает ПВК в лактат. 3) Пируваткиназа – аллостерический фермент. Положительный модулятор – АДФ. Отрицательный модулятор – АТФ, ацетил-КоА, жирные кислоты. Гликолиз обратим. Биологическое значение обратимости гликолиза: -освобождение тканей от лактата, -возможность осуществления глюконеогенеза 2)Витамин D. Химическая природа витамина, гормонально-активные формы. Участие витамина в обмене веществ. Рахит. Витамин D Суточная потребность в витамине D 15-25мкг Пищевые источники: -сливочное масло, -желток яиц, -печень, -рыбий жир. Синтез витамина D3 происходит в мальпигиевом слое эпидермиса под действием УФ-лучей из 7-дегидрохолестерина Затем транспортный белок переносит витамин D3 в печень. Роль витамина D в обмене кальция В печени происходит гидроксилирование в положении 25 В этом участвуют: -ионы магния, -НАДФН+Н+, -цитохром Р450-редуктаза, -цитохром Р450, -кислород. Образуется 25-оксихолекальциферол, который из печени поступает в плазму крови и затем транспортируется в почки. В почках происходит гидроксилирование в положении 1 В этом участвуют: -ионы магния, -НАДФН+Н+, -кислород, -почечная -ферредоксинредуктаза, -почечный ферредоксин, -цитохром Р450. Образуется кальцитриол (1,25-диоксихолекальциферол) Паратгормон активирует гидроксилирование в почках Гормонально активные кальцитриолы -24,25-диоксихолекальциферол -23,25-диоксихолекальциферол -24,26-диоксихолекальциферол Рахит заболевание, в основе которого лежат изменения фосфорно-кальциевого обмена и нарушение отложения в костной ткани фосфата кальция, ведущие к деформации скелета. у взрослых недостаточность витамина D вызывает остеомаляцию и кариес у беременных. Витамин-D-дефицитный рахит возникает при авитаминозе D. Витамин-D-толерантный рахит может быть связан: -с нарушением функции паращитовидных желёз -с нарушением функции почек. Рахит развивается -при дефиците витамина D в пище, -при недостаточном солнечном облучении, -при заболеваниях почек, -при недостаточной продукции паратгормона (нарушение гидроксилирования в почках), -при дисбактериозе кишечника, -при синдромах нарушенного всасывания (целиакия, муковисцидоз), -под влиянием экологических факторов (замещение кальция в костях другими микроэлементами- стронций, свинец, цинк), -недоношенность предрасполагает к рахиту, так как наиболее интенсивное поступление кальция и фосфора от матери к плоду происходит в последние месяцы беременности. Биохимия рахита -понижение концентрации кальция и фосфора в крови, при этом Са/Р возрастает, -снижение всасывания кальция и фосфора в кишечнике, -снижение реабсорбции кальция и фосфора в почках, -нарушается минерализация костной ткани, повышается активность щелочной фосфатазы, -снижается синтез цитрата, который в норме связывает кальций. 3)Какова судьба гемоглобина, попавшего в плазму крови в результате гемолиза эритроцитов? Он превращается в билирубин. Если гемоглобина освобождается очень много и ретикулогистиоцитарная система не справляется с его переработкой, возникают гемоглобинемия и гемоглобинурия. Билет 29.
Фосфолипазы - ферменты класса гидролаз, катализирующие катаболизм глицерофосфолипидов. Различают фосфолипазы секреторные, входящие в состав панкреатического сока, и клеточные фосфолипазы. Клеточные фосфолипазы А1, A2, D, С различаются по специфичности к отщепляемой группе. Все фосфолипазы - кальцийзависимые ферменты. Каждое из семейств фосфолипаз неоднородно и включает ферменты, значительно отличающиеся по мол. массам, субъединичному составу и др. св-вам. Все фосфолипазы наиб. активно катализируют гидролиз на пов-сти раздела фаз фосфолипид - вода; медленно гидролизуют водорастворимые субстраты. Фосфолипазы A1 в большинстве своем - внутриклеточные ферменты, часто мембраносвязанные, не нуждаются в коферменте. Их мол. массы варьируют в пределах 15-90 тыс.; оптимальная каталитич. активность проявляется при рН 4,0 (для лизосо-мальных ферментов) или 8,0-9,5 (для ферментов микросом, плазматич. мембран и цитозоля); широко распространены в животных тканях (печень, сердце, мозг) и в микроорганизмах (Bacillus subtilis, В. megateiium, Mycobacter phlei, Escherichia coli). Фосфолипазы A2 - наиб, изученные представители фосфолипаз. Известны 3 группы фосфолипаз A2: 1) ферменты ядов змей, рептилий и насекомых, существующие в виде большого кол-ва изоформ. 2) ферменты поджелудочной железы млекопитающих, продуцирующиеся в организме в виде зимогенов (предшественников с большей мол. массой) и активирующиеся трипсином; 3) внутриклеточные ферменты из крови и тканей животных, среди к-рых имеются как р-римые, так и мембра-носвязанные. Фосфолипазы A2 первых двух подгрупп являются водорастворимыми ферментами, обладают высокой стабильностью благодаря большому числу (6-7) дисульфидных связей; оптимальная каталитич. активность при рН 7,5-9,0; рI от 4,0 до 10,5; кофермент - Ca2+. Для мн. представителей этих подгрупп фосфолипаз известны первичная и пространственная структура; в активном центре обнаружены остатки гистидина и аспара-гиновой к-ты. Cв-ва внутриклеточных фосфолипаз A2 (третья подгруппа) зависят от субклеточной локализации фермента. Фосфолипазы L выделены из растений, микроорганизмов, яда пчел, тканей млекопитающих. Ферменты этой группы крайне неспецифичны, катализируют гидролиз разл. сложноэфирных связей, обладают литическим (разрушающим) действием по отношению к биол. мембранам что обусловливает их токсичность. Фосфолипазы С обнаружены у бактерий Clostridium, Bacillus и Pseudo-monas, а также в клетках млекопитающих (печень, мозг, поджелудочная железа). Для нек-рых из них характерна строгая специфичность по отношению к спиртовой группе молекулы субстрата, напр. к остатку холина (фосфолипазы Cx) и миоинозита (фосфолипазы Си). Мол. м. фосфолипаз С от 23 до 51 тыс., ионы Zn2+ являются для них коферментом и стабилизатором; оптимальная каталитич. активность при рН ок. 7 для фосфолипаз Cx и при рН < 7 для фосфолипаз Си. Фосфолипазы D обнаружены в растениях (овощи, водоросли), микроорганизмах и в тканях животных. Их мол. м. 90-116 тыс.; оптимальная каталитич. активность при рН 4,7-8,0. Катионные ПАВ ингибируют фосфолипазы D, анионные - активируют. Помимо гидролитич. ф-ции фосфолипазы обладают трансацилазной (фосфолипазы A1, A2 и L) и транс фосфатидилазной (фосфолипазы Си D) активностью. Фосфолипазы играют важную роль в обмене липидов в живых организмах. Их используют для определения структуры фосфоглицеридов и места их локализации в мембранах. Распад и обновление фосфолипидов Известно, что молекулы белков расщепляются в тканях полностью. Поэтому для молекулы белков можно определить время обновления. Фосфолипиды также активно распадаются в тканях, но для каждой части молекулы время обновления различно. Например, время обновления фосфатной группы отличается от времени обновления 1-ацильной группы, и обусловлено это наличием ферментов, вызывающих частичный гидролиз фосфоли-пидов, вслед за которым снова может происходить их синтез (рис. 11.7). К сожалению, в настоящее время нет достаточно полных данных о фосфолипазном спектре той или иной ткани. Хорошо известно, что фосфолипаза A1атакует эфирную связь фосфолипидов в положении 1. Фосфолипаза А2 катализирует гидролиз эфирной связи в положении 2 гли-церофосфолипидов, в результате чего образуются свободная жирная кислота и лизофосфолипид (в случае фосфатидилхолина – лизолецитин), который реацилируется ацил-КоА при участии ацилтрансферазы. Фосфолипаза С атакует эфирную связь в положении 3, что заканчивается образованием 1,2-диглицерида и фосфорильного основания. Фосфолипаза D катализирует отщепление от фосфолипида азотистого основания. Долгое время считалось, что фосфолипаза D содержится только в растительных тканях. В последнее время ее удалось обнаружить в растворимой фракции мозга крысы, а затем в микросомах мозга и других органов, а в самое последнее время-в митохондриях печени крысы. Нет ясности в отношении фосфолипазы В. Возможно, что это-смесь ферментов, обладающих свойствами фосфолипаз А1и А2. Не исключено, что фосфолипаза В-фермент, действующий только на лизофосфолипид (например, лизолецитин), т.е. это лизофосфолипаза. Липотропные вещества - витаминоподобные вещества холин, инозит, биотин и а/к метионин являются липотропными веществами - т. е. участвуют в обмене жиров, и их основная функция состоит в предупреждении ненормального или чрезмерного накопления жира в печени. Они увеличивают производство лецитина, который сохраняет холестерин более растворимым, очищает печень и увеличивает сопротивляемость заболеваниям. Из-за того, что многие из нас потребляют слишком много жира, и большая его часть - это насыщенный жир, то в этой ситуации липотропные вещества крайне необходимы. Липотропные вещества необходимы и для того, чтобы сохранить здоровье, т. к. они помогают вилочковой железе вырабатывать антитела, стимулировать рост и активность фагоцитов (клеток, которые окружают и поглощают вирусы и микробы), помогают в разрушении чужеродной и патологической ткани. Биотин (коэнзим R или витамин Н). Принадлежит к витаминам группы В. Доза для взрослых 150-300 мкг. Биотин нужен для синтеза аскорбиновой кислоты, необходим для нормального метаболизма жиров и белка. Может синтезироваться кишечными бактериями. Сырые яйца препятствуют его усвоению организмом. Синергичен с витаминами А, В2, Вв, ниацином. Сохраняет кожу здоровой, предохраняет волосы от седины, облегчает боли в мышцах, уменьшает проявления экземы и дерматита. Источники: орехи, фрукты, пивные дрожжи, говяжья печень, молоко, почки и нешлифованный рис, желток яйца. Холин. Группа В, липотропное вещество. Действует вместе с инозином, способствуя утилизации жиров и холестерина. Одно из веществ, способных проникать через так называемый гематоэнцефалический барьер, который в норме защищает мозг от колебаний в пищевом рационе и поступает прямо в мозговые клетки для того, чтобы синтезировать химические соединения, способствующие укреплению памяти. Облегчает работу печени, помогает выводить яды и лекарства из организма. Источники: желток яйца, мозги, сердце, зеленые листовые овощи, дрожжи, печень, завязь пшеницы, лецитин. Фолиевая кислота (фолацин). Группа В; доза для взрослых составляет 400 мкг. Фолиевая кислота способствует метаболизму белков, важна для образования нуклеиновых кислот РНК и ДНК, необходима для деления клеток организма, усвоения сахара и аминокислот. Защищает от кишечных паразитов и пищевых отравлений, обеспечивает здоровый вид кожи, действует как анальгетик при болях, улучшает аппетит. Cодержится в темно-зеленых овощах с листьями, моркови, дрожжах, печени, яичном желтке, дыне, абрикосах, тыкве, авокадо, бобах, грубых пшеничной и ржаной муке. При варке разрушается. При систематическом употреблении алкоголя следует увеличить прием фолиевой кислоты. |
