химия в быту. Практикум учебнометодические рекомендации для студентов химикобиологического факультета
 Скачать 0.97 Mb. Скачать 0.97 Mb.
|
|
ОПРЕДЕЛЕНИЕ КИСЛОТНОГО ЧИСЛА ДЛЯ ГУБНОЙ ПОМАДЫ В состав губных помад входят воски растительного и животного происхождения, содержащие в своем составе эфиры и свободные кислоты. Но в губную помаду помимо восков дополнительно вводят карбоновые кислоты: в качестве консерванта (бензойная кислота), в качестве увлажнителя (сорбиновая кислота) и т. д. Но переизбыток кислот пагубно влияет на губы и полость рта. Кислотное число определяют методом нейтрализации свободных кислот раствором щелочи. ГОСТом Р 52342-2005 установлено кислотное число 15 мг/г КОН. ОБОРУДОВАНИЕ: 1. Бюретка 2. рН-метр 3. Стакан химический (100 мл.) – 1 шт. 4. Цилиндр мерный (50 мл.) – 1 шт. 5. Магнитная мешалка РЕАКТИВЫ: 1. Смесь толуол-спирт (1: 1) 2. Гидоксид калия спиртовой раствор (0,2 М) ХОД РАБОТЫ: В стакане взвесить 0,8 г. губной помады и добавляют 40 мл. смеси толуол-спирт. Содержимое стакана нагревают на водяной бане до полного растворения. После охлаждения реакционной смеси в стакан опускают электроды и титруют при постоянном перемешивании спиртовым раствором калия до рН 10,2-10,5. Кислотное число вычисляют по формуле: Х = (V · 11,2) : m V – объем 0,2 М раствора гидроксида калия, израсходованного на титрование кислоты, мл.; 11,2 – массовая концентрация гидроксида калия в 0,2 М растворе, мг/ мл; m – масса навески. ОПРЕДЕЛЕНИЕ ВОДОРОДНОГО ПОКАЗАТЕЛЯ (рН) ДЛЯ ЭМУЛЬСИОННЫХ, ЖИРОВЫХ, ТОНАЛЬНЫХ КРЕМОВ, СКРАБОВ Согласно ГОСТу Р 52341-2005 и Р 52343-2005 рН для тонального крема 5,0-8,5. Для других видов косметических изделий – 5,0-9,0. ОБОРУДОВАНИЕ: 1. рН-метр 2. Весы 3. Стакан химический (100 мл) – 1 шт. 4. Цилиндр мерный – 1 шт. 5. Термометр (100° С) – 1 шт. ХОД РАБОТЫ: 10 г тонального крема растворяют в 90 мл дистиллированной воды, нагревают при перемешивании до температуры 80° С до полного разрушения эмульсии. Охлаждают до комнатной температуры, отделяют водный слой и измеряют рН. За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определений. ОПРЕДЕЛЕНИЕ МАССОВОЙ ДОЛИ ВОДЫ И ЛЕТУЧИХ ВЕЩЕСТВ В ЭМУЛЬСИОННЫХ, ЖИРОВЫХ, ТОНАЛЬНЫХ КРЕМАХ И СКРАБАХ Летучие вещества – это так называемые отдушки. Эти вещества призванны обеспечивать стойкий аромат средства и «забивать», если необходимо, запах основы. Отдушки – это соединения синтетических и натуральных душистых веществ, сейчас чаще применяются синтетические, а раньше доминировали эфирные масла. Некоторые из синтетических душистых веществ, после периода активного применения (20-50 лет) были запрещены, или их использование было сильно ограничено из-за негативного действия на здоровье человека. К числу наиболее известных веществ такого рода относятся мускус-кетон и мускус-амбретт. По ГОСТу Р 52341-2005 массовая доля воды и летучих веществ должна быть от 10 % до 90 %. ОБОРУДОВАНИЕ: Стакан химический (100 мл.) – 1 шт. Сушильный шкаф Эксикатор Стеклянная палочка – 1 шт. РЕАКТИВЫ: Прокаленный речной песок ХОД РАБОТЫ: В стакан с 10 г. прокаленного песка взвешивают 5 г. анализируемого продукта. Стакан с продуктом после тщательного перемешивания содержимого помещают в сушильный шкаф и высушивают при температуре 103º С в течение 3 часов. По окончании высушивания стакан с продуктом охлаждают в эксикаторе в течение 30 минут. Массовую долю воды и летучих веществ (Х1) в процентах вычисляют по формуле: Х1 = (m2 – m3): (m2- m1) · 100% Массовую долю cухого вещества (Х2) в процентах вычисляют по формуле: Х2 = (m3 – m1): (m2- m1) · 100% m1 – масса стакана с песком, г; m2 – масса стакана с песком и продуктом до высушивания, г; m3 – масса стакана с песком и продуктом после высушивания, г. ОПРЕДЕЛЕНИЕ СТОЙКОСТИ К ВОДЕ ЖИДКОЙ ТУШИ ДЛЯ РЕСНИЦ Водостойкая тушь - ее основу составляют летучие растворители, различные виды воска животного происхождения (пчелиный воск), различные виды воска растительного происхождения (карнаубский воск), воск минерального происхождения (парафин), красители (оксид железа, ультрамарин и т. д.) и полимеров. Такая тушь не содержит водочувствительных ингредиентов, поэтому она имеет хорошую стойкость к слезам, поту или дождю. Неводостойкая тушь - ее основа: вода, мягкие поверхностно-активные вещества, различные виды воска животного, растительного и минерального происхождения, красители, утолщенные полимеры (арабская смола, генетически модифицированная целлюлоза) и консерванты. Эти туши стойки к действию слёз, но они легко удаляются с помощью мыла и воды. Неводостойкая тушь по своим свойствам похожа на краски на водной основе. ОБОРУДОВАНИЕ: 1. Предметное стекло – 1 шт. 2. Стакан химический (100 мл.) – 1 шт. 3. Термометр 4. Магнитная мешалка ХОД РАБОТЫ: На предметное стекло наносят тушь для ресниц. Через 10-20 мин., когда тушь высохнет предметное стекло помещают в стакан с водой температурой 18-20° С и перемешивают магнитной мешалкой. Тушь для ресниц не должна смываться с предметного стекла в течение 1 мин., тушь для ресниц влагоустойчивая – в течение 5 мин., тушь для ресниц водостойкая в течение 10 мин. ОПРЕДЕЛЕНИЕ КОЛЛОИДНОЙ СТАБИЛЬНОСТИ ЭМУЛЬСИОННЫХ КРЕМОВ И КРЕМОВ-ГЕЛЕЙ Коллоидная стабильность характеризует выделение масла из крема в процессе механического воздействия. Показатели коллоидной стабильности и термостабильности, регламентируются нормативными документами для косметических кремов. Вряд ли кого-либо сможет удовлетворить расслаивающийся крем. ОБОРУДОВАНИЕ: Центрифуга 2. Баня водяная 3. Весы 4. Термометр ХОД РАБОТЫ: Центрифужную пробирку на 2/3 заполняют кремом и взвешивают на весах. Пробирку помещают в водяную баню и выдерживают 20 мин. При температуре 42-45° С густые эмульсии, при температуре 22-25° С – жидкие эмульсии. Пробирку вынимают из воды, насухо вытирают с внешней стороны и устанавливают в гнездо центрифуги. Центрифугирование производят в течение 5 мин. при частоте вращения 100 с-1. Пробирку вынимают и определяют стабильность эмульсии. При стабильной эмульсии расслоение не наблюдается. Для частоты результата опыт повторить дважды. ОПРЕДЕЛЕНИЕ ТЯЖЕЛЫХ МЕТАЛЛОВ В КОСМЕТИЧЕСКИХ КРЕМАХ Цель работы: определение содержания следов тяжелых металлов в косметическом креме с помощью фотометрического метода. Методы определения следов металлов основаны на образование окрашенных комплексов между ионами металлов и органическими реагентами. Анализ проводят фотометрическим или спектрофотометрическим методом. В основе cпектрофотометрии лежит закон Ламберта - Бугера - Бэра в соответствии с которым оптическая плотность линейно зависти от длины оптического пути и концентрации определяемого вещества. Светофильтры фотоэлектроколориметра выбирают таким образом, чтобы максимум поглощения раствора соответствовал максимуму пропускания светофильтра. Оптическую плотность растворов измеряют в кюветах различной длины от 1 до 50мм. Чем выше интенсивность окраски раствора, тем тоньше должны кюветы. Подготовка крема к работе: Реактивы и оборудование: Кислота соляная, «х. ч.», разбавленная 1:1 Вода дистиллированная Фильтр беззольный, «синяя лента» 4 Стакан химический термостойкий Колба мерная (100мл) Цилиндр мерный Плитка электрическая Пипетка Подготовку образца к анализу проводят по следующей процедуре. Навеску анализируемого крема массой около 2г помещают в стакан вместимостью 100 мл, приливают 25 мл соляной кислоты, нагревают для отделения органического слоя. После охлаждения отфильтровывают через беззольный фильтр или отделяют на делительной воронке органическую часть. Осадок промывают 2-3 раза по 15 мл дистиллированной водой. Фильтрат собирают в мерную колбу на 100 мл и доводят объем до метки дистиллированной водой. Затем берут аликвотную часть (50 мл) для определения металлов в мерный цилиндр. Содержание металла (X, %) вычисляют по формуле: С — концентрация раствора реагента, найденная по графику; т — масса навески крема. ОПРЕДЕЛЕНИЕ МЕДИ При взаимодействии диэтилдитиокарбамата натрия с ионами меди образуется комплексное соединение меди (II), окрашенное в желто-коричневый цвет РЕАКТИВЫ: Аммиак водный (1:4) Днэтилдитиокарбамат натрия (0,1%; хранят в темном месте). Сегнетова соль (50%) Крахмала (0,25%) ОБОРУДОВАНИЕ: Пипетки. Фотоэлектроколориметр. Цилиндр. Мешалка магнитная. ХОД РАБОТЫ: Приготовление стандартного раствора соли меди 0,1965 г сульфата меди CuSO4∙5H2O (точная навеска) взвешивают на аналитических весах, переносят в мерную колбу вместимостью 500 мл, растворяют в небольшом количестве дистиллированной воды, доводят водой до метки и перемешивают. Полученный раствор разбавляют в 10 раз (Сu - 0,01 мг/мл). Приготовление эталонных растворов В мерную колбу на 100 мл наливают аликвотную часть анализируемого раствора, 1-2 мл НС1 (1:1), 1 мл сегнетовой соли, 5 мл NH3 (1:4), 1 мл крахмала, 5 мл трилона Б и 5 мл раствора ДЭДТК Na. доводят водой объем раствора до метки. Измеряют оптическую плотность растворов при длине волны 440 нм на фотоэлектроколориметре КФК-2 в кюветах толщиной 5см относительно раствора сравнения. В качестве раствора сравнения используют холостую пробу (все реактивы, кроме меди). По полученным данным строят калибровочный график. Анализ крема: В мерный цилиндр вместимостью 100 мл отбирают 50 мл кислотной вытяжки из косметического крема, нейтрализуют раствором аммиака по универсальному индикатору, добавляют 1 мл сегнетовой соли, 5 мл раствора аммиака, 1 мл раствора крахмала,5 мл раствора диэтилдитиокарбамата натрия. Объем доводят водой до метки и перемешивают. Через 10 мин измеряют величину оптической плотности в тех же условиях, что и для стандартных растворов. По полученной величине оптической плотности с помощью калибровочного графика находят содержание меди в анализируемом растворе в мг/л. Чувствительность метода составляет 0,1 мг/л. ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА Метод основан на образовании в кислой среде окрашенного в красный цвет нестойкого комплекса роданида железа (III). Fe3+ + 3KSCN Fe(SCN)3 + 3К+ РЕАКТИВЫ: Калий (аммоний) роданид (20%) Кислота соляная (1:1). Стандартный раствор железо-аммонийных квасцов, 10 мг Fe/л. Вода дистиллированная. ОБОРУДОВАНИЕ: Пипетка. Фотоэлектроколориметр. Цилиндр. Мешалка магнитная. ХОД РАБОТЫ: Приготовление стандартного раствора соли железа 0,864 г невыветренных железо-аммонийных квасцов NH4Fe(SO4)2 ∙ 12 H2O взвешивают на аналитических весах, переносят в колбу на 1000 мл, растворяют в небольшом количестве дистиллированной воды с добавлением 5 мл серной кислоты (плотность 1,84 г/мл), доводят водой до метки и перемешивают. Раствор содержит 0.1 г железа в I л. Приготовление эталонных растворов В мерные колбы емкостью по 50 мл последовательно вливают из пипетки 0,5;1,0; 2,0; 3,0; 4,0; 5,0 мл стандартного раствора соли железа, добавляют в каждую из колб по 1 мл НСl (1:1) и по 5 мл 10 %-го роданида аммония (или калия). Во всех колбах объем растворов доводят до метки и перемешивают. Измеряют оптическую плотность приготовленных эталонных растворов в кювете толщиной 1см при длине волны 400-450 им относительно раствора сравнения. По полученным данным строят калибровочный график. Анализ крема: В мерный цилиндр вместимостью 100 мл отбирают 50 мл кислотной вытяжки из косметического крема, добавляют 1 мл раствора соляной кислоты и 5 мл раствора роданида калия. Перемешивают и через 2 мин измеряют величину оптической плотности в тех же условиях, что и для стандартного раствора. V. АНАЛИЗ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ Цель: провести качественный и количественный анализ лекарственных препаратов, являющихся производными различных органических веществ. Исследуемый материал: таблетки анальгина, фурацилина, ацетилсалициловой кислоты, дротаверина гидрохлорида (но-шпа), папаверина гидрохлорида, кофцил (аскофен). 1. АНАЛИЗ ПРОИЗВОДНЫХ ПИРАЗОЛА РЕАКТИВЫ: Соляная кислота (0,01 N) Хлорид железа (р-р) Йодат калия (КIO3 р-р) Йод (0,1 N) ОБОРУДОВАНИЕ: Штатив с пробирками Спиртовка Колба для титрования (100 мл.) Ступка Воронка для фильтрования Бюретка Мерный пальчик ХОД РАБОТЫ: - 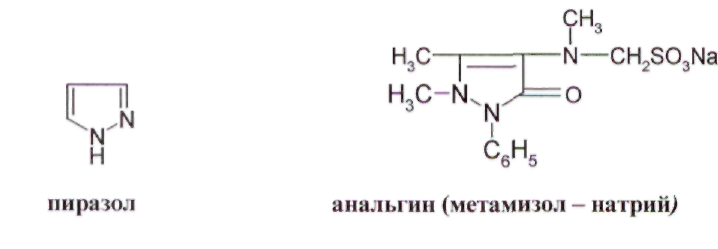 Качественные реакции подлинности препарата Около 0,05 г анальгина растворяют в 5 мл воды. Для проведения реакций берут 1 мл раствора. С раствором железа (III) хлорида. К раствору лекарственного вещества прибавляют 2–3 капли раствора железа (III) хлорида, перемешивают, после возникновения окрашивания добавляют 3 капли раствора хлороводородной кислоты и перемешивают. Наблюдают эффект реакции: анальгин – темно-синее окрашивание, переходящее в темно-зеленое, по- том – в желтое; С раствором серебра нитрата. К раствору лекарственного вещества прибавляют 5 капель раствора серебра нитрата и перемешивают. Наблюдают эффект реакции: анальгин – постепенно исчезающее сине-фиолетовое окрашивание, затем выпадает белый осадок переходящий в темный. С раствором натрия гексациано (III) феррата. К раствору лекарственного вещества прибавляют 5 капель реактива, 2 капли раствора хлороводородной кислоты, 1 каплю раствора железа (III) хлорида и перемешивают. Наблюдают эффект реакции. анальгин – синее окрашивание. С раствором натрия нитрита. К раствору лекарственного вещества прибавляют 1 каплю раствора натрия нитрита и 10 капель раствора серной кислоты. Наблюдают эффект реакции: анальгин – зеленовато-синее исчезающее окрашивание, выделение газа. 0,03-0,05 г лекарственного вещества помещают в фарфоровую чашку, прибавляют несколько кристалликов салициловой кислоты, 2-3 капли концентрированной серной кислоты; при слабом нагревании появляется красное окрашивание. Количественное определение анальгина 1. Навеску лекарственного препарата массой 0,05 г поместите в колбу для титрования, растворите в 5 мл воды, добавьте 1 мл 0,01 N раствора соляной кислоты и оттитруйте 0,1 N раствора йода осторожно по каплям, взбалтывая до появления розового окрашивания. 1 мл 0,1 моль/л раствора йода соответствует 0,01757 г анальгина C13H16N3NaO4S·H2O, которого должно быть от 0,475 до 0,525 г, считая на среднюю массу одной таблетки. М анальгина = 351,36 Содержание анальгина в процентах (Х) в препарате вычисляют по формуле: VKT 100 Х  = = а V- объём 0,1 N раствора йода, мл; К- поправочный коэффициент; Т-титр по определяемому веществу, г/мл (=0,008); а - масса навески лекарственного препарата, г. Содержание анальгина должно быть не менее 99,0 % и не более 101,0 %. 2 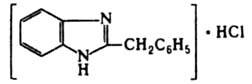 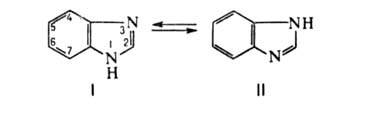 . АНАЛИЗ ПРОИЗВОДНЫХ ИМИДАЗОЛА И БЕНЗИМИДАЗОЛ . АНАЛИЗ ПРОИЗВОДНЫХ ИМИДАЗОЛА И БЕНЗИМИДАЗОЛбензимимидазол дибазол РЕАКТИВЫ: Нитрат кобальта (спирт. р-р) Соляная кислота (р-р) Йод (0,1 моль/л) Резорцин Этанол Натрия гидроксид (0,02 М) Фенолфталеин ОБОРУДОВАНИЕ: 1. Штатив с пробирками 2. Спиртовка 3. Колба для титрования (100 мл.) 4. Ступка 5. Чашка фарфоровая 6. Бюретка ХОД РАБОТЫ: Реакции подлинности Дибазол. К 0,03 г порошка прибавляют 1-2 капли 3 % спиртового раствора кобальта нитрата, появляется голубое окрашивание. Дибазол. 0,03 г порошка растворяют в 2 мл воды, прибавляют 2-3 капли Раствора хлороводородной кислоты, 3-4 капли раствора йода (0,1 моль/л) и взбалтывают; образуется красновато-серебристый осадок. Количественное определение Около 0,1 г лекарственного вещества растворяют в 2 мл этанола, предварительно нейтрализованного по фенолфталеину, прибавляют 1 мл воды и титруют 0,02 М раствором натрия гидроксида до розового окрашивания, устойчивого в течение 30 секунд (индикатор – фенолфталеин). Молекулярная масса дибазола 244,73. 1 мл 0,02 М раствора натрия гидроксида соответствует 0,004894 г C4H12N2·HCl (дибазола). 3. АНАЛИЗ ПРОИЗВОДНЫХ САЛИЦИЛОВОЙ КИСЛОТЫ 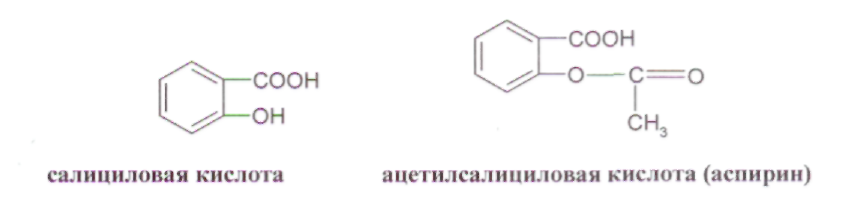 РЕАКТИВЫ: Хлорид железа (р-р) Серная кислота (конц., р-р) Формалин (р-р) Натрия гидроксид (0,1 N) Этиловый спирт Фенолфталеин ОБОРУДОВАНИЕ: Штатив с пробирками Спиртовка Колба для титрования (100 мл.) Ступка Чашка фарфоровая Бюретка ХОД РАБОТЫ: Реакции подлинности 0,2 г препарата помещают в фарфоровую чашку и прибавляют 0,5 мл концентрированной серной кислоты (осторожно!), перемешивают и добавляют 1-2 капли воды, ощущается запах уксусной кислоты. Затем добавляют 1-2 капли формалина; появляется розовое окрашивание: 0,5 г порошка растертых таблеток кипятят в течение 3 минут с 5 мл раствора гидроксида натрия, затем охлаждают и подкисляют разбавленной серной кислотой; выделяется белый кристаллический осадок. Раствор сливают в другую пробирку и добавляют к нему 2 мл спирта и 2 мл концентрированной серной кислоты: раствор имеет запах уксусно-этилового эфира. К полученному осадку добавляют раствор хлорида железа (III) - появляется фиолетовое окрашивание (в некоторых случаях вишневое). Количественное определение ацетилсалициловой кислоты Растворить 0,2 г ацетилсалициловой кислоты в 20 мл спирта, титровать 0,1М раствором NaOH, используя 0,1 мл раствора красителя фенолфталеина в качестве индикатора, до изменения окраски из бесцветной в малиновую. 1 мл 0,1М раствора NaOH эквивалентен 12,21 мг АСК. Содержание ацетилсалициловой кислоты в процентах (Х) в препарате вычисляют по формуле: VKTb 100 Х  = = а V-объем раствора гидроксида натрия (0,1М), пошедший на титрование, мл; а - навеска порошка растертых таблеток, взятых для анализа (0,2)г; Т-титр по определяемому веществу, г/мл; (0,009) К - поправочный коэффициент к концентрации титранта; b – средняя масса одной таблетки в граммах. 4. АНАЛИЗ ПРОИЗВОДНЫХ 5-НИТРОФУРАНА 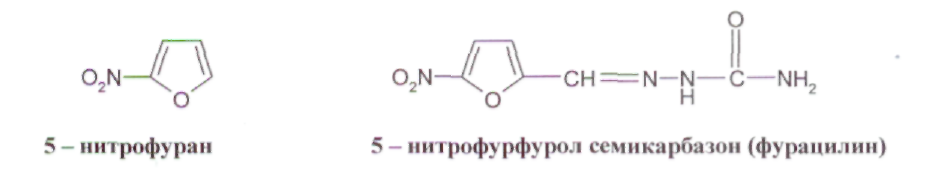 РЕАКТИВЫ: Калия гидроксид (спирт. р-р) Натрия гидроксид (0,1 N) Ацетон Хлорид натрия (тв.) Йод (0,01 моль/л) Кислота серная (р-р) Тиосульфат натрия (0,01 моль/л) Крахмал ОБОРУДОВАНИЕ: Штатив с пробирками Мерный пальчик Колба мерная (100 мл.) Бюретка Колба для титрования (50 мл.) – 2 шт. Весы Баня водяная ХОД РАБОТЫ: Реакции подлинности раствор препарата в 10 % растворе натрия гидроксида нагревают до кипения, в пары вносят влажную лакмусовую бумагу. Обнаруживают выделяющийся аммиак по посинению красной лакмусовой бумаги и по запаху. 0,01 г препарата растворяют в смеси 5 мл воды и 5 мл раствора гидроксида натрия, появляется оранжево - желтое окрашивание. 0,02 г препарата растворяют в 2 мл ацетона, прибавляют 2 капли 0,1 N раствора гидроксида калия в 50 % этиловом спирте. Наблюдается темно-красное окрашивание. Количественное определение фурацилина Около 0,02 г препарата помещают в мерную колбу вместимостью 100 мл, прибавляют 1 г хлорида натрия (для лучшей растворимости), 70 мл воды и растворяют при нагревании до 70-80 °С на водяной бане. Охлажденный раствор доводят водой до метки и перемешивают. 5 мл раствора йода (0,01 моль/л), помещают в колбу вместимостью 50 мл с притертой пробкой, прибавляют 0,1 мл (2 капли) раствора NaOH и вносят 5 мл приготовленного раствора фурацилина. Оставляют на 1-2 минуты в темном месте. Затем к раствору прибавляют 2 мл разбавленной H2SО4, и выделившийся йод титруют раствором натрия тиосульфата (0,01 моль/л, 1/2 М). Индикатор - крахмал. 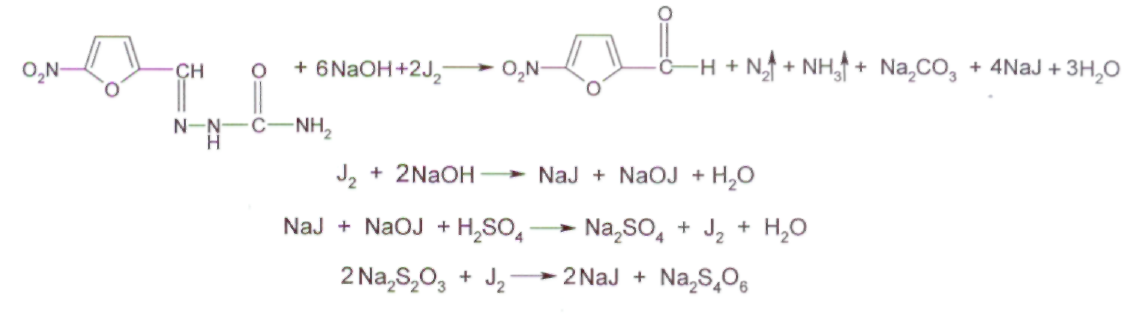 М фурацилина = 198,14 1 мл 0,01 н раствора йода или ½ объема тиосульфата натрия (см. уравнение реакции) соответствует 0,0004954 г фурацилина, которого в препарате должно быть не менее 97,5 %. Содержание фурацилина (X, %) вычисляют по формуле: 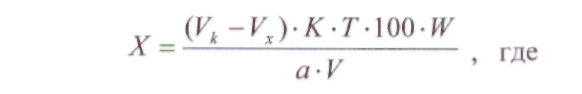 Vk – объем р-ра Na2S2О3, пошедшего на контр. титрование, мл; Vх – объем р-ра Na2S2О3, на титрование рабочего раствора, мл; а - навеска фурацилина, г; Т-титр по определяемому веществу, г/мл; (0.0002) К - поправочный коэффициент 0,01 М р-ра Na2S2О3; W— объем мерной колбы (100 мл); V- объем аликвоты (5 мл) 5. АНАЛИЗ ПРОИЗВОДНЫХ БЕНЗИЛИЗОХИНОЛИНА 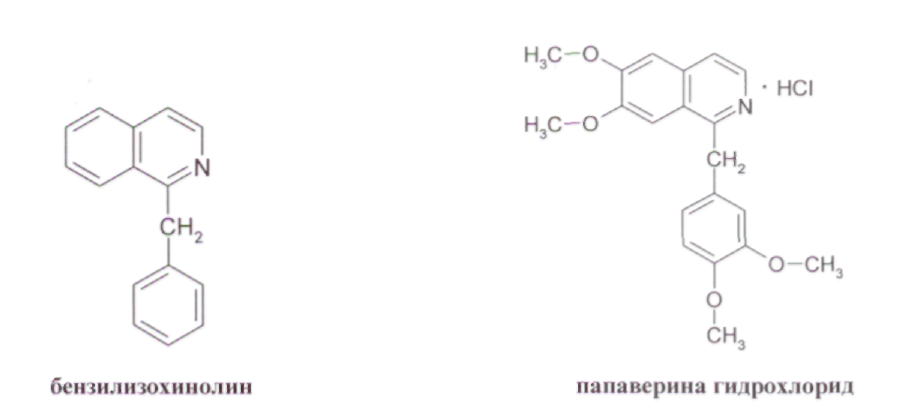 РЕАКТИВЫ: Кислота азотная (конц.) Реактив Марки Натрия гидроксид (0,02 N) Реактив Фреде Ацетат натрия (р-р) Этиловый спирт Нитрат серебра (р-р) Фенолфталеин ОБОРУДОВАНИЕ: Штатив с пробирками Мерный пальчик Бюретка Колба для титрования (50 мл.) – 2 шт. Баня водяная ХОД РАБОТЫ: Реакции подлинности 0,01 г препарата смачивают 1 каплей концентрированной азотной кислоты, наблюдается желтое окрашивание, переходящее в оранжевое при нагревании на водяной бане; 0,01 г порошка прибавляют 1-2 капли раствора формальдегида в концентрированной серной кислоте (реактив Марки) и слабо нагревают на водяной бане. Появляется фиолетовое окрашивание. К 0,01 г порошка прибавляют 3-5 капель раствора аммония молибдата в концентрированной серной кислоте (реактив Фреде). Появляется зеленое окрашивание. 0,05 г препарата растворяют в 2-3 мл воды при нагревании до 60°С прибавляют 1 мл раствора натрия ацетата, при стоянии образуются кристаллы основания папаверина; Фильтрат дает реакцию на хлориды с раствором серебра в азотной кислоте; Количественное определение папаверина гидрохлорида 0,15 г порошка прибавляют 1 мл свежепрокипяченной охлажденной воды, 2 мл 96 % этанола, нейтрализованного по фенолфталеину, 2-3 капли раствора фенолфталеина и титруют раствором натрия гидроксида (0,02 моль/л) до розового окрашивания. М папаверина гидрохлорида = 375,86 1 мл 0,02 моль/л раствора гидроксида натрия соответствует 0,007517 г. папаверина гидрохлорида С20Н21NO4·НСl Расчет содержания папаверина гидрохлорида (X, г) в таблетках проводят по формуле: VKTb Х  = = а V- объем раствора гидроксида натрия (0,1 М ), пошедший на титрование, мл; а- навеска порошка растертых таблеток, взятая для анализа (0,15 г); b- средняя масса одной таблетки в граммах; К- поправочный коэффициент к концентрации титранта; Т - титр стандартного раствора по определяемому веществу; 6. АНАЛИЗЛЕКАРСТВЕННЫХ ФОРМ Лекарственная форма: кофицил, аскофен таблетки Состав лекарственной формы КОФИЦИЛ: Ацетилсалициловая кислота – 0,3 г. Парацетамол – 0,1 г. Кофеин – 0,05 г. Состав лекарственной формы АСКОФЕН: Ацетилсалициловая кислота – 0,2 г. Парацетамол – 0,2 г. Кофеин – 0,04 г. РЕАКТИВЫ: Хлорид железа (III) (р-р) Кислота соляная (конц., 0,1 н) Кислота серная (конц.) Натрия гидроксид (р-р) Аммиак (10%) Пероксид водорода (5%) Йод (0,1N) Дихромат калия (р-р) Метилоранж Фенолфталеин Диэтиловый эфир Этиловый спирт ОБОРУДОВАНИЕ: Штатив с пробирками Мерный пальчик Бюретка Колба для титрования (100 мл.) – 2 шт. Мерная колба (50 мл.) Обратный холодильник Ступка ХОД РАБОТЫ: Реакции подлинности Ацетилсалициловая кислота): 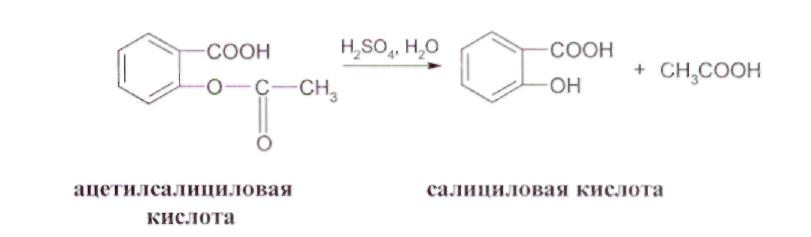 1. 0,5 г порошка растертых таблеток кипятят в течение 3 минут с 5 мл раствора гидроксида натрия, затем охлаждают и подкисляют разбавленной серной кислотой; выделяется белый кристаллический осадок. Раствор сливают в другую пробирку и добавляют к нему 2 мл спирта и 2 мл концентрированной серной кислоты: раствор имеет запах уксусно-этилового эфира. К полученному осадку добавляют раствор хлорида железа (III) - появляется фиолетовое окрашивание (в некоторых случаях вишневое). Кофеин (1,3,7' - Триметилксантин): 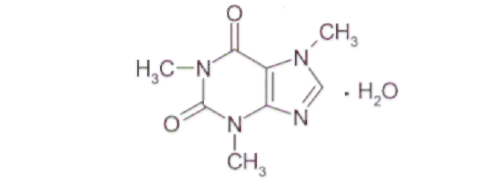 1. 0,01 г лекарственного препарата помещают в фарфоровую чашку, прибавляют 10 капель разбавленной соляной кислоты, 10 капель пероксида водорода (5%) и выпаривают на водяной бане досуха. Остаток смачивают 1-2 каплями раствора аммиака; появляется пурпурно - красное окрашивание (мурексидная проба). 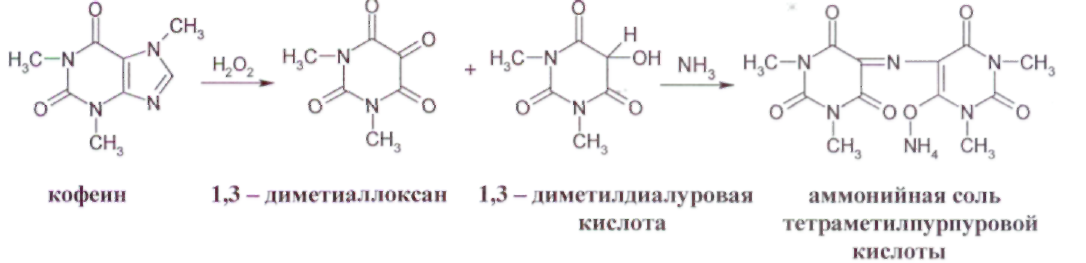 2. 0,05 г лекарственного препарата растворяют в 5 мл горячей воды, охлаждают, добавляют 10 капель 0,1 N раствора йода; не должно появиться ни осадка, ни помутнения. При прибавлении нескольких капель разбавленной соляной кислоты образуется бурый осадок растворимый в избытке щелочи. Парацетамол (n.- гидроксифенилацетамид): 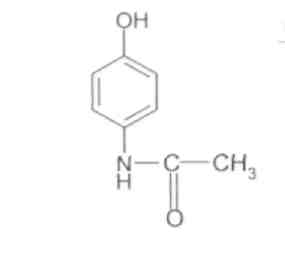 1. 0,05 г лекарственного вещества кипятят с 1 мл концентрированной соляной кислоты в течение 1 минуты, раствор разбавляют 10 мл воды и охлаждают. К фильтрату прибавляют 1 каплю раствора дихромата калия; раствор окрашивается в фиолетовый цвет. 2. 0,1 г лекарственного препарата нагревают с 2 мл концентрированной серной кислоты до начала кипения (избегая обугливания) и охлаждают. К смеси прибавляют 2 мл воды и вновь нагревают. Ощущается запах уксусноэтилового эфира. Количественное определение: 1. Ацетилсалициловая кислота Растворить 0,2 г ацетилсалициловой кислоты в 20 мл спирта, титровать 0,1М раствором NaOH, используя 0,1 мл раствора красителя фенолфталеина в качестве индикатора, до изменения окраски из бесцветной в малиновую. 1 мл 0,1 М раствора NaOH эквивалентен 12,21 мг С7Н6О2. 2. Кофеин К 0,05 г порошка добавляют 2-3 мл воды, 3-4 мл эфира и титруют 0,1 н раствором соляной кислоты до розового окрашивания водного слоя (индикатор – метиловый оранжевый). 1 мл 0,1 N раствора соляной кислоты соответствует 0,0240 г кофеина. 3. Парацетомол Около 0,3 г (точная навеска) порошка растертых таблеток помещают в коническую колбу емкостью 100 мл, прибавляют 20 мл разведенной соляной кислоты и кипятят с обратным холодильником в течение 30 минут. Раствор охлаждают до 15-20º С и переносят в мерную колбу емкостью 50 мл, доводят объем раствора водой до метки, перемешивают и фильтруют в сухую колбу. 25 мл фильтрата переносят в коническую колбу, прибавляют 1 г бромида калия, 3 капли раствора тропеолина 00 и 2 капли раствора метиленового синего и титруют 0,1 М раствором нитрита натрия, прибавляя по 1 мл через 1 минуту, а в конце титрования (за 1 мл до эквивалентного количества) по 0,1 мл через 2 минуты. Конец титрования определяют по переходу красновато-фиолетовой окраски в голубовато-зеленую. 1 мл 0,1 М раствора нитрита натрия соответствует 0,01792 г С8H9NО2. ПРИЛОЖЕНИЕ 1. Приготовление рабочих градуировочных растворов фтористого натрия концентрацией 1·10-3 - 1·10-5 моль/дм3 Для приготовления 1·10-2 моль/дм3 раствора фтористого натрия 10 мл стандартного раствора (1·10-1) разбавляют дистиллированной водой до 100 мл в мерной колбе. Этот раствор имеет значение pF = 2 Для приготовления 1·10-3моль/дм3 раствора фтористого натрия 10 мл основного стандартного раствора разбавляют дистиллированной водой до 100 мл в мерной колбе. Этот раствор имеет значение рF = 3 (массовую концентрацию фторид-иона 19 мг/дм3). 1· 104 моль/дм3 раствор фтористого натрия готовят разбавлением 10 см3 1·103 моль/дм3 раствора до 100 см3 дистиллированной водой в мерной колбе. Этот раствор имеет значение рF = 4 (массовую концентрацию фторид-иона 1,9 мг/дм3). Для приготовления 1·10-5 моль/дм3 раствора фтористого натрия 1 см3 1·10-3моль/дм3 раствора разбавляют дистиллированной водой до 100 см3 в мерной колбе. Данный раствор имеет значение pF=5 (массовую концентрацию фторид-иона 0,19 мг/дм3). Все рабочие градуировочные растворы готовят в день анализа и хранят в полиэтиленовой посуде. 2. Градуировка иономера Калибровку электрода рекомендуется проводить в растворах фтористого натрия известной концентрации. При построении калибровочного графика или настройке иономера следует пользоваться зависимостью логарифма активности ионов фтора от концентрации фтористого натрия, приведенной в таблице 1 Таблица 1
Калибровочные растворы приготавливают последовательным десятикратным' разбавлением исходного раствора 0,1 М NaF дистиллированной водой. Для его приготовления следует растворить 4,20 г фторида натрия в 1 дм дистиллированной воды. Перед измерениями следует промыть электрод дистиллированной водой в течение 10 - 15 мин. с двукратной сменой воды. Измерения целесообразно проводить, начиная с меньшем концентрации ионов фтора. Измерения потенциала электрода следует проводить относительно хлорсеребряного электрода с электролитическим ключом («двойным ключом»), заполненным 0,1 М раствором сульфата магния. Примечание. Для получения более устойчивых результатов следует проводить калибровку и измерения с добавлением фонового раствора. В этом случае контрольные растворы следует разбавлять дистиллированной водой и буферным раствором для регулирования ионной силы (БРОИС) так, чтобы объем БРОИС составил половину общего объема контрольного раствора. ( Состав БРОИС (г. на 1 дм3) - NaС1 - 58,5, СН3СООН - 15,0, СНзСООNа·ЗН2О -102,0; лимоннокислый натрий - 0,26.). Калибровочный график строят в координатах потенциал - логарифм концентрации ионов фтора (Е – 1gCF). При длительных перерывах в работе электрод следует промыть дистиллированной водой, осушить фильтровальной бумагой и надеть защитный колпачок. При последующем введении электрода в эксплуатацию следует повторить операции. Не допускается механическое повреждение рабочей кристаллической мембраны электрода и использование электрода в растворах, содержащих вещества, образующие осадки и пленки на поверхности электрода. 3. Приготовление раствора массовой концентрации Р2О5 1 мг/мл 4.00 – 5,00 г однозамешенного фосфорнокислого калия высушивают и сушильном шкафу при температуре 100-105° С в течение 2 ч. затем охлаждают в эксикаторе в течение 40-50 мин. После этого взвешивают навеску однозамещенного фосфорнокислого калия массой 1.9170 г и помешают в мерную колбу вместимостью 1000 мл. доводят объем раствора водой до метки и перемешивают. 1 мл приготовленного раствора содержит 1 мг Р2О5. Раствор хранят в полиэтиленовой посуде. Раствор пригоден в течение 1 года. посуде Раствор пригоден в течение 1 года 4. Приготовление раствора массовой концентрации Р2О5 0,25 мг/мл Пипеткой отбирают 25 мл раствора с концентрацией 1 мг/мл помешают в мерную колбу вместимостью 100 мл, доводят объем раствора водой до метки и перемешивают. 1 мл приготовленного раствора содержит 0,25 мг Р2О5. Раствор хранят в полиэтиленовой посуде. Раствор пригоден в течение 2 месяцев 5. Приготовление молибденового реактива 20 г молибденовокислого аммония растворяют в 400 мл воды, нагретой до 50° С. 1.00 г ванадиевокислого аммония растворяют в 300 мл воды, нагретой до 80° С и добавляют 20 мл азотной кислоты. После охлаждения растворов до комнатной температуры их переносят в мерную колбу вместимостью 1000 мл, добавляют 120 мл азотной кислоты, перемешивают, доводят объем раствора водой до метки и снова перемешивают. При необходимости фильтруют. Хранят в банке из темного стекла. Раствор пригоден в течение 20 сут. 6. Построение градуировочного графика для определения фосфатов Для построения градуировочного графика приготовить растворы сравнения. Для этого в семь мерных колб, объемом 100 мл последовательно вносят из бюретки 1, 2, 3, 4, 5, 6, 7 мл раствора однозамещенного фосфорнокислого калия. Добавляют 50 мл воды, 25 мл молибденового реактива и доводят объем раствора водой до метки. Растворы тщательно перемешивают. Одновременно готовят контрольный раствор, не содержащий Р2О5. Через 10 мин. измеряют оптическую плотность приготовленных растворов по отношению к контрольному раствору на спектрофотометре при длине волны 430 – 450 нм в кюветах с толщиной поглощающего свет слоя 30 мм. По полученным данным строят градуировочный график, откладывая по оси абсцисс массу Р2О5 в миллиграммах раствора сравнения, а по оси ординат – соответствующие им значения оптической плотности. 6. Приготовление стандартного раствора Na2SiO3 Навеску силиката натрия с массой SiО2 около 0,1 г, переносят в мерную колбу вместиместью 500 мл, растворяют в воде и доводят объем раствора водой до метки. Раствор не должен содержать взвешенного твердого вещества. Полученный раствор следует хранить в полиэтиленовой посуде 7. Построение градуировочного графика для определения силикатов Для построения градуировочного графика готовят растворы сравнения. Для этого в 7 мерных колб, вместимостыо 100 мл каждая последовательно вносят из бюретки 1; 2; 3: 4; 5: 6; 7 мл стандартного раствора силиката натрия, добавляют 50 мл. дистиллированной воды, добавляют 1 мл раствора серной кислоты и 5 мл 10%-ного раствора щавелевой кислоты и доводят объем раствора до метки 100 мл. Параллельно готовят контрольный раствор (50 мл воды, 1 мл раствора серной кислоты и 5 мл 10 %-ного раствора молибдената аммония и доводят объем раствора водой до метки). Оптическую плотность растворов сравнения измеряют на фотоэлектроколориметре с синим светофильтром при длине волны 380-410 нм в кюветах с толщиной поглощающего свет слоя 30 мм через 5 мин, считая с момента разбавления. 8. Приготовление раствора смеси щавелевой кислоты и сернокислого марганца В мерной колбе, вместимостью 100 мл, растворяют 10 г щавелевой кислоты и 1 г сернокислого марганца в 60 мл воды при 60° С, добавляют 20 мл раствора серном кислоты, доводят объем раствора водой до метки. 9. Приготовление жесткой воды 0,107 г сульфата магния и 0,194 г хлорида кальция (в пересчете на безводные соли) растворить в дистиллированной воде в мерной колбе, вместимостью 1000 мл и тщательно перемешать. 10. Построение градуировочного графика для определения сульфатов В мерные колбы на 50 мл. под номерами от 1до 8 прилить 0,02 М раствор сульфата натрия: 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8 мл и добавить в каждую по 5 мл 0,5 М раствора хлорида бария. Полученные растворы разбавить дистиллированной водой до метки. Содержимое колб перемешать и через 15 мин. после образования суспензии измерить оптическую плотность растворов на фотоколориметре. Использовать кюветы длиной 5 см; длину волны 590 нм.; раствор сравнения – вода. Построить калибровочную кривую (зависимость оптической плотности (D)от концентрации (С). 11. Приготовление аммиачного буферного раствора 10 г хлорида аммония растворить в небольшом количестве дистиллированной воды, добавить 50 мл раствора аммиака (ω=25%) и доводят дистиллированной водой до метки 500 мл. Хранить в плотно закрытой склянке. СОСТАВ ЗУБНЫХ ПАСТ Зубная паста Жемчуг ПРОИЗВОДИТЕЛЬ: ОАО Невская косметика СОСТАВ: 1 туба содержит: вода, сорбитол, глицерин, диоксид кремния абразивный, диоксид кремния загущающий, ПЭГ-ая смола, глицерофосфат кальция, ароматизатор, натрия монофторфосфат, натрий фосфорнокислый, натрия метилпарабен, натрия сахарин, натрия пропилпарабен, триклозан, диоксид титана. Зубная паста Колгейт тотал ПРОИЗВОДИТЕЛЬ: Colgate - Palmolive, США. СОСТАВ: 1 туба содержит: вода, осажденный карбонат кальция, сорбитол, оксид алюминия, лаурилсульфат натрия, монофторфосфат натрия и фторид натрия – 0,32-0,1%, силикат натрия, соединение триклозана с сополимером PVM/MA – триклогард, каррагенан, натриевая соль КМЦ, сахаринат натрия, метилпарабен, экстракты мелисы, фенхеля, мяты, красители; в тубе 50 и 100 мл. Зубная паста Лакалют Сенситив ПРОИЗВОДИТЕЛЬ: ТАЙСС НТУРВАРЕН ГмбХ, ГЕРМАНИЯ. СОСТАВ: 1 туба содержит: вода, сорбитол, кремния диоксид, кремний каллоидный, ПЭГ-32, гидроксиэтилцеллюлоза, полоксамер 188, кокамидопропил бетаин, олафлур, фторид натрия, лактат алюминия, титана диоксид, аллантоин, натрия сахаринат, хлоргексидина биглюконат, ароматизатор, бисаболол, сахаринат натрия. Зубная паста MACLINS ПРОИЗВОДИТЕЛЬ: Smith Kline Beecham, Великобритания. СОСТАВ: 1 туба содержит: антибактериальный реагент триклозан, монофторфосфат натрия (0,8%), глицерофосфат кальция (0,13%). Зубная паста AQUAFRESH ПРОИЗВОДИТЕЛЬ: Smith Kline Beecham, Великобритания. СОСТАВ: 1 туба содержит: монофторфосфат натрия (0,75%), фторид натрия (0,0013%) и глицерофосфат кальция (0,13%). В состав пасты также входит небольшое количество коллоидного диоксида кремния и бензойной кислоты. Зубная паста 32-НОРМА НЕЖНАЯ МЯТА ПРОИЗВОДИТЕЛЬ: ОАО Концерн «КАЛИНА» (Россия) СОСТАВ: 1 туба содержит: диоксид кремния, сорбитол, натрий лаурилсульфат, экстракт шалфея, натрий карбоксиметилцеллюлоза, натрия монофторфосфат, натриевая соль метилпарабена, натрия сахаринат, 2-бром-2-нитропропан-1,3-диол, диоксид титана, фтор. Зубная паста SENSODYNE ПРОИЗВОДИТЕЛЬ: ГлаксоСмитКляйн Консьюмер Хелскер Великобритания. СОСТАВ: вода, сорбит, глицерин, диоксид кремния, пирофосфат калия, кокамидопропилбетаин (ПАВ), хлорид калия, фторид натрия, искусственный подсластитель, диоксид титана. СОСТАВ СТИРАЛЬНЫХ ПОРОШКОВСтиральный порошок TIDEПРОИЗВОДИТЕЛЬ: Procter&Gamble, произведено в России.СОСТАВ: 15-30% - анионные ПАВ, фосфаты, менее 5% - катионные ПАВ, неионогенные ПАВ, поликарбосиликаты, кислородсодержащий отбеливатель, энзимы, оптический отбеливатель. Стиральный порошок ARIELl AUTOMAT ПРОИЗВОДИТЕЛЬ: Procter&Gamble, произведено в России. СОСТАВ: менее 5% - катионные и неионогенные ПАВ, поликарбокислоты, фосфонаты, 5-15% - анионные ПАВ, кислородсодержащие отбеливатели, 15-30% - фосфаты. Дополнительно: энзимы, оптический отбеливатель. Стиральный порошок LANZA ПРОИЗВОДИТЕЛЬ: Reckitt Benckiser (Польша) СОСТАВ: ПАВ, смягчители воды, СМС, энзимы, оптические отбеливатели, отдушка. Стиральный порошок DOSIA ПРОИЗВОДИТЕЛЬ: Reckitt Benckiser (Польша) СОСТАВ: анионные и неионогенные ПАВ; фосфаты; сульфаты; силикаты; сода; полимеры; ферменты; оптический отбеливатель; КМЦ; отдушка; пеногаситель. Стиральный порошок PERSIL POWER PEARLS AUTOMATПРОИЗВОДИТЕЛЬ: торговая марка - Henkel, произведено ОАО "Эра" (Тосно). СОСТАВ: АПАВ, НПАВ, кислородсодержащий отбеливатель, силикат, фосфаты, фосфонаты, сода, биодобавки-энзимы, оптический отбеливатель, полимеры-антиресорбенты, отдушка, сульфат натрия, цветные активные гранулы, пеногаситель, активатор отбеливания. Стиральный порошок ПЕМОС БИО STANDART SYSTEM ПРОИЗВОДИТЕЛЬ: ОАО "Пемос" (Пермь). СОСТАВ: ПАВ, карбонаты, силикат, сульфат, энзимы, полимеры, оптический отбеливатель, отдушка. Стиральный порошок BIMAX UNIVERSALПРОИЗВОДИТЕЛЬ: "Нэфис Косметикс" (Казань). СОСТАВ:ПАВ, комплексообразователи, антиресорбенты, силикаты, перборат натрия, активатор, энзимы, оптические отбеливатели, отдушка, сульфат натрия и другие добавки. Стиральный порошок E-AUTOMATПРОИЗВОДИТЕЛЬ: Cussons International (Польша).СОСТАВ: неионогенные и анионные ПАВ, пербрат натрия, фосфаты, сульфат, карбонаты, ТАЭД, силикат, антисорбенты, пеногаситель, биодобавки энзимы, оптический отбеливатель, отдушка. Стиральный порошок SORTI СУПЕР ЭКОНОМ БИО ПРОИЗВОДИТЕЛЬ: ОАО "Нэфис Косметикс" (Казань). СОСТАВ: ПАВ, комплексообразователи, карбоксиметилцеллюлоза, силикаты, сода кальцинированная, натрий двууглекислый, энзимы, оптические отбеливатели, отдушка, сульфат натрия и другие добавки. Стиральный порошок БИОЛАН СТАНДАРТПРОИЗВОДИТЕЛЬ: Московский завод СМС. СОСТАВ: АПАВ, НПАВ, сульфаты, силикаты, антикоррозийные вещества, антиресорбенты, оптические отбеливатели, энзимы, комплексообразователи, парфюмерная отдушка. |
