Аналитическая химия. !курс лекций 5 семестр. Предмет аналитической химии
 Скачать 4.18 Mb. Скачать 4.18 Mb.
|
ГЛАВА 2 2.1. Аналитические реакции Химические методы обнаружения веществ основаны на проведении аналитических реакций. Аналитическиминазывают химические реакции, результат которых несёт определённую аналитическую информацию, например, реакции, сопровождающиеся выпадением осадка, выделением газа, появлением запаха, изменением окраски, образованием характерных кристаллов. 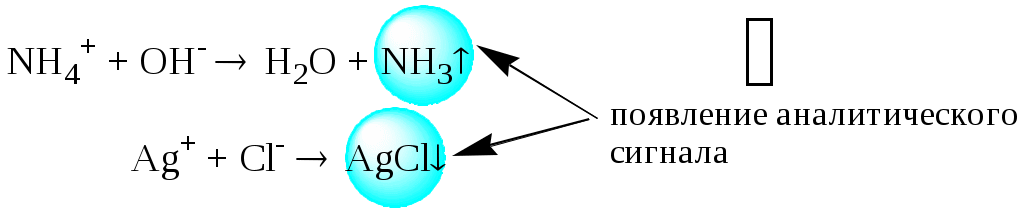 Наиболее важными характеристиками аналитических реакций является избирательность и предел обнаружения. В зависимости от избирательности (числа веществ, вступающих в данную реакцию или взаимодействующих с данным реагентом) аналитические реакции и вызывающие их реагенты бывают:  Предел обнаружения (mmin, P или Сmin, P) - наименьшая масса или концентрация вещества, которую с заданной доверительной вероятностью P можно отличить от сигнала контрольного опыта (более подробно см. главу 10). 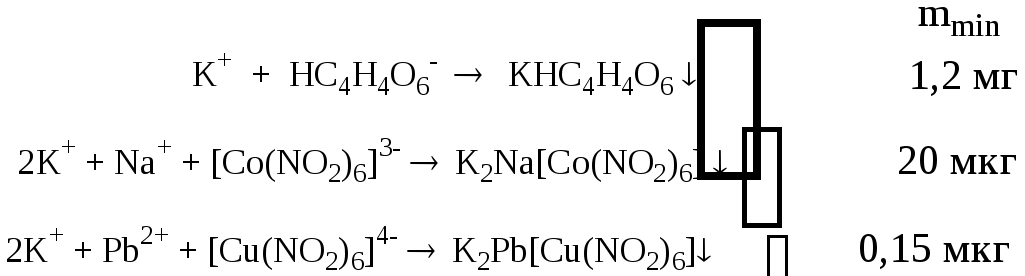 2.2. Систематический и дробный анализ Обнаружение элементов при совместном присутствии можно проводить дробным и систематическим методами анализа. Систематическим называется метод качественного анализа, основанный на разделении смеси ионов с помощью групповых реагентов на группы и подгруппы и последующем обнаружении ионов в пределах этих подгрупп с помощью селективных реакций. Название систематических методов определяется применяемыми групповыми реагентами. Известны систематические методы анализа: сероводородный, кислотно-основный, аммиачно-фосфатный. Каждый систематический метод анализа имеет свою групповую аналитическую классификацию. Недостатком всех систематических методов анализа является необходимость проведения большого числа операций, длительность, громоздкость, значительные потери обнаруживаемых ионов и т.д. Дробным называется метод качественного анализа, предполагающий обнаружение каждого иона в присутствии других с использованием специфических реакций либо проведение реакций в условиях, исключающих влияние других ионов. Обычно обнаружение ионов дробным методом проводят по следующей схеме – вначале устраняют влияние мешающих ионов, затем обнаруживают искомый ион с помощью селективной реакции. 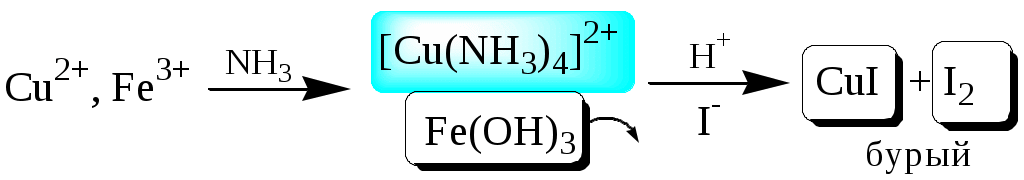 Устранение мешающего влияния ионов может быть проведено двумя путями 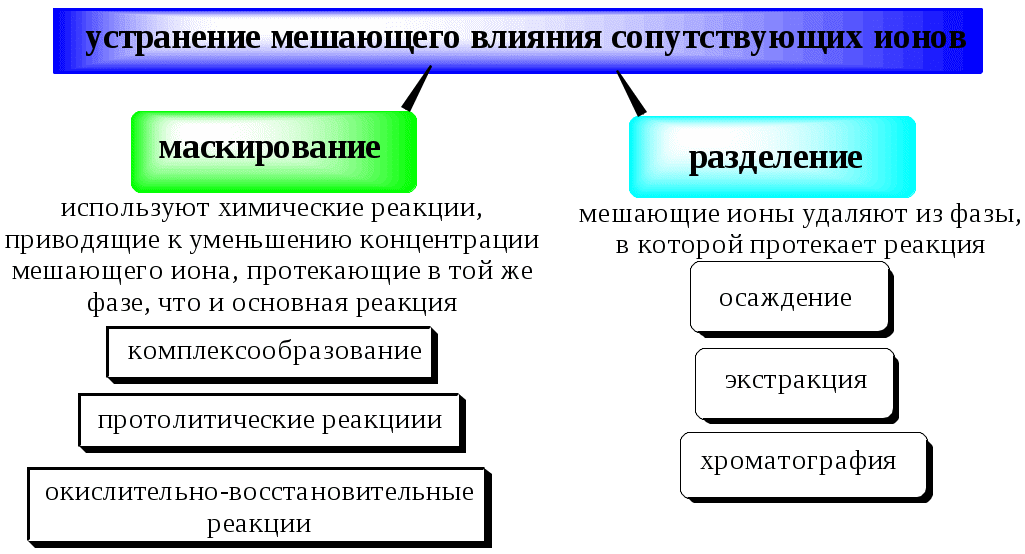 Например комплексообразование 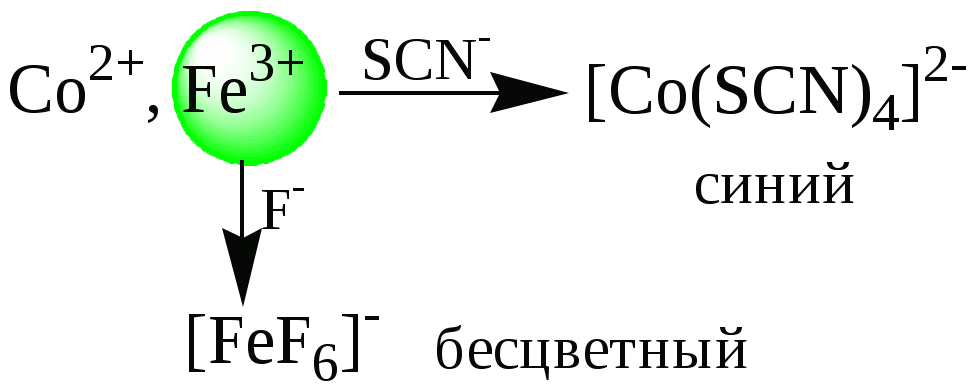 изменение рН среды окислительно-восстановительные реакции 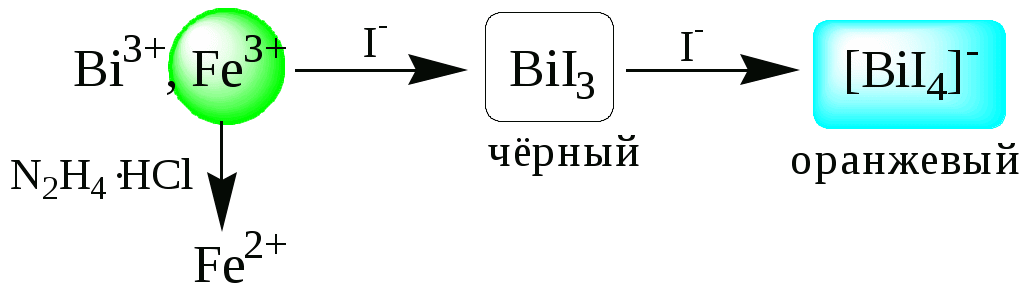 осаждение 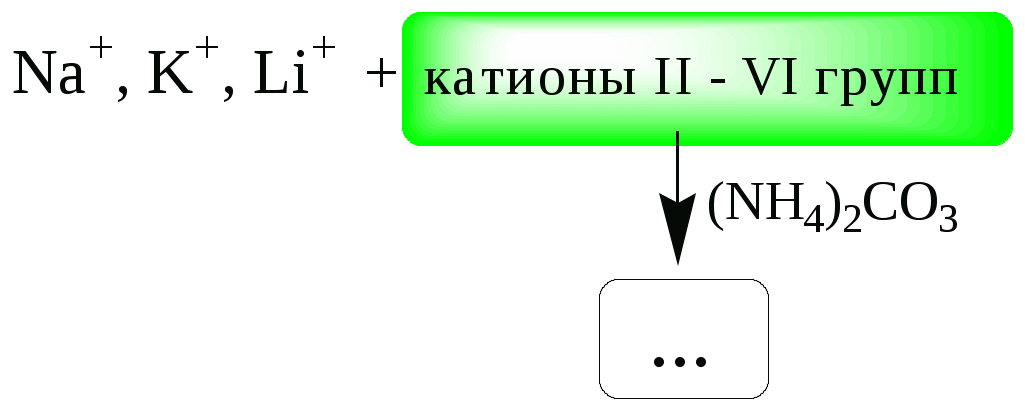 экстракция 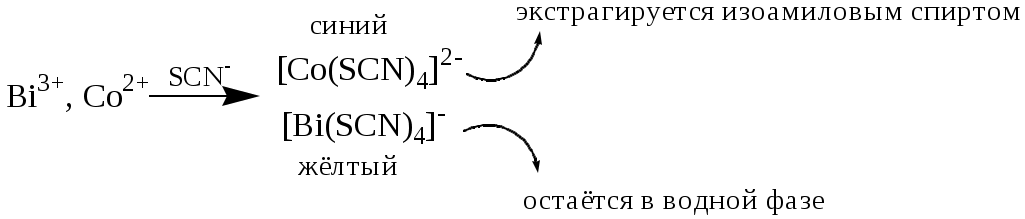 2.3. Общая характеристика, классификация и способы обнаружения катионов Согласно кислотно-основной классификации катионы в зависимости от их отношения к растворам HCl, H2SO4, NaOH (или KOH) и NH3 разделяют на 6 групп. Каждая из групп, за исключением первой, имеет свой групповой реагент. 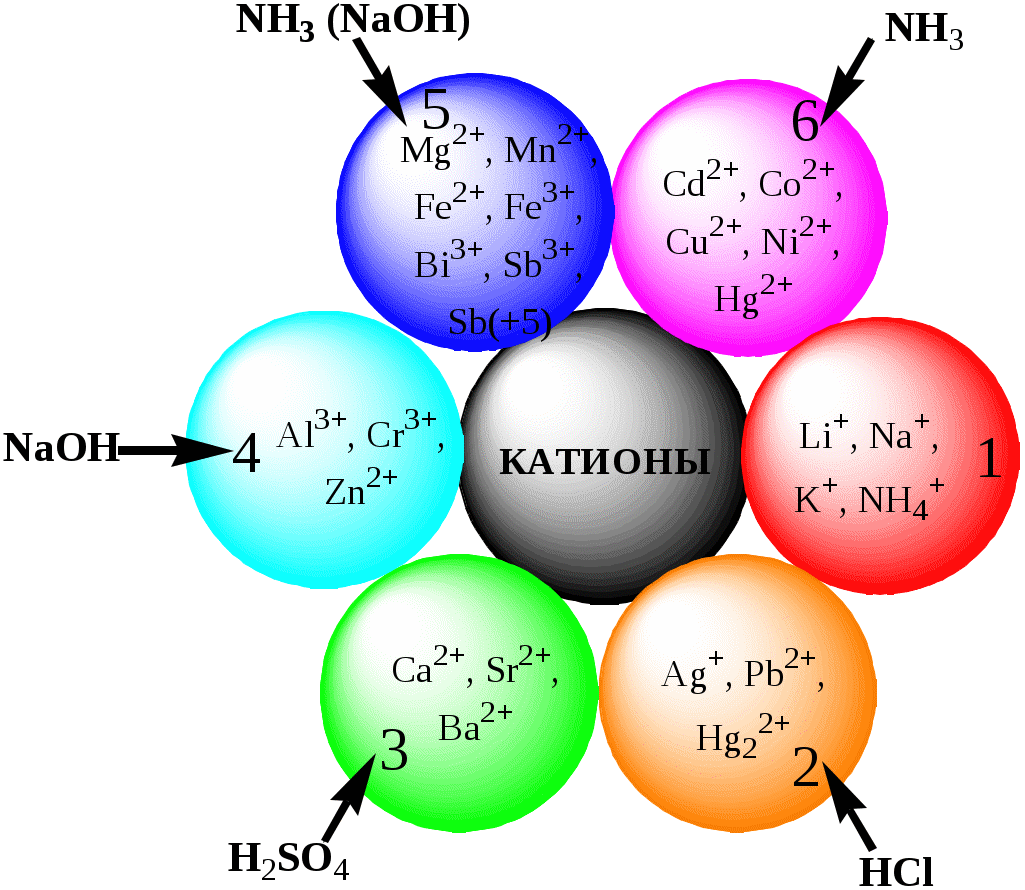 Первая аналитическая группа катионовК первой аналитической группе катионов относятся катионы K+, Na+, NH4+, Li+. Группового реагента данные катионы не имеют. Ионы аммония и калия образуют малорастворимые гексанитрокобальтаты, перхлораты, хлорплатинаты, а также малорастворимые соединения с некоторыми крупными органическими анионами, например, дипикриламином, тетрафенилборатом, гидротартратом и др. Водные растворы солей катионов I группы, за исключением солей, образованных окрашенными анионами, бесцветны. Гидратированные ионы K+, Na+, Li+ являются очень слабыми кислотами, более выражены кислотные свойства у NH4+ (рКa = 9,24). Несклонны к реакциям комплексообразования. В окислительно-восстановительных реакциях ионы K+, Na+, Li+ не участвуют, так как имеют постоянную и устойчивую степень окисления, ионы NH4+ обладают восстановительными свойствами. Обнаружение катионов I аналитической группы проводят по следующей схеме 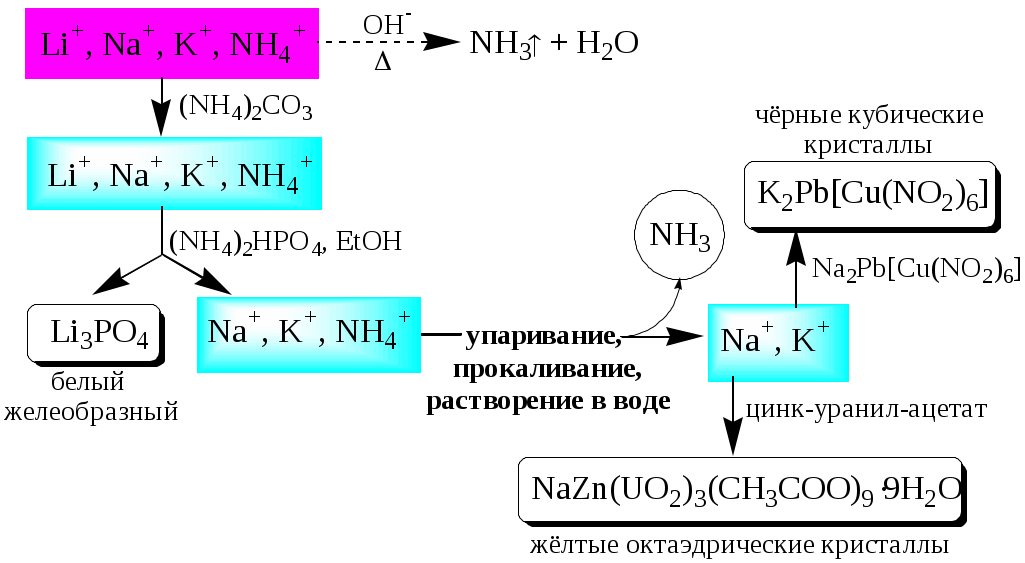 Обнаружению K+, Na+, Li+ мешают катионы р- и d-элементов, которые удаляют, осаждая их (NH4)2CO3. Обнаружению K+ мешает NH4+, который удаляют прокаливанием сухого остатка или связыванием с формальдегидом: 4 NH4+ + 6CHOH + 4ОН- (CH2)6N4 + 10H2O Вторая аналитическая группа катионовКо второй аналитической группе относятся катионы Ag+, Pb2+ и Hg22+. Катионы данной группы образуют малорастворимые гидроксиды, хлориды, хроматы, карбонаты, сульфаты, сульфиды, иодиды, арсенаты, арсениты. Большинство солей в растворе бесцветны. Окрашены хроматы, дихроматы, иодиды, сульфиды и др. В присутствии восстановителей ионы Ag+ и Hg22+ восстанавливаются до элементарного состояния. Сильные окислители окисляют Pb2+ в Pb (IV), Hg22+ в Hg2+. Катионы данной группы склонны к образованию комплексных соединений. Групповым реагентом является хлороводородная кислота, осаждающая Ag+, Pb2+ и Hg22+ в виде белых осадков AgCl, Hg2Cl2, PbCl2. Осадок AgCl темнеет на свету в результате восстановления Ag+ до Ag. Осадок AgCl растворим в концентрированных растворах HCl и хлоридов и легко растворяется в растворе NH3. Осадок Hg2Cl2 при действии NH3 чернеет вследствие образования Hg. Осадок PbCl2 растворяется в избытке HCl и хлорид-ионов, а также в горячей воде. Схема систематического анализа: 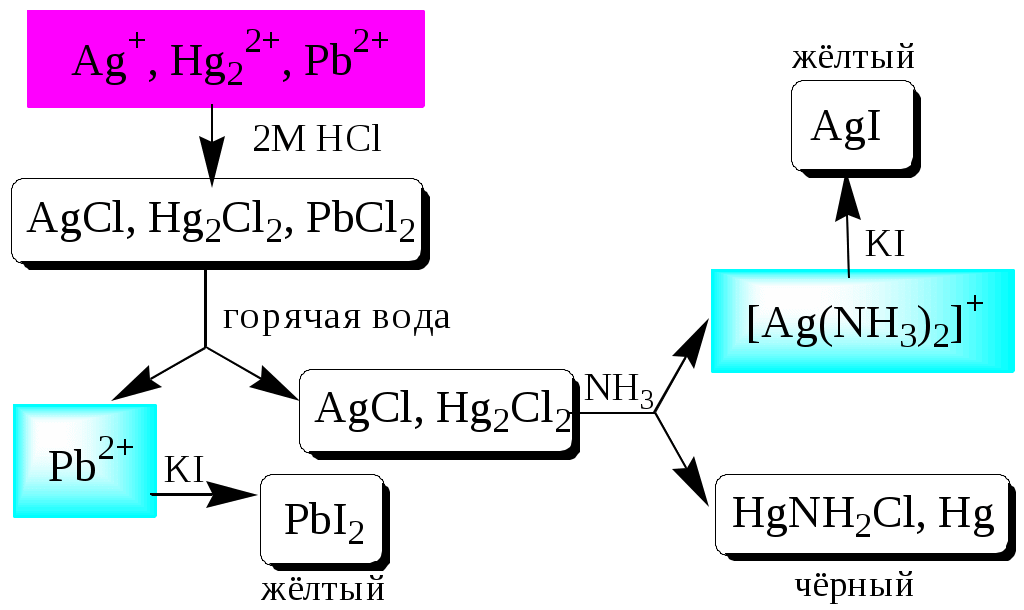 Третья аналитическая группа катионов К третьей аналитической группе относятся катионы Ca2+, Sr2+ и Ba2+. Образуют малорастворимые карбонаты, сульфаты, хроматы, фосфаты, оксалаты, фториды. В водных растворах бесцветны. К реакциям комплексообразования несклонны. Степень окисления постоянна и равна +2. Групповым реагентом является разбавленная H2SO4. Осадки сульфатов не растворяются в кислотах и щелочах. Для полноты осаждения к раствору прибавляют этанол. Схема систематического анализа: 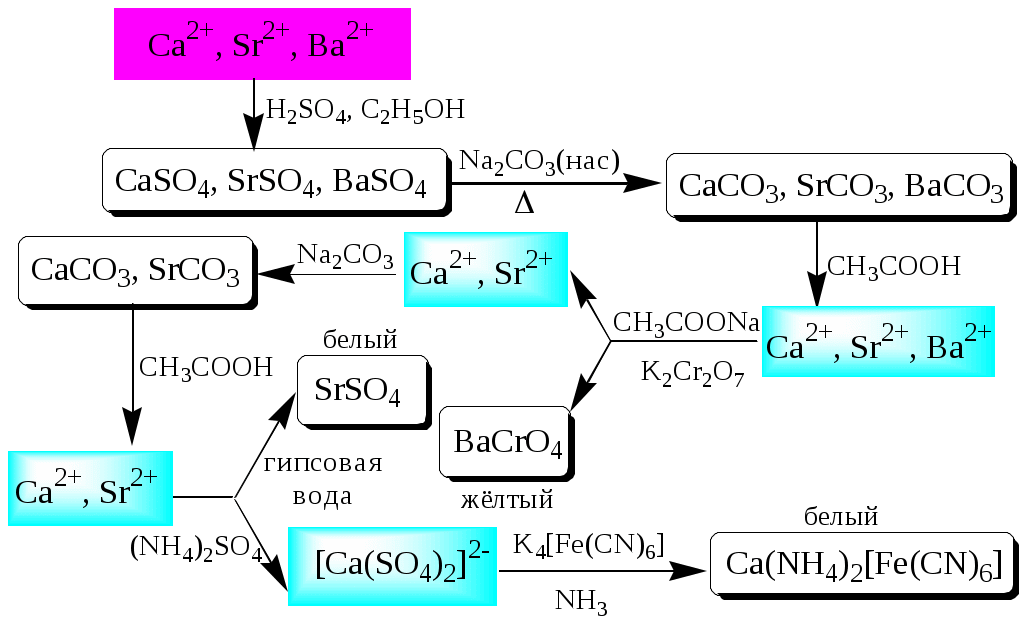 Четвёртая аналитическая группа катионов К четвёртой аналитической группе относятся катионы Al3+, Cr3+, Zn2+. Образуют малорастворимые гидроксиды, фосфаты, карбонаты, сульфиды. Сульфиды и карбонаты алюминия и хрома при взаимодействии с водой образуют гидроксид металла и H2S (сульфиды) или CO2 (карбонаты). В водных растворах катионы данной группы, за исключением [Cr(H2O)6]3+, бесцветны. Гидратированные катионы четвёртой группы обладают выраженными кислотными свойствами. Образуют комплексные соединения, например, [Al(OH)4]-. Ионы Al3+ и Zn2+ имеют постоянную степень окисления. Ионы Cr3+ могут участвовать в окислительно-восстановительных реакциях. Групповым реагентом является NaOH, в избытке которого гидроксиды катионов четвёртой аналитической группы, обладающие амфотерными свойствами, растворяются с образованием комплексных соединений типа [Al(OH)4]-, [Cr(OH)4]-, [Zn(OH)4]2-. Схема систематического анализа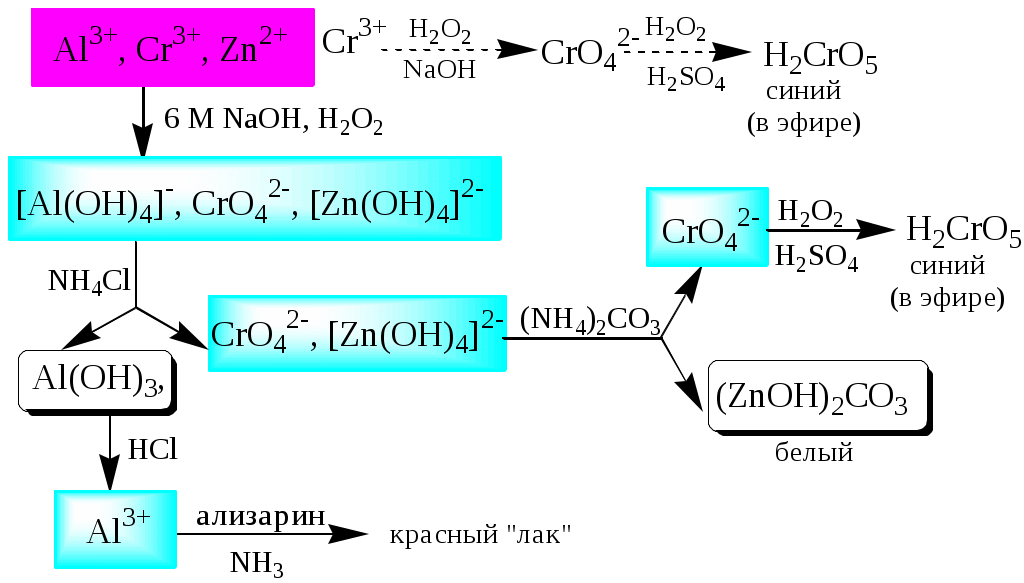 Пятая аналитическая группа катионов К пятой аналитической группе относятся катионы Mg2+, Mn2+, Fe2+, Fe3+, Bi3+, Sb (III) и Sb (V). Образуют малорастворимые гидроксиды, карбонаты, сульфиды (кроме Mg2+), фосфаты. Растворы солей магния, висмута (III) и сурьмы (III, V) бесцветны. Растворы солей Fe (II) имеют бледно-зелёную окраску, Fe (III) - от жёлтой до коричневой (вследствие образования гидроксокомплексов) и Mn (II) - бледно-розовую окраску. Разбавленные растворы солей Fe (II) и Mn (II) бесцветны. Ионы Fe2+, Fe3+, Bi3+, Sb (III) и Sb (V) способны образовывать комплексные соединения, например, [Fe(CN)6]3-, Fe(CN)6]4-, [SbCl6]3-, [SbCl6]-, [BiI4]-. Все катионы данной группы (кроме Mg2+) проявляют окислительно-восстановительные свойства: Fe3+,Bi3+, Sb (V) - окислители; Fe2+, Sb (III) - восстановители. Групповым реагентом является раствор NH3, от действия которого выпадают в осадок гидроксиды: белые Mg(OH)2, Mn(OH)2, Fe(OH)2, Bi(OH)3, Sb(OH)3, SbO(OH)3 и красно-бурый Fe(OH)3. Окраска Fe(OH)2 c течением времени изменяется до зелёной, а затем образуется красно-бурый Fe(OH)3. Осадки гидроксидов растворяются в кислотах и не растворяются в избытке щёлочи и аммиака. Схема систематического анализа 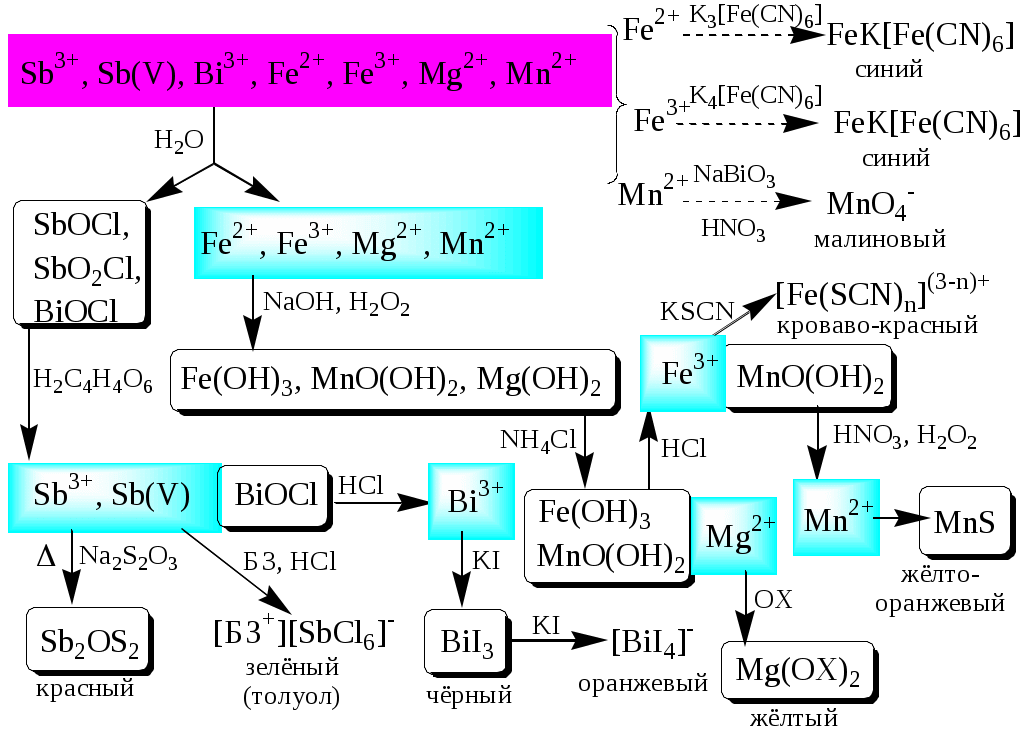 Шестая аналитическая группа катионов К шестой аналитической группе относятся катионы Cu2+, Co2+, Cd2+, Ni2+ и Hg2+. Образуют малорастворимые сульфиды, карбонаты, оксалаты, фосфаты, арсенаты, силикаты, хроматы, иодиды меди (I) и ртути (II). Большинство растворимых в воде солей окрашены: соли никеля - зелёные, кобальта - красные, меди - синие. Характерным свойством катионов VI группы является способность образовывать комплексные соединения, в том числе внутрикомплексные соединения с органическими реагентами. Все катионы VI аналитической группы, за исключением Cd2+, участвуют в реакциях окисления-восстановления. Ионы Hg2+ и Cu2+ проявляют себя как окислители, ионы Co2+ и Ni2+ - как восстановители. Групповым реагентом является раствор NH3. Гидроксиды катионов данной группы растворяются в избытке аммиака с образованием окрашенных аммиачных комплексов (катион тетраамминртути – бесцветный). Схема систематического анализа 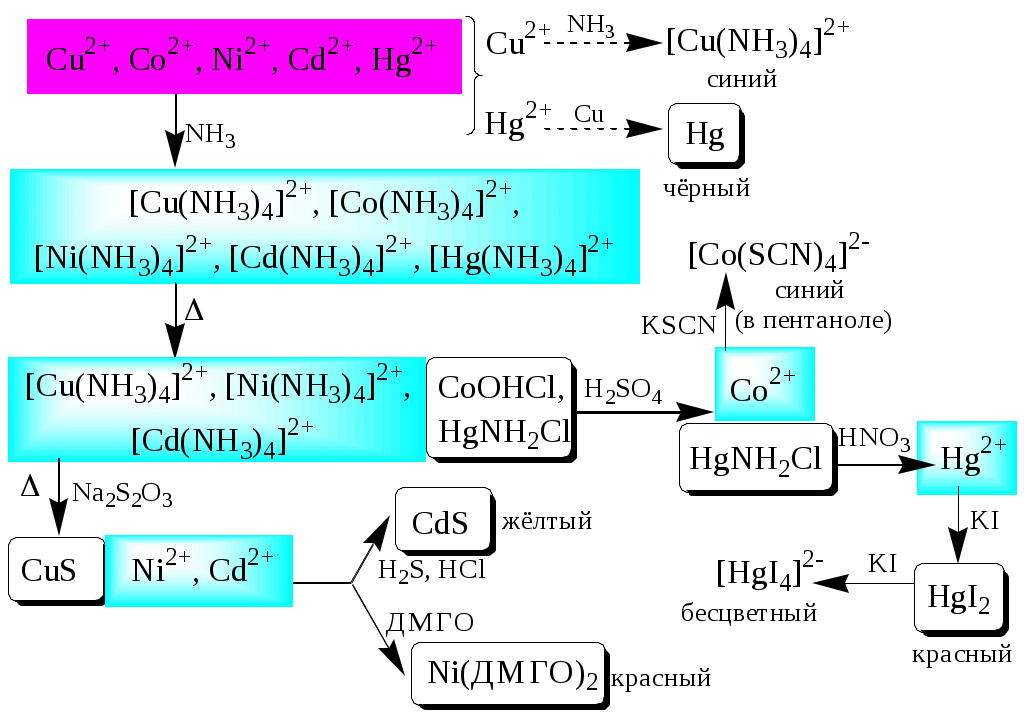 2.4. Общая характеристика, классификация и способы обнаружения анионов Реакции обнаружения анионов могут быть основаны на их окислительно-восстановительных свойствах, способности образовывать малорастворимые соединения, а также на взаимодействии с кислотами с образованием газообразных продуктов. Классификации анионов не является строго установленными. Например, в зависимости от растворимости солей бария и серебра анионы разделяют на: 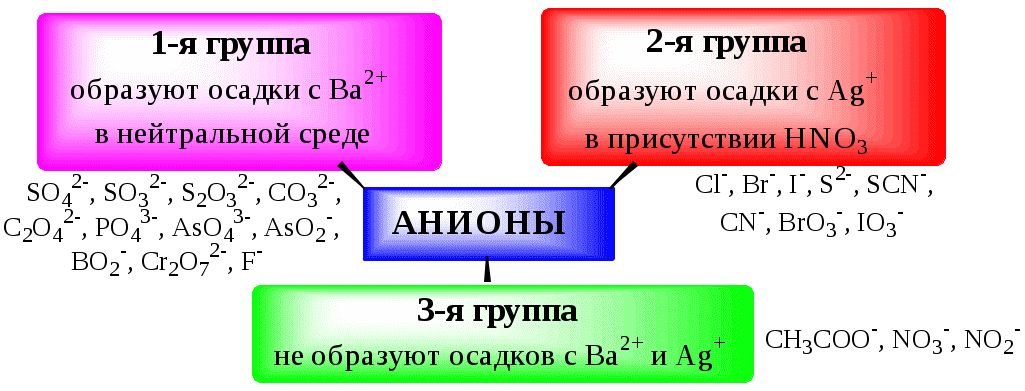 По окислительно-восстановительным свойствам анионы можно разделить на следующие группы: 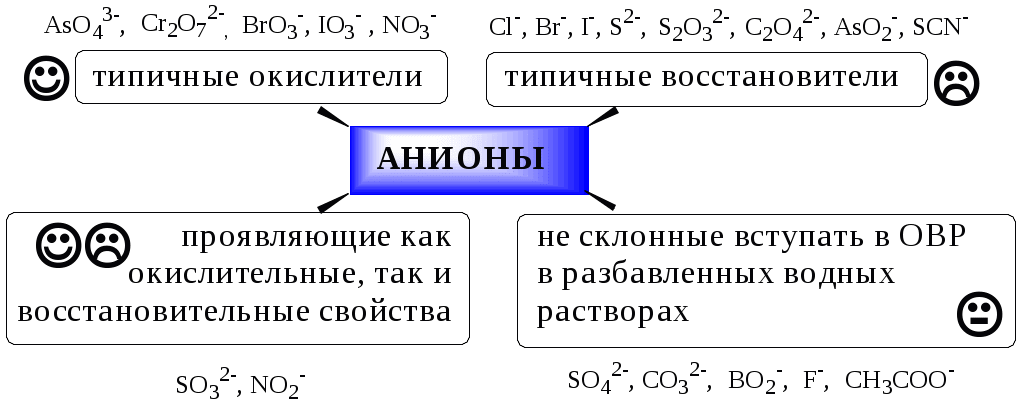 Анионы обычно обнаруживают дробным методом, и групповые реагенты используют только для установления наличия или отсутствия анионов той или иной группы. Обнаружение некоторых анионов может проводиться систематическим методом: Систематический анализ смеси серусодержащих анионов 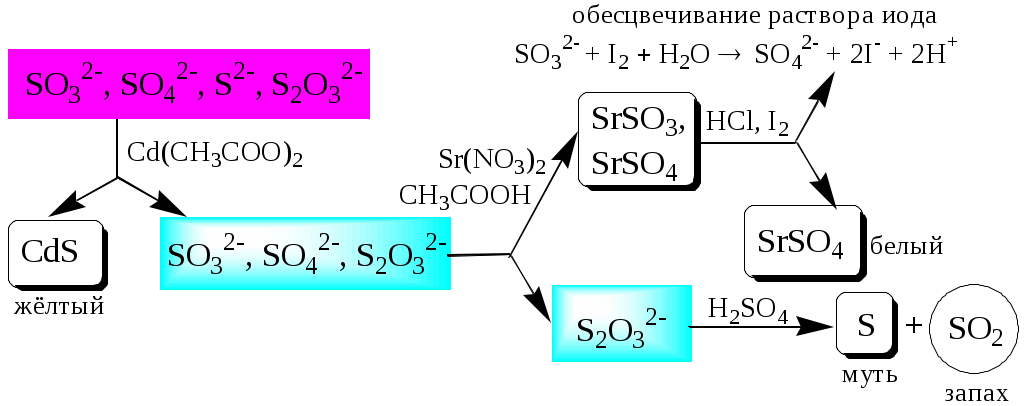 Систематический анализ смеси Cl-, Br-, I- - ионов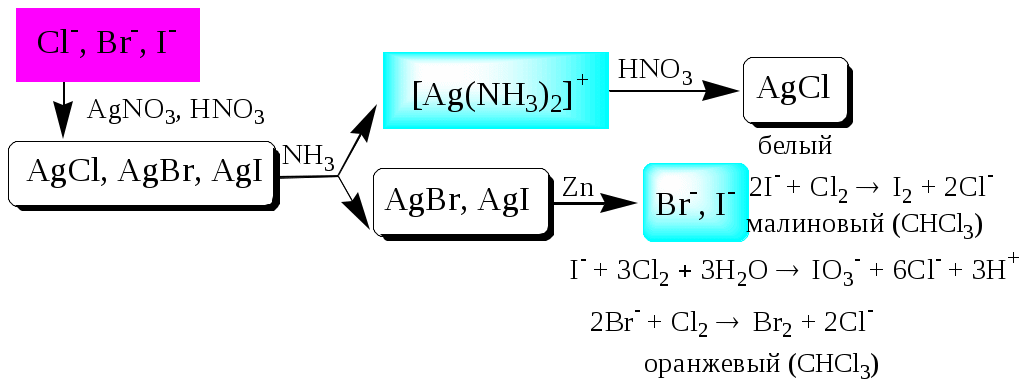 Обнаружение анионов целесообразно начинать с предварительных испытаний: установление рН раствора Если среда кислая (рН2) , в ней не могут присутствовать анионы летучих и неустойчивых кислот (SO32-, S2O32-, CO32-, NO2-). Кроме того, в кислой среде в растворе не могут одновременно присутствовать анионы-окислители и анионы восстановители. испытание на выделение газообразных веществ под действием разбавленных кислот Исследуемый раствор обрабатывают 1 М H2SO4. Выделение СО2 указывает на присутствие СО32-, SО2 - SО32-, NО2 - NО2-, одновременно SО2 и осадка S - на присутствие S2О32-. Выделение I2 говорит об одновременном присутствии I- и анионов-окислителей. испытание на присутствие анионов I группы. К исследуемому раствору добавляют раствор BaCl2 при рН 7-9. Отсутствие осадка указывает на отсутствие анионов 1 группы, хотя S2O32-, BO2 образуют осадки с BaCl2 в концентрированных растворах. испытание на присутствие анионов II группы К исследуемому раствору добавляют раствор AgNO3 в присутствии разбавленного раствора НNO3. Отсутствие осадка указывает на отсутствие анионов 2 группы. испытание на присутствие анионов-окислителей. К исследуемому раствору добавляют раствор KI в присутствии разбавленной H2SO4. Если при этом не выделяется I2 , то анионы-окислители отсутствуют. испытание на присутствие анионов-восстановителей К исследуемому раствору добавляют раствор KMnO4 в нейтральной среде и нагревают. Выпадение темно-бурого осадка указывает на присутствие анионов-восстановителей. Дополнительно можно проверить наличие сильных восстановителей по обесцвечиванию раствора I2. Далее проводят реакции обнаружения анионов, отсутствие которых не было доказано в предварительных испытаниях. Раствор, в котором проводят обнаружение, не должен содержать никаких катионов кроме K+, Na+, NH4+. Мешающие катионы удаляют путем кипячения с раствором Na2CO3 (готовят «содовую вытяжку»). |
