тесты ОХ. Р аздел Теоретические основы органической химии. Углеводороды. Методы исследования органических соединений
 Скачать 398.54 Kb. Скачать 398.54 Kb.
|
C) – M, – ID) + M, + IE) + I 3. Мерой прочности химической связи является: А) Полярность молекулы. В) Энергия связи. С) Ковалентность связи. D) Электроотрицательность элементов. Е) Длина связи. 4. Соединение, в котором имеется π,π – сопряженная система: А) Уксусная кислота. В) Этанол. С) н-бутан. D) Бензол. Е) Циклопропан. 5. Индуктивный эффект всегда направлен в сторону: А) Заместителей. В) Углеродной цепи. С) Более электроотрицательного атома. D) Наиболее длинной углеродной цепи. Е) -связи. 6. Электронные эффекты нитро группы в нитробензоле: А) + I, – М В) – I, – М С) – I D) – I, + М Е) + I, + М. 7. Электронные эффекты альдегидной группы в бензальдегиде: А) + M, – I B) – M, + I C) – M, – I D) + M, + I E) + I 8. Передача электронного влияния заместителей по системе σ – связей называется: А) Индуктивным эффектом. В) Мезомерным эффектом. С) Поляризуемостью. D) Ароматичностью. Е) Основность. 9. Электронные эффекты карбоксильной группы в уксусной кислоте: А) + M, – I B) – M, + IC) – M, – ID) + M, + IE) – I 10. Соединение, в котором имеется р,π – сопряженная система: А) Бутадиен-1,3. В) Изопрен. С) Толуол. D) Бензол. Е) Винилхлорид. 11. Соединение, в котором имеется сопряженная двойная связь: А) СН2 = СН – СН = СН2 В) СН2 = С = СН – СН = СН2 С) СН2 = СН – СН2 – СН = СН2 D) СН2 = С = СН2 Е) СН2 = СН – СН2 – СН2 – СН = СН2 12. Только положительный индуктивный эффект (+J) проявляет заместитель: А) – ОН В) – СН3 С) – COOH D) – NH2 Е) – Вr 13. Мезомерный эффект возникает при передаче влияния заместителей: А) По -связям углеродной цепи. В) По - и -связям углеродной цепи. С) По системе -связи. D) По -связям сопряженной системы. Е) По -связям замкнутого цикла. 14. Электронные эффекты брома в бромбензоле: А) + M, – I B) – M, + IC) – M, – ID) + M, + IE) + I 15. Электроноакцепторные заместители: А) – СООН В) – CI С) – C2H5 D) – CHO Е) – СН3 16. В молекуле СH2 = СНNО2 нитрогруппа оказывает влиние: А) +М В) –М С) +J, +М D) +J, +М Е) –І, –М 17. Заместитель проявляет электроноакцепторные свойства: A) В феноле. B) В йодбензоле. C) В анилине. D) В этилбензоле. E) В метилфениловом эфире. 18. Электронные эффекты гидроксильной группы в феноле: А) + M, – I B) – M, + IC) – M, – ID) + M, + IE) + IПРОСТРАНСТВЕННАЯ ИЗОМЕРИЯ 1. Конфигурация стереомера по конфигурационному стандарту: А) Относительная конфигурация. В) Абсолютная конфигурация. С) Конформация. D) Хиральность. Е) Таутомерия. 2. В молекуле (СН3)2СНСН2СН(NH2)СООН встречается изомерия: А) Таутомерия. В) Цис-транс изомерия. С) Диастереомерия. D) Энантиомерия. Е) Е, -изомерия. 3. Энантиомеры отличаются друг от друга: А) Химическими свойствами. В) Температурой плавления. С) Температурой кипения. D) Плотностью. Е) Знаком оптической активности. 4. Е, -изомерия существует для: А) 1-бром-1,2-дихлорпентена-1 В) 1,1- дихлорпентена-1 С) 1,1-дибромпентена-1 D) 1,1-дийиодпентена-1 Е) Пентена-1 5. Для изображения конформационных изомеров за минимальный отсчет поворота принимают угловой градус: А) 180о В) 360о С) 90о D) 60о Е) 30о 6. Для хлоряблочной (2-гидрокси-3-хлорбутандионовой) кислоты существует: А) 2 стереоизомера. В) 3 стереоизомера. С) 4 стереоизомера. D) 6 стереоизомеров. Е) 8 стереоизомеров. 7. Оптически активное соединение: А) 2-аминопропановая кислота. В) Пропановая кислота. С) Пропантриол-1,2,3. D) 2-аминоэтановая кислота. Е) Этаналь. 8. Укажите соединение, существующее в виде антиподов: А) Гидрохинон. В) α-аминомасляная кислота. С) Уксусная кислота. D) Этандиол-1,2 Е) 2-метилпропаналь. 9.π – Диастереомерия характерна для: А) Алканов. В) Алкенов. С) Спиртов. D) Аренов. Е) Циклоалканов. 10. Число ассиметрических атомов углерода в фруктозе: А) 1 В) 2 С) 3 D) 4 Е) 5 11. В молекуле СН3СН(NH2)СООН встречается изомерия: А) Таутомерия. В) Энантиомерия. С) Диастереомерия. D) Цис-транс изомерия. Е) Е, -изомерия. 12. -Диастереомеры образует: А) 2,3-дигидроксипропановая кислота. В) 2-гидроксибутановая кислота. С) 2,3-дигидроксибутандиовая кислота. D) Молочная кислота. Е) 2-гидроксибутандиовая кислота. 13. Вид изомерии между малеиновой и фумаровой кислотами: А) Цис-транс изомерия. В) Энантиомерия. С) Диастереомерия. D) Таутомерия. Е) Структурная изомерия. 14. В виде Е, Z-стереоизомеров существует: А) 1,2,2-трихлорэтен. В) 1,1-дихлор-2,2-дифторэтан. С) 1,2-дифтор-1,2-дихлорэтан. D) 1,1-дихлорэтен. Е) 1-бром-2-иод-1,2-дифторэтен. 15. Оптически активное соединение: А) 2-метилпропаналь. В) Пропаналь. С) 2-гидроксипропаналь. D) Пропанол-2 Е) Пропантриол-1,2,3 16. Стереоизомер с одним хиральным центром: А) 3-гидроксипропановая кислота. В) 2-аминоэтанол. С) Аминоуксусная кислота. D) 2-гидроксипропановая кислота. Е) Пропантриол-1,2,3. 17. Цис-транс изомерия не существует для: А) Бутена-2 В) Гексена-2 С) Гексена-3 D) Пропана. Е) 1-хлорбутена-2 18. n в формуле N = 2n является: А) Числом центров хиральности. В) Числом общего числа атомов С. С) Числом стереоизомеров. D) Числом общего числа атомов Н. Е) Числом функциональных групп. 19. Оптические изомеры: А) -диастереоизомеры. В) Энантиомеры. С) -диастереомеры. D) Эпимеры. Е) Рацематы. 20. Порядок расположения атомов в пространстве без учета различий, возникающих вследствие вращения вокруг одинарных связей, называется: А) Конфигурацией. В) Конформацией. С) Таутомерией. D) Изомерией. Е) Структурной изомерией. 21. Молекулы, которые относятся к конфигурационным изомерам: А) Отличаются по положению двойной связи. В) Отличаются по расположению атомов в пространстве. С) Не отличаются по расположению атомов в пространстве. D) Имеют одинаковые пространственное строение. Е) Отличаются по распределению электронной плотности π-связи. 22. Абсолютной конфигурации стереоизомеров соответствует: А) Пространственное строение глицеринового альдегида. В) Е - , Z – система. С) Цис-транс система. D) R- , S – система. Е) D- , L – система. 23. Цис-транс-изомерия относится к изомерии: А) Конформационной. В) Структурной. С) Конфигурационной. D) Положения. Е) Функциональных групп. 24. Стереоизомеры – это: А) Вещества, имеющие одинаковый количественный и качественный состав, но различное строение. В) Вещества, имеющие одинаковое строение, т.е. с одним и тем же порядком соединения атомов, отличающиеся расположением тех же атомов в пространстве. С) Вещества, имеющие сходное строение, образующие гомологический ряд. D) Вещества, имеющие в составе несколько одинаковых функциональных групп. Е) Вещества, имеющие одинаковое строение, но различный качественный и количественный состав. 25. Соединения, имеющие асимметрический атом углерода: A) CH3–CH(NH2) –COOH B) CH3–CH2–CHBr–CH3 C) (CH3)2CH – CH2 – CH(OH) –CH3 D) HOOC–CH2 – CH(OH) – CH2–COOH E) HOOC–CH2 – CH(OH) – COOH 26. Энантиомеры – это: А) Стереоизомеры, молекулы которых относятся друг к другу как предмет и совместимое с ним зеркальное изображение. В) Стереоизомеры, молекулы которых не относятся друг к другу как предмет и несовместимое с ним зеркальное изображение. С) Изомеры строения. D) Изомеры функциональных групп. Е) Изомеры положения. 27. Различные стереоизомеры молекулы, возникающие в результате вращения вокруг одинарных связей, называют: А) Конфигурацией. В) Конформациями. С) Таутомерами. D) Энантиомерами. Е) Диастереомерами. 28. Для изображения конформации используют проекционные формулы: А) Хеуорса. В) Фишера. С) Ньюмена. D) Байера. Е) Колли-Толленса. 29. Оптически не активная смесь равных количеств энантиомеров называется: А) Рацематом. В) Эпимером. С) Антиподом. D) Мезоформой. Е) Диастереоизомером. 30. Энантиомерами являются: А) D – глюкоза и D – фруктоза. В) L – фруктоза и L – глюкоза. С) D – глюкоза и L – фруктоза. D) D – глюкоза и L – глюкоза. Е) D – фруктоза и L – манноза. 31. Для изображения конформаций на плоскости используют проекционные формулы: А) Фишера. В) Байера. С) Хеуорса. D) Вант-Гоффа. Е) Ньюмена. 32. Рацематом является: А) Д – винная кислота. В) L – винная кислота. С) (Д, L) – винная кислота. D) Мезовинная кислота. Е) Д – молочная кислота. 33. Оптически активное соединение: А) 2-метилпропаналь. В) Пропаналь. С) 2-гидроксипропаналь. D) Пропанол-2. Е) Пропантриол-1,2,3. 34. В конформациях циклогексана валентные углы приближаются к углу: А) 120о В) 180о С) 109о D) 90о Е) 60о 35. Молочная (2-гидроксипропановая) кислота имеет число стереоизомеров: А) 2 В) 3 С) 4 D) 1 Е) 6 36. Не имеет асимметрического атома углерода: A) CH3 – CH(OH) –COOH B) (CH3)2CBr – CH2 – COOH C) C6H5 – CH(NH2) – COOH D) CH3 – CH(NH2) –CH2–COOH E) CH3 – CHCl – COOH КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1. По теории Бренстеда-Лоури кислотами являются: А) Акцепторы протона. В) Доноры электронной пары. С) Доноры протона. D) Акцепторы электронной пары. Е) Доноры катионов. 2. Этиловый спирт относится к: А) Карбоновым кислотам. В) SH-кислотам. С) NH-кислотам. D) СH-кислотам. Е) ОH-кислотам. 3. Не является основанием Льюиса: А) Фуран. В) Пиридин. С) Тиофен. D) Метилциклогексан. Е) Нафталин. 4. Обладает наибольшей кислотностью:  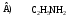 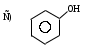   5. Электронодонорные заместители: А) Стабилизируют анион и увеличивают кислотность соединения. В) Дестабилизируют анион и уменьшают кислотность соединения. С) Не влияет на кислотность соединения. D) Стабилизируют анион и уменьшают кислотность соединения. Е) Дестабилизируют анион и увеличивают кислотность соединения. 6. Нейтральные молекулы или ионы, способные присоединять протон: А) Кислоты Бренстеда. В) Основания Бренстеда. С) Кислоты Льюиса. D) Основания Льюиса. Е) ОН-кислоты. 7. Самое сильное основание в ряду: А) п-толуидин. В) Анилин. С) п-нитроанилин. D) 2,4,6-тринитроанилин. Е) 2,4-динитроанилин. 8. Присоединение галогеноводорода к этилену относится к кислотно-основному взаимодействию, где этилен: А) р-основание. В) -основание. С) Кислота Бренстеда. D) Кислота Льюиса. Е) СН-кислота. 9. Наибольшими кислотными свойствами обладает: А) НСООН В) СН3СООН С) СН2FСООН D) СНF2СООН Е) СF3СООН 10. По теории Бренстеда-Лоури основаниями являются А) Доноры протона. В) Доноры электронной пары. С) Акцепторы электронной пары. D) Акцепторы катионов. Е) Акцепторы протона. 11. Наибольшими кислотными свойствами обладает: А) СН3SН В) СН3ОН С) С2Н5NН2 D) СН3 – СН2 – СН3 Е) СН3 – СН = СН – СН3 12. Электроноакцепторные заместители: А) Повышают основность соединения. В) Понижают основность соединения. С) Не влияют на основность соединения. D) Повышают, затем уменьшают основность соединения. Е) Уменьшают, затем увеличивают основность соединения. 13. Фенол относится к: А) Карбоновым кислотам. В) SH-кислотам. С) NH-кислотам. D) СH-кислотам. Е) ОH-кислотам. 14. Ацетилен относится к: А) Оксониевым основаниям. В) SH-кислотам. С) NH-кислотам. D) СH-кислотам. Е) ОH-кислотам. 15. Наибольшую кислотность имеет: А) Муравьиная кислота. В) Уксусная кислота. С) Пропионовая кислота. D) Бутановая кислота. Е) Пентановая кислота. 16. Основания Бренстеда: А) Способны присоединять протон. В) Имеют гидроксильную группу. С) Способны отдавать протон. D) Имеют вакантную орбиталь. Е) Имеют отрицательный заряд. 17. Наибольшей кислотностью обладает: А) о-Нитрофенол. В) Фенол. С) Пикриновая кислота (2,4,6-тринитрофенол). D) п-крезол (п -метилфенол). Е) о-крезол (о-метилфенол). 18. Сильное основание: А) RСООН В) RNH2 С) ROR D) ROH Е) RSH 19. Наибольшую кислотность имеет: А) n-Нитроанилин. В) Анилин. С) о-Крезол. D) n-Нитрофенол. Е) Фенол. 20. По теории Бренстеда-Лоури соединения имеющие протон связанный с кислородом: А) SH – кислоты. В) OH – кислоты. С) NH – кислоты. D) СН – кислоты. Е) ОН – основания. 21. Наибольшими основными свойствами обладает: А) NН3 В) Н2О С) СН3NН2 D) СН3ОН Е) СН3SН 22. По теории Бренстеда-Лоури соединения присоединяющие протон за счет электронной пары атома азота: А) -основания. В) Сульфониевые основания. С) Оксониевые основания. D) Аммониевые основания. Е) NH-кислоты. 23. По теории Льюиса кислотами являются : А) Доноры электронной пары. В) Акцепторы электронной пары. С) Акцепторы протона. D) Доноры протона. Е) Акцепторы катионов. 24. Наибольшую кислотность имеет: А) СН3 – СООН В) СН3 – СН2 – СООН С) СН2СI – СООН D) СН2СI – СН2 – СООН Е) СН3 – СН2 – СООН 25. Наибольшую кислотность имеет: А) Пропионовая кислота. В) Уксусная кислота. С) Трихлоруксусная кислота. D) Монохлоруксусная кислота. Е) Дихлоруксусная кислота. 26. Кислоты Бренстеда: А) Способны присоединять протон. В) Способны присоединять положительные частицы. С) Способны отдавать протон. D) Имеют вакантную орбиталь. Е) Имеют отрицательный заряд. 27. Наиболее сильная кислота: А) рК = 10,5 В) рК = 7,6 С) рК = 3,8 D) рК = 5,8 Е) рК = 4,9 28. Обладает наибольшей основностью: |
