Химия задача. Решение в данном соединении комплексообразователь Fe
 Скачать 183.02 Kb. Скачать 183.02 Kb.
|
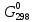 = – z∙F ∙ЭДС∙10–3 = –6 ∙ 96500 ∙0,786 ∙ 10–3 = – 455,1 кДж; = – z∙F ∙ЭДС∙10–3 = –6 ∙ 96500 ∙0,786 ∙ 10–3 = – 455,1 кДж; 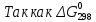 < 0, то реакция протекает в прямом направлении. < 0, то реакция протекает в прямом направлении. 2) Рассмотрим метод ионно-электронного баланса для ОВР, которая протекает в нейтральной среде. KMnO4 + K2SO3 + H2O = K2SO4 + MnO2↓ + KOН. Определим степень окисления каждого элемента: +1 +7 -2 +1 +4 -2 +1 -2 +1 +6 -2 +4 -2 +1 -2 +1 K Mn O4 + K2 S O3 + H2O = K2 S O4 + MnO2↓ + K O Н. Видим, что KMnO4 – окислитель (Mn+7), K2SO3 – восстановитель (S+4). Написав реакцию в диссоциированном виде, получаем: К+ + MnO4– + 2К++ SO32– +H2O → 2К++SO42– + MnO2↓ + К++ OН–. Затем напишем полуреакции окисления-восстановления. Общее число электронов, участвующих в ОВР: 6. В нейтральной среде для уравнивания используются молекулы воды, ионы H+ и OН–:
Получили сокращенное ионно-молекулярное уравнение. В правой части 6H+ и 8OН– образуют 6 молекул воды и 2OН–. Сократив молекулы воды в левой и правой части и подставив найденные коэффициенты, уравниваем реакцию: 2KMnO4 + 3Na2SO3 + H2O → 2MnO2↓ + 2KOН + 3Na2SO4. Находим значения стандартных электродных потенциалов окислителя и восстановителя (табл. П 2): потенциал окислителя Е0(MnO4–,2H2О/MnО2,4OН–) = 1,23 B; потенциал восстановителя Е0(SO42–,H2O/SO32–,2H+) = 0,172 B. Так как потенциал окислителя больше потенциала восстановителя, делаем вывод, что реакция протекает слева направо. Это подтверждают и расчёты: ЭДС = Е0 (MnO4–,2H2О/MnО2,4OН–) – Е0(SO42–,H2O/SO32–,2H+) = = 1,23 – 0,172 = 1,06 B. Δ 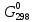 = – z∙F ∙ЭДС∙10–3 = –6 ∙ 96500 ∙1,06 ∙ 10–3 = – 613,7 кДж; = – z∙F ∙ЭДС∙10–3 = –6 ∙ 96500 ∙1,06 ∙ 10–3 = – 613,7 кДж;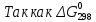 < 0, то реакция протекает в прямом направлении. < 0, то реакция протекает в прямом направлении. 3) Рассмотрим метод ионно-электронного баланса для ОВР, которая протекает в щелочной среде. NaNO2 + KMnO4 + KOH → NaNO3 + K2MnO4 + H2O. Определив степень окисления каждого элемента, видим, что KMnO4 – окислитель (Mn+7), NaNO2 – восстановитель (N+3). +1 +3 –2 +1 +7 –2 +1 –2 +1 +1 +5 –2 +1 +6 –2 +1 –2 Na N O2 + K Mn O4 + K O H → Na N O3 + K2 Mn O4 + H2O. Написав реакцию в диссоциированном виде, получаем: Na+ +NO2– + К+ + MnO4– + К++ OH– → Na+ +NO3– + 2К+ + MnO42– +H2O Напишем полуреакции окисления-восстановления: в щелочной среде баланс частиц уравнивается ионами OH–, которые добавляются к восстановленной форме, и молекулами воды, добавляемыми к окисленной форме. Общее число электронов, участвующих в окислительно-восстановительной реакции: 2.
Получили сокращенное ионно-молекулярное уравнение. Подставив найденные коэффициенты, уравниваем реакцию: NaNO2 + 2KMnO4 + 2KOH → NaNO3 + 2K2MnO4 + H2O. Находим значения стандартных электродных потенциалов окислителя и восстановителя (табл. П 2): потенциал окислителя Е0 (MnO4–/ MnO42–) = 0, 56 B; потенциал восстановителя Е0(NO2–,2OH– /NO3–,H2O) = 0,01 B. Так как потенциал окислителя больше потенциала восстановителя, делаем вывод, что реакция протекает слева направо. Это подтверждают и расчёты: ЭДС = Е0(MnO4–/MnO42–) – Е0(NO2–,2OH– /NO3–,H2O) = = 0,56 – 0,01 = 0,55 B. 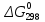 = – z∙ F ∙ЭДС∙10–3 = –2 ∙ 96500 ∙0,55 ∙ 10–3 = – 105,15 кДж; = – z∙ F ∙ЭДС∙10–3 = –2 ∙ 96500 ∙0,55 ∙ 10–3 = – 105,15 кДж; 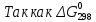 < 0, то реакция протекает в прямом направлении. < 0, то реакция протекает в прямом направлении. Пример 6.3. Рассчитайте электродвижущую силу гальванического элемента по стандартным значениям энергии Гиббса (Δ 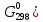 для реакции: для реакции: Zn (т) + 2Сu(OH)2 (т) = ZnO (т) + Cu2O (т) + 2H2O (ж). Напишите реакции, происходящие на электродах, составьте схему гальванического элемента. Р е ш е н и е Находим табличные значения Δ 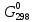 участников реакции участников реакции (табл. П 1): Zn(т) + 2Cu(OH)2(т) = ZnO(т) + Cu2O(т) + 2H2O(ж) ∆ 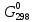 ,кДж/моль, 0 –356,9 –318,2 –146,4 – 237,3 ,кДж/моль, 0 –356,9 –318,2 –146,4 – 237,3Рассчитываем Δ 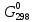 реакции согласно закону Гесса: реакции согласно закону Гесса:Δ 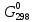 = [Δ = [Δ 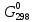 (ZnO (т))+ Δ (ZnO (т))+ Δ 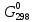 (Cu2O (т)) + 2·Δ (Cu2O (т)) + 2·Δ 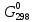 (H2O (ж))] – (H2O (ж))] –– Δ 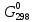 (Zn (т)) – 2 Δ (Zn (т)) – 2 Δ 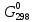 (Cu(OH)2 (т)) = [(–318,2) + (–146,4) + (Cu(OH)2 (т)) = [(–318,2) + (–146,4) ++ 2·(– 237,3)] – 2·(–356.9) = –225,6 кДж/моль. Полученное отрицательное значение ∆G0298 показывает, что реакция протекает самопроизвольно в прямом направлении. Величину ЭДС рассчитываем по формуле Томсона: ЭДС = 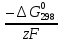 = – = – 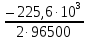 = 1,1658 B. = 1,1658 B.Определим степени окисления всех элементов в уравнении реакции 0 +2 –2 +1 +2 –2 +1 –2 +1 –2 Zn(т) + 2 Cu(OH)2 (т) → ZnO(т) + Cu 2O(т) + 2 H2O(ж) Поскольку большая часть веществ находится в твердой фазе, реакции на электродах сначало укажем схематически: Анод: Zn – 2ē = Zn+2 – окисление Катод: Cu+2 + ē = Cu + – восстановление  Суммарная реакция Zn0 + 2Cu2+ = Zn2+ + 2Cu+. Суммарная реакция Zn0 + 2Cu2+ = Zn2+ + 2Cu+.2 ē Более полно реакции на электродах имеют вид: Анод: Zn0(т) + 2OH–(р) – 2е = ZnO (т) + Н2О (ж). Катод: 2Cu(OH)2 (т) + 2Н+(р) + 2е = Cu2O (т) + 3Н2О (ж). Cхема гальванического элемента: (А) Zn | ZnO(т), H2O(ж) || Cu(OH)2(т) | Cu2O(т), H2O(ж) (К). Пример 6.4. Составьте схему работы гальванического элемента, образованного двумя данными металлами, погруженными в растворы солей с известными концентрациями ионов, рассчитайте ЭДС этого элемента. Дано: Cr, Pb; растворы CrCl3 и Pb(NO3)2; С(Сr3+) = 0,01 M; С(Pb2+) = 0,001 M. Р е ш е н и е Для составления схемы гальванического элемента, необходимо рассчитать значения потенциалов двух электродов при данных условиях по уравнению Нернста (6.4). Для первого электрода: E(Cr3+/Cr) = E0(Cr3+/Cr) + 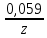 lg C(Cr3+) = lg C(Cr3+) = –0,740 + 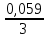 lg0,01 = –0,70 B. lg0,01 = –0,70 B.Для второго электрода: E(Pb2+/Pb) = E0(Pb2+/Pb) + 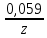 lg C(Pb2+) = lg C(Pb2+) = –0,126 + 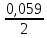 lg 0,001 = –0,124 B. lg 0,001 = –0,124 B.В данном гальваническом элементе более отрицательным электродом является система Cr|Cr3+, более положительным – Pb|Pb2+. На электродах протекают следующие реакции: Анод: Cr – 3ē = Cr+3 – окисление; Катод: Pb+2 + 2ē = Pb0 – восстановление. Электродвижущая сила этого элемента рассчитывается по формуле 6.1: ЭДС = Е(Pb2+/Pb) – E(Cr3+/Cr) = –0,124 – (–0,70) = 0,576 B. Схема гальванического элемента примет вид: (А) Cr | CrCl3 (0,01 M) || Pb(NO3)2 (0,001 M) | Pb (К). Пример 6.5. При электролизе раствора CoSO4 током I = 4,25 А масса катода возросла на 1,50 г. Рассчитайте количество электричества, если выход по току металла Bi = 75 % и время, за которое оно пропущено. Составьте схему электролиза раствора CoSO4: а) c нерастворимым анодом; б) с растворимым анодом. Р е ш е н и е Составим схему электролиза с нерастворимым анодом. В растворе присутствуют следующие ионы: CoSO4 → Co2+ + 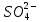 (электролитическая диссоциация); (электролитическая диссоциация);Следовательно, при составлении схемы электролиза необходимо учитывать ионы Со2+, 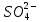 – и молекулы воды. – и молекулы воды. Так как стандартный потенциал кобальта равен E0(Co2+/Co)= – 0,28В (табл. П 2), то на катоде будет восстанавливаться металл и выделяться водород (табл.6.1). На аноде 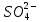 (кислородсодержащий анион) не может окисляться (табл.6.2), поэтому будет окисляться вода с выделением кислорода. Образовавшиеся ионы водорода при взаимодействии с сульфат-анионами образуют в растворе серную кислоту. (кислородсодержащий анион) не может окисляться (табл.6.2), поэтому будет окисляться вода с выделением кислорода. Образовавшиеся ионы водорода при взаимодействии с сульфат-анионами образуют в растворе серную кислоту. Схема электролиза водного раствора CoSO4 с нерастворимым (инертным) анодом:
CoSO4 + 2Н2О → Со + H2 + О2 + H2SO4. Из-за выделения водорода на катоде совместно с восстанов-лением ионов Со(II) выход по току металла меньше 100 %. Рассмотрим схему электролиза с растворимым кобальтовым анодом:
Co + 2Н2О → Со(OH)2 + H2 . Количество электричества по закону Фарадея составит: Q = | ||||||||||||||||||||
